МИНИСТЕРСТВО СЕЛЬСКОГО ХОЗЯЙСТВА РОССИЙСКОЙ ФЕДЕРАЦИИ
ФГОУ ВО «ОРЛОВСКИЙ ГОСУДАРСТВЕННЫЙ АГРАРНЫЙ УНИВЕРСИТЕТ ИМЕНИ Н.В. ПАРАХИНА»
ФАКУЛЬТЕТ «БИОТЕХНОЛОГИИ И ВЕТЕРИНАРНОЙ МЕДИЦИНЫ»
КАФЕДРА БИОТЕХНОЛОГИИ
Допустить к защите
«____» _________________ 2017 г.
_________________/ Солохина И.Ю./
КУРСОВОЙ ПРОЕКТ
по дисциплине «Управление информационными ресурсами на биотехнологических предприятиях»
по теме: «Организация информационный системы и основных ресурсов на предприятии по биофармацевтике»
Автор проекта _________ Буряк Д.А. группа 251
Направление подготовки: 19.03.01- Биотехнология
Курсовой проект защищен с оценкой _____________
Руководитель курсового проекта________к.б.н., доцент Солохина И.Ю.
Члены комиссии ________________
________________
________________
Регистрация: «____» __________2017 г.
Лаборант_______________________
Орел-2017
МИНИСТЕРСТВО СЕЛЬСКОГО ХОЗЯЙСТВА РОССИЙСКОЙ
ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ
ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ
«ОРЛОВСКИЙ ГОСУДАРСТВЕННЫЙ АГРАРНЫЙ УНИВЕРСИТЕТ
ИМЕНИ Н.В.ПАРАХИНА»
ФАКУЛЬТЕТ БИОТЕХНОЛОГИИ И ВЕТЕРИНАРНОЙ МЕДИЦИНЫ
КАФЕРДРА БИОТЕХНОЛОГИИ
ЗАДАНИЕ НА КУРСОВОЙ ПРОЕКТ
Студент(ка) Буряк Д.А. Шифр________Группа 2 курс Био (о.о)
Направление подготовки 19.03.01- Биотехнология
Тема: «Организация информационных ресурсов на предприятии по биофармацевтике»
Срок сдачи студентом законченной работы: «__» ____________2017 год
Исходные данные для выполнения курсового проекта: провести анализ основных литературных источников, патентов, ГОСТов, методик по теме исследования, рассмотреть биотехнологическую схему и техническую схему производства генно-инженерного инсулина, провести исследование организации основных информационных ресурсов и документации на предприятии по производству генно-инженерного инсулина.
Руководитель курсового проекта
к.б.н., доцент Солохина И.Ю.
Задание принял к исполнению «__» ___________2017 года
Подпись студента ______________________
Орел-2017 год
СОДЕРЖАНИЕ
ВВЕДЕНИЕ.. 4
ГЛАВА 1. ЛИТЕРАТУРНЫЙ ОБЗОР. 6
1.1. Описание биофармацевтического предприятия на примере компании "Форт". 6
1.2. Актуальность производства и применения рекомбинантного инсулина. 8
1.3. История получения инсулина. 8
1.4 Строение и механизм действия инсулина. 12
ГЛАВА 2. ТЕХНОЛОГИЧЕСКАЯ ЧАСТЬ.. 15
2.1. Способы получения инсулина. 15
2.2. Технологическая схема производства рекомбинантного инсулина. 19
ГЛАВА 3. ОРГАНИЗАЦИЯ ОСНОВНЫХ ИНФОРМАЦИОННЫХ РЕСУРСОВ И ДОКУМЕНТАЦИИ НА ПРЕДПРИЯТИИ ПО ПРОИЗВОДСТВУ ГЕННО- ИНЖЕНЕРНОГО ИНСУЛИНА.. 21
3.1. Промышленный регламент на получение генно-модифицированного инсулина с помощью р ДНК-биотехнологии. 21
3.2. Контроль качества инсулина с помощью оборудования Agilent 29
3.3. Срок годности инсулина, его упаковка, маркировка, концентрация и хранение. Виды инсулина по продолжительности действия. 31
3.4. Патенты на производство генно-инженерного инсулина. 33
ЗАКЛЮЧЕНИЕ.. 34
СПИСОК ЛИТЕРАТУРЫ... 36
ПРИЛОЖЕНИЕ.. 39
ВВЕДЕНИЕ
В своей работе я раскрываю тему организации информационных ресурсов на предприятии по биофармацевтике.
Термин "биофармацевтика" произошел от греческих слов "bio" — жизнь и "pharmakeutike" — лекарственный, врачебный. Существует несколько определений, из которых наиболее полно выражает суть данного понятия следующее. Биофармацевтика – это направление фармацевтики, которое занимается получением и использованием для терапевтических или профилактических целей сложных макромолекул, полученных с использованием методов биотехнологии и генной инженерии.
К биофармацевтическим препаратам относятся: факторы свертывания крови (фактор VIII и фактор IX), тромболитические агенты (тканевый активатор плазминогена), гормоны (инсулин, соматотропин, глюкагон), гемопоэтические факторы роста (эритропоэтин, колониестимулирующие факторы), интерфероны (интерфероны-α, -β, -γ), интерлейкины (интерлейкин-2), вакцины (гепатит B), моноклональные антитела, дополнительные продукты (фактор некроза опухоли, терапевтические белки).
Наиболее распространенные биопрепараты используются для лечения: сахарного диабета, малокровия, лейкемии, рассеянного склероза, ревматоидных артритов, нейтропении, глюкозилцерамидного липидоза (болезнь Гоше).
Сегодня биофармацевтические субстанции можно получать с помощью клеток млекопитающих, микробных клеток, растительных клеток и мхов.
Производство лекарственных препаратов должно удовлетворять жестким требованиям надлежащей производственной практики (GMP), и фармацевтическое предприятие обязано соответствовать этим нормам на всех стадиях производства, вплоть до тех пор, пока лекарство не попадет в руки конечного пользователя. Существуют нормы оценки качества готовой продукции, требования к правильной упаковке, маркировке препаратов, условиям и срокам их хранения. На самом предприятии также действуют требования безопасности.
Целью курсовой работы является изучение информационных ресурсов, их организации на предприятии по биофармацевтике, в частности на производстве инсулина.
В связи с этим задачи данной курсовой работы можно сформулировать следующим образом:
1) Собрать обзор литературы по данной теме;
2) Рассмотреть историю открытия, строение и свойства инсулина, способы его производства;
3) Указать технологическую схему производства рекомбинантного инсулина;
4) Рассмотреть организацию информационных ресурсов на предприятии по указанному производству.
Актуальность использования для лечения сахарного диабета генно-инженерного инсулина состоит в том, что он имеет ряд преимуществ по сравнению с инсулином, производимым другими способами: идентичность гормону, вырабатываемому человеком, высокая чистота, высокая производительность способа.
История получения инсулина.
В 1920 году хирург Фредерик Бантинг, изучая обмен углеводов, выдвинул свою идею, которую сформулировал так: «Перевязать протоки поджелудочной железы у собак. Дождаться атрофии ацинусов, выделить секрет из островковых клеток, чтобы облегчить глюкозурию» [22].
В университете Торонто профессор Джон Маклеод, к которому он обратился, его идею воспринял без энтузиазма, однако выделил ему лабораторию. Ассистентом Бантинга стал Чарльз Бест. Эксперимент начался летом 1921 года.
Бантинг и Бест начали свои исследования с удаления поджелудочной железы у собак. У части животных они удаляли поджелудочную железу, у других перевязывали панкреатический проток и удаляли железу через некоторое время. Затем атрофированная поджелудочная железа помещалась в гипертонический раствор и замораживалась. Полученную в результате этого после разморозки субстанцию вводили собакам с удаленной поджелудочной железой и клиникой сахарного диабета. Исследователи зафиксировали снижение уровня глюкозы, улучшение самочувствия животного.
Новые результаты экспериментов с использованием поджелудочных желез крупного рогатого скота, позволили понять, что можно обойтись без сложной процедуры перевязки панкреатического протока.
В конце 1921 к команде исследователей присоединился Бертен Коллип, биохимик. С его помощью, используя фракционное осаждение с различными концентрациями спирта и другие методы очистки, были получены экстракты островков поджелудочной железы, которые могли быть безопасно введены в организме человека. Это эффективное и нетоксичное вещество и использовалось в первых клинических испытаниях [24].
В январе 1922 Бантинг и Бест начали клинические испытания инсулина на человеке. Сначала они испытали полученный инсулин на себе. В результате введения препарата оба почувствовали слабость, головокружение, но никаких токсических эффектов препарата отмечено не было.
Первым пациентом с диабетом, получившим инсулин 11 января 1922г. стал 14-летний мальчик Леонард Томпсон. После первой инъекции 15 мл инсулина никаких существенных изменений в состоянии пациента отмечено не было, незначительно снизился уровень глюкозы в крови и в моче, кроме того, у пациента развился стерильный абсцесс. Причиной этому стало то, что введенный инсулин был недостаточно очищенным. Следующие 11 дней Коллип упорно работал в лаборатории над улучшением экстракта, и 23 января мальчику была сделана вторая инъекция инсулина, после чего тот стал стремительно поправляться [23].
Известие о первом успешном применении инсулина 23 января 1922 г. стало международной сенсацией. Бантинг и его коллеги буквально воскрешали сотни больных диабетом. Ему писали множество писем с просьбами о спасении от болезни, приезжали к нему в лабораторию. Однако на тот момент существовало еще много недостатков – препарат инсулина был недостаточно стандартизован, средств самоконтроля не было и дозы инсулина приходилось отмерять грубо, на глазок. Поэтому нередко случались и гипогликемические реакции организма, когда уровень глюкозы падал ниже нормы.
Усовершенствование инсулина и его внедрение в повседневную врачебную практику продолжались. Университет Торонто начал продавать различным фармацевтическим компаниям лицензии на производство инсулина, и уже к 1923 г. этот гормон стал доступен всем больным сахарным диабетом.
Разрешение на производство лекарства получили компании «Лили» (США) и «Ново Нордиск» (Дания), которые и сейчас являются лидерами в этой области.
Бантингу в 1923 г. университет Торонто присвоил степень доктора наук, он был избран профессором. Также было открыто отделение медицинских специально исследований для Бантинга и Беста, которым назначили высокие персональные оклады.
В 1923 г. Бантингу и Маклеоду была присуждена Нобелевская премия по физиологии и медицине, которую они добровольно разделили с Бестом и Коллипом.
В 1926 г. ученому-медику Абелю удалось синтезировать инсулин в кристаллическом виде. Через 10 лет датский исследователь Хагедорн получил инсулин пролонгированного (продленного) действия, а еще через 10 лет был создан нейтральный протамин Хагердона, который до сих пор остается одним из самых популярных видов инсулина.
Химический состав инсулина установил британский молекулярный биолог Фредерик Сенгер, получивший в 1958 г. за это Нобелевскую премию. Инсулин стал первым белком, последовательность аминокислот которого была полностью расшифрована.
Пространственное строение молекулы инсулина было установлено с помощью метода рентгеновской дифракции в 1990-х гг. Дороти Кроуфт Ходжкин, которая тоже была удостоена Нобелевской премии.
После получения Бантингом бычьего инсулина проводились опыты с инсулином, полученным из поджелудочных желез свиней и коров, а также других животных (например, китов и рыб).
Молекула человеческого инсулина состоит из 51 аминокислоты. Свиной инсулин отличается от него только лишь одной аминокислотой, коровий – тремя, что не мешает им нормализовать уровень сахара достаточно хорошо. Однако у инсулина животного происхождения есть существенный недостаток – у значительной части больных он вызывает аллергическую реакцию. Поэтому были необходимы дальнейшие работы по усовершенствованию инсулина.
В 1955 г. была расшифрована структура человеческого инсулина, и начались интенсивные работы по его выделению. Впервые это удалось в 1981 г. американским ученым Жильберу и Ломедико. Несколько позже появился инсулин, полученный из пекарских дрожжей методом генной инженерии. Инсулин стал первым из человеческих белков, синтезированным в 1978 г. генетически модифицированной бактерией Е. coli. Именно с него в биотехнологии началась новая эпоха. С 1982 г. американская компания «Генентех» стала продавать человеческий инсулин, синтезированный в биореакторе. Этот инсулин не оказывает аллергизирующего действия на человеческий организм.
С 1987 года компания Novo Nordisk начала промышленное производство человеческого инсулина на основе генетически измененных дрожжевых клеток: наряду с получением уникальной чистоты конечного продукта, это лишало компанию зависимости от поставок поджелудочных желез животных, что обозначало возможность производить идеальный инсулин в неограниченном количестве [21].
Однако совершенства в производстве инсулина пока не достигнуто, он имеет свои побочные эффекты (например, возникновение липодистрофии в местах введения и др.), поэтому деятельность по улучшению или изменению качества синтезируемых инсулинов все еще продолжается.
Способы получения инсулина
Инсулин человека можно производить четырьмя способами:
1) экстракцией из поджелудочных желез человека;
2) полным химическим синтезом (оба этих способа не подходят из-за неэкономичности: недостатка сырья для массового производства первым способом и недостаточной разработанности второго способа);
3) полусинтетическим методом с помощью ферментно-химической замены в положении 30 В-цепи аминокислоты аланина в свином инсулине на треонин;
4) биосинтетическим способом по генно-инженерной технологии.
Два последних метода позволяют получить человеческий инсулин высокой степени очистки.
В настоящее время инсулин человека, в основном, получают двумя способами: модификацией свиного инсулина (синтетико-ферментативным методом) и генно-инженерным способом.
Инсулин оказался первым белком, полученным для коммерческих целей с использованием технологии рекомбинантной ДНК. Существует два основных подхода для получения генно-инженерного инсулина человека.
В первом случае осуществляют раздельное (разные штаммы-продуценты) получение обеих цепей с последующим фолдингом молекулы (образование дисульфидных мостиков) и разделением изоформ.
Во втором - получение в виде предшественника (проинсулина) с последующим ферментативным расщеплением трипсином и карбоксипептидазой В до активной формы гормона. Наиболее предпочтительным в настоящее время является получение инсулина в виде проинсулина, обеспечивающее правильность замыкания дисульфидных мостиков (в случае раздельного получения цепей проводят последовательные циклы денатурации, разделения изоформ и ренатурации).
При обоих подходах возможно как индивидуальное получение исходных компонентов, так и в составе гибридных белков. Помимо А- и В-цепи или проинсулина, в составе гибридных белков могут присутствовать:
- белок носитель, который обеспечивает транспортировку гибридного белка в периплазматическое пространство клетки или культуральную среду;
- аффинный компонент, существенно облегчающий выделение гибридного белка.
Оба компонента могут одновременно присутствовать в составе гибридного белка. Кроме этого, при создании гибридных белков может использоваться принцип мультимерности, позволяющий существенно повысить выход целевого продукта. Это означает, что в гибридном белке существует несколько копий целевого полипептида [2].
В Великобритании с помощью E.coli синтезированы обе цепи человеческого инсулина, которые затем были соединены в молекулу биологически активного гормона. Для синтеза одноклеточным организмом на его рибосомах молекулы инсулина, необходимо ввести микроорганизму ген гормона и тем самым снабдить его нужной программой.
Химическим способом получают ген, который программирует биосинтез предшественника инсулина или два гена, программирующие в отдельности биосинтез цепей А и В инсулина.
Следующий этап – включение гена предшественника инсулина (или гены цепей порознь) в геном E.coli. Это задача генной инженерии.
Из E.coli вычленяют плазмиду соответствующей рестриктазой, синтетический ген встраивается в плазмиду (клонированием с функционально активной С-концевой частью β-галактозидазы E.coli). В результате E.coli приобретает способность синтезировать белковую цепь, состоящую из галактозидазы и инсулина. Синтезированные полипептиды отщепляют от фермента химическим путем, затем проводят их очистку. В бактериях синезируется около 100000 молекул инсулина на одну бактериальную клетку.
Природа гормонального вещества, продуцируемого E.coli, обусловлена тем, какой ген встраивается в геном одноклеточного организма. Если клонирован ген предшественника инсулина, бактерия синтезирует предшественник инсулина, который подвергается затем обработке рестриктазами.
Для получения очищенного инсулина человека выделенный из биомассы гибридный белок подвергают химико-ферментативной трансформации и соответствующей хроматографической очистке (фронтальной, гельпроникающей, анионообменной) [16].
Различия в строении проинсулина и инсулина представлены на рисунке в приложении 2.
В Институте РАН получен рекомбинантный инсулин с использованием генно-инженерных штаммов E.coli. Из выращенной биомассы выделяется предшественник, гибридный белок, экспрессируемый в количестве 40% от всего клеточного белка, содержащий препроинсулин. Превращение его в инсулин in vitro осуществляется в той же последовательности, что и in vivо – отщепляется лидирующий полипептид, препроинсулин превращается в инсулин через стадии окислительного сульфитолиза с последующим восстановительным замыканием трех дисульфидных связей и ферментативным вычленением связывающего С-пептида. После ряда хроматографических очисток, включающих ионообменные, гелевые и ВЭЖХ, получают человеческий инсулин высокой чистоты и природной активности [8].
Можно использовать штамм со встроенной в плазмиду нуклеотидной последовательностью, экспрессирующей гибридный белок, который состоит из линейного проинсулина и присоединенного к его N-концу через остаток метионина фрагмента белка А Staphylococcus aureus.
Культивирование насыщенной биомассы клеток рекомбинантного штамма обеспечивает начало производства гибридного белка, выделение и последовательная трансформация которого in tube приводят к инсулину.
Возможен и другой путь: получается в бактериальной системе экспрессии слитой рекомбинантный белок, состоящий из проинсулина человека и присоединенного к нему через остаток метионина полигистидинового "хвоста". Его выделяют, используя хелатную хроматографию на колонках с Ni-агарозой, из телец включения и расщепляют бромцианом.
Выделенный белок является S-сульфонированным. Картирование и масс-спектрометрический анализ полученного проинсулина, очищенного ионнообменной хроматографией на анионите и ОФ (обращеннофазовой) ВЭЖХ (высокоэффективной жидкостной хроматографией), показывают наличие дисульфидных мостиков, соответствующих дисульфидным мостикам нативного проинсулина человека.
В последнее время пристальное внимание уделяется упрощению процедуры получения рекомбинантного инсулина методами генной инженерии. Так, например, можно получить слитой белок, состоящий из лидерного пептида интерлейкина 2 присоединенного к N-концу проинсулина, через остаток лизина. Белок эффективно экспрессируется и локализуется в тельцах включения. После выделения белок расщепляется трипсином с получением инсулина и С-пептида.
Полученные инсулин и С-пептид очищались ОФ ВЭЖХ. При создании слитых конструкций весьма существенным является соотношение масс белка носителя и целевого полипептида. С-пептиды соединяются по принципу "голова-хвост" с помощью аминокислотных спейсеров, несущих сайт рестрикции Sfi I и два остатка аргинина в начале и в конце спейсера для последующего расщепления белка трипсином. ВЭЖХ продуктов расщепления показывает, что отщепление С-пептида проходит количественно, а это позволяет использовать способ мультимерных синтетических генов для получения целевых полипептидов в промышленном масштабе [20].
Сухая биомасса инсулина
Описание. Растворы инсулина представляют собой прозрачную бесцветную или слегка желтоватую жидкость кислой реакции (pH 2,0–3,5), которые готовят разведением кристаллического инсулина в воде, подкисленной соляной кислотой с добавлением глицерина и 0,25–0,30% раствора фенола или трикрезола для консервирования.
Фармакологическое действие: Взаимодействует со специфическим рецептором внешней мембраны клеток и образует инсулин-рецепторный комплекс. Через активацию биосинтеза цАМФ в жировых клетках и клетках печени или непосредственно проникая в мышечные клетки, инсулин-рецепторный комплекс стимулирует внутриклеточные процессы, в том числе синтез ряда ключевых ферментов (гексокиназы, пируваткиназы, гликогенсинтетазы и др.). Снижение содержания глюкозы в крови обусловлено повышением ее внутриклеточного транспорта, усилением поглощения и усвоения тканями, стимуляцией липогенеза, гликогеногенеза, синтеза белка, снижением скорости продукции глюкозы печенью и др. Продолжительность действия препаратов инсулина в основном обусловлена скоростью всасывания, которая в свою очередь зависит от нескольких факторов (от дозы, способа и места введения). После п/к начало эффекта - через 0.5 ч, максимальный эффект - через 1-3 ч, продолжительность действия - 8 ч.
Показания: Сахарный диабет типа 1 (инсулинзависимый). Сахарный диабет типа 2 (инсулиннезависимый): стадия резистентности к пероральным гипогликемическим средствам, частичная резистентность к этим препаратам (при проведении комбинированной терапии), интеркуррентные заболевания, беременность.
Противопоказания: Гиперчувствительность, гипогликемия.
Побочные действия: В начале терапии - нарушение зрения, отеки конечностей. При введении слишком большой дозы инсулина или нарушении режима питания (пропуск приема пищи), а также при чрезмерной физической нагрузке - гипогликемия ("холодный" пот, бледность кожных покровов, нервозность, тремор, беспокойство, чрезмерная утомляемость или слабость, нарушение ориентации, головокружение, головная боль, выраженное чувство голода, временное нарушение зрения, тошнота, тахикардия, в тяжелых случаях - потеря сознания, кома). Системные аллергические реакции: повышенное потоотделение, рвота, затруднение дыхания, сердцебиение, головокружение [18].
Срок хранения - 1 год со дня изготовления.
ВР 1. Подготовка воды
Мембранные дистилляторы предназначены для получения обессоленной воды, соответствующей требованиям ГОСТ 6709-97 "Вода дистиллированная". Производительность дистилляторов - от 3 до 15 л/час (лабораторные установки в экономичной комплектации), а также от 5-30 л/ч (лабораторные установки). Процесс фильтрации включает в себя следующие стадии: предварительную очистку на активированном угле, мембранную фильтрацию и деионизацию воды с помощью ионообменных смол. Фильтр предварительной очистки удаляет из поступающей водопроводной воды взвешенные частицы, хлор, высокомолекулярную органику и ионы тяжелых металлов. Мембранная фильтрация основана на явлении обратного осмоса, при котором вода, проходя через полупроницаемую мембрану, очищается от растворенных в ней солей, низкомолекулярных органических примесей, а также бактерий и микроорганизмов. На фильтре с ионообменными смолами происходит полная доочистка фильтрата от растворенных солей [18].
ВР 3. Синтез цепей А и В.
Синтез цепей проводят химическим методом. Цепь А содержит 21 аминокислотный остаток, цепь В - 30 остатков
ТП 6. Подготовка питательной среды
Основной питательной средой для культивирования культуры E.coli является бульон по Миллеру. Состав: гидролизат казеина, дрожжевой экстракт, натрия хлорид, агар-агар. Конечное значение рН (при 25°С) 7,0±0,2.Так же используется бульон Хоттингера. Состав: гидролизат Хоттингера, натрия хлорид, вода дистиллированная.
Стерилизацию питательной среды проводят в автомате для непрерывной стерилизации – УНС. Питательная среда последовательно проходит секцию нагревания, секцию выдерживания и секцию охлаждения [18].
ТП 9. Очистка
Очистку инсулина проводят методами хроматографии: фронтальной, гельпроникающей, анионообменной. При очистке инсулина и его производных на сорбентах с сильными катионообменными свойствами (например, SP-Sepharose FF) можно использовать буферные системы на основе ацетата аммония с низким содержанием мочевины.
ТП 11. Сушка
Сушка продукта проводится в сублимационной сушилке.
Раздел VII. Методы анализа
Активность инсулина измеряется в единицах действия (ЕД) или в международных единицах действия (МЕ - русск. или IU – англ.). 1 единица соответствует активности 1/24 мг (41,66 мкг) кристаллического инсулина. Этот действующий в настоящее время стандарт появился в 1958 году. ВОЗ в 1982 году внесла последние корректировки в стандарт, которые не затронули определение единицы, а касались изменений, связанных с появлением человеческих генно-инженерных инсулинов.
ЗАКЛЮЧЕНИЕ
Итак, в данной работе подробно рассмотрено производство биофармацевтического предприятия на примере предприятия по производству генно-инженерного инсулина. Также можно сделать вывод о преимуществах генно-инженерного инсулина и его производства по сравнению с другими видами инсулина и со способами их производства.
В ходе выполнения работы решены поставленные задачи, а именно собран литературный обзор по данной теме; описаны способы производства инсулина, история его открытия, строение и свойства; дана технологическая схема производства генно-инженерного инсулина; а также приведены нормативно-правовые акты, которые действуют на предприятиях по производству инсулина, рассмотрена организация информационных ресурсов на предприятии.
Выполнена главная цель данной работы – изучение организации информационных ресурсов на предприятии по биофармацевтическому производству, а именно по производству рекомбинантного инсулина.
Были изучены основные нормативно-правовые документы и стандарты, которые регулируют производство рекомбинантного инсулина:
· Письмо Департамента государственного контроля качества, эффективности, безопасности лекарственных средств и медтехники Минздрава РФ от 26.07.1999 N 293-22/47 (с изм. от 19.08.1999) "Разъяснения о порядке контроля качества и сертификации препаратов инсулина".
· Решение Совета Евразийской Экономической Комиссии от 3 ноября 2016 года N 89 "Об утверждении правил проведения исследований биологических лекарственных средств Евразийского экономического союза".
· ГОСТ 6709-97 "Вода дистиллированная".
· ГОСТ ISO 8537 – 2011 " Шприцы инъекционные однократного применения стерильные с иглой или без иглы для инсулина".
· ГОСТ 12.1.033-81 "Система стандартов безопасности труда (ССБТ). Пожарная безопасность. Термины и определения (с Изменением N 1)".
СПИСОК ЛИТЕРАТУРЫ
1. Ефимов, А.С., Скробонская Н.А. Клиническая диабетология.-- К.: Здоровья, 1998. – 320 с.
2. Основы фармацевтической биотехнологии: Учебное пособие / Т.П. Прищеп, В.С. Чучалин, К.Л. Зайков, Л.К. Михалева. – Ростов-на-Дону.: Феникс; Томск: Издательство НТЛ, 2006. – 308 с.
3. Покрышкин, В.И., Тихонова, Ю.В. Препараты моноинсулина в лечении сахарного диабета//Новые лекарственные препараты. - 1984. – 248 с.
4. ГОСТ 6709-72 Вода дистиллированная. Технические условия (с Изменениями N 1, 2). – Введ. 1974-01-01. – М.: ФГУП "СТАНДАРТИНФОРМ", 2010. – 17 с.
5. ГОСТ ISO 8537-2011 Шприцы инъекционные однократного применения стерильные с иглой или без иглы для инсулина. Технические требования и методы испытаний. – Введ. 2013-01-01. – М.: Стандартинформ, 2013. – 21 с.
6. ГОСТ 12.1.033-81 Система стандартов безопасности труда (ССБТ). Пожарная безопасность. Термины и определения (с Изменением N 1). Введ. 1982-07-01. – М.: ИПК Издательство стандартов, 2001. 6 с.
7. Анатомия инсулина человека [Электронный ресурс] / EuroLab – Медицинский портал. – Режим доступа: http://www.eurolab.ua/anatomy/265. – (дата обращения 29.03.2017 г.).
8. Гулина, Е.И. Генно-инженерный инсулин в России [Электронный ресурс] / Е.И. Гулина, Т.Г. Маркова // Международный студенческий научный вестник – науч. журн. – 2012. – Режим доступа: http://www.scienceforum.ru/2016/pdf/23406.pdf. – (дата обращения: 28.03.2017).
9. Гусаров, Д.А. Вирусная безопасность биофармацевтических препаратов [Электронный ресурс] / Д.А. Гусаров// Разработка и регистрация лекарственных средств: научно-производственный журнал – 2016.— № 14. – Режим доступа: http://pharmjournal.ru/. – (дата обращения: 05.04.2017 г.).
10. Диабет I типа. Инсулин и его инъекции [Электронный ресурс] / Библиотека обучающей и информационной литературы. razlib.ru. – Режим доступа: http://www.razlib.ru/medicina/pervaja_pomosh_diabetiku/p4.php. – (дата обращения: 06.04.2017 г.).
11. Инсулинов упаковка и хранение [Электронный ресурс] / Портал о диабете. Диабетунет.ру. – Режим доступа: http://www.diabetunet.ru/insulin/insulinov-upakovka-i-khranenie. – (дата обращения: 29.03.2017 г.).
12. Компания "Форт" [Электронный ресурс]. – Режим доступа: http://fort-bt.ru/. – (дата обращения: 28.03.20017 г.).
13. Контроль качества инсулина с помощью оборудования Agilent [Электронный ресурс] / МИЛЛАБ. Оборудование для лабораторий и наукоемких технологий. – Режим доступа: http://www.millab.ru/about/news/production_news/view/213-otkrytie-insulina/. – (дата обращения: 15.04.2017 г.).
14. Об утверждении правил проведения исследований биологических лекарственных средств Евразийского экономического союза [Электронный ресурс]: решение Совета Евразийской Экономической Комиссии от 3 ноября 2016 года N 89. – Режим доступа: http://docs.cntd.ru/document/456026116. – (дата обращения: 30.04.2017 г.).
15. Понятие "доза инсулина" при ИЗСД [Электронный ресурс] / Saydiabetu.net. – Режим доступа: http://saydiabetu.net/lechenie/tradicionnaya-medicina/insulin/doza-insulina/. – (дата обращения: 2.04.2017 г.).
16. Препараты поджелудочной железы. Изготовление инсулина в фармации [Электронный ресурс] / MEDICALPLANET. – Режим доступа: http://medicalplanet.su/farmacia/328.html. – (дата обращения: 29.03.2017 г.).
17. Производство инсулина [Электронный ресурс] / Сахарный диабет. Инфопортал. – Режим доступа: http://www.saharniy-diabet.com/insulin/tehnologiya-proizvodstva/iz-chego-delayut-svinoy-genno-inzhenernyy-rekombinantnyy. – (дата обращения: 2.04.2017 г.)
18. Регламент на производство инсулина генно-модифицированным методом – изложение [Электронный ресурс] / works.doklad.ru – Учебные материалы. – Режим доступа: http://works.doklad.ru/view/OYDuqLLPNpM.html. – (дата обращения: 26.03.2017 г.).
19. Строение инсулина [Электронный ресурс] / Студопедия. – Режим доступа: http://studopedia.ru/3_135516_stroenie-insulina.html. (дата обращения: 2.04.2017 г.).
20. Типы инсулина и методы его получения [Электронный ресурс] / KazEdu. – Режим доступа: https://www.kazedu.kz/referat/115453. – (дата обращения: 28.03.2017 г.).
21. Яушева, Е.В. История создания инсулина. Взгляд в прошлое [Электронный ресурс] / Е.В. Яушева // Актуальная эндокринология – рецензируемы интернет-журнал – 21.12.2015. – Режим доступа: http://actendocrinology.ru/archives/3787. – (дата обращения: 05.04.2017 г.).
22. Banting Notebook: 1920-21. Fisher Rare Book Library, University of Toronto, Toronto, Canada
23. Rosenfeld L. Insulin: discovery and controversy. Clin. Chem. 2002;48(12): 2270-88. Available at http://www.ncbi.nlm.nih.gov/pubmed/12446492
24. Stylianou C, Kelnar C. The introduction of successful treatment of diabetes mellitus with insulin. J. R. Soc. Med. 2009;102(7): 409 p.
ПРИЛОЖЕНИЕ
Приложение 1. Полный цикл производства препаратов компании "Форт" 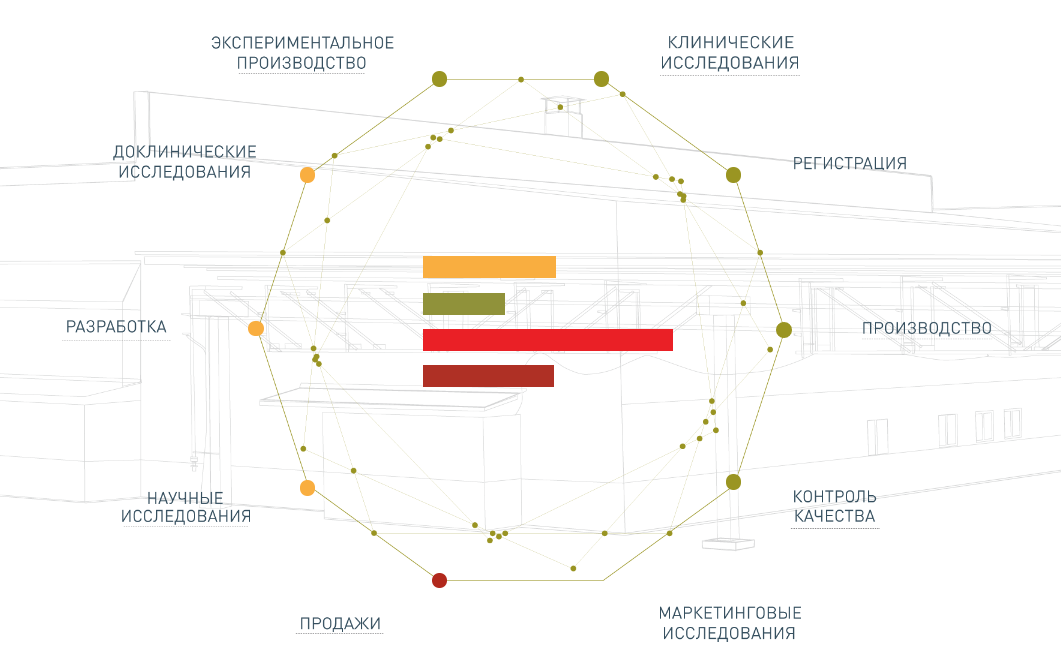
Приложение 2. Сравнение строения проинсулина и инсулина.


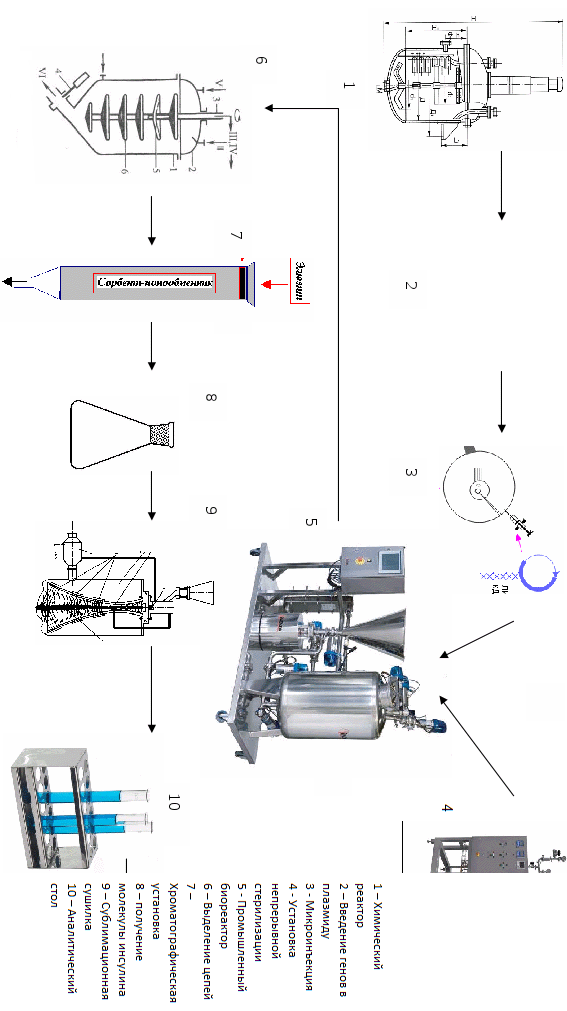
Приложение 3. Аппаратурная схема производства и спецификация оборудования
Приложение 4. Патент РФ № 2 495 131 "Способ получения рекомбинантного инсулина гларгина".

Приложение 5. Патент РФ № 2 447 149 " Рекомбинантная плазмидная ДНК pmsin4, кодирующая гибридный полипептид - предшественник инсулина человека, штамм BL21(DE3)/pmsin4 - продуцент рекомбинантного инсулина человека, способ получения рекомбинантного инсулина человека".

Приложение 6. Патент РФ 2 500 420 " Фармацевтическая композиция с быстрым действием инсулина". 
Приложение 7 Патент РФ № 2 407 540 " Способ промышленного получения рекомбинантного инсулина человека".

Приложение 8. Патент РФ № 2 506 945 "Лекарственные формы инсулина, обладающие быстрым усвоением".

Приложение 9. Патент РФ № 2 354 702 "Рекомбинантная плазмидная ДНК phins11, кодирующая гибридный белок-предшественник инсулина человека, клетка Escherichia coli, трансформированная рекомбинантной плазмидной ДНК pHINS11, штамм бактерий Escherichia coli JM109/pHINS11 - продуцент гибридного белка-предшественника инсулина человека и способ получения инсулина человека".

МИНИСТЕРСТВО СЕЛЬСКОГО ХОЗЯЙСТВА РОССИЙСКОЙ ФЕДЕРАЦИИ
ФГОУ ВО «ОРЛОВСКИЙ ГОСУДАРСТВЕННЫЙ АГРАРНЫЙ УНИВЕРСИТЕТ ИМЕНИ Н.В. ПАРАХИНА»
ФАКУЛЬТЕТ «БИОТЕХНОЛОГИИ И ВЕТЕРИНАРНОЙ МЕДИЦИНЫ»
КАФЕДРА БИОТЕХНОЛОГИИ
Допустить к защите
«____» _________________ 2017 г.
_________________/ Солохина И.Ю./
КУРСОВОЙ ПРОЕКТ
по дисциплине «Управление информационными ресурсами на биотехнологических предприятиях»
по теме: «Организация информационный системы и основных ресурсов на предприятии по биофармацевтике»
Автор проекта _________ Буряк Д.А. группа 251
Направление подготовки: 19.03.01- Биотехнология
Курсовой проект защищен с оценкой _____________
Руководитель курсового проекта________к.б.н., доцент Солохина И.Ю.
Члены комиссии ________________
________________
________________
Регистрация: «____» __________2017 г.
Лаборант_______________________
Орел-2017
МИНИСТЕРСТВО СЕЛЬСКОГО ХОЗЯЙСТВА РОССИЙСКОЙ
ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ
ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ
«ОРЛОВСКИЙ ГОСУДАРСТВЕННЫЙ АГРАРНЫЙ УНИВЕРСИТЕТ
ИМЕНИ Н.В.ПАРАХИНА»
ФАКУЛЬТЕТ БИОТЕХНОЛОГИИ И ВЕТЕРИНАРНОЙ МЕДИЦИНЫ
КАФЕРДРА БИОТЕХНОЛОГИИ
ЗАДАНИЕ НА КУРСОВОЙ ПРОЕКТ
Студент(ка) Буряк Д.А. Шифр________Группа 2 курс Био (о.о)
Направление подготовки 19.03.01- Биотехнология
Тема: «Организация информационных ресурсов на предприятии по биофармацевтике»
Срок сдачи студентом законченной работы: «__» ____________2017 год
Исходные данные для выполнения курсового проекта: провести анализ основных литературных источников, патентов, ГОСТов, методик по теме исследования, рассмотреть биотехнологическую схему и техническую схему производства генно-инженерного инсулина, провести исследование организации основных информационных ресурсов и документации на предприятии по производству генно-инженерного инсулина.
Руководитель курсового проекта
к.б.н., доцент Солохина И.Ю.
Задание принял к исполнению «__» ___________2017 года
Подпись студента ______________________
Орел-2017 год
СОДЕРЖАНИЕ
ВВЕДЕНИЕ.. 4
ГЛАВА 1. ЛИТЕРАТУРНЫЙ ОБЗОР. 6
1.1. Описание биофармацевтического предприятия на примере компании "Форт". 6
1.2. Актуальность производства и применения рекомбинантного инсулина. 8
1.3. История получения инсулина. 8
1.4 Строение и механизм действия инсулина. 12
ГЛАВА 2. ТЕХНОЛОГИЧЕСКАЯ ЧАСТЬ.. 15
2.1. Способы получения инсулина. 15
2.2. Технологическая схема производства рекомбинантного инсулина. 19
ГЛАВА 3. ОРГАНИЗАЦИЯ ОСНОВНЫХ ИНФОРМАЦИОННЫХ РЕСУРСОВ И ДОКУМЕНТАЦ














