Цель работы: практическое применение знаний об аккумуляторной батареи.
Задача работы: Изучить основные параметры аккумуляторной батареи
Теоретические сведения и методические указания
Тип и конструкция аккумуляторной батареи определяются условиями ее разряда. При пуске двигателя стартерные токи достигают нескольких сотен ампер. Такой ток может дать только батарея специальной конструкции. Батареи, предназначенные для пуска двигателя стартером, называются стартерными аккумуляторными батареями.
Стартерный аккумулятор представляет собой химический источник тока. В нем происходит непосредственное преобразование химической энергии в электрическую. Причем, в отличие от гальванических батарей, он является вторичным химическим источником тока, т.е. допускающим многоразовое использование. После разряда производится повторный заряд путем пропускания через аккумулятор тока внешней зарядной цепи.
При этом из продуктов реакции разряженного аккумулятора регенерируются исходные активные материалы.
К стартерным аккумуляторным батареям предъявляются следующие требования: максимальное рабочее напряжение; минимальное внутреннее сопротивление; малое изменение напряжения в процессе разряда; быстрый заряд; максимальное количество энергии, приходящееся на единицу массы; малые габариты и масса; большая механическая прочность и малая стоимость. Наиболее полно перечисленным требованиям отвечают свинцово-кислотные аккумуляторы, принцип действия которых заключается в следующем. Свинцово-кислотный аккумулятор строится на основе определенной электрохимической системы. В нее входит окислитель, восстановитель и электролит. Восстановитель в процессе рабочей реакции (называемой токообразующей) отдает ионы и окисляется (отрицательный электрод), а окислитель восстанавливается (положительный электрод).
В свинцово-кислотных аккумуляторах восстановителем служит губчатый свинец (Pb), а окислителем – двуокись свинца (PbO2). Электролит ‑ водный раствор серной кислоты (H2SO4) с плотностью от 1,2 до 1,4 г/см3.
Различают три этапа работы аккумулятора: 1) первая после изготовления заливка электролитом; 2) разряд; 3) заряд. При первой заливке электролита в аккумулятор со свинцового электрода начнут отщепляться в раствор положительные ионы свинца, при этом сам электрод будет заряжаться отрицательно, а электролит – положительно (рис.1.1). Примерно через 20 минут после окончания заливки этот процесс прекратится за счет противодействующих электрохимических реакций. Одновременно электролит омывает и положительный электрод (окислитель) аккумулятора. При этом некоторое количество двуокиси свинца переходит в раствор, где при соединении с водой ионизируется на четырехвалентные ионы Pb+4 и одновалентные ионы ОН-. Четырехвалентные ионы свинца Pb+4 осаждаются на окислителе (положительном электроде PbO2) заряжая его положительно относительно раствора электролита.
Поэтому в этой схеме можно выделить два источника ЭДС: источник Е1 – отрицательный электрод – электролит; источник Е2 – электролит ‑ положительный электрод. Источники Е1 и Е2 соединены последовательно.
Их сумма достигает номинального напряжения аккумулятора – 2,154 В. Поэтому батарея, состоящая из таких аккумуляторов называется сухозаряженной, т.е. через 20 минут после заливки электролита она может использоваться для стартерного пуска. Если после заливки произвести заряд батареи, то суммарное напряжение Е1 + Е2 каждого аккумулятора повысится до 2,4 В. Если заряд продолжать более 2 часов, то зарядный ток начнет использоваться на электролиз воды, плотность электролита быстро возрастает, электроды аккумуляторов разрушатся и батарея выйдет из строя. Этот процесс имеет место и при чрезмерно длительной зарядке батареи, бывшей в эксплуатации.
Факт электролиза воды можно определить визуально по бурному выделению пузырьков газа из электролита (аккумулятор «кипит»). Поэтому при выполнении лабораторной работы необходимо следить за интенсивностью выделения пузырьков газа через заливные горловины аккумуляторов, соблюдая при этом необходимые меры безопасности.
Второй этап работы аккумулятора – разряд. Для этого замыкается ключ К2 (рис.1.1) и к электродам подключается сопротивление разряда(нагрузки) Rразр.. Химические процессы идут в обратном направлении.
Плотность электролита уменьшается за счет образования воды. Поэтому измерение плотности электролита (концентрации H2SO4) служит удобным и точным средством определения степени заряженности аккумулятора.
При зарядке аккумулятора к электродам подключается внешний источник ЭДС Езар в согласной полярности (замыкается ключ К1) и химические процессы, определяемые уравнением записанным выше, идут в обратном направлении.
Устройство стартерных аккумуляторных батарей удобно изучать по наглядным пособиям, в достаточном количестве имеющимся на кафедре.
Батареи маркируются цифровыми и буквенными символами, нанесенными на корпус, например: 6СТ55ТРАЗ. Эта надпись означает: 6 ‑ число аккумуляторов в батарее; СТ – стартерная; 55 – номинальная емкость С20 батареи в ампер-часах; Т – материал моноблока, термопласт; Р – материал сепаратора, мипор; З – батарея залита электролитом и заряжена на заводе-изготовителе; А – батарея с общей крышкой.
Однако нанесение символов, определяющих материал моноблока и сепаратора, не является обязательным.
На корпусе батареи должна быть нанесена дополнительная маркировка, содержащая: товарный знак предприятия-изготовителя; знаки полярности выводов; дату изготовления; номинальное напряжение; максимальный разрядный ток стартерного пуска при температуре минус 18°С. Такой ток должна отводить стартеру батарея при окружающей температуре минус 18°С в течение 30 с. Последнюю маркировку наносят на батарею в случае, если этот ток больше 3 С20.
Основные параметры аккумуляторной батареи
1. ЭДС батареи. ЭДС свинцово-кислотного аккумулятора, как любого другого химического источника тока, зависит только от химических и физических свойств веществ, участвующих в электрохимических процессах, и совершенно не зависит от размеров электродов и количества активных материалов. ЭДС аккумулятора и батареи определяется вольтметром с большим внутренним сопротивлением (1 кОм и более) по формуле
ЕБ = Е · n, (1.1)
где Е – ЭДС одного аккумулятора; n – число аккумуляторов в батарее.
ЭДС аккумулятора может быть определена также по эмпирической формуле
Е = 0,84 + ρ25, (1.2)
где ρ25 – плотность электролита, измеренная денсиметром при температуре + 25°С.
Однако на практике можно считать, что ЭДС почти не зависит от температуры, т.к. при изменении температуры на 100°С она изменяется только на 0,06 В.
2. Внутреннее сопротивление. Внутреннее сопротивление аккумулятора складывается из четырех составляющих:
Rвн = Rэл + Rс + Rм + Rn, (1.3)
где Rэл – сопротивление электролита; Rс – сопротивление сепараторов; Rм – сопротивление активной массы; Rn – сопротивление решеток и соединительных элементов.
Поскольку при разряде аккумулятора губчатый свинец и двуокись свинца превращаются в сульфат свинца с высоким сопротивлением, а плотность электролита уменьшается до 1,1 г/см3 и ниже, то внутреннее сопротивление аккумулятора по мере его разряда увеличивается. Внутреннее сопротивление разряженного аккумулятора в два раза выше, чем заряженного.
Все составляющие внутреннего сопротивления зависят от температуры, однако наиболее сильно изменяется Rэл. При температуре -20 °С Rэл в четыре раза больше чем при плюс 30 °С. Этот факт является одной из причин затрудненного пуска двигателя при низкой температуре.
3. Емкость аккумулятора. Емкостью аккумулятора называется максимальное количество электричества, которое аккумулятор может сообщить во внешнюю цепь при полном разряде от начального напряжения Uнач = 2,154 В до конечного Uкон= 1,750 В за время tρ:
 (1.4)
(1.4)
где Сρ – емкость аккумулятора; Q – количество электричества; Jρ(t) – ток разряда; tp – время разряда.
Обычно разряд аккумулятора происходит при постоянном токе разряда Jρ, тогда
Cρ = Jρ · tρ. (1.5)
Емкость аккумулятора измеряется в амперчасах (А·ч). Один амперчас равен 3600К электрического заряда. На практике емкость аккумулятора определяют параметром С20. Это число, умножив которое на коэффициент 0,05, получим ток разряда, который аккумулятор должен отдавать во внешнюю цепь в течение 20 часов (tρ=20 ч) до полного разряда (Е=10,750 В).
Емкость аккумуляторной батареи существенно снижается с увеличением силы разрядного тока. Использование активных веществ (Pb, PbO2) при большей силе разрядного тока составляет 5…10%. Снижение емкости при этом связано в основном с резким уменьшением концентрации серной кислоты в порах пластин из-за большого количества сульфата свинца, который оседает на поверхности пластин и изолирует активную массу от контакта с электролитом.
При разряде, например, батареи 6СТ-75 номинальным током 3,75 А при температуре 25 °С емкость составляет 75 А·ч, а при разряде током 250 А емкость резко падает и составляет всего 25 А·ч.
4. Энергозапас. Энергозапасом Wρ аккумулятора называется максимальное количество энергии, которое он может отдать во внешнюю цепь за время полного разряда tρ:
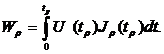 (1.6)
(1.6)
При постоянном разрядном токе Jρ это выражение можно представить в виде
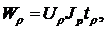 (1.7)
(1.7)
где Uρ ‑ среднее напряжение аккумулятора за время tρ.
Содержание работы
1. Изучить конструкцию аккумуляторной батареи (АБ) и ее маркировку.
2. Выполнить необходимые измерения и сделать заключение о техническом состоянии АБ.
3. Ознакомиться с имеющимся в лаборатории зарядным оборудованием, правилами его эксплуатации и характеристиками.
4. Установить режим и подсоединить АБ для зарядки. Произвести частичную подзарядку батареи.
Порядок выполнения работы
1. Ознакомьтесь с правилами техники безопасности.
2. Изучите по наглядным пособиям (при самостоятельной подготовке): конструкции АБ и их материалы; маркировку автомобильных АБ; характерные эксплуатационные неисправности батарей.
3. Заготовьте журнал по приведенной ниже форме (при подготовке).
4. Ознакомьтесь с необходимыми для работы приборами (при подготовке).
5. Произведите внешний осмотр АБ и запишите результаты в журнал. При визуальном осмотре необходимо обращать внимание на дату выпуска АБ, на целостность выводов и перемычек, наличие трещин, целостность мастики, чистоту поверхности батареи.
6. Измерьте уровень и плотность электролита в аккумуляторах батареи, для чего необходимо: вывернуть пробки из заливочных отверстий аккумуляторов; проверить уровень электролита с помощью мерной стеклянной трубки (уровень должен быть на 10‑15 мм выше защитной сетки аккумулятора); измерить плотность (удельный вес) электролита ареометром, температуру электролита и определить температурную поправку; завернуть пробки аккумуляторов; данные измерений внести в табл.1.1 журнала.
7. Вычислите степень заряженности аккумуляторов по плотности электролита (самостоятельно, вне лаборатории, при обработке) и внесите в табл.1.1.
8. Вычислите ЭДС покоя аккумуляторов по плотности электролита (самостоятельно, вне лаборатории, при обработке) и внесите в табл.1.1.

Рис.1.1. Схема испытаний АБ
9. Соберите схему (рис.1.1). Произведите необходимые измерения и определите внутреннее сопротивление АБ. Вычислите значение нормального внутреннего сопротивления батареи и сравните с ним значение измеренного внутреннего сопротивления батареи. Данные внесите в табл.1.1.
10. Испытайте аккумуляторы нагрузочной вилкой. Данные внесите в табл.1.1.
11. Снимите вольт-амперную характеристику АБ по схеме (рис.1.1). Разберите схему. Данные измерений внесите в табл.1.2.
12. Сделайте заключение о техническом состоянии аккумуляторов и батареи в целом по результатам испытаний.
13. Оформите отчет по работе. Отчет должен содержать: название и цель работы, краткие сведения из теории, необходимые схемы, графики и таблицы, результаты работы, выводы.
ЖУРНАЛ
регистрации данных испытаний
Тип (марка) АБ
Дата изготовления батареи
Таблица 1.1
| №
пп
| Показатели
| Номер аккумулятора
1 2 3 4 5 6
| Среднее или суммарное значение показателя
|
| 1
| 2
| 3
| 4
| 5
| 6
| 7
| 8
| 9
|
| 1.
| Уровень электролита, мм
|
|
|
|
|
|
|
|
| 2.
| Плотность электролита, измеренная ареометром, кг/м3
|
|
|
|
|
|
|
|
| 3.
| Температура электролита, °С
|
|
|
|
|
|
|
|
| 4.
| Температурная поправка
|
|
|
|
|
|
|
|
| 5.
| Плотность электролита, приведенная к 25°С, г/см3
|
|
|
|
|
|
|
|
| 6.
| Плотность электролита после последней зарядки (узнать у преподавателя или лаборанта), г/см3
|
|
|
|
|
|
|
|
| 7.
| Степень разряженности аккумуляторов, %
|
|
|
|
|
|
|
|
| 8.
| ЭДС аккумуляторов, вычисленная по плотности, В
|
|
|
|
|
|
|
|
| 9.
| ЭДС аккумуляторов, измеренная вольтметром, В
|
|
|
|
|
|
|
|
| 10.
| Напряжение аккумуляторов, измеренное при разряде Uб, В
|
|
|
|
|
|
|
|
| 11.
| Ток разряда, Jраз, А
|
|
|
|
|
|
|
|
| 12.
| Внутреннее сопротивление аккумуляторов - измеренное, Ом
|
|
|
|
|
|
|
|
| 13.
| Внутреннее сопротивление аккумуляторов - нормальное, Ом
|
|
|
|
|
|
|
|
| 14.
| Напряжение аккумуляторов, измеренное нагрузочной вилкой, В (дробь: числитель – в начале измерения, знаменитель – через 5 с)
|
|
|
|
|
|
|
|
Таблица 1.2
| Параметры
| Замер
|
| 1
| 2
| 3
| 4
| 5
| 6
|
| 1
| 2
| 3
| 4
| 5
| 6
| 7
|
| Разрядный ток
|
|
|
|
|
|
|
| Напряжение
|
|
|
|
|
|
|
| Ток замыкания
|
|
|
|
|
|
|
Методика выполнения испытаний
При измерении плотности электролита необходимо:
- следить, чтобы ареометр не прилипал к стенке кислотно-мерной колбы;
- отсчеты делать по средней части мениска с точностью 0,5 деления шкалы ареометра (примечание: возможно применение поплавкового плотномера с дискретностью отсчета 0,02 г/см3);
- скорректировать показания ареометра в соответствии с температурой электролита. Температура электролита принимается равной температуре окружающего воздуха. Коррекция осуществляется по формуле
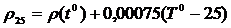 , (1.8)
, (1.8)
где ρ25 – расчетная плотность (приведенная к 250С); ρ(t) – плотность, измеренная при данной температуре, Т0 – температура электролита во время измерения.
Степень разряженности аккумулятора определяется по формуле
 , (1.9)
, (1.9)
где ρзар, ρразр, ρизм – соответственно плотность электролита: полностью заряженного аккумулятора, г/см3; полностью разряженного аккумулятора (принимается равной 1,110 г/см3 для всех аккумуляторов); измеренная при проверке и приведенная к 15°С.
ЭДС аккумулятора может быть определена двумя способами:
- точным вольтметром с большим внутренним сопротивлением (рис.1.2 при разомкнутой цепи);
по формуле 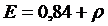 (1.10)
(1.10)
где ρ – расчетная плотность электролита.
Внутреннее сопротивление аккумуляторной батареи Rвн определяют экспериментально. При разомкнутом ключе К (рис.1.1) с помощью высокоомного вольтметра определяют ЭДС батареи ЕАБ. Затем замыкают ключ К и с помощью амперметра измеряют ток нагрузки JН.
Для замкнутой цепи составляют уравнение Кирхгофа:
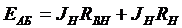 , (1.11)
, (1.11)
отсюда
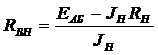 . (1.12)
. (1.12)
Оценить величину внутреннего сопротивления исправного заряженного аккумулятора можно по эмпирической формуле
 , (1.13)
, (1.13)
где С20 – номинальная емкость АБ.
Испытания нагрузочной вилкой позволяют судить о пригодности аккумуляторов для эксплуатации. Так как нагрузочная вилка потребляет от АБ очень большой ток (несколько десятков и даже сотен ампер), в результате чего в активной массе пластин аккумуляторов начинаются диффузионные процессы, способные внести ошибку в измерения ЭДС, то испытание нагрузочной вилкой следует производить только после измерений, необходимых для определения внутреннего сопротивления батареи.
При испытании нагрузочной вилкой нужно:
- завернуть пробки в заливные отверстия аккумуляторов;
- включить нагрузочную вилку сильным вдавливанием ее стержней в торцы выводных штырей аккумулятора и снять показания прибора (если добиться хорошего контакта вилки аккумулятора не удается, следует зачистить концы стержней вилки и выводы аккумулятора). Длительность испытания каждого аккумулятора не должна превышать 5 с.
В зависимости от состояния батарей и от нужд эксплуатации применяют зарядку при постоянной силе тока или при постоянном напряжении. Зарядку при постоянной силе тока применяют в условиях стационарных аккумуляторных цехов на зарядных станциях. Этим способом заряжают новые, отремонтированные и частично сульфатированные батареи. При зарядке этим способом батареи подбирают группами (батареи одинаковой емкости и одинаковой разряженности) и соединяют последовательно.
Число последовательно соединенных элементов не должно превышать
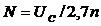 , (1.14)
, (1.14)
где UC – максимальное напряжение, обеспечиваемое источником тока; n – число элементов.
Величина зарядного тока должна составлять 0,1 С20, где С20 ‑ номинальная емкость батареи. При зарядке сульфатированных батарей силу тока выбирают в 2…3 раза меньшей. ЭДС аккумулятора по мере зарядки возрастает, поэтому зарядное напряжение в процессе зарядки необходимо повышать. Когда напряжение на одном аккумуляторе достигает 2,4 В и начинается газовыделение, силу тока снижают в два раза и доводят зарядку до конца.
Зарядка батарей при постоянном напряжении применяется для быстрой их подзарядки в условиях эксплуатации, при этом батареи подсоединяют к источнику тока параллельно. Шестивольтовые батареи подсоединяют к источнику тока напряжением 7 В, а двенадцативольтовые – напряжением 14 В. Сила зарядного тока при этом:
 , (1.15)
, (1.15)
где Еδ – текущее значение ЭДС батареи, В; UЗАР – напряжение источника зарядного тока.
По мере повышения ЭДС сила зарядного тока снижается до нуля. Зарядка происходит почти без газовыделения.
Заключение о техническом состоянии АБ
Заключение должно содержать сведения касающиеся: чистоты поверхности батареи, уровня электролита, замеченных механиченских повреждений (трещин, состояния перемычек и выводов), степени заряженности батареи, возможной сульфатации, величины емкости (ориентировочно по показаниям нагрузочной вилки) и других неисправностей в отдельности по аккумуляторам и в целом по батарее.
Если АБ не пригодна к эксплуатации, то должны быть даны рекомендации для приведения АБ в пригодное для эксплуатации состояние.
При определении технического состояния батареи можно ориентировочно исходить из данных табл.1.3.
Таблица 1.3
| Результаты испытаний
| Заключение
|
| Нагрузочной вилкой
| Ареометром
|
| 1
| 2
| 3
|
| Напряжение 1,7…1,9В держится устойчиво 5с. Разница напряжений в разных аккумуляторах батареи не более 0,1В
| Плотность электролита 1,25…1,28г/см3. Разница плотности в разных аккумуляторах батареи не более 0,01г/см3
| Аккумулятор исправен и полностью заряжен
|
| Напряжение падает в течение 5с более чем на 0,1 В
| Плотность электролита любая
| Низкая емкость аккумулятора, возможна сильная сульфатация
|
| Напряжение падает до 1,3…1,4В и не держится в течение 5с
| Плотность электролита 1,25…1,28 г/см3.
| Аккумулятор разряжен и залит электролитом повышенной плотности. Возможна сульфатация
|
| Напряжение падает до 1,3…1,4 В
| Плотность электролита 1,15…1,17 г/см3.
| Аккумулятор сильно разряжен, необходима немедленная подзарядка
|
| Напряжение одного или нескольких аккумуляторов равно нулю
| Плотность электролита в этих аккумуляторах несколько ниже, чем в других
| Возможно короткое замыкание. Необходим ремонт
|
Контрольные вопросы
1. Что представляет собой АБ?
2. Напишите уравнения химических процессов, происходящих в аккумуляторе при зарядке и разрядке.
3. Какие способы заряда АБ Вы знаете?
4. Каковы существующие способы заряда батарей, их достоинства и недостатки?
5. От чего зависит сила зарядного тока аккумулятора?
6. Чем опасен перезаряд аккумулятора? Каковы возможные причины перезарядки батареи на автомобиле?
7. Как изменяется вольт-амперная характеристика батареи с увеличением разряженности батареи?
8. Для чего необходимо знать вольт-амперную характеристику АБ?
9. Для чего измеряют уровень электролита в аккумуляторах, на что он влияет?
10. О каком параметре технического состояния АБ можно судить по плотности электролита?
11. Почему вводят температурную поправку для плотности электролита при оценке технического состояния аккумулятора?
12. Для определения какого параметра технического состояния аккумулятора необходимо знать плотность электролита после последней зарядки?
13. Какие параметры технического состояния аккумуляторов позволяет оценить нагрузочная вилка?
14. Что представляет собой нагрузочная вилка?
15. Каким образом можно оценить емкость аккумулятора с помощью нагрузочной вилки?
16. Каковы показания нагрузочной вилки разряженного и заряженного аккумулятора?
17. Как определить степень разряженности аккумулятора?
18. Что такое сульфатация?
19. Что такое ЭДС аккумулятора, как ее определяют?
20. Чем отличается напряжение аккумулятора, измеренное нагрузочной вилкой (с включенной нагрузкой), от ЭДС?
21. Какова связь между ЭДС батареи и плотностью электролита?
22. Каковы способы определения внутреннего сопротивления аккумуляторов?
23. По каким параметрам технического состояния аккумуляторов можно судить о степени сульфатации?
24. С какой неисправностью аккумулятора связаны малая емкость и большое внутреннее сопротивление аккумулятора?
25. Почему сульфатация уменьшает емкость батареи?
26. Назовите способ устранения частичной сульфатации?
27. Что такое емкость аккумулятора?
28. Что такое энергозапас аккумулятора?
Основная литература: ОЛ1ОЛ2
Дополнительная литература: ДЛ5ДЛ6
Практическая работа № 2



 (1.4)
(1.4)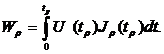 (1.6)
(1.6)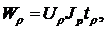 (1.7)
(1.7)
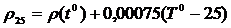 , (1.8)
, (1.8) , (1.9)
, (1.9)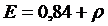 (1.10)
(1.10)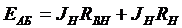 , (1.11)
, (1.11)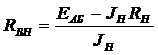 . (1.12)
. (1.12) , (1.13)
, (1.13)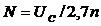 , (1.14)
, (1.14) , (1.15)
, (1.15)

