

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Типы сооружений для обработки осадков: Септиками называются сооружения, в которых одновременно происходят осветление сточной жидкости...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Типы сооружений для обработки осадков: Септиками называются сооружения, в которых одновременно происходят осветление сточной жидкости...
Топ:
Установка замедленного коксования: Чем выше температура и ниже давление, тем место разрыва углеродной цепи всё больше смещается к её концу и значительно возрастает...
Теоретическая значимость работы: Описание теоретической значимости (ценности) результатов исследования должно присутствовать во введении...
История развития методов оптимизации: теорема Куна-Таккера, метод Лагранжа, роль выпуклости в оптимизации...
Интересное:
Влияние предпринимательской среды на эффективное функционирование предприятия: Предпринимательская среда – это совокупность внешних и внутренних факторов, оказывающих влияние на функционирование фирмы...
Принципы управления денежными потоками: одним из методов контроля за состоянием денежной наличности является...
Мероприятия для защиты от морозного пучения грунтов: Инженерная защита от морозного (криогенного) пучения грунтов необходима для легких малоэтажных зданий и других сооружений...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
если для реакции необходимо столкновение двух реагирующих молекул. Эта зависимость носит название кинетического закона действующих масс (К. Гулльберг, П. Воге, 1867)
Для гомогенной реакции А + В →… этот закон изображается уравнением
ν = kc A c B ,
где k – константа скорости реакции [л/(моль с)], зависящая от природы реагентов, присутствия катализатора и температуры, но не зависящая от концентрации реагентов и численно равная скорость реакции при условии сАсв = 1.
Для гетерогенной реакции А + В(ж, т) →… взаимодействие происходит лишь на поверхности конденсированного (жидкого, твердого) вещества, поэтому концентрация такого вещества не входит в выражение закона действующих масс: ν = kc A.
Для реакций, уравнения которых не отражают механизма протекания этих реакций, необходимо рассматривать каждую элементарную стадию отдельно. Тройные и более столкновения (А + В + В +… →) маловероятны, поэтому такие реакции (например, N2 + ЗН2 = 2NH3) протекают всегда в несколько элементарных стадий (А + В →). Кинетический закон действующих масс применим только к каждой из этих стадий, но не к уравнению химической реакции в целом.
Энергетика реакций
Любая реакция сопровождается выделением или поглощением энергии в форме теплоты. В исходных веществах химические связи разрываются, и на это энергия затрачивается (т. е. она при этом поглощается системой), в продуктах же, наоборот, химические связи образуются, и при этом энергия выделяется. Разность между затраченной и выделившейся энергией называется тепловым эффектом химической реакции (обозначается Q). Если затрата энергии выше, чем ее выделение, то тепловой эффект будет отрицательным, или эндо‑ эффектом (‑Q) в противном случае – положительным, или экзо ‑эффектом (+Q).
|
|
Тепловой эффект является внешним признаком реакций, в термохимических уравнениях он указывается после продуктов:
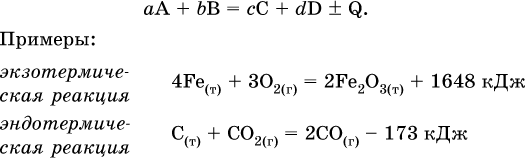
Такая запись означает, что при сгорании 4 моль железа в 3 моль кислорода с образованием 2 моль оксида железа (III) выделяется 1648 кДж теплоты, а при взаимодействии 1 моль углерода (в виде кокса) и 1 моль углекислого газа с получением 2 моль угарного газа поглощается извне 173 кДж теплоты.
Тепловые эффекты прямой и обратной реакций одинаковы по числу, но противоположны по знаку. Например, реакция
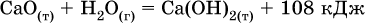
(обработка 1 моль оксида кальция водяным паром в количестве 1 моль с образованием 1 моль гидроксида кальция) сопровождается экзо ‑эффектом Q = +108 кДж, тогда как обратная реакция
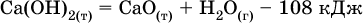
(разложение 1 моль гидроксида кальция на 1 моль оксида кальция и 1 моль водяного пара) сопровождается эндо‑ эффектом Q = ‑108 кДж.
При протекании реакций (особенно с участием газов) могут существенно меняться объем и температура реакционной системы. Если тепловой эффект определяется при постоянном давлении (1 атм для каждого газа в системе, а при отсутствии газов общее давление 1 атм) и постоянной температуре (обычно 298 К, или 25 °C), то он отвечает стандартной энтальпии реакции, характеризующей в целом всю систему (функция системы). Энтальпия реакции обозначается Δ Н °, знак Δ Н ° противоположен знаку Q:
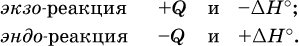
Значение Δ Н ° записывается после уравнения и отделяется от него запятой:
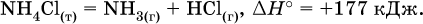
Реакции, протекающие с высоким экзо ‑эффектом, часто требуют только начального нагревания (инициирования), а далее протекают самопроизвольно, например процесс алюминотермии:

Помимо энтальпии, химическая система характеризуется еще одной функцией – стандартной энтропией реакции Δ S ° (кДж/К), связанной с неупорядоченностью системы (степенью беспорядка). Чем больше частиц в системе и чем выше ее температура, тем больше степень беспорядка. В идеальном кристалле (при абсолютном нуле температуры) степень беспорядка нулевая (идеальный порядок), в реальных твердых телах существует всегда некоторая степень беспорядка, в жидкостях она уже выше, но наибольшая степень беспорядка в газах, где молекулы не зависят друг от друга и двигаются весьма хаотично. Например, для льда, жидкой воды и водяного пара значения Δ S ° равны соответственно 0,039, 0,07 и 0,189 кДж/К.
|
|
Всякая химическая реакция, таким образом, имеет две энергетические характеристики – энтальпию Δ Н ° и энтропию Δ S °. Для самопроизвольных реакций характерно стремление к уменьшению энергии за счет теплопередачи в окружающую среду и одновременно к увеличению степени беспорядка. Эти факторы действуют в противоположных направлениях, поэтому результирующая величина будет равна их разности:
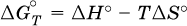
(здесь энтропия умножена на температуру для адекватности единиц, Δ Н ° и T Δ S° приведены в килоджоулях, так как К кДж/К = кДж).
Суммарная энергетическая функция системы называется стандартной энергией Гиббса реакции Δ G°T, индекс Т подчеркивает зависимость этой величины от температуры, что очевидно из уравнения (отметим еще, что Δ Н ° и Δ S ° мало зависят от температуры).
По значениям G°T можно судить о возможности протекания реакций в направлении слева направо по химическому уравнению:

Например, синтез аммиака
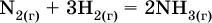
при 25 °C возможен:
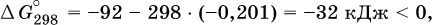
а при 350 °C невозможен:

Следовательно, при 25 °C имеется принципиальная возможность получения аммиака, а при сильном нагревании системы (реакция экзотермическая, Δ Н ° = ‑92 кДж) аммиак получить не удастся. Правда, при 25 °C реакция возможна только в принципе, так как она протекает очень медленно и с малым выходом. Ускорение реакций определяется факторами химической кинетики, а увеличение степени протекания – соответствующим смещением химического равновесия.
Обратимость реакций
Химическая реакция называется обратимой, если в данных условиях протекает не только прямая реакция (→), но также и обратная реакция т. е. из исходных веществ образуются продукты и одновременно из продуктов получаются реагенты:
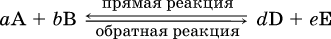
Обратимые реакции не доходят до конца. Концентрации реагентов уменьшаются, что приводит к уменьшению скорости прямой реакции 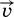
|
|
. Скорость же обратной реакции 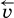
постоянно возрастает, поскольку увеличиваются концентрации продуктов.
Когда скорости прямой и обратной реакций станут одинаковыми (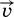
= 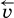
), наступит состояние химического равновесия, при котором не происходит дальнейшего изменения концентраций реагентов и продуктов.
В состоянии равновесия концентрации реагентов и продуктов постоянны, их называют равновесными концентрациями и обозначают [А], [В], [D] и [Е], в отличие от концентраций сА, св, cD и сЕ в любой другой момент времени. Установлено, что:
В состоянии равновесия произведение концентраций продуктов в степенях, равных стехиометрическим коэффициентам, деленное на такое же произведение концентраций реагентов, есть величина постоянная при T = const.
Такое соотношение обозначают Кс и называют константой равновесия данной реакции:
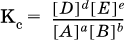
Это выражение носит название равновесный закон действующих масс (К. Гулльберг, П. Воге, 1867).
Значение Кс характеризует состояние равновесия в данной реакции и определяется соотношением концентраций, т. е. величина Кс не зависит от каждой в отдельности равновесной концентрации – [А], [В], [D] или [Е].
Химическое равновесие не означает, что наступило состояние покоя. Прямая и обратная реакции протекают и в состоянии равновесия, но с одинаковой скоростью. Поэтому оно называется подвижным (динамическим) равновесием.
Подвижное химическое равновесие можно нарушить, оказывая на систему внешнее воздействие и тем самым изменяя условия протекания реакции – температуру, давление, концентрацию. При любом нарушении (сдвиге) химического равновесия система перейдет (сместится) в другое состояние равновесия.
Влияние условий на смещение химического равновесия определяется принципом, который установлен французским ученым A.‑Л. Ле‑Шателье (1884).
Современная формулировка принципа смещения равновесия, называемого принципом Ле‑Шателье:
|
|
|

Наброски и зарисовки растений, плодов, цветов: Освоить конструктивное построение структуры дерева через зарисовки отдельных деревьев, группы деревьев...

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...

Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни...

История создания датчика движения: Первый прибор для обнаружения движения был изобретен немецким физиком Генрихом Герцем...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!