После выпуска металла из плавильной печи в ковш при температуре tк в течение времени tк металл выдерживается и охлаждается в ковше (рис.1,а). Это необходимо, чтобы доставить ковш от участка плавки к месту заливки форм, а также произвести ковшевые металлургические операции (например, добавка модификаторов для получения заданной структуры и свойств литого металла). По достижении требуемой температуры заливки tзал производится заливка металла в форму. С этого момента и до момента выбивки tв (извлечение из формы) металл охлаждается в форме (рис.1,б), отдавая ей свою теплоту перегрева Dtпер над ликвидусом, теплоту затвердевания в интервале ликвидус-солидус Dtинт, а затем – теплоту охлаждения в a-твердом состоянии от солидуса tс до температуры фазового превращения tпр и в (a + b)-состоянии до выбивки из формы.
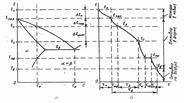
Рис.1. Изменение температуры сплава состава Со в процессе формирования отливки по диаграмме состояния (а) и во времени (б) при охлаждении в заливочном ковше, в форме и на воздухе
Дальнейшее охлаждение отливки происходит на воздухе.
За время tв охлаждения металла в форме от tзал до tв последовательно происходит ряд процессов, определяющих качество отливки:
течение металла при заполнении полости формы и внутри затвердевающей отливки;
кристаллизация металла, то есть переход из жидкого состояния в твердое с образованием центров кристаллизации, рост которых приводит к формированию литой структуры;
выделение растворенных в металле газов при понижении температуры расплава и в процессе его затвердевания с образованием крупных газовых пузырей (газовых раковин) и микроскопических пузырьков (пор);
выделение неметаллических включений, их всплывание в жидком металле и удаление, а также застревание в объеме кристаллизующегося твердожидкого металла;
ликвация примесей в результате избирательной кристаллизации и перемещения жидкой фазы, обогащенной примесями, по сечению отливки с образованием макроскопической (зональной) и микроскопической (дендритной) ликвации;
объемная усадка (сокращение объема) металла при понижении температуры и фазовом переходе с образованием концентрированных усадочных раковин и рассеянной усадочной пористости;
линейная усадка (сокращение наружных размеров) отливки, вызывающая появление деформаций, напряжений, коробления и трещин.
Перечисленные процессы, включающие сложный комплекс взаимосвязанных физических явлений теплообмена, гидродинамики, диффузии, фильтрации и т.д., при нерациональной технологии изготовления отливки приводят к появлению многообразных дефектов.
Литейные сплавы всегда кристаллизуются в интервале температур, и область затвердевания располагается между изотермическими поверхностями в отливке с температурами ликвидуса и солидуса.
Область затвердевания состоит из твердожидкой зоны (скелет из твердой фазы и включения жидкой фазы) и жидко-твердой зоны (жидкость с включениями разрозненных выделений твердой фазы).
Если из незатвердевшей отливки вылить жидкую фазу, то с ней удалится жидко-твердая зона. Поэтому граница между двумя зонами области называется выливаемостью.
В твердожидкой зоне выделяется участок, в котором жидкая фаза разобщена растущими кристаллами и не может подпитываться по микроканалам. Граница этого участка - граница питания; на диаграмме состояния она располагается несколько ниже границы выливаемости (нулевой жидкотекучести).
Границы 1, 2, 3, 4, 5 меняются в зависимости от условий охлаждения и характера кристаллизации. Для компактных дендритов и округлых кристаллов успевает образоваться 50-70 % твердой фазы, а граница выливаемости сдвигается к солидусу.
При образовании разветвленных дендритов твердый скелет образуется уже при 15-30 % твердой фазы, а граница выливаемости располагается ближе к ликвидусу(рис.3).
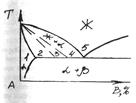
Рис.3. Границы двухфазной области кристаллизации
Последние исследования в области кристаллизации отливок показали, что во всех отливках можно предполагать определенную последовательность твердения от внешней поверхности к центру. Паттерсон разделяет последовательное затвердевание на четыре типа, а именно: А – экзогенное с ростом компактных кристаллов; В – экзогенное с ростом дендритных кристаллов; С – эндогенное с ростом компактных кристаллов; D – эндогенное с ростом дендритных кристаллов.
Механизм протекания процесса затвердевания сильно влияет на характер фронта кристаллизации, от которого, в свою очередь, зависят количество расплава, изолируемого в процессе затвердевания от остального объема жидкой фазы, и склонность к образованию некоторых характерных пороков
При одинаковых условиях затвердевания (одинаковая среда, в которую заливается металл при одинаковых условиях) с повышением содержания добавляемого элемента в сплаве происходит переход от экзогенного роста компактных кристаллов к эндогенной дендритной кристаллизации.
Как только температура сплава у стенок формы упадет до температуры ликвидуса, в этой зоне начинается кристаллизация. В случае если сплав затвердевает в интервале температур, то в зоне затвердевания присутствуют две фазы (твердая и жидкая). В момент, когда температура сплава упадет до температуры солидуса, затвердевают остатки жидкой фазы, и во всей отливке будет только твердая фаза. В процессе затвердевания одновременно могут существовать три зоны:
зона твердого металла (ξ), толщина которой со временем непрерывно увеличивается;
двухфазная зона (δ), ширина которой зависит от интервала затвердевания и градиента температуры;
зона расплава, ширина которой непрерывно уменьшается.
При дальнейшем понижении температуры сплава ниже температуры солидуса в сплаве может произойти вторичная кристаллизация. Отливка остывает в форме до тех пор, пока ее температура не понизится до значения, при котором ее можно извлечь из формы без опасности образования в ней внутренних напряжений.
Поверхность, которая образует границу между зоной твердого металла и двухфазной зоной, называется изосолидусом (температура соответствует солидусу). Поверхность, которая образует границу между двухфазной зоной и зоной расплава, называется изоликвидусом (здесь температура соответствует температуре ликвидуса заливаемого сплава). В чистых металлах или эвтектических сплавах, которые затвердевают не в интервале температур, двухфазная зона не образуется.
Ширина двухфазной зоны оказывает влияние, как на структуру сплава, так и на степень ликвации. Чем шире двухфазная зона, тем меньше образуется столбчатых (ориентированных) кристаллов. Существенное слияние оказывает ширина двухфазной зоны и на степень дендритной и зональной ликвации, являющейся следствием избирательного затвердевания составляющих сплава как внутри отдельных дендритов, так и стенок отливки.
Ширина двухфазной зоны влияет также на микропористость структуры. При широкой двухфазной зоне образуются изолированные островки расплава, при усадке которых образуются микропоры.
На ширину двухфазной зоны оказывают влияние:
интервал затвердевания сплава, чем больше интервал затвердевания, тем шире двухфазная зона;
температурный перепад по поперечному сечению отливки, который зависит от теплоаккумулирующей способности формы (металлические формы образуют резкий перепад температур), от теплопроводности заливаемого сплава (чем меньше теплопроводность, тем круче температурный перепад), от температуры заливки (чем выше температура металла при заливке, тем меньше температурный перепад вследствие прогрева формы) и от температуры затвердевания сплава.
С повышением температуры число и размеры кластеров уменьшаются. По мере приближения температуры расплава к точке кристаллизации устойчивость и продолжительность «жизни» их повышается, а при определенной температуре они приобретают полную устойчивость и становятся центрами кристаллизации. Происходит спонтанная кристаллизация, и кристаллы начинают расти на кластерах. Для начала кристаллизации необходимо уменьшить свободную энергию, то есть переохладить расплав, отвести некоторое количество теплоты, чтобы на имеющихся зародышах начался рост кристалла.
Зависимость свободной энергии G от температуры, как следует из рис.9 различна для жидкой и твердой фаз. При температуре меньше То, более низкую свободную энергию G имеет жидкая фаза, поэтому она будет более устойчивой.
При Тo кривые пересекаются - это температура термодинамического равновесия фаз и в этом случае Gт = Gж, то есть обе фазы обладают одинаковой энергией, достаточной для внешней работы.
 Процесс кристаллизации может устойчиво идти при условии Gт < Gж, для чего требуется, чтобы температура кристаллизации (Ткр) была ниже То.
Процесс кристаллизации может устойчиво идти при условии Gт < Gж, для чего требуется, чтобы температура кристаллизации (Ткр) была ниже То.
Рис. 9. Изменения свободной энергии жидкой Gж и твердой Gт фаз в зависимости от температуры
Разность температур То – Ткр = DТ называется переохлаждением, которое обеспечивает достаточную для начала кристаллизации разность свободных энергий Gж – Gт. За счет разности энергий возмещается работа, необходимая для образования и роста зародышей: А = 32 s3 [ М.То / r q(То- Ткр)]2, где s – поверхностное натяжение на грани растущего кристалла; М – молекулярная масса вещества кристалла; r – плотность вещества кристалла; q – теплота плавления 1 моля вещества кристалла; То –Ткр – степень переохлаждения.
Свободная энергия (энергия Гиббса) определяется соотношением: G = E – TS + pV = H – ST, где Е – внутренняя энергия, S – энтропия (мера разупорядоченности фазы, то есть мера рассеянной энергии); Т – абсолютная температура; р – давление; V – объем; Н – энтальпия.
При температуре равновесной кристаллизации То: Gт = Gж, то есть Нж – SжТо = Нт – SтТо.
Разность энтальпий жидкой и твердой фаз равна теплоте кристаллизации: DН = L = Hж – Тт = (Sж – Sт)То = DSto, то есть L = DSto.
При переохлаждении DТ с выделением теплоты кристаллизации происходит уменьшение объемной свободной энергии (химической составляющей энергии Гиббса): DGV = (Gж – Gт) V, где V – объем.
При образовании сферического зародыша: DGV = -LDT/To*4/3pr3 одновременно происходит повышение объемной и поверхностной энергии (GS) в результате образования поверхности раздела фаз DGS = s4pr2.
Следовательно, процесс кристаллизации протекает в результате изменения общей свободной энергии: DGобщ = DGV + DGS = -LDT / To 4/3 pr3 + s4pr2
После дифференцирования и преобразований находят критический радиус зародыша: rкр = 2sТо / LDT = 2sМто / r q (To - Ткр).





 Процесс кристаллизации может устойчиво идти при условии Gт < Gж, для чего требуется, чтобы температура кристаллизации (Ткр) была ниже То.
Процесс кристаллизации может устойчиво идти при условии Gт < Gж, для чего требуется, чтобы температура кристаллизации (Ткр) была ниже То.


