5.4.1 Фильтрация.
С появлением электронно-вычислительных устройств, широкое распространение начал получать спектральный анализ ЭЭГ. Популярность этого метода объясняется простотой и наглядностью представления результатов вычислений, когда быстро и точно можно сказать о преобладании на рассматриваемом участке ЭЭГ того или иного ритма и частоты.
Фильтрация предназначена для выделения из сигнала интересующего исследователя диапазона частот и удаления шумовых или не представляющих интерес составляющих. При анализе экспериментальных данных используются цифровые фильтры, реализованные вычислительными средствами. Наиболее употребительны фильтры Баттерворда и Чебышева-1,2, которые являются эквивалентами одноименных и популярных аналоговых фильтров.
Эти фильтры пропускают гармонические колебания без искажения их формы. Однако в результате фильтрации возникают амплитудные и фазовые искажения.
Амплитудные искажения. Амплитудно-частотная характеристика (АЧХ) фильтра зависит от его типа и порядка. АЧХ представляет отношение амплитуд гармоник на выходе к амплитудам на входе фильтра в зависимости от частоты. На рис. 4.35 приведены АЧХ четырех фильтров с полосой пропускания 8—12 Гц (альфа-диапазон). В полосе пропускания АЧХ близка к 1 (гармоники пропускаются фильтром), а в полосе задержания — близка к 0 (гармоники подавляются по амплитуде).

а) б) в) г)
Рис. Амплитудно-частотные характеристики фильтров с полосой пропускания 8-12 Гц: а — Баттерворда 2-го порядка; б — Баттерворда 8-го порядка; в — Чебышева-1 8-го порядка; г — Чебышева-2 8-го порядка
На границах полосы пропускания (частоты среза) наблюдается спад АЧХ, крутизна которого (крутизна среза) увеличивается с повышением порядка фильтра. Как видно из сравнения рис., а и б, фильтр Баттерворда 2-го порядка по сравнению с фильтром 8-го порядка имеет заметно более пологие срезы АЧХ.
В связи с конечной крутизной срезов (неотвесными срезами) имеют место два искажения: 1) в сигнале частично подавляются гармоники (уменьшается их амплитуда), близлежащие к частоте среза со стороны полосы пропускания; 2) частично пропускаются гармоники (с уменьшением их амплитуды), близлежащие к частоте среза в полосе задержания.
Фильтры Баттерворда сохраняют определенный баланс между этими двумя искажениями. Фильтр Чебышева-1 минимизирует первую погрешность, его АЧХ во всей полосе пропускания близка к 1 (рис. 4.35, в). Фильтр Чебышева-2 минимизирует вторую погрешность, его АЧХ во всей полосе задержания близка к 0 (рис. 4.35, г). В целом фильтры Чебышева при том же порядке имеют большую крутизну среза, чем фильтры Баттерворда.
Отметим также, что при увеличении порядка фильтра увеличивается объем и время вычислений (снижается быстродействие фильтра), но это является критичным только при использовании фильтрации в режиме реального времени, когда процесс фильтрации может не успевать за реальным сигналом, превышая длительность одного интервала дискретизации АЦП.
Присутствие нелинейностей. Этот недостаток относится к фильтрам Чебышева. Фильтры Чебышева-1 имеют нелинейности в виде колебаний АЧХ в полосе пропускания, а фильтры Чебышева-2 — в полосе задержания. Однако эти нелинейности невелики по амплитуде (на рис. 4.35 в, г они практически незаметны из-за высокого порядка фильтров) и не столь актуальны для области физиологии по сравнению с техническими приложениями, где они могут затруднить разделение узких близлежащих спектральных пиков. Кроме того, уровень нелинейности АЧХ регулируется специальным параметром e фильтра Чебышева. Уменьшение e вызывает соответствующее снижение быстродействия, но это может быть критично лишь при фильтрации в режиме реального времени.
Фазовые искажения являются одним из основных погрешностей, присущих классической фильтрации. Они являются следствием метода последовательного приближения, на котором базируется фильтрация, а именно: чтобы в любой момент времени t оценить амплитуду i -й гармонической составляющей сигнала с периодом Тi необходимо ее наблюдать в течение Тi с момента t. Тем самым каждая гармоника в результате фильтрации приобретает задержку во времени или фазовый сдвиг, пропорциональный Тi или 1/ fi, т. е. обратно пропорциональный частоте гармоники fi. На фазовые искажения также влияет порядок фильтра и полоса частот.

Рис. 4.36. Фазовые искажения при фильтрации:
канал 1 — исходный сигнал частотой 11 Гц; каналы 2-5 — результаты фильтрации в разных частотных диапазонах фильтрами Баттерворда m-го порядка; обозначения искажений: А — начального приближения; В — переходные при смене характера сигнала; С — временной сдвиг
Сложный характер фазовых искажений удобно продемонстрировать на упрощенном модельном примере рис. 4.36. На канале 1 приведен полигармонический сигнал с двумя участками нулевой амплитуды, а на каналах 2—5 показаны результаты фильтрации различными фильтрами. Здесь присутствуют искажения начального приближения (А), переходные амплитудные искажения при резкой смене характера сигнала (В) и постоянный временной фазовый сдвиг (С). Фазовые и переходные искажения увеличиваются с повышением порядка фильтра (ср. каналы 2 и 3). Для гармоник, лежащих в середине полосы пропускания, эти искажения уменьшаются при расширении полосы как в сторону низких, так и в сторону высоких частот (каналы 4, 5).
Поскольку фазовый сдвиг обратно пропорционален частоте гармоники, то для широкополосных сигналов (с многими гармониками высокой амплитуды) сложение их фазовых сдвигов может приводить к дополнительному искажению формы сигналов. Однако для области физиологии такой характер сигналов нетипичен.
Фурье-фильтрация. Указанные погрешности классической фильтрации побудили уже в первой версии CONAN-1.5 (1993 г.) предложить новый для электрофизиологии метод Фурье-фильтрации, основанный на использовании двукратного Фурье-преобразования. После первого преобразования сигнала в частотную область из комплекснозначного спектра удаляются гармоники в заданном диапазоне частот, после чего обратным Фурье-преобразованием по усеченному спектру восстанавливается отфильтрованный сигнал во временной области.
Принципиальными достоинствами такого метода по сравнению с классическими фильтрами являются:
практически полное отсутствие фазовых искажений;
практически бесконечная крутизна среза, вследствие чего частотная характеристика фильтра близка к прямоугольной — полное подавление гармоник в полосе задержания и отсутствие искажений в полосе пропускания;
минимальные амплитудные искажения, имеющие место только на границах полосы задержания за счет незначительного влияния эффектов утечки и амплитудной модуляции, уменьшающегося с увеличением разрешения по частоте.
При реализации Фурье-фильтрации нужно учитывать ограничение на длину обрабатываемой реализации сигнала. Поэтому фильтрацию длительных записей приходится производить поинтервально. Поскольку фазы гармоник на соседних интервалах в общем случае не совпадают, на стыках интервалов могут возникать небольшие амплитудные скачки, визуально более заметные при полосовой фильтрации в низкочастотном диапазоне. Для нивелирования этих скачков интервалы фильтрации следует выбирать с небольшим перекрытиям и усреднением результатов (Отметим, что этот эффект сказывается только при фильтрации сигналов большой протяженности. Так, при работе ДПФ на интервалах до 8192 отсчета для сигнала с частотой дискретизации 128 Гц во временном выражении это будет соответствовать 64 с. Поскольку большинство ЭЭГ-записей выпол-няются и анализируются на значительно меньших интервалах наблюдения, проблема стыковочных концов для них не актуальна. Кроме того, сглаживание стыков имеет, в основном, эстетическую ценность, поскольку их наличие практически не сказывается на результатах вычислительного анализа).
Работу фильтров на реальных сигналах иллюстрирует рис. 4.37, где приведена запись энцефалограммы и результаты ее фильтрации фильтрами нижних и верхних частот по методам Фурье-преобразования и Баттерворта. Так, в результате применения ФВЧ Баттерворта (канал 3) заметно пропускание низкочастотных составляющих (в данном случае — высокоамплитудного 10-герцового альфа-ритма) и существенные начальные искажения, а в результате применения ФНЧ Баттерворта (канал 5) заметно искажение формы сигнала и сдвиг по фазе.

Рис. 4.37. Запись ЭЭГ (первый канал) и результаты фильтрации ФВЧ (каналы 2, 3) и ФНЧ (каналы 4, 5) с частотой среза 15 Гц по методу Фурье-преобразования (каналы 2, 4) и фильтром Баттерворда 3-го порядка (каналы 3, 5)
Следует отметить, что данный метод неприменим в режиме реального времени, поскольку он требует накопления значительного временного интервала реализации сигнала и обладает недостаточным быстродействием при больших частотах оцифровки.
5.4.2. Сжатие данных.
Сжатие данных — процедура перекодирования данных, производимая с целью уменьшения их объёма. Применяется для более рационального использования устройств хранения и передачи данных.
Сжатие бывает без потерь (когда возможно восстановление исходных данных без искажений) или с потерями (восстановление возможно с искажениями, несущественными с точки зрения дальнейшего использования восстановленных данных). Сжатие без потерь обычно используется при обработке компьютерных программ и данных, реже — для сокращения объёма звуковой, фото- и видеоинформации. Сжатие с потерями применяется для сокращения объёма звуковой, фото- и видеоинформации, оно значительно эффективнее сжатия без потерь.
Сжатие основано на устранении избыточности информации, содержащейся в исходных данных. Примером избыточности является повторение в тексте фрагментов (например, слов естественного или машинного языка). Подобная избыточность обычно устраняется заменой повторяющейся последовательности более коротким значением (кодом). Другой вид избыточности связан с тем, что некоторые значения в сжимаемых данных встречаются чаще других, при этом возможно заменять часто встречающиеся данные более короткими кодами, а редкие — более длинными (вероятностное сжатие). Сжатие данных, не обладающих свойством избыточности (например, случайный сигнал или шум, зашифрованная информация), невозможно без потерь.
Для компьютерного анализа сжатие ЭЭГ, по возможности без потери диагностической информации, является чрезвычайно важным обстоятельством, поскольку уменьшает объем обрабатываемых данных и дает возможность быстро классифицировать энцефалограммы. К примеру, если анализировать сами числовые отсчеты сигнала, то, во-первых, этот процесс займет огромное время, а во-вторых, вариабельность самих ЭЭГ, относящихся к одной и той же патологии, очень высока и какая-либо классификация невозможна. Для представления ЭЭГ в сжатом виде возможно использование различных алгоритмов сжатия. Параметрическое описание ЭЭГ с помощью авторегрессионного анализа, которое, среди прочих возможностей, позволяет получить математическую модель сигнала, осуществив тем самым сжатие информации, присутствующей в исходной ЭЭГ.
Пусть x(t) - исследуемый сигнал, а x - дискретные значения этого сигнала, предшествующие рассматриваемому моменту. Для предсказания текущего значения x используем линейный предсказывающий (экстраполирующий) фильтр:
 (4.2.1)
(4.2.1)
где ~ xi - предсказанное значение,
~â
j - эмпирические коэффициенты авторегрессионной модели. Эти коэффициенты могут определяться по (2N+1) отсчетам процесса x(t) вблизи некоторой исходной точки, условно принимаемой за ноль отсчета. Для оценивания коэффициентов, прежде всего, подсчитывается (m+1) значение ординат текущей корреляционной функции:
 (4.2.2)
(4.2.2)
а затем определяются оценки  , m путем решения системы m линейных алгебраических уравнений:
, m путем решения системы m линейных алгебраических уравнений:
 (4.2.3)
(4.2.3)
На каждом i-м такте с помощью уравнения (4.2.3) с найденными коэффициентами  можно рассчитать ошибку предсказания
можно рассчитать ошибку предсказания
 . (4.2.4)
. (4.2.4)
Эта ошибка характеризует мгновенное значение неточности предсказания с помощью данного экстраполирующего фильтра. Последовательность значений 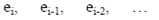 является последовательностью случайных величин (временным рядом) и для нее также можно ввести понятие текущей эмпирической корреляционной функции:
является последовательностью случайных величин (временным рядом) и для нее также можно ввести понятие текущей эмпирической корреляционной функции:
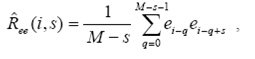 (4.2.5)
(4.2.5)
Для разделения ЭЭГ на отдельные квазистационарные сегменты введем показатель E, характеризующий суммарно степень несоответствия предсказанных и реальных свойств случайного процесса:
 (4.2.6)
(4.2.6)
Сопоставляя значение E с некоторым пороговым значением  , можно установить тот момент времени, когда
, можно установить тот момент времени, когда  и значит, по-видимому, сигнал изменил свои свойства. Тем самым устанавливают факт перехода к новому квазистационарному сегменту, причем выявленную временную точку выбирают в качестве исходной (l=0), после чего все расчеты повторяют.
и значит, по-видимому, сигнал изменил свои свойства. Тем самым устанавливают факт перехода к новому квазистационарному сегменту, причем выявленную временную точку выбирают в качестве исходной (l=0), после чего все расчеты повторяют.
Для решения вопроса о том, имеет ли место переход к новому сегменту или же наблюдается начало некоторой нестационарной волны (т.е. своего рода детерминированный аддитивный дрейф), предлагают вводить ограничение ошибки предсказания в соответствии с формулой:
 (4.2.7)
(4.2.7)
При этом нестационарные волны практически не будут влиять на процесс сегментации. Одновременно соотношение (4.2.7) дает критерий для их выявления. Параметрические описания такого типа фактически позволяют существенным образом уменьшить количество информации, необходимой для представления ЭЭГ: вместо отдельных отсчетов для представления кривой можно использовать соответствующую модель фильтра с числом коэффициентов, значительно меньшим, чем число исходных дискретных отсчетов. Как правило, таким способом удается добиться сжатия цифрового представления ЭЭГ в 30-50 раз. Однако при длительностях записи ЭЭГ в несколько минут объемы данных все равно будут достаточно большими. Кроме того, такой метод представления далеко не всегда позволяет сохранить диагностически ценную информацию, а ее потеря может сказаться при дальнейшем анализе ЭЭГ и формировании заключения. К тому же спектрально-корреляционные методы имеют преимущество над авторегрессионным в том, что их результаты можно использовать для визуальной оценки происходящих процессов - электроэнцефалографисты привыкли к таким способам представления ЭЭГ, чего нельзя сказать об авторегрессии.
Другим возможным подходом к проблеме представления ЭЭГ в сжатом виде с помощью алгоритмов цифровой обработки является так называемый турн-амплитудный анализ. Достоинством его является относительная известность среди врачей-нейрофизиологов (особенно электромиографистов, где он эффективно применяется) и простота по сравнению даже со спектральными оценками. Фактически, на ранних этапах автоматизированной диагностики он заменял построение спектра мощности сигнала. Несмотря на появление новых методов, на сегодняшний день турн-амплитудный анализ является едва ли не основной методикой при исследовании мышечной активности. Смысл ее в том, чтобы подсчитать в сигнале число так называемых турнов в секунду.
Корреляционный анализ.
К методам корреляционного анализа можно отнести построение автокорреляционной и кросскорреляционной функции.
Для определения автокорреляционной функции используется следующее соотношение:
 (4.2.14)
(4.2.14)
где X - рассматриваемый сигнал.
Автокорреляционная функция стационарных процессов обладает следующими свойствами:
1. Она является четной, т.е.
 (4.2.15)
(4.2.15)
Это следует из определения стационарного процесса, т.е. из условия независимости его характеристик от начала отсчета времени.
2. Абсолютное значение функции автокорреляции при любом τ не может превышать ее значение при τ =0.
3. Для стационарных случайных процессов справедливо соотношение
 (4.2.16)
(4.2.16)
Физически это соотношение объясняется тем, что случайные стационарные процессы обычно имеют конечное время корреляции.
Использование автокорреляционной функции является наиболее мощным средством выделения гармонических колебаний в случайном процессе. При этом можно находить числовые величины, характеризующие обрабатываемую ЭЭГ:
1. средняя частота (средний период) периодических колебаний;
2. периодичность процесса - коэффициент отношения мощности периодической
(квазипериодической) составляющей к мощности случайной составляющей;
3. устойчивость периодики - время затухания автокорреляционной функции.
Средний период колебаний на коррелограмме определяется путем подсчета времени задержки между вершинами волн и определения среднего значения. Эту величину также можно представить в виде средней частоты колебаний.
 (4.2.17)
(4.2.17)
где N – количество вершин волн;
ti – время задержки между соседними волнами.
Коэффициент периодичности процесса определяется следующим образом:
1. производится измерение отклонений на коррелограмме каждого колебания от пика до пика;
2. вычисляется средняя величина амплитуды колебания:
 (4.2.18)
(4.2.18)
3. определяется половина от этой средней амплитуды, которая представляется как средняя амплитуда периодической составляющей на данной коррелограмме:  (4.2.19)
(4.2.19)
4. определяется разница между максимальным значением автокорреляционной функции (оно определяется при нулевом значении времени τ =0) и вычисленным средним значением амплитуды периодической составляющей, - эта разница отражает амплитуду случайной составляющей:
 , (4.2.20)
, (4.2.20)
5. вычисляется отношение средней амплитуды периодической составляющей к амплитуде случайной составляющей. Эта количественная величина характеризует выраженность периодики на данной ЭЭГ:  , (4.2.21)
, (4.2.21)
Устойчивость периодики определяется по величине задержки, при которой амплитуда периодических колебаний на коррелограмме уменьшалась до 10% от максимальной. Фоновая ритмика ЭЭГ не является строго периодическим процессом, ее лишь приближенно можно так называть, т.е. она ближе к квазипериодическому процессу. В этом случае периодика на автокоррелограмме затухает и тем быстрее, чем процесс больше отличается от истинно периодического. Вообще, на ЭЭГ можно отметить три вида процессов: непериодический или случайный - типичным примером которого может служить ЭЭГ без доминирования какого-либо ритма; квазипериодический, каким является, например альфа-активность в затылочных отделах; периодический, наблюдаемый при усваивании ритма в пробах фото- и фоностимуляции. Это дает возможность, анализируя автокорреляционную функцию, определить реакцию усваиваемости или активации ритма при наличии внешней периодической стимуляции, т.е. оценить реактивную ЭЭГ. Также, как было отмечено выше, важным элементом анализа является идентификация доминирующего ритма анализируемой ЭЭГ, что также позволительно сделать благодаря автокорреляционной функции.
Поскольку, как было отмечено выше, при анализе ЭЭГ специалисту необходимо получать информацию о параметрах частотных ритмов, при рассмотрении автокорреляционной функции в рамках обработки ЭЭГ было установлено, что для углубленного исследования сигнала с ее u1087 помощью целесообразно полосовыми фильтрами выделить основные частотные ритмы, а затем построить их автокоррелограммы и проанализировать каждый их них отдельно, используя описанные выше параметры и алгоритмы представления автокорреляционной функции.
Для цифровой обработки формула для нахождения автокорреляционной функции принимает следующий вид:
 (4.2.22)
(4.2.22)
где 0 <τ < T - время, на которое сдвигается исходный сигнал;
T - число дискретных точек исходного сигнала, соответствующих обрабатываемому временному отрезку.
Шаг для анализа считается равным 1.

Рис. Пример корреляционных функций
Не менее важна при анализе ЭЭГ и кросскорреляционная функция. Она позволяет определить такие показатели, как степень связности, корреляции ЭЭГ двух разных точек мозга, выделить периодические составляющие, общие для обеих ЭЭГ, четко идентифицировать наличие амплитудной или частотной асимметрий левого и правого полушария. Для кросскорреляционной функции в соотношение (4.2.14) участвуют не один и тот же, а два процесса, т.е. выражение для нее имеет вид:
 , (4.2.23)
, (4.2.23)
а в цифровом виде ее можно, соответственно, представить как:
 (4.2.24)
(4.2.24)
где 0 <τ < T.
Данная функция дает представление о том, коррелированы или нет между собой выбранные каналы, а также показывает степень связности их между собой. В случае наличия патологического очага, как правило, интересно знать в каких областях головного мозга он присутствует. Анализируя спектр методов, применяемых для обработки и представления ЭЭГ, следует отметить, что эту информацию может дать картирование, но при этом учитываются только амплитудные показатели. А этого может оказаться мало. Кросскорреляционная функция, дополняя картирование, представляет информацию о том, влияет ли ЭЭГ по какому-либо каналу на другие каналы. Причем оценивается это влияние по параметрам частоты и фазы колебаний. Таким образом, в случае наличия патологического очага, распространяющегося сразу на несколько каналов, это четко будет видно на графике кросскорреляционной функции.
Степень сходства или связи двух ЭЭГ при кросскорреляционном анализе определяется величиной коэффициента кросскорреляции (Ккр). Ее обычно нормируют к пределам от +1 до -1. Если две ЭЭГ являются точными копиями, то фактически кросскорреляционная функция представляет собой автокорреляционную, и, соответственно, Ккр будет равен +1. Если две ЭЭГ точно соответствуют друг другу, но все их элементы сдвинуты на 180 градусов, т.е. являются противофазными, то Ккр будет равен -1. В тех случаях, когда два исследуемых процесса заключают в себе, кроме общих составляющих, также элементы, свойственные каждому из них в отдельности, величина связи, определяемая по Ккр, будет меньше единицы, и тем меньше, чем больше независимых элементов или частот в двух исследуемых ЭЭГ. В зависимости от соотношения фаз общих компонентов Ккр может иметь либо положительное, либо отрицательное значение. Для анализа ЭЭГ с помощью кросскорреляции были введены следующие параметры:
1. степень кросскорреляционной связи - отношение максимального значения кросскорреляционной функции к величине максимума автокорреляционной функции каждого из исследуемых процессов при τ = 0;
 , (4.2.25)
, (4.2.25)
2. временной сдвиг максимума кросскорреляционной функции - ВС, характеризующий временные отношения двух процессов. При этом отмечается степень корреляционной связи двух процессов как: слабая - Ккр менее 0.3; умеренная - от 0.3 до 0.5; значительная - от 0.5 до 0.7; высокая, или тесная – от 0.7 до 0.9; очень высокая, или очень тесная - от 0.9 до 1.
Большое значение при анализе ЭЭГ играет информация о степени связности отдельных ритмов, а также отдельных конкретных частот, причем пользователям желательно представлять ее в удобной и понятной форме. Конечно, можно использовать для этих целей кросскорреляционную функцию, но при этом пришлось бы загромождать экран обилием графиков, что было бы не совсем удобно для врача.
Оценивая мнения различных экспертов, здесь предлагается следующий подход к этой проблеме. Как было отмечено выше, степень сходства двух процессов оцениваются с помощью Ккр, соответственно, для оценки корреляции между подобными ритмами двух процессов можно, применив полосовые фильтры, выделить их и определить Ккр для каждого ритма отдельно, а затем построить график зависимости Ккр от частоты. Аналогично, то же можно проделать и с более узкими частотными полосами. Для выделения нужной частотной полосы используется полосовой фильтр Баттерворта второго порядка. На рис. приведем график зависимости Ккр от частоты с шагом 1 Гц в полосе от 1 до 35 Гц.
Спектральный анализ.
Наибольшее распространение в электроэнцефалографии получил метод спектрального анализа ЭЭГ. Этот метод обладает наибольшей информативностью при оценке составляющих ЭЭГ и, что самое главное, позволяет выявить такие стороны электрических процессов мозга, которые остаются недоступными при обычной визуальной оценке ЭЭГ.
Вычисление спектров мощности (спектрограмм - СГ) позволяет получить энергию каждой из частотных составляющих данной ЭЭГ и оценить их соотношение. Это дает возможность сравнивать электрические процессы разных отделов коры на одном отрезке времени, проводить сравнение спектров каждой данной области в динамике при повторных исследованиях, а также сравнивать в количественных величинах ЭЭГ разных больных.
Спектр мощности иначе можно назвать спектральной плотностью рассматриваемого процесса. Спектральную плотность можно ввести как преобразование Фурье от автокорреляционной функции. В общем случае спектральную плотность или спектр функции X(t) можно определить как
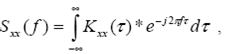 (4.2.26)
(4.2.26)
а взаимную спектральную плотность двух реализаций X(t) и Y(t) можно определить следующим образом:
 (4.2.27)
(4.2.27)
Учитывая, что в формулах (4.2.26) и (4.2.27) спектральные плотности определены для всех частот, как положительных, так и отрицательных, а также тот факт, что корреляционные функции - четные функции, то, очевидно, что спектры задаются только действительной частью преобразования Фурье, поэтому формулы (4.2.26) и (4.2.27) можно переписать в следующем виде:
 , (4.2.28)
, (4.2.28)
 (4.2.29)
(4.2.29)
Мнимую часть преобразования Фурье полезно определить для дальнейшего нахождения функции фазового сдвига процессов, т.е.
 , (4.2.30)
, (4.2.30)
 , (4.2.31)
, (4.2.31)
Второй способ нахождения спектра - это непосредственное преобразование Фурье от рассматриваемого сигнала. Для практического использования формулы (4.2.29) и (4.2.30) можно записать в следующем виде:
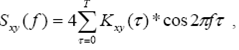 (4.2.32)
(4.2.32)
 (4.2.33)
(4.2.33)
где T - величина временного интервала, взятого для анализа.
Для корректного использования спектра мощности перед обработкой выбранного участка необходимо вычесть постоянную составляющую и пропустить сигнал через какое-либо сглаживающее окно, например Хэмминга, для устранения боковых лепестков и краевых эффектов.
Однако, в случае если нужно более высокое разрешение рассчитываемого спектра, то возможно пользоваться и формулами (4.2.29) и (4.2.30). Это целесообразно также и еще по одной причине. В данном случае предлагаемые методы обработки используются врачами, для которых физика процесса иногда играет даже большее значение, чем четкие математические расчеты. В случае обработки по формулам (4.2.32) и (4.2.33) в результате получается дискретное представление процесса с каким-то выбранным шагом по частоте. Это может привести к ситуации, когда, к примеру, имея шаг 0.5 Гц, на частоте 7 Гц получаем всплеск на графике спектра, на частоте 7.5 Гц - значение, близкое к минимуму, а при 8 Гц - опять всплеск. И хотя математически это верно, врачу трудно понять и согласиться с таким результатом. Прямое вычисление интеграла устраняет эту проблему - все переходы между разными частотами на графике спектра будут плавными и понятными для пользователя.
Турн-амплитудный анализ.
Другим возможным подходом к проблеме представления ЭЭГ в сжатом виде с помощью алгоритмов цифровой обработки является так называемый турн-амплитудный анализ. Достоинством его является относительная известность среди врачей-нейрофизиологов (особенно электромиографистов, где он эффективно применяется) и простота по сравнению даже со спектральными оценками. Фактически, на ранних этапах автоматизированной диагностики он заменял построение спектра мощности сигнала. Несмотря на появление новых методов, на сегодняшний день турн-амплитудный анализ является едва ли не основной методикой при исследовании мышечной активности. Смысл ее в том, чтобы подсчитать в сигнале число так называемых турнов в секунду. Турном (от английского turn - поворот) называется перемена знака изменения потенциала при условии прохождения им до очередного поворота разности потенциалов не менее определенного порога (для миографии обычно он установлен в 100 мкВ). Таким образом, принимаемый сигнал разбивается на участки по 1 секунде, и на каждом таком участке находится количество турнов и их средняя амплитуда. По значениям этих параметров в каждой такой точке строится график, представленный на рис., где на пересечении этих значений ставится крестик.
После проведения обследования получается облако из таких крестиков, которое и несет смысловое значение для врача. Существуют нормативные облака, с которыми сравнивается полученное и определяется наличие какого-либо патологического процесса. Положение облака на графике, а также его разброс дает представление об амплитуде и длительности пиков, т.е. фактически дает амплитудно-частотную оценку процесса. Важное значение имеет также значение отношения средней амплитуды к числу турнов за 1 секунду.
Специалисты-нейрофизиологи считают, что турн-амплитудный анализ является своего рода заменой спектральной оценки сигнала. По крайней мере, величина обратная числу турнов в секунду дает значение средней частоты односекундной выборки сигнала, а также амплитуду этой частоты.
При анализе биомедицинских сигналов этого бывает достаточно. Что касается электроэнцефалографии, то такая оценка будет явно недостаточной для получения полного описания процессов на ЭЭГ.

Рис. 8. Пример облака турн-амплитудного анализа.








 (4.2.1)
(4.2.1) (4.2.2)
(4.2.2) , m путем решения системы m линейных алгебраических уравнений:
, m путем решения системы m линейных алгебраических уравнений: (4.2.3)
(4.2.3) можно рассчитать ошибку предсказания
можно рассчитать ошибку предсказания . (4.2.4)
. (4.2.4)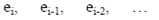 является последовательностью случайных величин (временным рядом) и для нее также можно ввести понятие текущей эмпирической корреляционной функции:
является последовательностью случайных величин (временным рядом) и для нее также можно ввести понятие текущей эмпирической корреляционной функции: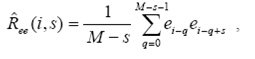 (4.2.5)
(4.2.5) (4.2.6)
(4.2.6) , можно установить тот момент времени, когда
, можно установить тот момент времени, когда  и значит, по-видимому, сигнал изменил свои свойства. Тем самым устанавливают факт перехода к новому квазистационарному сегменту, причем выявленную временную точку выбирают в качестве исходной (l=0), после чего все расчеты повторяют.
и значит, по-видимому, сигнал изменил свои свойства. Тем самым устанавливают факт перехода к новому квазистационарному сегменту, причем выявленную временную точку выбирают в качестве исходной (l=0), после чего все расчеты повторяют. (4.2.7)
(4.2.7) (4.2.14)
(4.2.14) (4.2.15)
(4.2.15) (4.2.16)
(4.2.16) (4.2.17)
(4.2.17) (4.2.18)
(4.2.18) (4.2.19)
(4.2.19) , (4.2.20)
, (4.2.20) , (4.2.21)
, (4.2.21) (4.2.22)
(4.2.22)
 , (4.2.23)
, (4.2.23) (4.2.24)
(4.2.24) , (4.2.25)
, (4.2.25)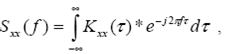 (4.2.26)
(4.2.26) (4.2.27)
(4.2.27) , (4.2.28)
, (4.2.28) (4.2.29)
(4.2.29) , (4.2.30)
, (4.2.30) , (4.2.31)
, (4.2.31)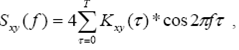 (4.2.32)
(4.2.32) (4.2.33)
(4.2.33)



