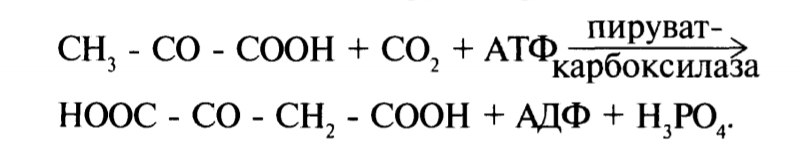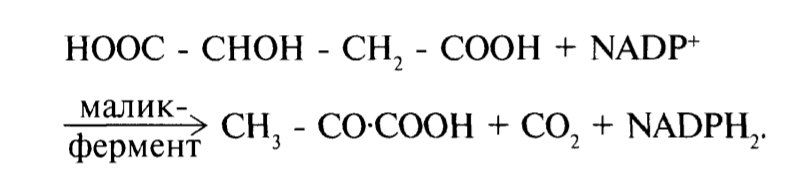СУБСТРАТНОГО ФОСФОРИЛИРОВАНИЯ. 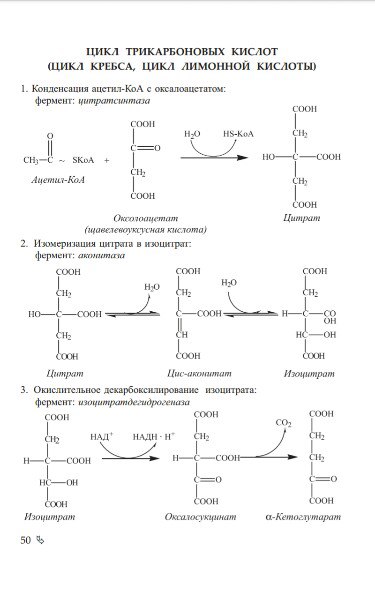

Реакции дегидрирования происходящие в ЦТК служат источником атомов водорода (НАДН2) для дыхательной цепи.
За счет субстратного фосфорилирования образуется энергия в виде ГТФ
2. Дайте характеристику процессу окислительного фосфорилирования. Поясните механизм сопряжения окисления и фосфорилирования.
Окислительным фосфорилированием называют синтез АТФ путем фосфорилирования АДФ за счет энергии трансмембранного электрохим потенциала, возникающего при освобождении энергии электронами окисленного субстрата в процессе миграции этих электронов по дыхательной цепи к вдыхаемому кислороду. То есть окисл фосфорилирование – это синтез АТФ, связанный с переносом электронов по дыхательной цепи, это синтез АТФ за счет энергии окисления субстрата. Происходит в аэробных условиях
Основные этапы окислительного фосфорилирования:
1. Образующиеся в реакциях катаболизма НАДН и ФАДН2 передают атомы водорода (т.е. протоны водорода и электроны) на ферменты дыхательной цепи.
2. Электроны движутся по ферментам дыхательной цепи и теряют энергию.
3. Энергия электронов используется на выкачивание протонов Н+ из матрикса в межмембранное пространство.
4. В конце дыхательной цепи электроны попадают на кислород и восстанавливают его до воды.
5. Протоны Н+ стремятся обратно в матрикс и проходят через АТФ-синтазу.
6. При этом они теряют энергию, которая используется для синтеза АТФ.
Под сопряжением окисления с фосфорилированием понимают превращение энергии электронов окисленного субстрата, проходящих по дыхательной цепи, в промежуточную форму – в энергию трансмембранного потенциала с последующим использованием ее для фосфорилирования АДФ, то есть для синтеза АТФ. Протонный градиент создается путем выталкивания ионов водорода в межмебранное пространство в 3 участках дых цепи: при переходе электронов с ФМНН2 через FeS-белок на KoQ, при переходе электронов с KoQH2 через FeS-белок на цитохром Ci при переходе электронов от цитохрома, а через цитохром а3 к кислороду. Эти участки цепи транспорта электронов обозначают как пункты сопряжения дыхания с фосфорилированием.
3. Поясните отрицательное влияние свободно-радикального окисления на клетки и организм. Приведите примеры заболеваний, тесно связанных с активацией свободно радикального окисления.
Первичные механизмы:
1. Деструкция жирных кислот фосфолипидов (липоперекиси, эндоперекиси).
2. Повреждение белков
• образование шиффовых оснований
• окисление тиоловых групп – инактивация тиоловых ферментов, транскрипционных факторов.
3. Повреждение ДНК – мутации, нарушение репарации.
Вторичные механизмы:
1. Повышение проницаемости мембран
• нарушение мембранных потенциалов,
• разобщение окислительного фосфори-лирования.
2. Повреждение лизосом – аутолиз клеток.
3. Повышение микровязкости мембран и нарушение активности
• мембранных рецепторов,
• мембраносвязанных ферментов,
• мембранного транспорта.
4. Канцерогенез.
Пример заболевания – ишемия.
Билет 14.
1. 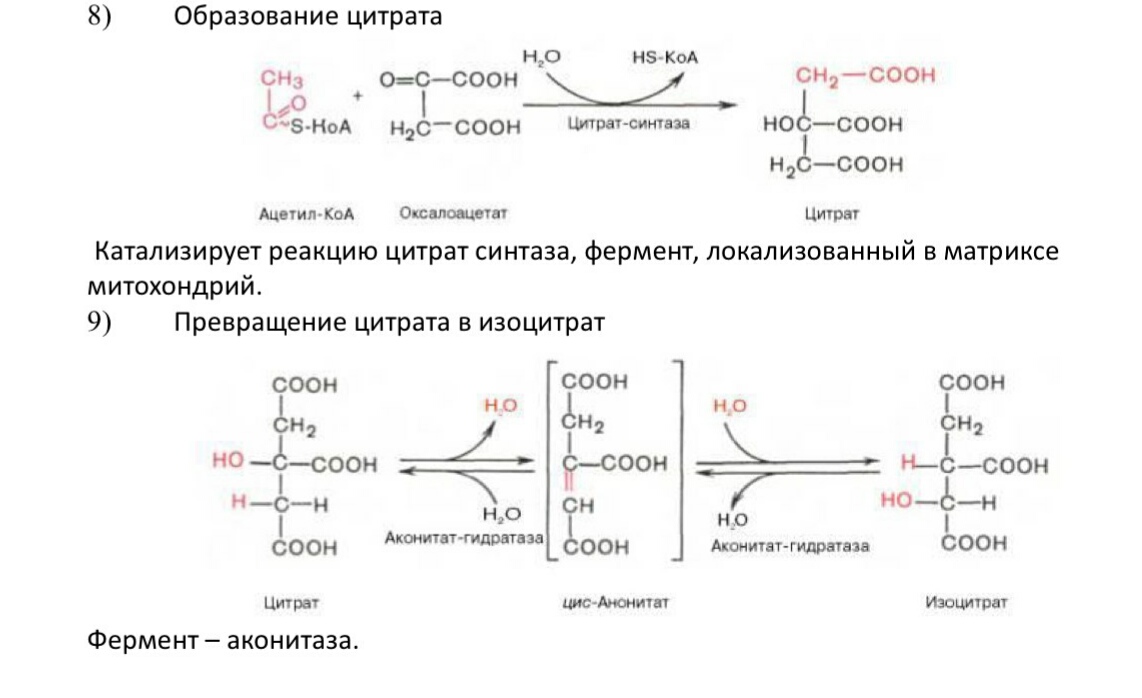
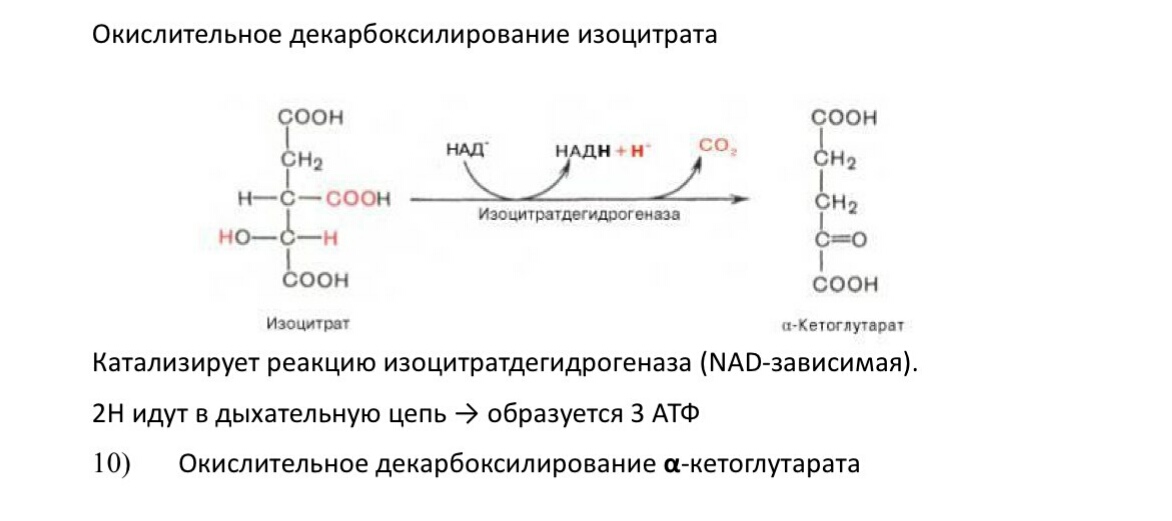
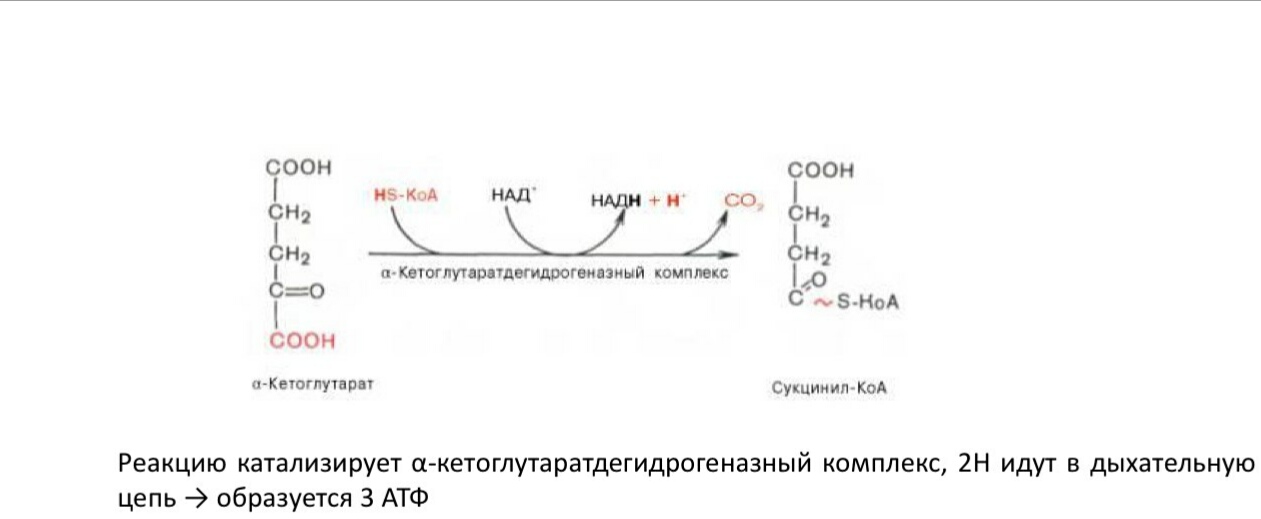
Напишите последовательность реакций цикла трикарбоновых кислот. Как регулируется цикл трикарбоновых кислот?
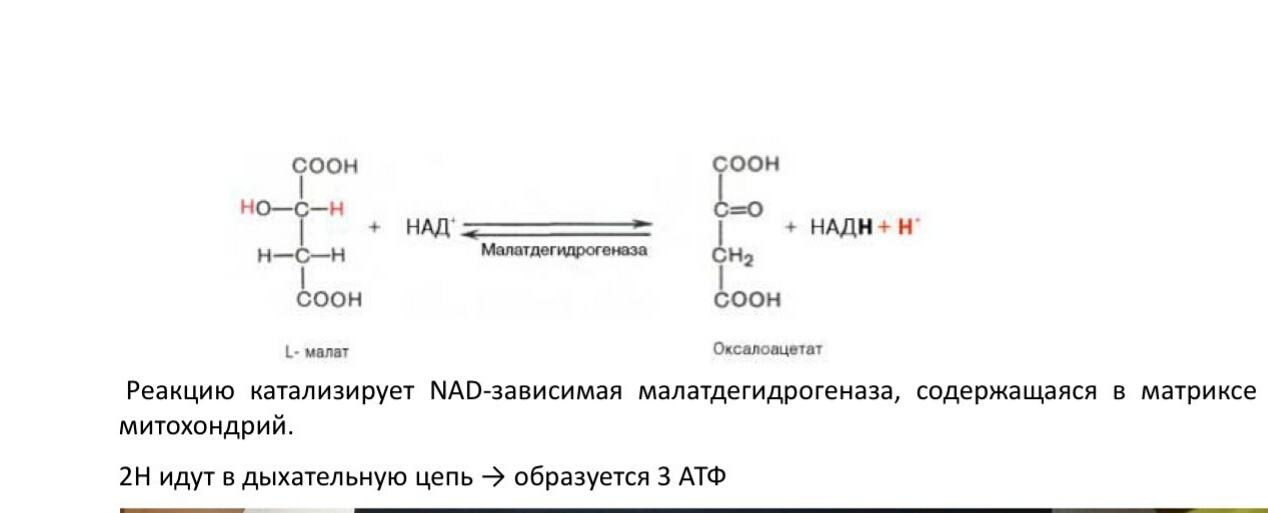
14) 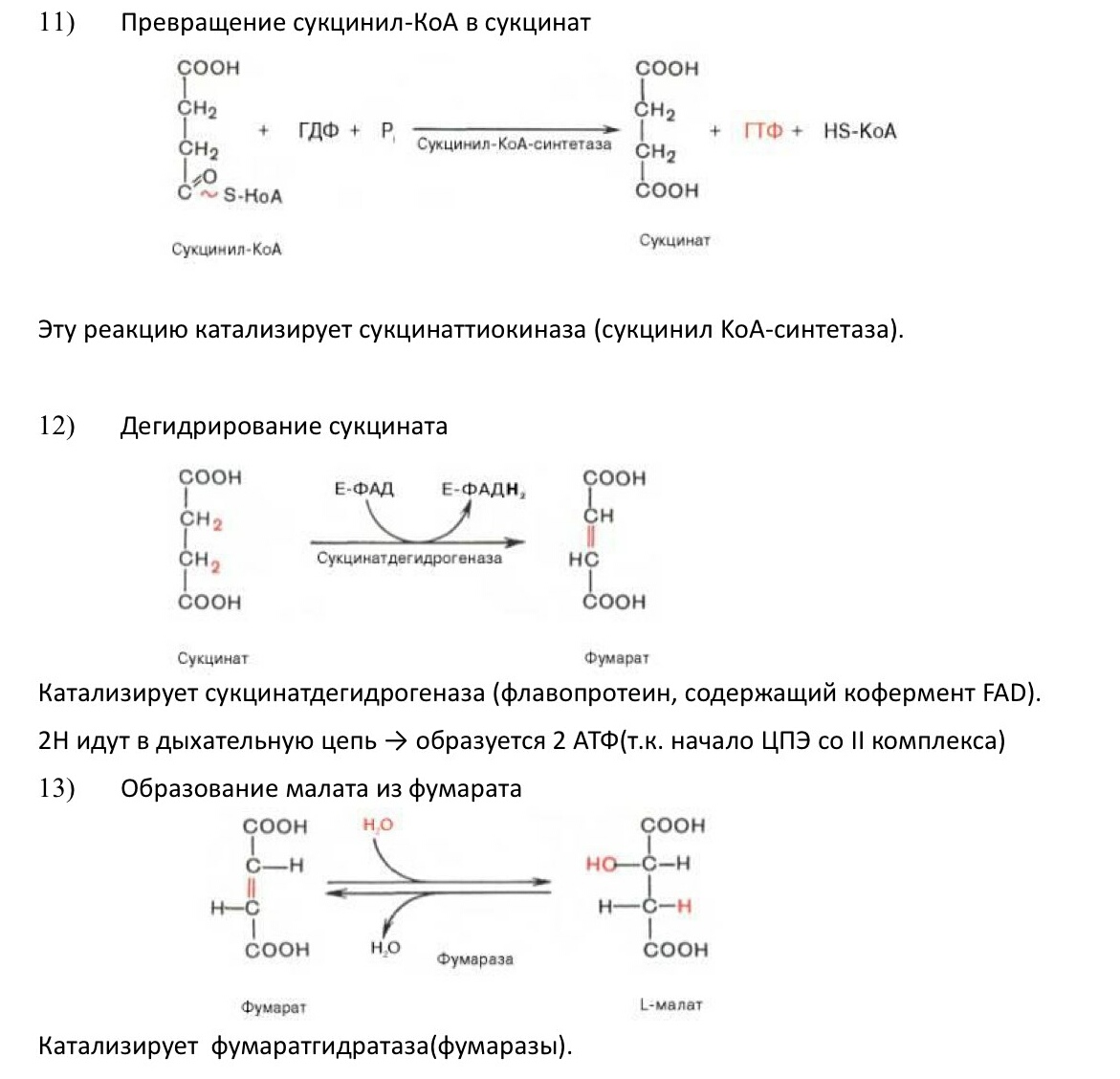
Дегидрирование малата
2. Дайте характеристику процессу окислительного фосфорилирования. Опишите строение АТФ-синтазы и механизм ее функционирования.
Окислительное фосфорилирование – основная часть биологического окисления или тканевого дыхания, т.е. процессов, идущих в организме с участием кислорода.
Окислительное фосфорилирование – это многоэтапный процесс, происходящий во внутренней мембране митохондрий и заключающийся в окислении восстановленных эквива- лентов (НАДН и ФАДН2) и сопровождающийся синтезом АТФ. Впервые механизм окислительного фосфорилирования был предложен П.Митчеллом. Согласно этой гипотезе перенос электронов, происходящий на внутренней митохондриаль- ной мембране, вызывает выкачивание ионов Н+ из матрикса митохондрий в межмембран- ное пространство. Это создает градиент концентрации ионов Н+ между цитозолем и за- мкнутым внутримитохондриальным пространством. Ионы водорода в норме способны воз- вращаться в матрикс митохондрий только одним способом – через специальный фермент, образующий АТФ – АТФ-синтазу.
По современным представлениям внутренняя митохондриальная мембрана содержит ряд мультиферментных комплексов, включающих множество ферментов. Эти ферменты называют дыхательными ферментами, а последовательность их расположения в мембране – дыхательной цепью.
Строение и механизм действия АТФ-синтазы. А - F0 и F1 - комплексы АТФ-синтазы, В состав
F0входят полипептидные цепи, которые образуют канал, пронизывающий мембрану насквозь.По этому каналу протоны возвращаются в матрикс из межмембранного пространства; белок F1 выступает в матрикс с внутренней стороны мембраны и содержит 9 субъединиц, 6 из которых образуют 3 пары α и β ("головка"), прикрывающие стержневую часть, которая состоит из 3 субъединиц γ, δ и ε. γ и ε подвижны и образуют стержень, вращающийся внутри неподвижной головки и связанный с комплексом F0. В активных центрах, образованных парами субъединиц α и β, происходит связывание АДФ, неорганического фосфата (Рi) и АТФ. Б- Каталитический цикл синтеза АТФ включает 3 фазы, каждая из которых проходит поочерёдно в 3 активных центрах: 1 - связывание АДФ и Н3РО4; 2 - образование фосфоангидридной связи АТФ; 3 - освобождение конечного продукта. При каждом переносе протонов через канал F0 в матрикс все 3 активных центра катализируют очередную фазу цикла. Энергия электрохимического потенциала расходуется на поворот стержня, в результате которого циклически изменяется конформация α- и β-субъединиц и происходит синтез АТФ.
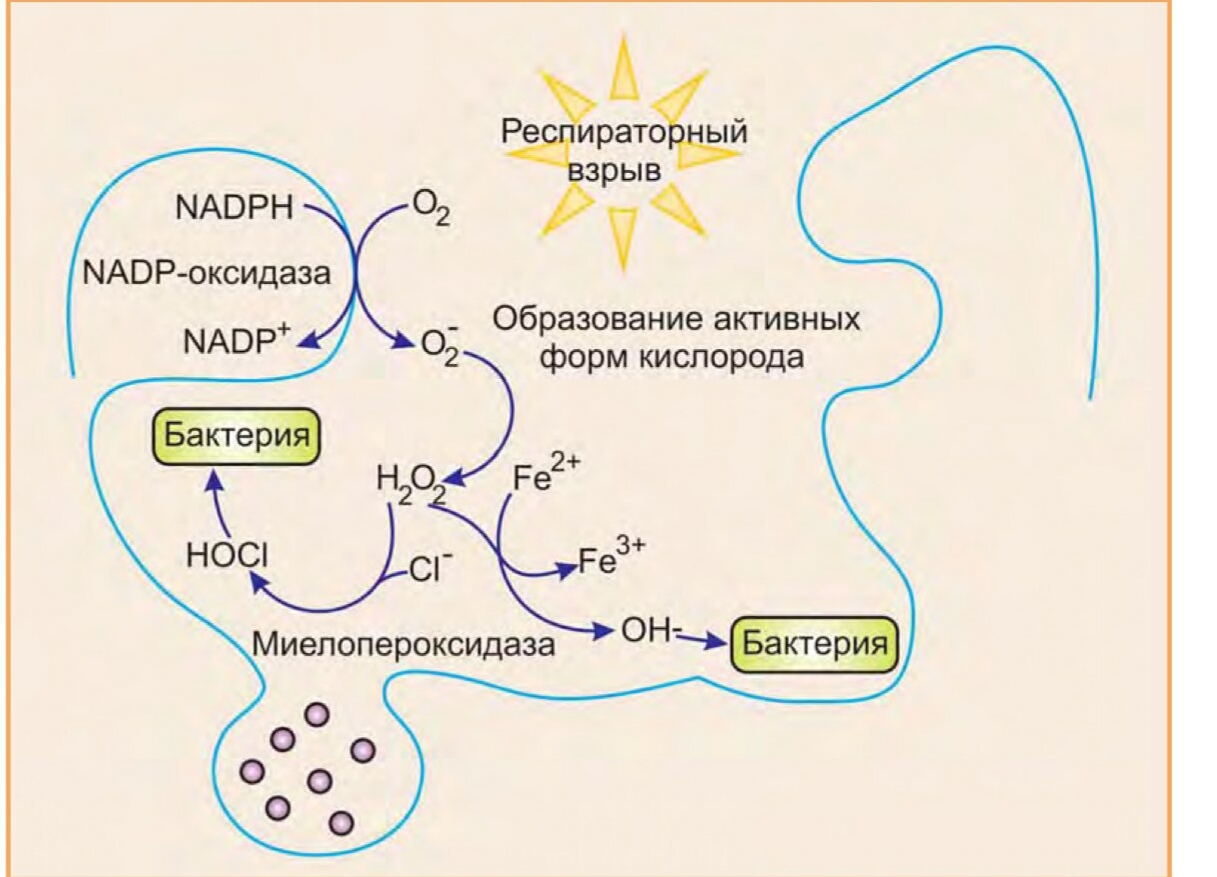
3. Охарактеризуйте фагоцитоз и напишите используемые в нем ферментативные реакции.
Фагоцитоз – активное поглощение и разрушение клетками твердых частиц. Фагоциты проявляют цитотоксическое действие и бактерицидное действие. Моноциты и Макрофаги формируют мононуклеарнофагоцитирующую систему – МНС. Основной компонент МНС – макрофаги, имеющие внутриклеточные ферменты и необходимый аппарат для их выработки. Взаимодействие твёрдых частиц с поверхностными рецепторами вызывает активацию фагоцитов, к-я заключается в повышении проницаемости цпм->повышение конц ионов Са, активирование аденилатциклазы, протеинкиназы (участвует в фосфорилированеии мембранных белков->их активирование) ->активирование НАДФН-оксидазы(цитоплазматический ферментный комплекс), к-я катализирует перенос электронов с НАДФН на молекулярный кислород с образованием супероксидного ангидрида -> В активированных фагоцитах усиливается окисление глюкозы и усиливается потребление кислорода. Это называется дыхательный(респираторный) взрыв (тк потребление кислорода возрастает уже в первые секунды активации фагоцита).РВ-универсальное проявление реактивности фагоцитирующих клеток.


Билет 15
1. Что такое анаболизм и катаболизм? Нарисуйте общую схему катаболизма, укажите этапы обмена веществ. Что значит специфические и общие пути катаболизма?
Анаболизм – это биосинтез белков, полисахаридов, липидов, нуклеиновых кислот и других макромолекул из малых молекул
- предшественников.
Поскольку он сопровождается усложнением структуры, то требует затрат энергии.
Источником такой энергии является энергия АТФ.
Также для биосинтеза некоторых веществ требуются богатые энергией
атомы водорода – их источником является НАДФН.
Катаболизм – расщеплениеиокислениесложныхорганическихмолекулдоболее простых
конечных продуктов.
Оно сопровождается высвобождением энергии, заключенной в сложной структуре веществ.
Большая часть высвобожденной энергии рассеивается в виде тепла.
Меньшая часть этой энергии "перехватывается" коферментами окислительных реакций
НАД и ФАД, некоторая часть сразу используется для синтеза АТФ. 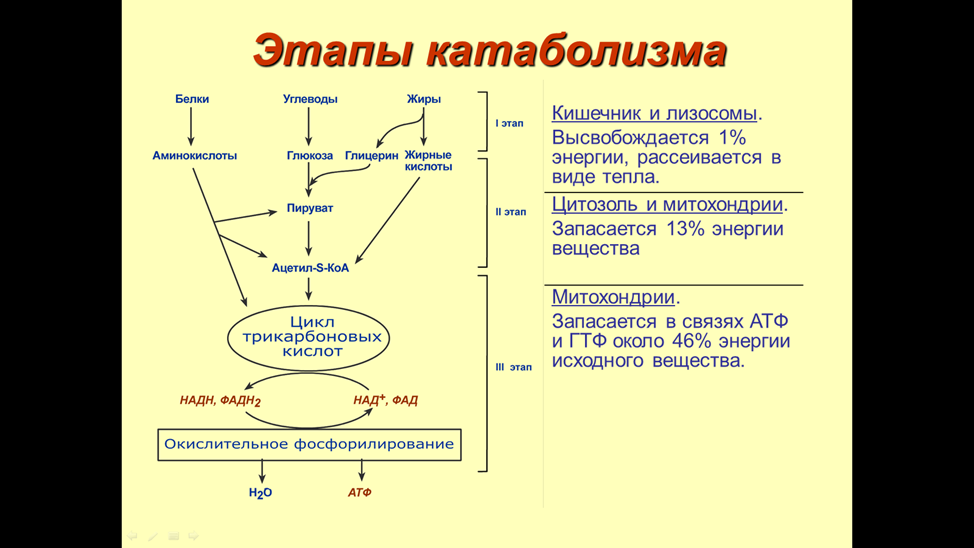
Общий путь катаболизма — совокупность биохимических процессов, которая включает в себя:
- окисление пирувата до ацетил-КоА;
- окисление ацетил-КоА в цикле трикарбоновых кислот
- выделение и аккумулирование энергии при дегидрировании метаболитов общего пути катаболизма в митохондриальных цепях переноса электронов[1].
Именно в общем пути катаболизма образуется основная масса субстратов для реакций дегидрирования. Совместно с дыхательной цепью и окислительным фосфорилированием общий путь катаболизма является основным источником энергии в форме АТФ.
Специфический путь катаболизма – совокупность биохимических процессов, которая включает в себя:
- Расщепление полимеров до мономеров (белки – в аминокислоты, углеводы в моносахариды, липиды – в глицерол и жирные кислоты). Химическая энергия при этом рассеивается в виде тепла.
- Расщепление мономеров на общие продукты, в подавляющем большинстве в ацетил-КоА. Химическая энергия частично рассеивается в виде тепла, частично накапливается в виде восстановленных коферментных форм (НАДН, ФАДН2), частично запасается в макроэргических связях АТФ (субстратное фосфорилирование).
2. Каким образом регулируется окислительное фосфорилирование? Назовите и охарактеризуйте ингибиторы окислительного фосфорилирования.
Окислительное фосфорилирование регулируется дыхательным контролем. 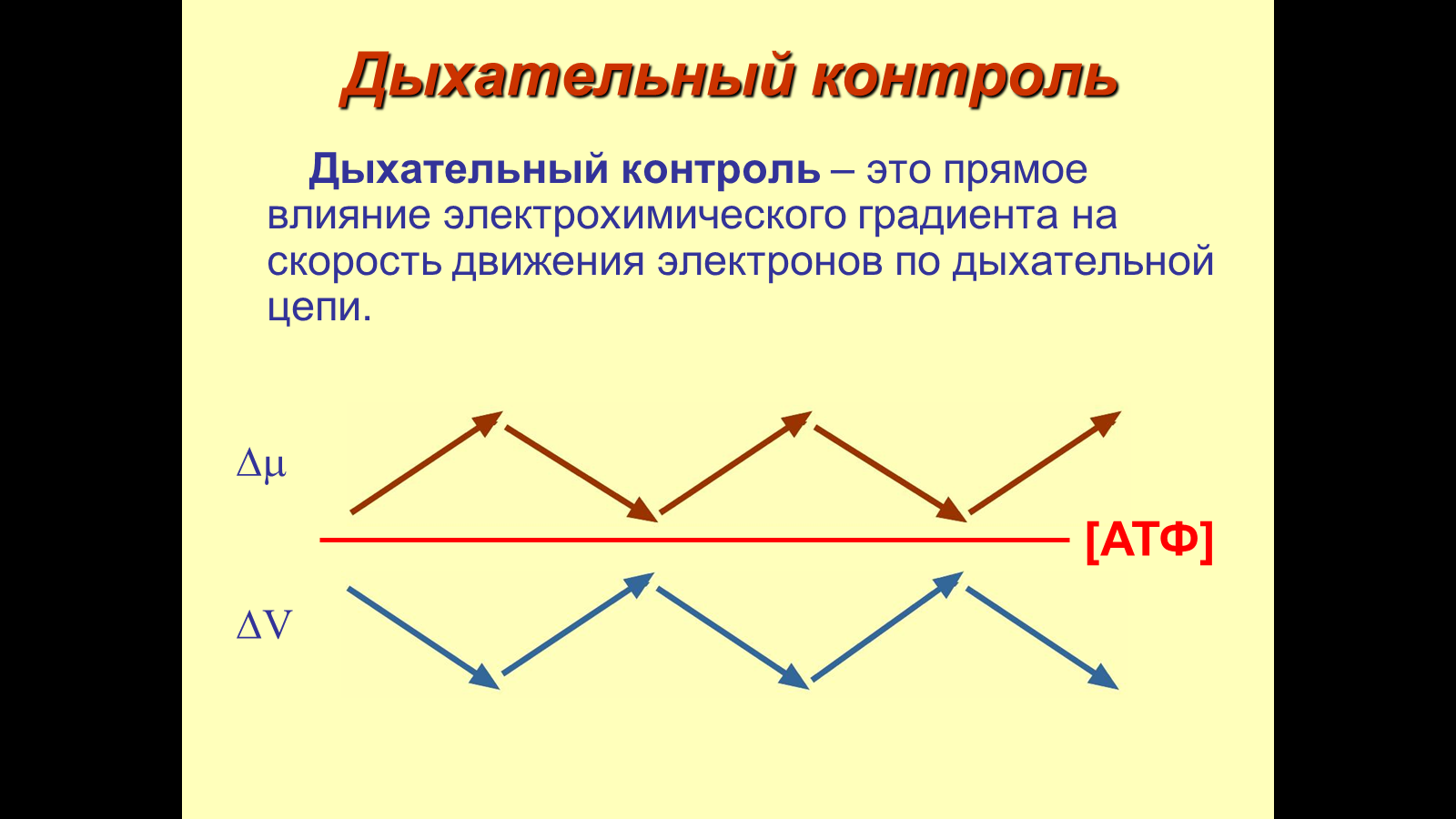
Величина градиента напрямую зависит от соотношения АТФ и АДФ, количественная сумма которых в клетке постоянна
[АТФ] + [АДФ] = const
Возрастание протонного градиента возникает при отсутствии АДФ и накоплении АТФ, т.е. когда АТФ-синтаза лишена своего субстрата и ионы Н+ не проникают в матрикс митохондрии.
При этом ингибирующее влияние градиента усиливается и продвижение электронов по цепи замедляется.
Снижение протонного градиента возникает при наличии АДФ и прохождении ионов Н+ через канал Fо в матрикс. В этом случае:
- протонный градиент снижается,
- скорость потока электронов возрастает,
- усиливается выкачивание ионов Н+ в межмембранное пространство,
- увеличивается окисление НАДН и ФАДН2 (как источников электронов),
- снимается ингибирующее влияние НАДН на цикл лимонной кислоты и ПВК-дегидрогеназу.
Итог: активация реакций катаболизма углеводов и жиров как источника энергии
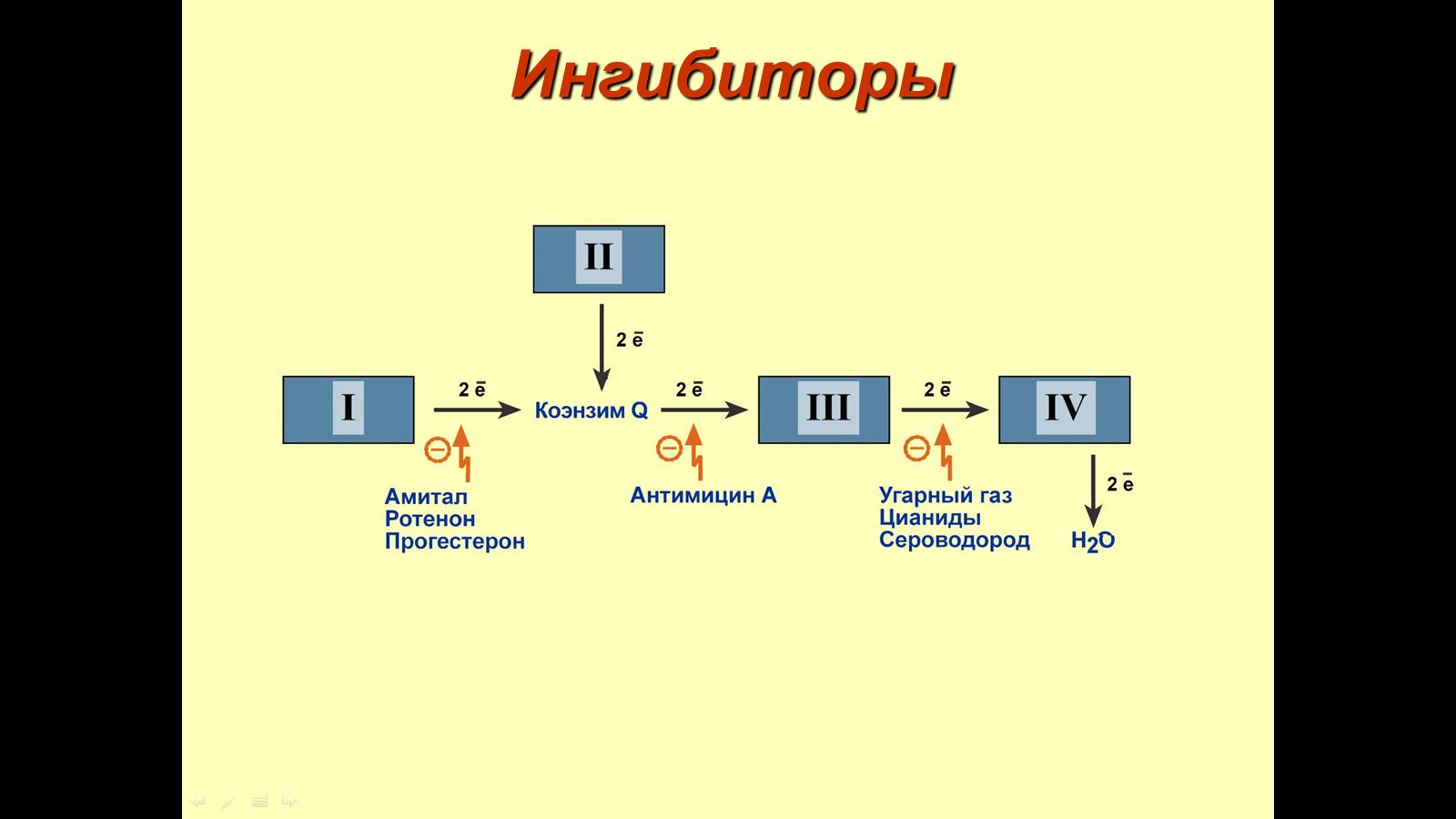
Ингибиторы блокируют ферменты дыхательной цепи и замедляют движение электронов от НАДН и ФАДН2 на кислород.
Три основные группы ингибиторов:
- действующие на I комплекс, например, амитал, ротенон, прогестерон,
- действующие на III комплекс, например, антимицин А,
- действующие на IV комплекс, например, сероводород (H2S), угарный газ (СО), цианиды (-CN).
3.Поясните пути и напишите неферментативные реакции образования активных форм кислорода. Что такое “утечка” электронов из ферментативных реакций? 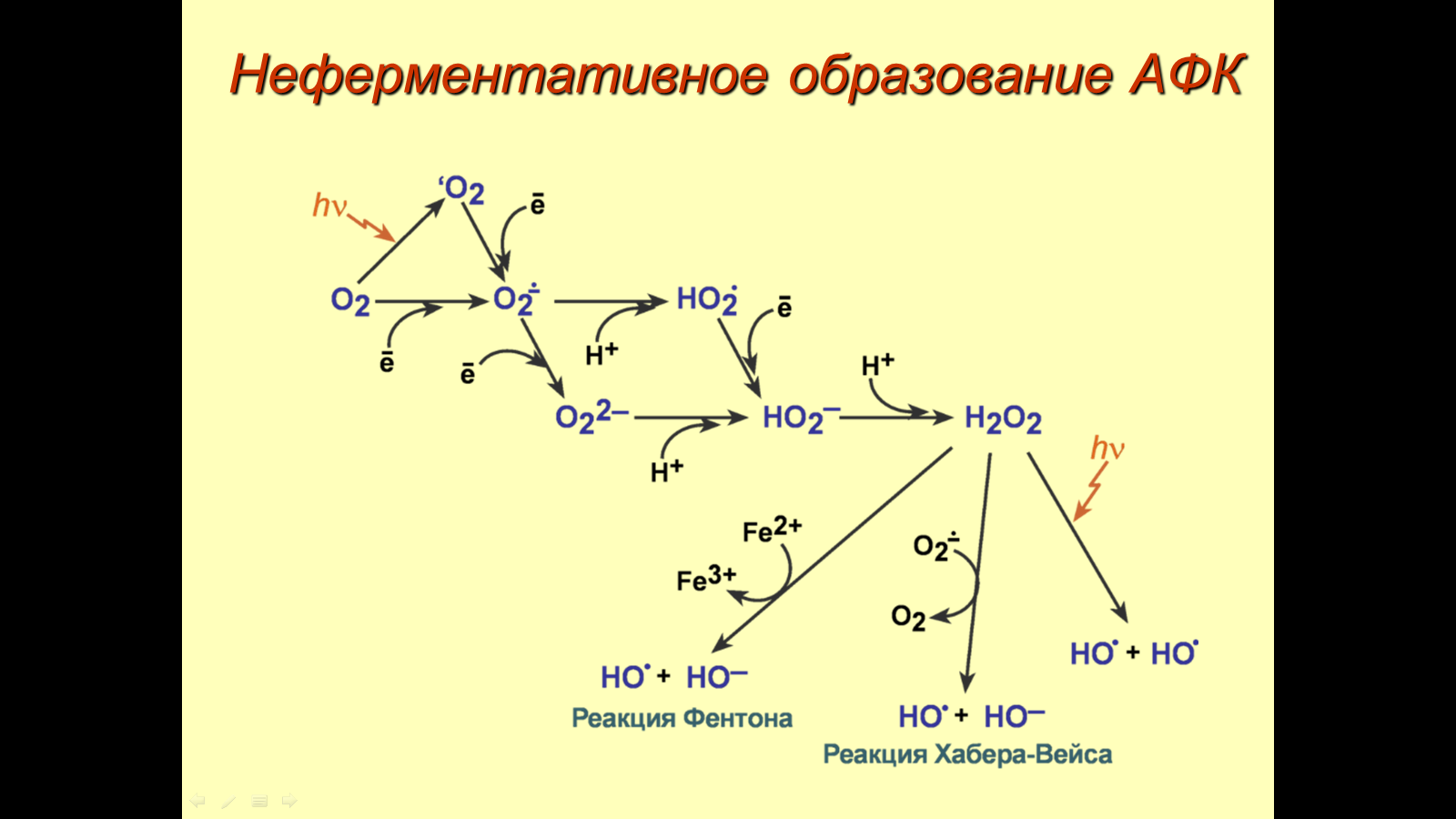
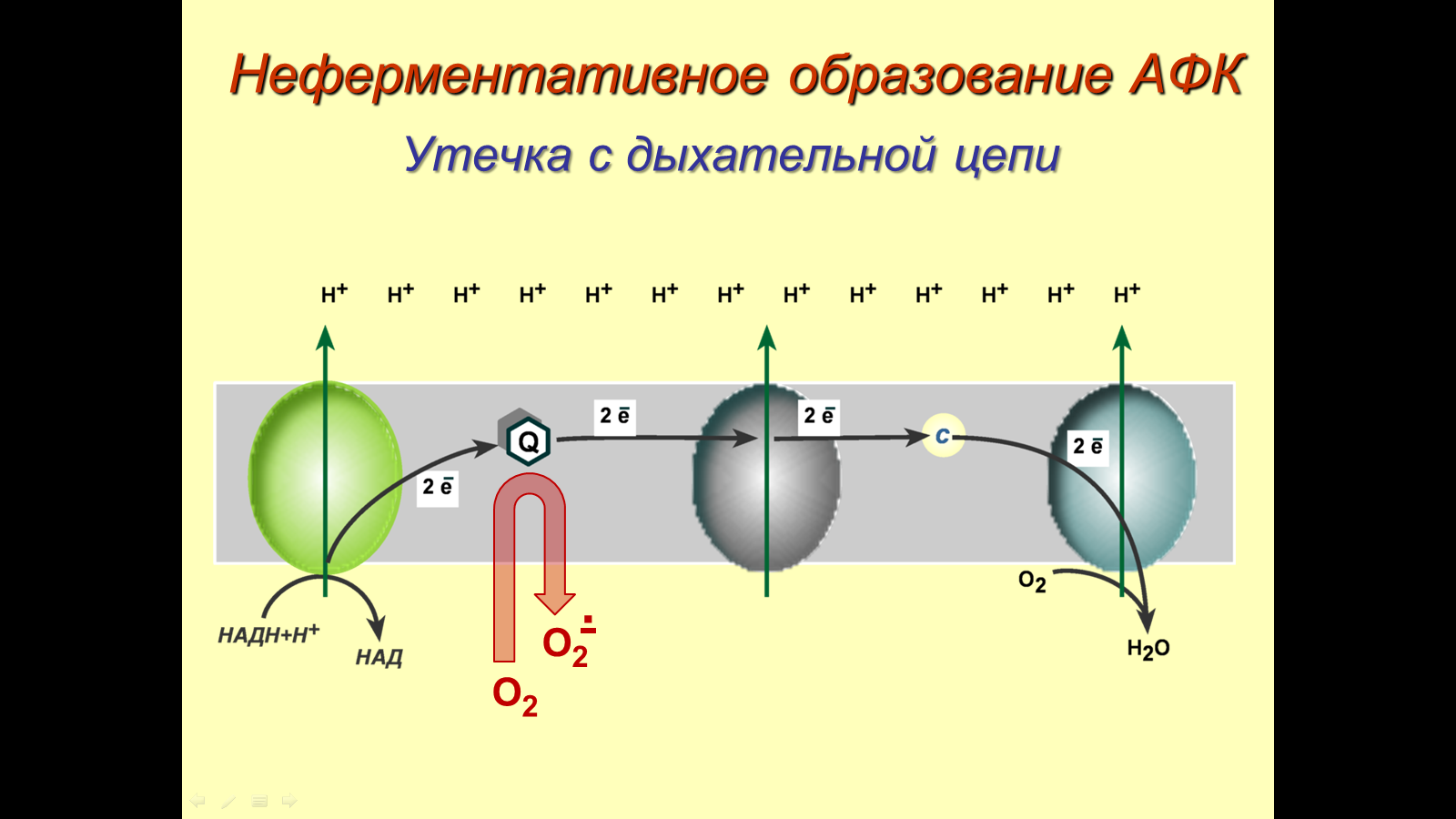
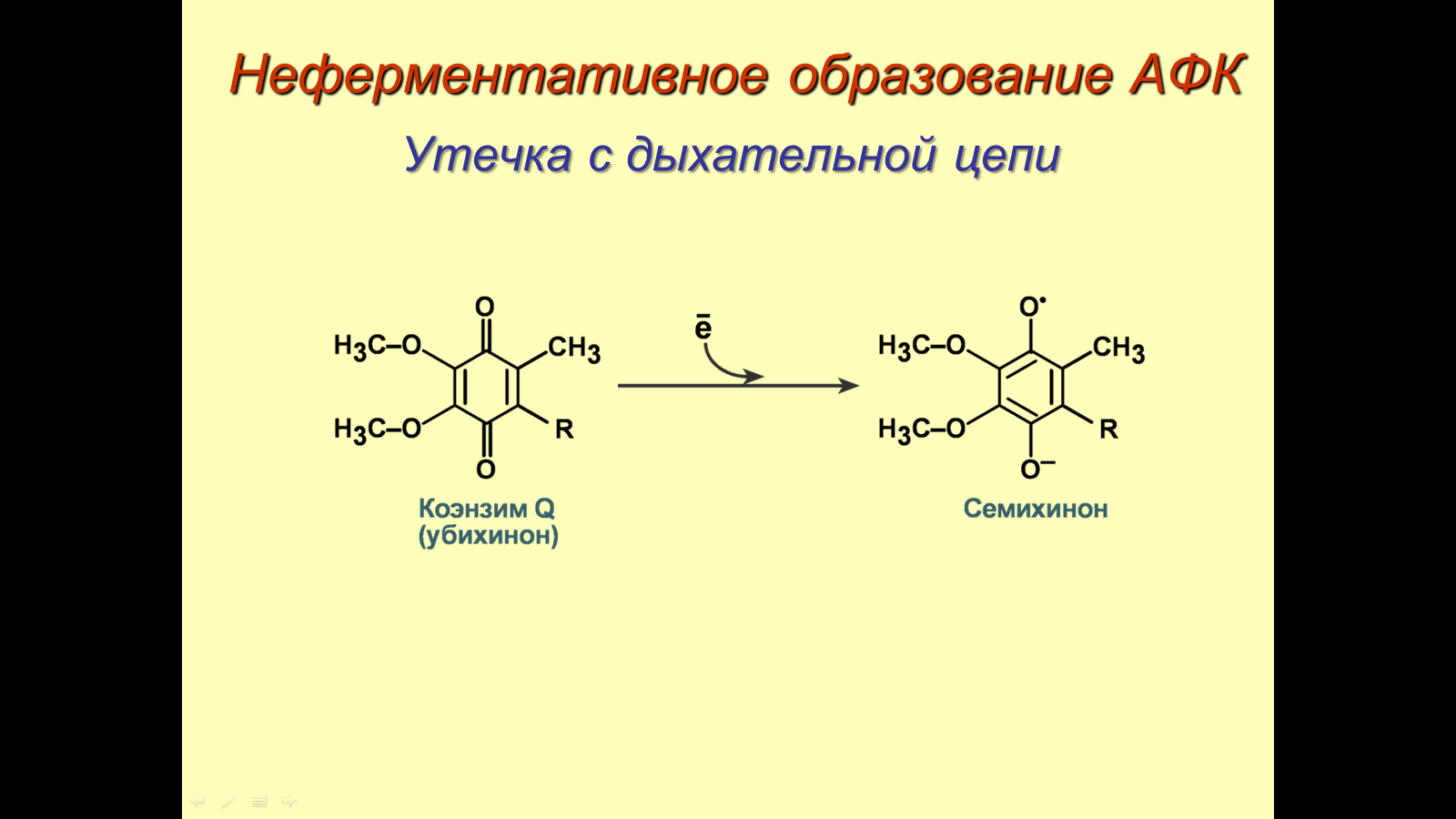
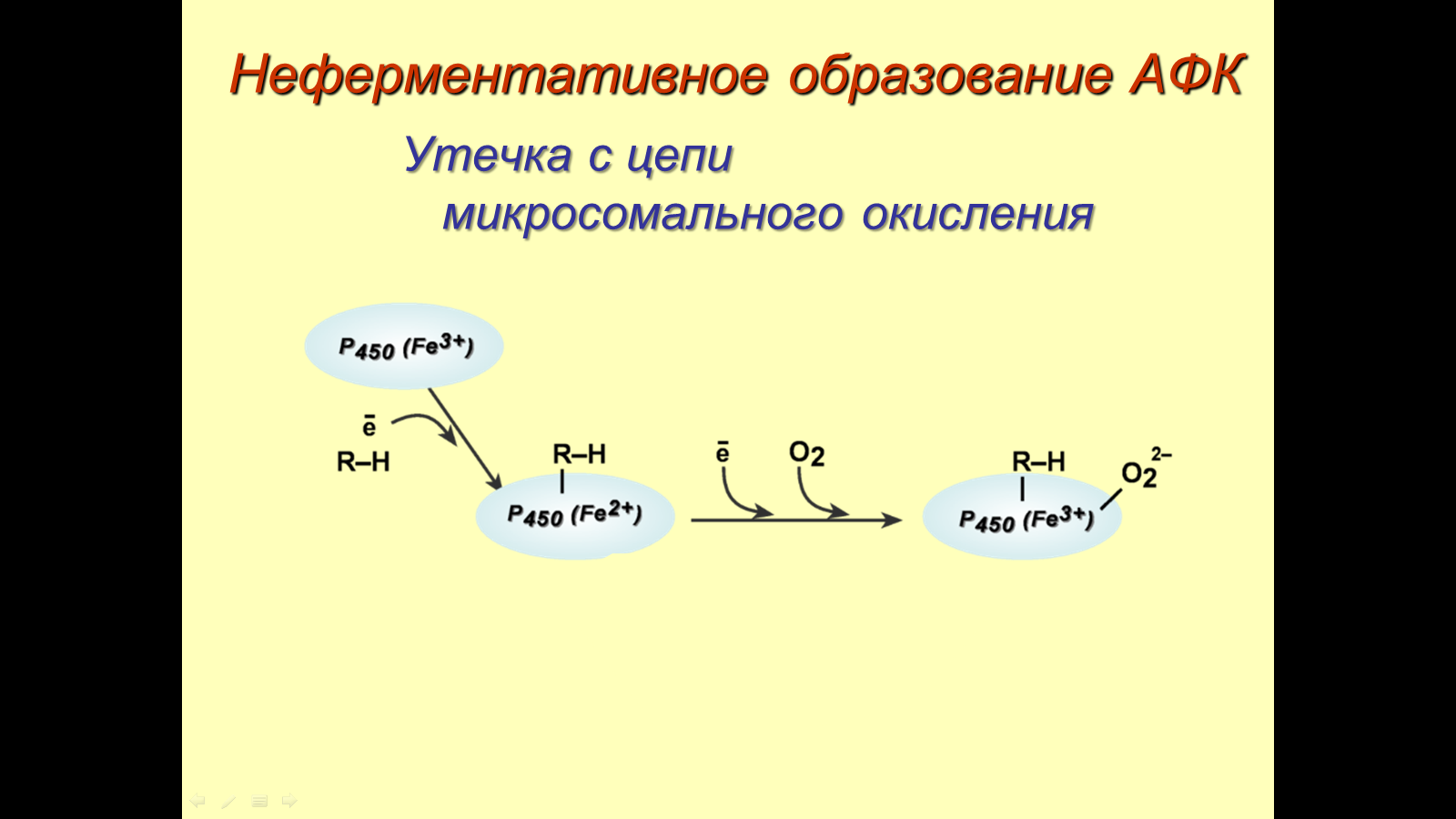
 Утечка электронов из ферментативных реакций – захват электронов из ферментативных реакций с образованием активных форм кислорода
Утечка электронов из ферментативных реакций – захват электронов из ферментативных реакций с образованием активных форм кислорода
БИЛЕТ 16.
1. Напишите последовательность реакций цикла трикарбоновых кислот. Поясните анаболические функции цикла трикарбоновых кислот. Отметьте анаплеротические реакции и их значение.
Последовательность реакций ЦТК:
1. 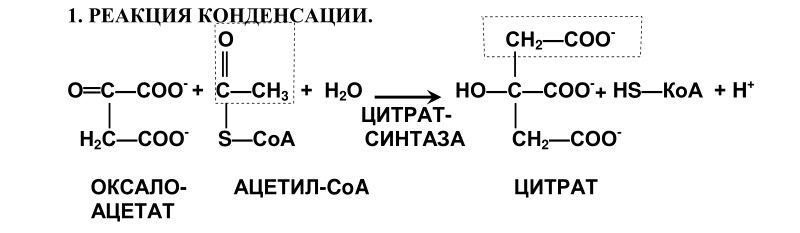 Реакция конденсации
Реакция конденсации
2. Превращение цитрата в изоцитрат. 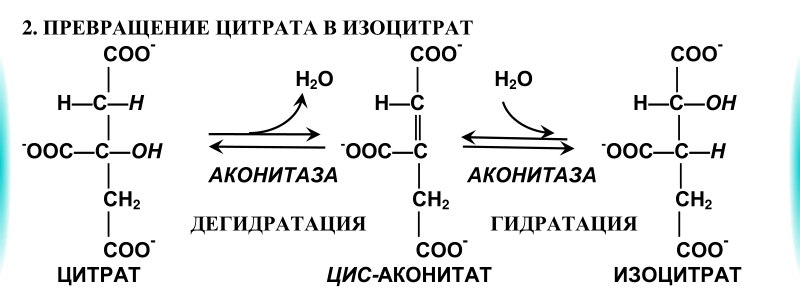
3. Реакция окислительного декарбоксилирования изоцитрата 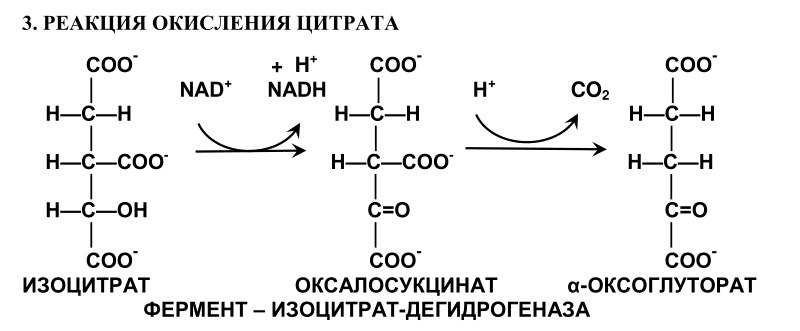
4. Окислительное карбоксилирование α-кетоглутарата 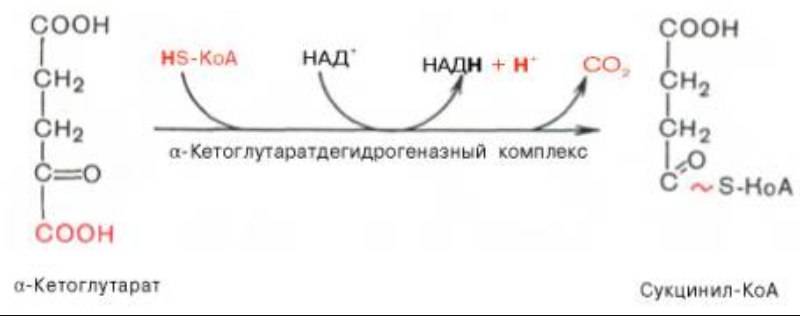
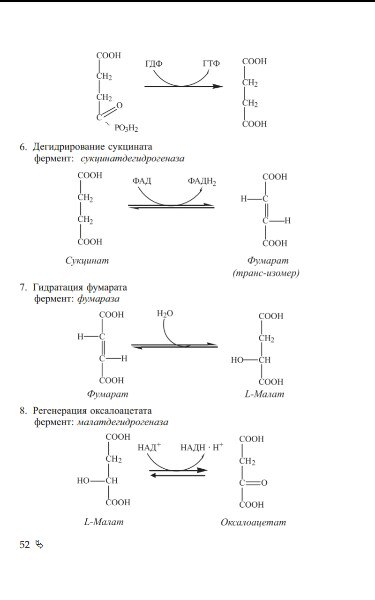
5. Реакция субстратного фосфорилирования 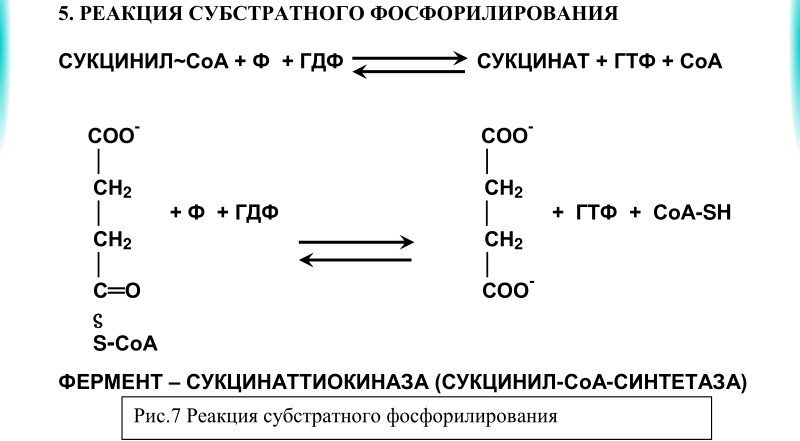
6. Реакция дегидрирования (оксиления) сукцината
7. Реакция гидратации фумарата
8. Реакция дегидрирования малата (регенерация оксалоацетата) 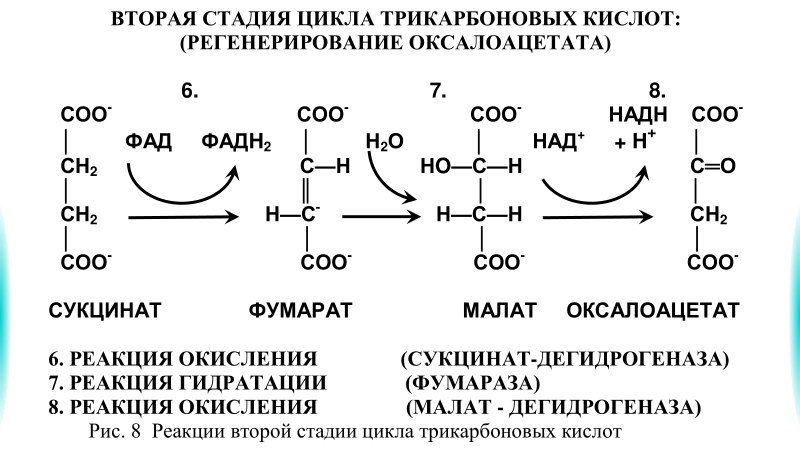
Анаболическая функция ЦТК заключается в том, что некоторые промежуточные продукты ЦТК: α-кетоглутарат, сукцинат, оксалоацетат могут использоваться для синтеза заменимых аминокислот путем трансаминирования.
Реакции, обеспечивающие пополнение фонда промежуточных продуктов ЦТК, называются анаплеротическими(пополняющими). Важнейшая из них – реакция синтеза оксалоацетата из пирувата.(фермет - пируваткарбоксилаза). 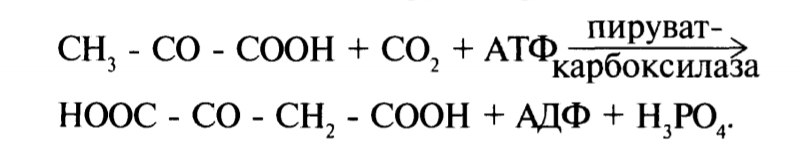
Метаболиты ЦТК являются донорами водорода для образования восстановленных коферментов, участвующих в реакциях синтеза жирных икслот, стероидов и других веществ. Малат и изоцитрат обеспечивают образование около половины общего фонда NADPH, испольщуемого в восстановительных синтезах. Пр.: образование малата в цитозоле клетки, реакцию катализирует NADP-зависимая дегидрогеназа(малик-фермент):
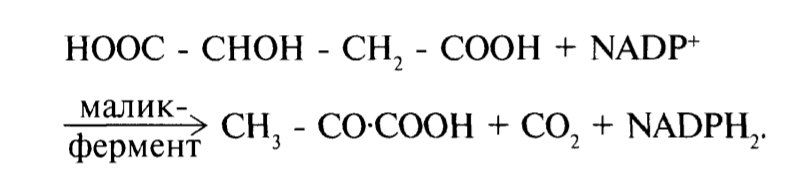
2. Поясните механизмы разобщения и окисления и фосфорилирования и его физиологическое значение. Назовите и охарактеризуйте вещества-разобщители.
Некоторые химические вещества (протонофоры) могут переносить протоны или другие ионы (ионофоры) из межмембранного пространства чрез мембраны в матрикс, минуя протонные каналы АТФ_синтазы. В результате этого исчезает электрохимический потенциал и прекращается синтез АТФ. Это явление называется разобщением дыхания и фосфорилирования. В результате разобщения количество АТФ снижается, а АДФ увеличивается. В этом случае скорость окисления NADH и FADH2 возрастает, возрастает и количество поглощенного кислорода, но энергия выделяется в виде тепла, и коэффициент P/O резко снижается. Т.о., разобщители – это вещества, которые снижают величину электрохимического градиента, что приводит к увеличению скорости движения электронов по ферментам дыхательной цепи, в результате чего уменьшается синтез АТФ и возрастает катаболизм. Как правило, разобщители – лиофильные вещества, легко проходящие через липидный слой мембраны. Протонофоры уменьшаются и химический, и электрический компоненты электрохимического градиента. К ним относят динитрофенол, присоединяющий ионы водорода на внешней поверхности митохондриальной мембраны и отдающих их на внутренней поверхности. Липолиз в бурой жировой ткани приводит к активизации работы дыхательной цепи и возрастанию электрохимического градиента, но благодаря белку термогенину (физиологический протонофор) бОльшая часть энергии ионов водорода рассеивается в виде тепла, обеспечивая поддержание температуры тела при охлаждении. Также к протонофорам относятся салицилаты, жирные кислоты и трийодтиронин.
3. Поясните причины активации свободнорадикальных процессов при ишемии и гипоксии. Какова роль этих процессов в повреждении тканей?
Образование АФК при ишемии:
1. Конверсия ксантиндегидрогеназы в ксантиноксидазу, способную активно продуцировать АФК при окислении пуринов.
2. Выброс катехоламинов при болевом синдроме и их окисление в адренохром, что сопровождается образованием АФК.
3. Необратимое ингибирование активности антиоксидантных ферментов (СОД и GSH-пероксидазы) вследствие накопления АФК.
4. Активация нейтрофилом продуктами фосфолиполиза и протеолиза (при некрозе), что способствует началу «респираторного взрыва» и приводит к гиперпродукции свободных радикалов
Механизм повреждающего действия свободных радикалов заключается в:
А)первичные механизмы повреждающего действия
1. Деструкции жирных кислот фосфолипидов (липоперекиси, эндоперекиси).
2. Повреждение белков (образование шиффовых оснований, окисление тиоловых групп – инактивация тиоловых ферментов, транскрипционных факторов)
3. Повреждение ДНК – мутации, нарушение репарации.
Б)вторичные механизмы
1.Повышение проницаемости мембран (нарушение мембранных потенциалов, разобщение окислительного фосфорилирования)
2. Повреждение лизосом – аутолиз клеток.
3. Повышение микровязкости мембран и нарушение активности мембранных рецепторов, мембранных ферментов, мембранного транспорта.
4. Канцерогенез.
Билет 17
1. В процессе окислительного декарбоксилирования принимают участие ферменты: пируватдегидрогеназа (E1), дегидролипоат-ацетилтрансфераза (E2), дигидролипоат-дегидрогеназа (E3), фосфатаза, киназа; коферменты: ТДФ, липоевая кислота, ФАД, НАД, КоА.
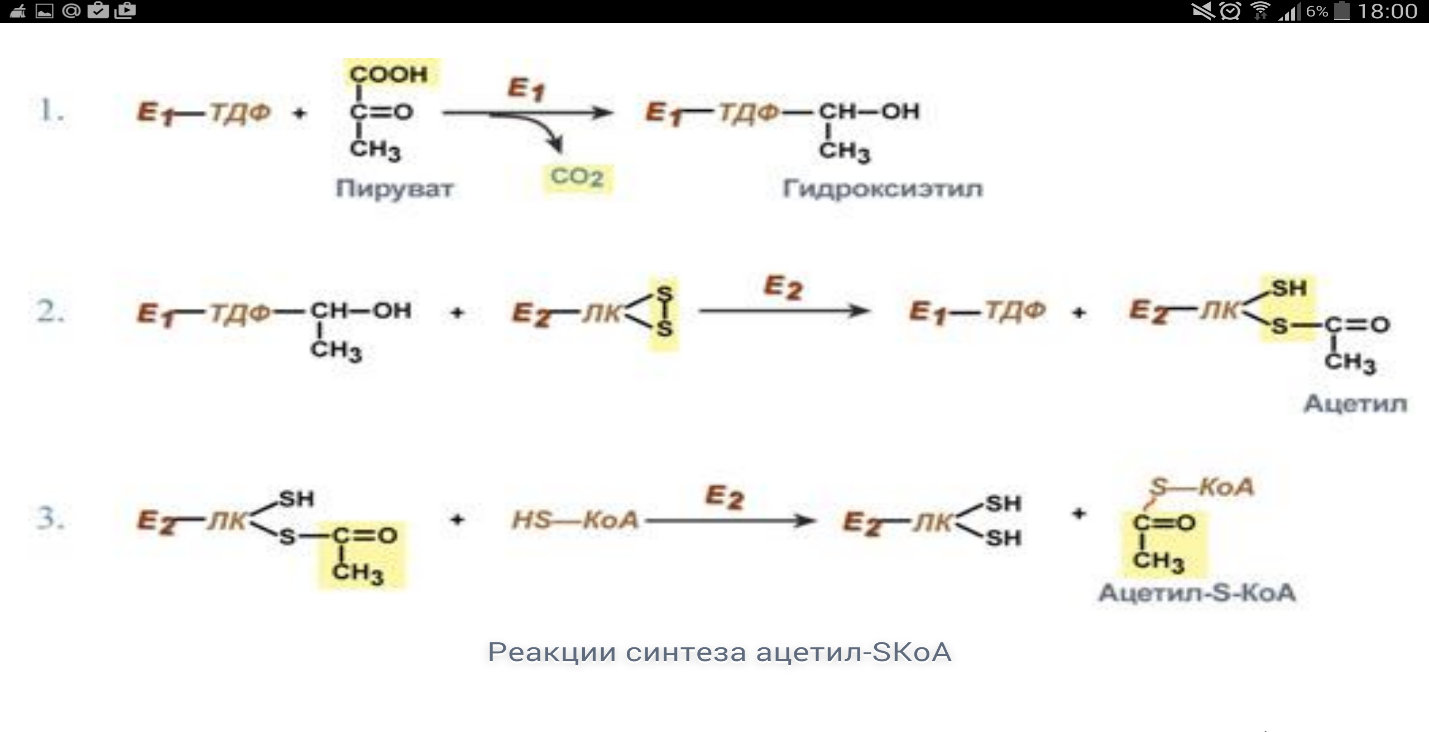
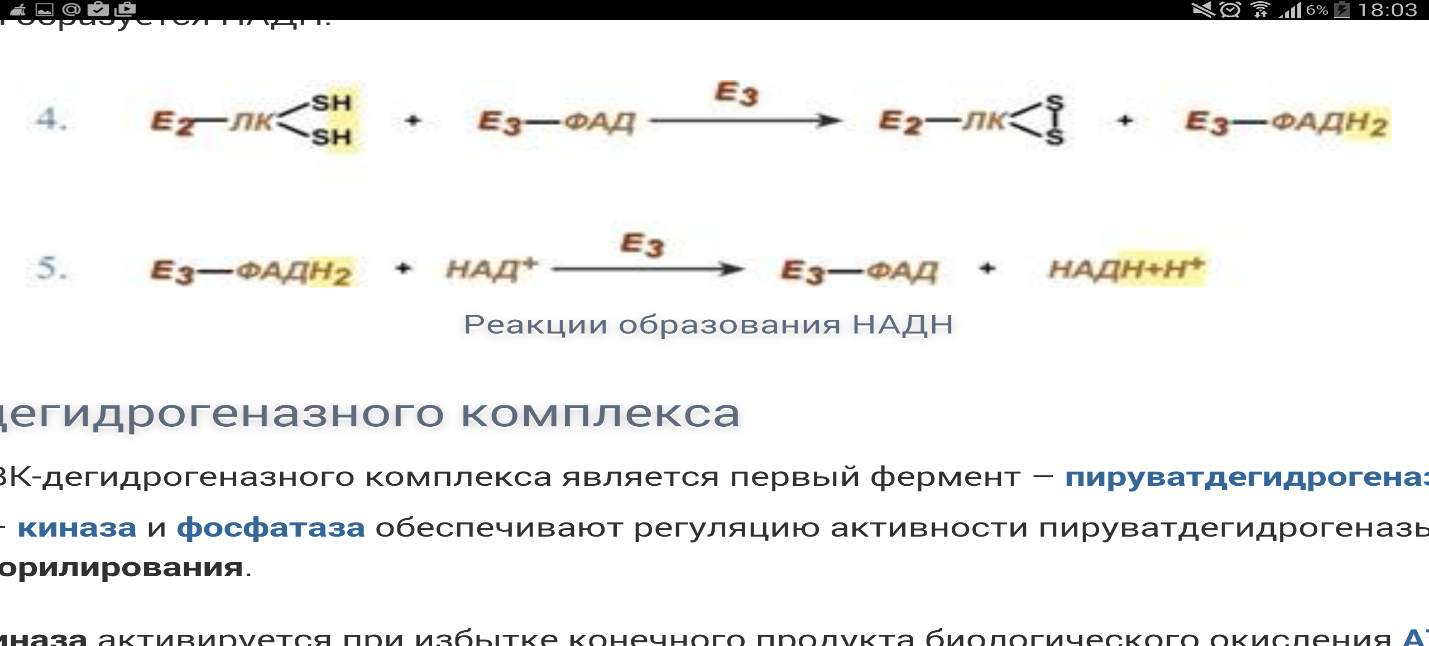
Ферменты цикла трикарбоновых кислот: цитратсинтаза, аконитаза, изоцитратдегидрогеназа, альфа-кетоглутаратдегидрогеназа, сукцинаттиокиназа, сукцинатдегидрогеназа, фумараза, малатдегидрогеназа.
2. Окислительное фосфорилирование регулируется с помощью дыхательного контроля.
Дыхательный контроль- это прямое влияние электрохимического градиента на скорость движения электронов по дыхательной цепи. Величина градиента напрямую зависит от соотношения АТФ и АДФ.
Работа механизма дыхательного контроля:
1.если АТФ не используется и его концентрация в клетках возрастает, то прекращается и поток электронов к кислороду;
2.расход АТФ и превращение его в АДФ увеличивает окисление субстратов и поглощение кислорода
3. 
К активным формам кислорода относят:
Активные формы кислорода бразуются во многих клетках в результате последовательного присоединения 4 электронов к 1 молекуле кислорода.

Образование активных форм кислорода:

Пероксид водорода способствует образованию гидроксильного радикала:
Билет 18
1 ) Опишите строение пируватдегидрогеназного комплекса. Как регулируется пируватдегидрогеназный комплекс? Дайте характеристику витаминов и коферментов, используемых в процессе.
Строение пируватдегидрогеназного комплекса. Пируватдегидрогеназный комплекс состоит из 512 субъединиц объединенных в сложный мультиферментный комплекс. В его состав входят 3 фермента: пируватдегидрогеназа (Е1), дигидролипоамидацилтрансфераза (Е2) и дигидролипоамиддегидрогеназа (Е3), а также 5 коферментов: тиаминдифосфат (ТДФ), липоевая кислота (связанная через свою карбоксильную группу с ε- аминогруппой лизина, входящего в состав фермента – дигидролипоамидацилтрансферазы, и далее называемая липоамид), ФАД, НАД+ и СоА. Три кофермента (ТДФ, липоамид и ФАД) ковалентно связаны в активных центрах ферментов Е1, Е2 и Е3 соответственно, а НАД+ и СоА выполняют роль вто- рых субстратов в химических реакциях (мигрирующие коферменты).
Особенностью ферментов и белков комплекса является то, что все ферменты и белковые компоненты мультиферментного комплекса кодируются в ядерной ДНК и синтезируются в цитозоле. После их поступления в митохондриальный матрикс (при этом затрачивается энергия АТФ и протонного градиента) они подвергаются финальному фолдингу с помощью митохондриальных шаперонов, приобретают функциональную активность и объединяются в мультиферментный комплекс.
В этом комплексе происходит преобразование пирувата в ацетил-СоА, содер жащий макроэргическую тиоэфирную связь и удаление из пирувата 2-х электронов в составе молекулы НАДН.
Активность ПДК регулируется различными способами:
- доступностью субстратов;
- ингибированием продуктами реакции- Продукты пируватдегидрогеназной реакции аллостерически активируют киназу ПДК. Активированная киназа фосфорилирует и инактивирует ферменты комплекса. Таким образом, при накоплении НАДН и ацетил-СоА тормозится превращение пирувата в ацетил-СоА;
-аллостерическим путѐм- Пируват аллостерически активирует нефосфорилиро- ванную форму ПДК, действуя согласно с другими субстратами НАД+ и СоА;
-путѐм ковалентной модификации- Осуществляется фосфорилированием и дефосфорилированием. В состав ПДК входят 2 регуляторных субъединицы: киназа ПДК – фосфорилирует ферменты комплекса и инактивирует ПДК; а фосфатаза – дефосфорилирует ферменты, превращая ферментативный комплекс в активную форму.
Активность пируватдегидрогеназного комплекса увеличивается при повышении концентрации АДФ, внутриклеточного кальция, под влиянием гормонов: инсулина и адреналина.
2 ) Назовите и охарактеризуйте макроэргические субстраты. Напишите строение АТФ. В каких реакциях общих путей катаболизма образуются макроэргические соединения?
Макроэргические соединения – соединения, содержащие макроэргическую связь, при гидролизе которой освобождается энергия больше чем 30 кДж/моль.
К клеточным макроэргическим соединениям относят фосфоенолпируват, 1,3-дифосфоглицерат, которые образуются в гликолизе (в процессе распада глюкозы до пирувата). К ним относят также сукцинил~СоА (образуется в цикле трикарбоновых кислот, переносит фосфатную группу на ГДФ) и креатинфосфат, являющиеся субстратами, так называемого субстратного фосфорилирования, при котором их макроэргическая связь используется для синтеза АТФ.
Макроэргическими соединениями являются также ацил~СоА и все со- единения, содержащие сложную тиоэфирную группу, а также карбамоилфосфат (образуется в первой реакции цикла мочевины) и аргининфосфат, гистидинфосфат (имидазолфосфат) и все нуклеозиддифосфаты и нуклеозитрифосфаты.
Эти молекулы обладают большим потенциалом переноса фосфатной группы на АДФ с образованием АТФ, потому что энергия, выделяемая при распаде этих макроэргических молекул более высокая, чем требуется для синтеза АТФ из АДФ. По отношению к АДФ, перечисленные макроэргические молекулы доноры энергии.
В молекуле аденозинтрифосфорной кислоты (АТФ) две высокоэнергетические (макроэргические связи) β и γ.
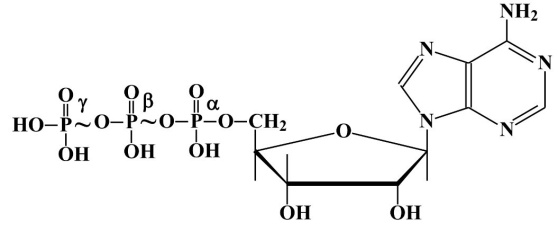
Одним из источников нуклеозидтрифосфатов, главным образом АТФ, является субстратное фосфорилирование. К таким реакциям относятся реакции гликолиза:
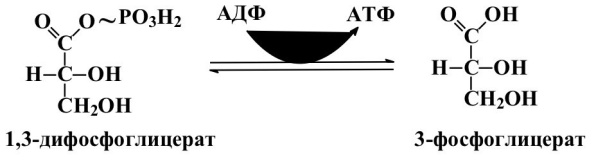
И вторая реакция субстратного фосфорилирования АДФ с образовани- ем енольной формы пирувата и АТФ, протекающая под действием фермента пируваткиназы:
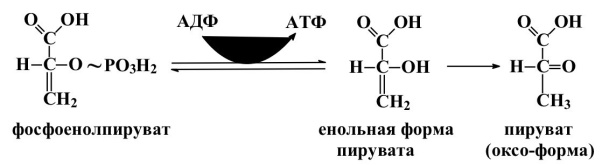
В мышцах в процессе мышечного сокращения активно протекает еще одна реакция субстратного фосфорилирования, катализируемая креатинфос- фаткиназой.
Для эукариотов глав- ным источником АТФ является окислительное фофорилирование, использу- ющее энергию электронов, освобождающихся при дегидрировании субстра- тов, при восстановлении кислорода, через реализацию трансмембранного протонного градиента потенциала.
3. Напишите ферментативные реакции образования пероксида водорода. Какова дальнейшая судьба и роль пероксида водорода?
Пероксид водорода образуется с помощью фермента супероксидазы из:
а) диоксида 2∙О2- + 2H+ → Н2О2 + О2
б) протонированной формы диоксида 2 НО2∙ → Н2О2 + О2
Пероксид водорода не является радикалом и, будучи нейтральной молекулой, легко проникает через гидрофобные мембраны. Токсические эффекты перекиси водорода проявляются при концентрации более 5х10^-5, которая наблюдается в очагах воспаления благодаря активации фагоцитирующих клеток. Пероксид водорода занимает особое место в генерации АФК в лейкоцитах для уничтожения инфицирующих микроорганизмов.
Н2О2 в присутствии миэлопероксидазы и перксидазы эозинофилов служит источником гипогалогенидов (например, HClO), которые тоже токсичны и подавляют микрофлору:
HCl + Н2О2 → HClO + H2O
В организме пероксид водорода постоянно разрушается за счет ферментов каталазы
(2Н2О2 → 2Н2О +О2) и пероксидазы (SH2 + Н2О2 → S + 2H2O).
Свободно проникая внутрь клетки, перокисид водорода взаимодействует с ионами металлов (железо, медь), в результате чего образуется гидроксид-радикал (гидроксильный радикал) НО∙:
Н2О2+ Cu+ → Cu2+ + ОН- + НО∙
Билет 19
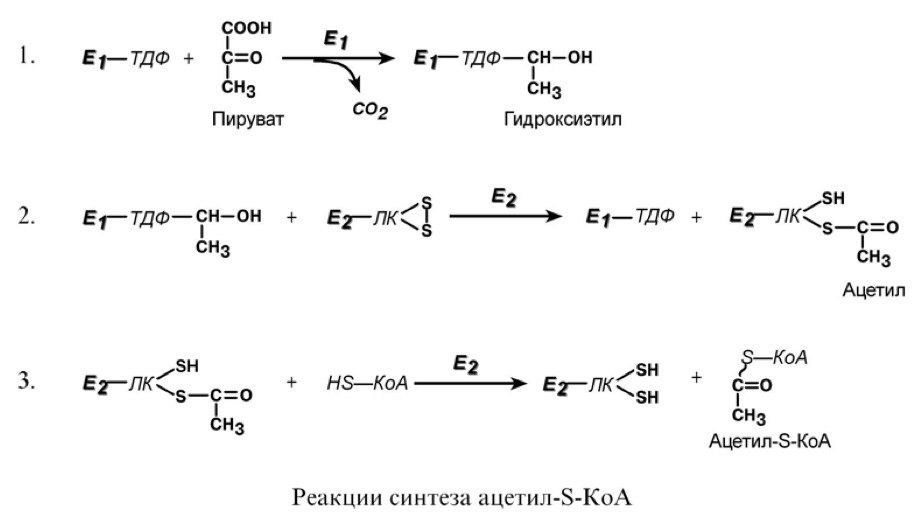
1 ) Напишите суммарную и отдельные реакции окислительного декарбоксилирования пирувата.
Суммарное уравнение реакции отражает декарбоксилирование пирувата, восстановление НАД до НАДН и образование ацетил-S-KoA.
Суть первых трех реакций сводится к декарбоксилированию пирувата (катализируется пируватдегидрогеназой, Е1), окислению пирувата до ацетила и переносу ацетила на коэнзим А.
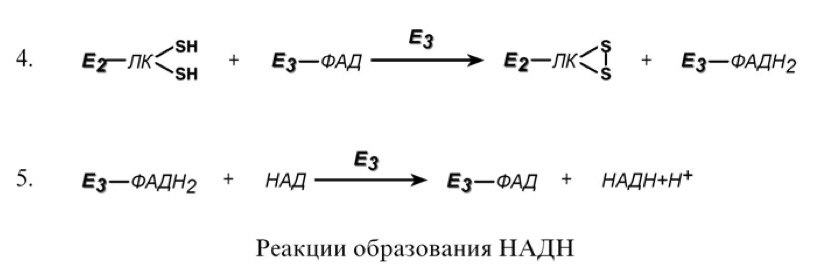
Оставшиеся 2 реакции необходимы для возвращения липоевой кислоты и ФАД в окис- ленное состояние (катализируются дигидролипоат-дегидрогеназой, Е3). При этом образуется НАДН.
2) Дайте характеристику митохондриям, их функции и дисфункции. Что такое митохондриальные болезни? Укажите причины и развитие гипоэнергетических состояний.
Функции митохондрий.
1) Оксидазный путь использования кислорода в клетке: протекает в митохондриях, потребляет 90% О2 и обеспечивает процесс окислительного фосфорилирования.
2) Ферментативная функция – большинство ферментов в клетке связаны с мембранами. Например, в мембранах митохондрий сосредоточены ферменты дыхательной цепи, в мембранах эндоплазматического ретикулума – ферменты обмена ксенобиотиков, синтеза белка и т.д.
3) Энергоспрягающая функция – мембраны митохондрий превращают энергию градиента концентрации протонов в энергию связей АТФ.
4) В присутствии О2, митохондрии выкачивают ПВК и НАДН2 из цитоплазмы, прерывая реакцию образования лактата. При аэробном окислении из 1 глюкозы образуется 38 АТФ, соответственно для образования достаточного количества АТФ необходимо мало глюкозы (в 19 раз меньше чем в анаэробных условиях).
Дисфункции митохондрий
Известно, что митохондрии играют доминирующую роль в обеспечении тканей организма энергией, генерации супероксид - радикала, реализации механизмов программированной гибели клетки и участвуют в депонировании внутриклеточных ионов Са2+. Это определяет центральную роль митохондрий в развитии многих патологических процессов.
Приобретенные нарушения митохондриальных функций при различных патологических процессах, возникают преимущественно как следствие повреждения митохондриальных структур под влиянием свободно-радикальных процессов, активизации механизмов деградации митохондрий, стимуляции апоптогенных сигналов, увеличения концентрации ионов кальция в цитоплазме клеток органов-мишеней.
Наиболее распространенными факторами являются нарушения липидного обмена, гипергликемия, формирование белковых агрегатов в клетках, ишемии\реперфузии, токсических повреждениях. Существуют наследственные заболевания, ассоциированные с врожденными мутациями в митохондриальном геноме.
Основным следствием нарушения энергетического обмена в митохондриях является нарушение синтеза АТФ и подавление β-окисления липидов. Показано, что существует определенный пороговый уровень снижения внутриклеточного содержания АТФ, после достижения которого, начинается резкое подавление любых энергозатратных процессов в клетке.
Известно, что нарушение переноса электронов между компонентами дыхательной цепи сопровождается генерацией митохондриями супероксидного радикала. Он способствует активизации процессов перекисного окисления липидов, оксидативных повреждений белков и нуклеиновых кислот. Увеличение митохондриями активных форм кислорода может оказать на клетку не только повреждающий, но и иррегуляторный эффект.
Механизм повреждающего действия активных форм кислорода на клетки.
Наиболее серьезными следствием токсического действия активных форм кислорода являются:
1. Выраженная активация свободнорадикального перекисного окисления липидов;
2. Повреждение ДНК и РНК
3. Повреждение белков, в том числе и белков - ферментов.
По существу эти три события и составляют молекулярную основу окислительного стресса.
Избыточная активация перекисного окисления липидов, происходящая главным образом, в клеточных и субклеточных мембранах, приводит к глубокому нарушению их структуры и функции.
Для защиты организма от повреждающего действия активных форм кислорода, особенно, от кислородных радикалов, существует так называемая антиоксидантная система.
Схема повреждения клетки свободными радикалами в результате ПОЛ (Перекисная теория гибели клеток):
1. Формирование активных форм кислорода, прежде всего гидроксильного радикала – OH•, обладающего максимальной реактогенностью, под влиянием различных инициирующих факторов инфекционной и неинфекционной природы.
2. Извлечение водорода из боковых цепей ненасыщенных жирных кислот с образованием углеродсодержащего радикала и воды.
3. Взаимодействие углеродсодержащего радикала с молекулярным кислородом с образованием перекисного радикала:
RCOORC + O2 > RCOO.
4. Извлечение водорода из белковой цепи ненасыщенных жирных кислот пероксидным радикалом с образованием липидной гидроперекиси.
Состояния, при которых синтез АТФ снижен, объединяют термином "гипоэнергетические". Причинами гипоэнергетических состояний могут быть голодание, гиповитаминозы В1, РР, В2; гипоксия. Гипоксия может возникнуть: при недостатке кислорода во вдыхаемом воздухе; при заболеваниях лёгких и нарушении лёгочной вентиляции; при нарушениях кровообращения, вызванных заболеваниями сердца, спазмом и тромбозом сосудов, кровопотерей. Причинами гипоксии могут быть также наследственные или приобретенные нарушения структуры гемоглобина. Частой причиной гипоэнергетических состояний могут быть нарушения процессов использования кислорода в клетках. Причинами этих нарушений могут быть:
• действие ингибиторов и разобщителей в ЦПЭ;
• железодефицитные анемии;
• снижение уровня гемоглобина и других железосодержащих белков (цитохромов, FeS-белков), в результате чего нарушаются перенос электронов и синтез АТФ;
• наследственные дефекты ферментов ЦПЭ и цитратного цикла.
3) Ферментативные реакции образования супероксид анион-радикала, активных форм азота и хлора. Какова дальнейшая судьба и роль этих активных ферментов?
а) образование супероксид анион-радикала
не обладает сильными окислительными свойствами, но представляет большую опасность, поскольку является источником образования более активных АФК

б) образование активных форм хлора
в) образование активных форм азота
Билет № 20
























 Утечка электронов из ферментативных реакций – захват электронов из ферментативных реакций с образованием активных форм кислорода
Утечка электронов из ферментативных реакций – захват электронов из ферментативных реакций с образованием активных форм кислорода Реакция конденсации
Реакция конденсации