Вопросы по теме биохимия печени
Роль печени в обмене углеводов, липидов, аминокислот и белков.
Печень – самая крупная железа пищеварительного тракта, выполняющая регуляторную гомеостатическую функцию, участвуя в белковом, липидном, углеводном, минеральном обмене.
Роль печени в углеводном обмене.
Печень играет ведущую роль в поддержании физиологической концентрации глюкозы в крови. Из общего количества поступающей из кишечника глюкозы печень извлекает ее большую часть и тратит на синтез гликогена, окислительный распад, синтез жирных кислот. При физиологической гипогликемии в печени активируется распад гликогена.
В печени активно протекает глюконеогенез, превращение галактозы в глюкозу; превращение фруктозы в глюкозу; образование глюкуроновой кислоты.
Роль печени в липидном обмене.
Участие печени в обмене липидов тесно связано с ее желчевыделительной функцией. Желчь усиливает действие панкреатической липазы и участвует в образовании хиломикронов.
При дефиците глюкозы, в печени активируется окисление жирных кислот. В условиях избытка глюкозы в гепатоцитах происходит синтез триглицеридов и фосфолипидов из жирных кислот, которые поступают в печень из кишечника.
В печени, синтезируются кетоновые тела, ацетоацетат и гидрооксимаслянная кислота,
Синтез холестерина в основном происходит в печени и кишечнике, где образуется более 90% всего холестерина. Печеночные клетки полностью ответственны за удаление избыточного количества холестерина из организма путем выведения, как самого холестерина, так и его производных (желчные кислоты) с желчью.
Печень - основное местом образования ЛПВП и ЛПОНП.
Роль печени в белковом обмене.
Печень играет ключевую роль в обмене белков. В этом направлении она выполняет следующие основные функции:
- синтез специфических белков плазмы. Все альбумины плазмы, 75—90% альфа-глобулинов и 50% бетта-глобулинов синтезируются гепатоцитами.
- образование мочевины и мочевой кислоты;
- синтез холина и креатина;
- трансаминирование и дезаминирование аминокислот, что весьма важно для взаимных превращений аминокислот, а также для процесса глюконеогенеза и образования кетоновых тел.
Печень является единственным органом, где синтезируются факторы свертывания крови: протромбин, фибриноген, проконвертин и проакцелерин. В печени происходит и синтез ингибиторов свертывания крови: антитромбина и антиплазмина.
Основная масса ферментов также образуется в печени.
Конечные этапы катаболических изменений белков в печени одновременно представляют ее детоксикационную функцию.
Распад гема. Образование и физико-химические свойства билирубина.
Физико-химические свойства
Чистый билирубин представляет собой коричневые ромбические кристаллы.[5] Нерастворим в воде, трудно растворим в диэтиловом эфире, глицерине, в этаноле. Растворим в бензоле, хлороформе, хлорбензоле и разведённых растворах щёлочей. Билирубин поглощает синий свет с длиной волны 450—460 нм, химически трансформируясь в водорастворимую форму — люмирубин.
Распад гема - многостадийный процесс
За сутки у человека распадается около 9 г гемопротеинов, в основном это гемоглобин эритроцитов.
Эритроциты в норме живут 90-120 дней, после чего лизируются в клетках ретикулоэндотелиальной системы – макрофагах селезенки (главным образом), купферовских клетках печени и макрофагах костного мозга. При разрушении эритроцитов в кровеносном русле высвобождаемый гемоглобин образует комплекс с белком-переносчиком гаптоглобином (фракция α2-глобулинов крови) и также переносится в клетки РЭС селезенки, печени и костного мозга.
Синтез билирубина
В клетках РЭС гем в составе гемоглобина окисляется молекулярным кислородом. В реакциях последовательно происходит разрыв метинового мостика между 1-м и 2-м пиррольными кольцами гема с их восстановлением, отщеплением железа и белковой части и образованием оранжевого пигмента билирубина. Высвобождаемое железо может либо запасаться в клетке в комплексе с ферритином, либо выделяться наружу и связываться с трансферрином.

Реакции распада гемоглобина и образования билирубина
Билирубин – токсичное, жирорастворимое вещество, способное разобщать окислительное фосфорилирование в клетках. Особенно чувствительны к нему клетки нервной ткани.
Выведение билирубина
Из клеток ретикуло-эндотелиальной системы билирубин попадает в кровь. Здесь он находится в комплексе с альбумином плазмы, в гораздо меньшем количестве – в комплексах с металлами, аминокислотами, пептидами и другими малыми молекулами. Образование таких комплексов не позволяет выделяться билирубину с мочой. Билирубин в комплексе с альбумином называется свободный (неконъюгированный) или непрямой билирубин.
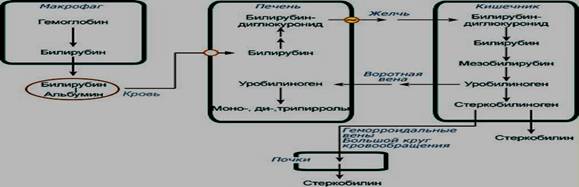
(Этапы метаболизма билирубина в организме)
Из сосудистого русла в гепатоциты билирубин попадает с помощью белка-переносчика (транспортный белок органических анионов) или по механизму флип-флоп. Далее при участии цитозольного связывающего белка лигандина (Y-протеин) билирубин транспортируется в ЭПР, где протекает реакция связывания билирубина с УДФ-глюкуроновой кислотой, при этом образуются моно- и диглюкурониды. Кроме глюкуроновой кислоты, в реакцию конъюгации могут вступать сульфаты, фосфаты, глюкозиды.
Билирубин-глюкуронид получил название связанный (конъюгированный) или прямой билирубин.

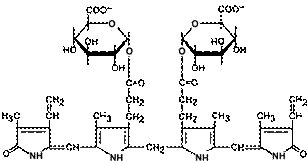
| 
|
| (Реакции синтеза билирубин-диглюкуронида)
| (Строение билирубин-диглюкуронида (прямой билирубин))
|
После образования билирубин-глюкурониды АТФ-зависимым переносчиком секретируются в желчные протоки и далее в кишечник, где при участии бактериальной β-глюкуронидазы превращаются в свободный билирубин. Одновременно, даже в норме (особенно у взрослых), некоторое количество билирубин-глюкуронидов может попадать из желчи в кровь по межклеточным щелям.
Таким образом, в плазме крови обычно присутствуют две формы билирубина: свободный (непрямой), попадающий сюда из клеток РЭС (80% и более всего количества), и связанный (прямой), попадающий из желчных протоков (в норме не более 20%).
Превращение в кишечнике
В кишечнике билирубин подвергается восстановлению под действием микрофлоры до мезобилирубина и мезобилиногена (уробилиногена). Часть уробилиногена всасывается и с кровью портальной вены попадает в печень, где либо распадается до моно-, ди- и трипирролов, либо окисляется до билирубина и снова экскретируется. При этом при здоровой печени в общий круг кровообращения и в мочу мезобилирубин и уробилиноген не попадают, а полностью задерживаются гепатоцитами.
Оставшаяся в кишечнике часть пигментов ферментами бактериальной флоры толстого кишечника восстанавливается до стеркобилиногена. Далее
· малая часть стеркобилиногена может всасываться и катаболизировать в печени, подобно уробилиногену,
· незначительное количество стеркобилиногена через геморроидальные вены попадает в большой круг кровообращения, отсюда в почки и в мочу. После окисления на воздухе из стеркобилиногена образуется стеркобилин мочи,
· однако основное количество стеркобилиногена достигает нижних отделов толстого кишечника и выделяется. В прямой кишке и на воздухе стеркобилиноген окисляется в стеркобилин, окрашивая кал,
· аналогично уробилиноген, появляющийся в моче при патологии печени, окисляется в уробилин.
Микросомальное окисление
Микросомы - замкнутые пузырьки, которые состоят из мембран ЭР. Микросомальные оксидазы - ферменты, катализирующие восстановление одного атома молекулы О2 с образованием воды и включение другого атома кислорода в окисляемое вещество. Суммарное уравнение реакции гидроксилирования вещества RH ферментами микросомального окисления:
RH+O2+NADFH2=ROH+H2O+NADF
Система включает несколько белков, составляющих электронтранспортные цепи (ЦПЭ). В ЭР существуют две такие цепи:
первая состоит из двух ферментов - NADPH-P450 редуктазы и цитохрома Р450,
вторая включает фермент NADH-цитохром-b5 редуктазу, цитохром b5 и ещё один фермент - стеароил-КоА-десатуразу.
Первая ЦПЭ. NADPH-P450 редуктаза - цитохром Р450. В большинстве случаев донором электронов (e) для этой цепи служит NADPH, окисляемый NАDРН-Р450 редуктазой. Фермент в качестве простетической группы содержит 2 кофермента - FAD и FMN. Протоны и электроны с NADPH переходят последовательно на коферменты NADPH-P450 редуктазы. Восстановленный FMN окисляется цитохромом Р450.
Цитохром Р450 - гемопротеин, содержит простетическую группу гем и имеет участки связывания для кислорода и субстрата (ксенобиотика). Название цитохром Р450 указывает на то, что максимум поглощения комплекса цитохрома Р450 лежит в области 450 нм.
Вторая ЦПЭ. Окисляемый субстрат (донор электронов) для NADH-цитохром b5 -редуктазы - NADH. Протоны и электроны с NADH переходят на кофермент редуктазы FAD, следующим акцептором электронов служит Fe3+ цитохрома b5. Цитохром b5 в некоторых случаях может быть донором электронов (e) для цитохрома Р450 или для стеароил-КоА-десатуразы, которая катализирует образование двойных связей в жирных кислотах, перенося электроны на кислород с образованием воды.
NADH-цитохром b5 редуктаза - двухдоменный белок. Глобулярный цитозольный домен связывает простетическую группу - кофермент FAD, а единственный гидрофобный "хвост" закрепляет белок в мембране.
Цитохром b5- гемсодержащий белок, который имеет домен, локализованный на поверхности мембраны ЭР, и короткий "заякоренный" в липидном бислое спирализованный домен.
NADH-цитохром b5 -редуктаза и цитохром b5, являясь "заякоренными" белками, не фиксированы строго на определённых участках мембраны ЭР и поэтому могут менять свою локализацию.
Таким образом, в результате первой фазы обезвреживания происходит модификация веществ с образованием функциональных групп, повышающих растворимость гидрофобного соединения. В результате модификации возможна потеря молекулой её биологической активности или даже формирование более активного соединения, чем вещество, из которого оно образовалось.
Немикросомальное окисление. Этот путь биотрансформации медикаментов осуществляется такими путями:
1. Реакции гидролиза. Например, гидролиз ацетилхолина, кокаина, новокаина, атропина, кислоты ацетилсалициловой, новокаинамида, изониазида с образованием с образованием изоникотиновой кислоты.
2. Реакции окислительного дезаминирования. Например, алифатические амины окисляются моноаминоксидазами митохондрий в соответствующие альдегиды. Например, окислительное дезаминирование катехоламинов, тирамина и других биогенных аминов.
3. Реакции окисления спиртов. Окисление многих спиртов и альдегидов катализируется ферментами растворимой фракции (цитозоля) клетки — алкогольдегидрогеназой, ксантиноксидазой. Например, окисление спирта этилового до ацетальдегида, хлоралгидрата до трихлоруксусной кислоты.
Реакции конъюгации.
В биотрансформации лекарственных средств реакции конъюгации (комплексообразование) представляют собой биосинтетические процессы, в результате которых медикаменты или их метаболиты взаимодействуют с метаболитами организма (эндогенными субстратами), такими, как глюкуроновая кислота, глицин, сульфат, ацетат, метил, глутатион, образуя соответствующие конъюгаты (комплексы). Образующиеся в результате конъюгации комплексы, легко удаляются из организма путем экскреции.
Реакции конъюгации лекарственных средств осуществляются такими путями:
I. Глюкуронирование. В реакции участвует активная форма глюкуроновой кислоты — уридиндифосфатглюкуроновая кислота. Кроме лекарственных (левомицетин) и других чужеродных соединений, глюкуронированию подвергаются многие клеточные метаболиты (билирубин, тироксин, эстрон, тестостерон).
2. Глициновая конъюгация происходит с образованием гиппуровых кислот. Этому виду биотрансформации подвергаются ароматические карбоновые кислоты—бензойная, салициловая, никотиновая.
3. Ацетилирование — основной путь биотрансформации сульфаниламидов, гидразидов иэоникотиновой кислоты (изониазид, солюзид, фтивазид, тубазид), анилина и других ароматических аминов.
Вопросы по теме биохимия печени
Роль печени в обмене углеводов, липидов, аминокислот и белков.
Печень – самая крупная железа пищеварительного тракта, выполняющая регуляторную гомеостатическую функцию, участвуя в белковом, липидном, углеводном, минеральном обмене.









