

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...
Топ:
Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов...
Теоретическая значимость работы: Описание теоретической значимости (ценности) результатов исследования должно присутствовать во введении...
Проблема типологии научных революций: Глобальные научные революции и типы научной рациональности...
Интересное:
Финансовый рынок и его значение в управлении денежными потоками на современном этапе: любому предприятию для расширения производства и увеличения прибыли нужны...
Национальное богатство страны и его составляющие: для оценки элементов национального богатства используются...
Подходы к решению темы фильма: Существует три основных типа исторического фильма, имеющих между собой много общего...
Дисциплины:
|
из
5.00
|
Заказать работу |
Содержание книги
Поиск на нашем сайте
|
|
|
|
Основные законы стехиометрии.
*Закон сохранения массы веществ формулируется так:
Масса веществ, вступивших в реакцию, равна массе продуктов реакции.
*Закон постоянства состава (Ж. Л. Пруст, 1801—1808гг.) — любое определенное химически чистое соединение, независимо от способа его получения, состоит из одних и тех же химических элементов, причём отношения их масс постоянны, а относительные числа их атомов выражаются целыми числами. Это один из основных законов химии.
*ЭКВИВАЛЕНТЫ ПРОСТЫХ И СЛОЖНЫХ ВЕЩЕСТВ. ЗАКОН ЭКВИВАЛЕНТОВ
Эквивалентом вещества называется такое его количество, которое соединяется с 1 молем атомов водорода или замещает то же количество атомов водорода в химических реакциях.
Эквивалентной массой называется масса 1 эквивалента вещества.
Закон эквивалентов: Все вещества реагируют и образуются в эквивалентных соотношениях.
Эквивалентное соотношение означает одинаковое число моль эквивалентов. Т.о. закон эквивалентов можно сформулировать иначе: число моль эквивалентов для всех веществ, участвующих в реакции, одинаково.
* По химическим уравнениям можно рассчитать массу, объем и количество реагирующих и образующихся веществ.
Для расчетов очень важно выбрать соответствующие друг другу единицы измерения массы, объема и количества веществ. С этой целью можно воспользоваться таблицей 7.
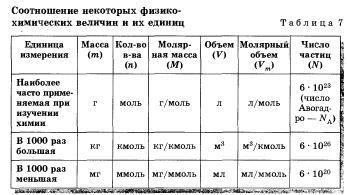
Для того чтобы решить расчетную задачу по химии, можно воспользоваться следующим алгоритмом — сделать пять шагов:
1. Составить уравнение химической реакции.
2. Над формулами веществ записать известные и неизвестные величины с соответствующими единицами измерения
(только для чистых веществ, то есть не содержащих принеси). Если по условию задачи в реакцию вступают вещества, содержащие примеси, то сначала надо определить содержание чистого вещества.
|
|
3. Под формулами веществ с известными и неизвестными записать соответствующие значения этих величин, найденные по уравнению реакции.
4. Составить и решить пропорцию.
5. Записать ответ.
Строение вещества. Современная квантово-механическая модель строения атома. Теория многоэлектронных атомов.
Ядро и электронная оболочка атома
Каждый атом состоит из ядра и электронной оболочки (рис.1). Электронная оболочка атома – это совокупность элементарных частиц – электронов, каждому из которых присущ корпускулярно-волновой характер.
Электрон как частица обладает массой покоя. Me=9,1095·10ˉ31 кг и несет отрицательный электрический заряд, равный 1,6022·10ˉ19 Кл. Абсолютное (без учета знака) значение этого заряда является наименьшим и называется элементарным зарядом.
Атом в целом не заряжен (электрически нейтрален). Это обусловлено тем, что сумма отрицательных зарядов электронов компенсирована положительным зарядом ядра атома: в каждом атоме число элементарных отрицательных зарядов в оболочке равно числу элементарных положительных зарядов в ядре.
Между положительно заряженным ядром атома и отрицательно заряженными электронами его оболочки действуют электростатические (кулоновские) силы притяжения. Геометрический размер атома, условно записываемый диаметром его электронной оболочки, имеет порядок 10ˉ10 м, а диаметр атомного ядра – порядок 10ˉ14 м, т.е по размеру ядро в 10000 меньше, чем атом. Отсюда следует, что:
Квантово - механическое объяснение строения атома
Орбитальная модель атома
Современные квантово-механические представления о строении электронной оболочки атома исходят из того, что движение электрона в атоме нельзя описать определенной траекторией. Можно рассматривать лишь некоторый объем пространства, в котором находится электрон. Поскольку электрон обладает одновременно свойствами частицы и волны, то подходом к объяснению строения электронной оболочки может быть как корпускулярная теория, так и волновая теория; обе они приводят к одинаковому наглядному представлению, сформулированному как орбитальная модель атома.
|
|
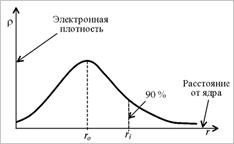
1. Обоснование орбитальной модели атома, исходящее из корпускулярного характера электрона, состоит в следующем. Как следует из рис.2, вероятность пребывания электрона в атомном ядре равна нулю, она незначительна вблизи ядра, но быстро возрастает при удалении от ядра. На некотором расстоянии вероятность достигает максимума, а затем медленно уменьшается, ассимптотически приближаясь к нулю на расстоянии, стремящемся к бесконечности. Таким образом, невозможно ограничить то пространство, в котором может находиться электрон, т.е. нельзя (без дополнительных условий) указать размеры атома. Исходя из корпускулярного характера электрона можно говорить о 90 %-ой вероятности его пребывания в ограниченном объеме пространства, которое называется атомная орбиталь.
|
| Рис. 2.Зависимость электронной плотности (или вероятности пребывания электрона на расстоянии r ядро-электрон) в атоме от расстояния от ядра |
2. Обоснование орбитальной модели атома, исходящее из волнового характера электрона, состоит в следующем. Электрон заполняет пространство вокруг атомного ядра в форме стоячей волны, которую наглядно можно представить как электронное облако. Плотность электронного облака, понимаемого как облако электрического заряда электрона,− электронная плотность окажется различной и зависящей от расстояния ядро-электрон (рис.1). При ограничении электронной плотности до значения ~ 90 % получается та же орбитальная модель атома.
Атомная орбиталь – это геометрический образ, отвечающий объему пространства вокруг атомного ядра, который соответствует 90 %-ой вероятности нахождения в этом объеме электрона (как частицы) и одновременно 90 %-ой плотности заряда электрона (как волны).
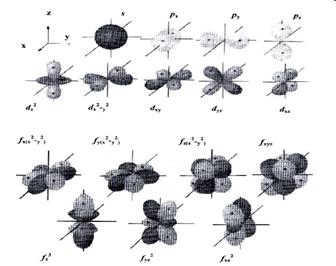
Модель атомной орбитали (электронного облака) очень удобна для наглядного описания распределения электронной плотности в пространстве. При этом s-орбиталь имеет сферическую форму, р-орбиталь – форму гантели, d-орбиталь – четырехлепесткового цветка или удвоенной гантели, f-орбиталь – еще более сложную форму (рис.3).
|
|
|
| Рис. 3. Формы s-, p-, d- и f -орбиталей |
Если в атомной орбитали находится только один электрон (как в атоме водорода), то говорят об однократно занятой или полузаполненной, полузаселенной атомной орбитали. Если же в атомной орбитали находятся два электрона (как в атоме гелия), то говорят о двукратно занятой или полностью заполненной, полностью заселенной атомной орбитали. Полузаселенные АО играют важнейшую роль при формировании химических связей.
В соответствии с квантово-механическим описанием состояния электрона в атоме каждый электрон является индивидуальной частицей. Такие его свойства, как масса и заряд не выявляют различий между электронами, особенно между теми электронами, которые находятся на одной атомной орбитали (как в атоме гелия). Собственной характеристикой каждого электрона в атоме является спин.
Два электрона, находящиеся в одной атомной орбитали, различаются по спину.
Спин - квантово-механическое свойство электрона, которое невозможно точно объяснить с помощью традиционных представлений на основе механического поведения макрочастиц. Без учета волновых свойств электрона спин можно интерпретировать путем сравнения электрона с шаром, вращающимся вокруг выбранной оси. Спин характеризует направление вращения и, следовательно, при двух возможных направлениях механического вращения должно существовать два разных спина электрона.
Спин - неотъемлемая характеристика электрона в атоме; два электрона на одной атомной орбитали обладают антипараллельными спинами.
Атомную орбиталь удобно изображать в виде квадрата, называемого квантовой ячейкой, а каждый электрон − вертикальной стрелкой, обозначающей один из двух возможных спинов электрона. Квантовая ячейка с одной стрелкой означает атомную орбиталь с одним электроном, т.е. полузаселенную орбиталь, с двумя стрелками − атомную орбиталь с двумя электронами, т.е. полностью заселенную орбиталь, без стрелок - вакантную орбиталь, т. е. без электронов.
Энергетические подуровни
многоэлектронного атома. принципы
построения электронной оболочки
|
|
Квантово-механические расчеты показывают, что в многоэлектронных атомах энергия электронов одного уровня не одинакова; электроны заполняют атомные орбитали разных видов и имеют разную энергию.
Энергетический уровень характеризуется главным квантовым числом n. Для всех известных элементов значения n изменяются от 1 до 7. Электроны в многоэлектронном атоме, находящемся в основном (невозбужденном) состоянии, занимают энергетические уровни от первого до седьмого.
Энергетический подуровень характеризуется орбитальным квантовым числом l. Для каждого уровня (n = const) квантовое число l принимает все целочисленные значения от 0 до (n-1), например, при n=3 значениями l будут 0, 1 и 2. Орбитальное квантовое число определяет геометрическую форму (симметрию) орбиталей s-, p-, d-, f -подуровня. Очевидно, что во всех случаях n> l; при n=3 максимальное значение l равно 2.
Существующие подуровни для первых четырех энергетических уровней, числа атомных орбиталей и электронов в них приведены в таблице 1.
Закономерность заполнения электронных оболочек атомов определяется принципом запрета, установленным в 1925 г. швейцарским физиком Паули.
Принцип Паули: в атоме не могут находится два электрона в тождественных состояниях.
Различие электронов, занимающих разные атомные орбитали одного подуровня (n, l = const), кроме s-подуровня, характеризуется магнитным квантовым числом m  . Это число называется магнитным, поскольку оно характеризует поведение электронов во внешнем магнитном поле. Если значение l определяет геометрическую форму атомных орбиталей подуровня, то значение квантового числа m
. Это число называется магнитным, поскольку оно характеризует поведение электронов во внешнем магнитном поле. Если значение l определяет геометрическую форму атомных орбиталей подуровня, то значение квантового числа m  устанавливает взаимное пространственное расположение этих орбиталей.
устанавливает взаимное пространственное расположение этих орбиталей.
Таблица 1
Энергетические уровни, подуровни и орбитали
многоэлектронного атома
| Энерге-тический уровень n | Энергетический подуровень | Обозначение орбитали | Число орби-
талей
n 
| Число электронов
2n 
| |
| l | вид орбитали | ||||
| s | 1s | ||||
 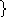 2 2
| s p | 2s 2p | 3 4 | 2 8 | |
 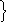 3 3
| s p d | 3s 3p 3d | 3 9 | 6 18 | |
  4 4
| s p d f | 4s 4p 4d 4f | 3 16 | 6 32 |
Магнитное квантовое число ml в пределах данного подуровня (n, l = const) принимает все целочисленные значения от + l до – l, включая нуль. Для s-подуровня (n = const, l = 0) возможно только одно значение ml = 0, откуда следует, что на s-подуровне любого (от первого до седьмого) энергетического уровня содержится одна s-АО.
Для p-подуровня (n> 1, l = 1) ml может принимать три значения +1, 0, -1, следовательно, на p-подуровне любого (от второго до седьмого) энергетического уровня содержится три p-АО.
Для d-подуровня (n> 2, l = 2) ml имеет пять значений +2, +1, 0, -1, -2 и, как следствие, d- подуровень любого (от третьего до седьмого) энергетического уровня обязательно содержит пять d- АО.
|
|
Аналогично, для каждого f- подуровня (n> 3, l = 3) m  имеет семь значений +3, +2, +1, 0, -1, -2, -3 и поэтому любой f- подуровень содержит семь f- АО.
имеет семь значений +3, +2, +1, 0, -1, -2, -3 и поэтому любой f- подуровень содержит семь f- АО.
Таким образом, каждая атомная орбиталь однозначно определяется тремя квантовыми числами - главным n, орбитальным l и магнитным m l.
При n = const строго определены все относящиеся к данному энергетическому уровню значения l, а при l = const – все относящиеся к данному энергетическому подуровню значения ml.
Ввиду того, что каждая орбиталь может максимально заполняться двумя электронами, число электронов, которое может разместиться на каждом энергетическом уровне и подуровне, вдвое больше числа орбиталей на данном уровне или подуровне. Поскольку электроны, находящиеся в одной атомной орбитали, имеют одинаковые значения квантовых чисел n, l и ml, то для двух электронов на одной орбитали используется четвертое, спиновое квантовое число s, которое определяется спином электрона.
В соответствии с принципом Паули можно утверждать, что каждый электрон в атоме однозначно характеризуется своим набором четырех квантовых чисел – главного n, орбитального l, магнитного m и спинового s.
Заселение электронами энергетических уровней, подуровней и атомных орбиталей подчиняется следующему правилу (принцип минимума энергии): в невозбужденном состоянии все электроны обладают наименьшей энергией.
Это означает, что каждый из электронов, заполняющих оболочку атома, занимает такую орбиталь, чтобы атом в целом имел минимальную энергию. Последовательное квантовое возрастание энергии подуровней происходит в следующем порядке:
1 s – 2 s – 2 p – 3 s – 3 p – 4 s – 3 d – 4 p – 5 s - …..
Заполнение атомных орбиталей внутри одного энергетического подуровня происходит в соответствии с правилом, сформулированным немецким физиком Ф.Хундом (1927 г.).
Правило Хунда: атомные орбитали, принадлежащие к одному подуровню, заполняются каждая вначале одним электроном, а затем происходит их заполнение вторыми электронами.
Правило Хунда также называют принципом максимальной мультиплетности, т.е. максимально возможного параллельного направления спинов электронов одного энергетического подуровня.
На высшем энергетическом уровне свободного атома может находиться не более восьми электронов.
Электроны, находящиеся на высшем энергетическом уровне атома (во внешнем электронном слое), называются внешними; число внешних электронов у атома любого элемента никогда не бывает больше восьми. Для многих элементов именно число внешних электронов (при заполненных внутренних подуровнях) в значительной степени определяет их химические свойства. Для других электронов, у атомов которых есть незаполненный внутренний подуровень, например 3 d- подуровень у атомов таких элементов, как Sc, Ti, Cr, Mn и др., химические свойства зависят от числа как внутренних, так и внешних электронов. Все эти электроны называются валентными; в сокращенных электронных формулах атомов они записываются после условного обозначения атомного остова, т. е. после выражения в квадратных скобках.
основные законы стехиометрии.
*Закон сохранения массы веществ формулируется так:
Масса веществ, вступивших в реакцию, равна массе продуктов реакции.
*Закон постоянства состава (Ж. Л. Пруст, 1801—1808гг.) — любое определенное химически чистое соединение, независимо от способа его получения, состоит из одних и тех же химических элементов, причём отношения их масс постоянны, а относительные числа их атомов выражаются целыми числами. Это один из основных законов химии.
*ЭКВИВАЛЕНТЫ ПРОСТЫХ И СЛОЖНЫХ ВЕЩЕСТВ. ЗАКОН ЭКВИВАЛЕНТОВ
Эквивалентом вещества называется такое его количество, которое соединяется с 1 молем атомов водорода или замещает то же количество атомов водорода в химических реакциях.
Эквивалентной массой называется масса 1 эквивалента вещества.
Закон эквивалентов: Все вещества реагируют и образуются в эквивалентных соотношениях.
Эквивалентное соотношение означает одинаковое число моль эквивалентов. Т.о. закон эквивалентов можно сформулировать иначе: число моль эквивалентов для всех веществ, участвующих в реакции, одинаково.
* По химическим уравнениям можно рассчитать массу, объем и количество реагирующих и образующихся веществ.
Для расчетов очень важно выбрать соответствующие друг другу единицы измерения массы, объема и количества веществ. С этой целью можно воспользоваться таблицей 7.

Для того чтобы решить расчетную задачу по химии, можно воспользоваться следующим алгоритмом — сделать пять шагов:
1. Составить уравнение химической реакции.
2. Над формулами веществ записать известные и неизвестные величины с соответствующими единицами измерения
(только для чистых веществ, то есть не содержащих принеси). Если по условию задачи в реакцию вступают вещества, содержащие примеси, то сначала надо определить содержание чистого вещества.
3. Под формулами веществ с известными и неизвестными записать соответствующие значения этих величин, найденные по уравнению реакции.
4. Составить и решить пропорцию.
5. Записать ответ.
|
|
|

Своеобразие русской архитектуры: Основной материал – дерево – быстрота постройки, но недолговечность и необходимость деления...

Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Историки об Елизавете Петровне: Елизавета попала между двумя встречными культурными течениями, воспитывалась среди новых европейских веяний и преданий...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!