

Состав сооружений: решетки и песколовки: Решетки – это первое устройство в схеме очистных сооружений. Они представляют...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Состав сооружений: решетки и песколовки: Решетки – это первое устройство в схеме очистных сооружений. Они представляют...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...
Топ:
Проблема типологии научных революций: Глобальные научные революции и типы научной рациональности...
Когда производится ограждение поезда, остановившегося на перегоне: Во всех случаях немедленно должно быть ограждено место препятствия для движения поездов на смежном пути двухпутного...
Отражение на счетах бухгалтерского учета процесса приобретения: Процесс заготовления представляет систему экономических событий, включающих приобретение организацией у поставщиков сырья...
Интересное:
Средства для ингаляционного наркоза: Наркоз наступает в результате вдыхания (ингаляции) средств, которое осуществляют или с помощью маски...
Лечение прогрессирующих форм рака: Одним из наиболее важных достижений экспериментальной химиотерапии опухолей, начатой в 60-х и реализованной в 70-х годах, является...
Национальное богатство страны и его составляющие: для оценки элементов национального богатства используются...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Вопросы к семинару:
1. Гетероциклические соединения: определение, классификация. Понятие о гетероатоме пиррольного типа и p-избыточных системах. Электронное строение пиррола, фурана, тиофена. Влияние природы гетероатома на ароматичность и реакционную способность этих гетероциклов.
2. Химические свойства: кислотные свойства пиррола, ацидофоб-ность фурана и пиррола, особенности протекания реакций электрофильного замещения, реакции гидрирования.
4. Способы получении пиррола, фурана, тиофена. Превращение пятичленных гетероциклов по Юрьеву.
5. Диазолы: определение, классификация. Понятие о гетероатоме пиридинового типа и амфотерных системах. Прогнозирование реакционной способности на основе анализа строения.
6. Химические свойстве диазолов: кислотно-основные свойства, прототропная таутомерия и ее причины, реакции электрофильного и нуклеофильного замещения, реакции гидрирования.
7. Биологически активные соединения и лекарственные препараты: хлорофилл, гемин, триптофан, гистидин, норсульфазол, пенициллины, дибазол (получение, анализ реакционной способности, качественные реакции, применение).
Опыты к лабораторной работе:
1. Получение фурфурола из древесных опилок
2. Разложение фурфурола кислотами
3. Реакция фурфурола с фуксинсернистой кислотой
4. Окисление фурфурола
5. Конденсация фурфурола с фенилгидразином
6. Взаимодействие антипирина и амидопирина с азотистой кислотой
7. Взаимодействие антипирина и амидопирина с хлоридом железа (III).
Задания к самостоятельной работе:
Вариант 1
1. Напишите возможные структурные формулы гомологов тиофена состав С6Н8S. Назовите их. Объясните, почему тиофен является p‑избыточной системой.
|
|
2. Сравните строение и химические свойства имидазола и пиррола. Объясните причины ароматичности этих соединений.
3. Напишите схемы реакций: а) пиразола с соляной кислотой, б) пиррола с калием в жидком аммиаке, в) имидазола с иодистым метилом.
4. Заполните схемы превращений, назовите реагенты и продукты реакций. Укажите тип каждой реакции:

5. Напишите структурные формулы продуктов А, Б и В в схеме превращений:

6. Приведите схему щелочного гидролиза фурацилина, назовите все продукты, укажите, какой из них определяют в продуктах гидролиза.
Вариант 2
1. Напишите структурные формулы следующих гетероциклических соединений: а) 3-этилпиррол, б) 4(5)-метилимидазол, в) 6-нитро-3-этилиндол, г) пирролин. Объясните значение цифр 4 и 5 в названии соединения «б».
2. Объясните значение электронного вклада гетероатома в формирование делокализованной p-электронной системы в молекулах фурана, пиррола и тиофена. Как природа гетероатома сказывается на ароматичности указанных гетероциклов?
3. Напишите схемы реакций: а) пиррола с амидом натрия, б) пиразола с иодистым метилом, в) имидазола с соляной кислотой. Укажите в каких из них проявляются кислотные, основные, нуклеофильные свойства гетероциклов.
4. Напишите уравнения реакций сульфирования и нитрования пиррола и имидазола. Объясните, почему в этих реакциях надо использовать разные (какие?) сульфирующие и нитрующие средства.
5. Напишите структурные формулы продуктов «А» и «Б» в схеме превращений, укажите область применения конечного продукта:

6. Приведите формулы, названия по систематической номенклатуре для антипирина и амидопирина. Перечислите качественные реакции на эти препараты, укажите аналитический эффект.
Вариант 3
1. Напишите структурные формулы следующих гетероциклических соединений: а) 2-аминотиазол, б) a-метилпиррол, в) 6-бром-3-этилиндол, г) a-нитротетрагидрофуран. В какой лекарственный препарат входит соединение «а»?
|
|
2. Что общего и разного в условиях проведения реакции нитрования пиррола и фурана по сравнению с условиями нитрования бензола?
3. Напишите схемы реакций: а) пиррола с метилмагнийбромидом, б) имидазола с амидом натрия, в) пиразола с соляной кислотой. Какие свойства указанных гетероциклов иллюстрируют эти реакции?
4. Объясните, почему для тиазола возможны реакции SE, SN, АЕ. Подтвердите соответствующими уравнениями.
5. Заполните схему превращений, назовите все соединения:

6. Приведите схему синтеза амидопирина из антипирина. Опишите ход выполнения качественных реакций на амидопирин, укажите аналитические эффекты.
Вариант 4
1. Назовите приведенные соединения:

2. Сравните электронное строение и химические свойства пиррола и пиразола. Объясните, для какого из этих гетероциклов и почему характерна прототропная таутомерия.
3. Запишите формулами, заполните схему:

4. Напишите уравнения реакций (не менее 4-х), отражающих химические свойства имидазола.
5. Напишите структурные формулы продуктов А, Б и В в схеме превращений, назовите их:

6. Приведите формулы и назовите лекарственные препараты, содержащие ядро тиазола и тиазолидина. Укажите область применения.
Вариант 5
1. Напишите структурные формулы следующих соединений: а) 2‑метил-5-нитротиазол, б) гетероауксин, в) 4‑гидроксифурфурол, г) 4-метокси-5-хлорпиразол.
2. Приведите формулы и названия пятичленных гетерециклов, содержащих в цикле атом "пиррольного типа". Объясните строение атома "пиррольного типа".
3. Запишите уравнениями реакций следующие превращения:

4. Поясните термин «С-ацилирование и N-ацилирование» и объясните, почему при взаимодействии с ацетилхлоридом пиррол дает продукт С-ацилирования, а имидазол - N-ацилирования. Подтвердите уравнениями реакций.
5. Заполните схему превращений, назовите продукты реакций:

6. В состав каких биологически активных веществ и лекарственных препаратов входит ядро индола и бензимидазола? Приведите формулы и названия этих соединений по заместительной номенклатуре. Укажите их применение.
Вариант 6
1. Назовите следующие соединения:

2. Приведите формулы (не менее пяти) и названия пятичленных гетероциклов, содержащих атом азота «пиридинового типа». Объясните строение гетероатома «пиридинового типа».
|
|
3. Предложите одностадийные синтезы 2-аминотиазола, 5-нитрофурфурола, 2-метилпирролина, 3-ацетилимидазолий хлорида из соответствующих гетероциклических соединений. Укажите тип каждой реакции.
4. Антипирин обработали нитритом натрия в уксусной кислоте. На продукт реакции подействовали цинком в соляной кислоте, а затем избытком иодистого метила. Напишите уравнения реакций, назовите все соединения по заместительной номенклатуре. Перечислите цветные качественные реакции на исходное вещество и конечный продукт превращения.
5. Запишите формулами, укажите под действием каких реагентов протекают следующие превращения:

6. Проанализировав строение норсульфазола, объясните его способность к гидролизу. Приведите уравнения реакций гидролиза в кислой и щелочной средах.
Вариант 7
1. Приведите структурные формулы следующих соединений: а) 3,4‑диметилфурандикарбоновая кислота, б) 5-гидрокси-3(2-аминоэтил)индол, в) 2,5-диметил-6-этилбензимидазол.
2. Какими структурными особенностями обусловлен ароматический характер и тиофена и фурана? Какой из этих гетероциклов более ароматичен и почему?
3. Приведите схемы превращений: а) фурана в тиофен, б) a‑метилфурана в a-метилпиррол, в) 5-нитрофурфурола в фурацилин.
4. Предложите одностадийные способы получения 3-броминдола, тиазолидина, 3-пропилимидазолий иодида, 5-нитрофурфурола из соответствующих гетероциклических соединений. Укажите тип каждой реакции.
5. Заполните схему, назовите все соединения:

6. На примере пиразола объясните явление прототропной изомеризации. Приведите формулы и названия (тривиальные и по систематической номенклатуре) двух лекарственных препаратов, содержащих ядро пиразола. Укажите область их применения.
Вариант 8
1. Напишите структурные формулы следующих соединений: а) 3,4‑диметилтиофен, б) 4-гидроксипиразол, в)a-амино-b-[4(5)-имидазолил] пропионовая кислота, г) 5-изопропилтиазол. Отнесите гетероциклы, лежащие в основе этих соединений, к p‑избыточным или p-амфотерным. Дайте определение этим понятиям.
2. Сравните электронное строение и химические свойства пиразола и бензола. Объясните причину общих и разных свойств.
|
|
3. Приведите структурные формулы лекарственных препаратов, содержащих ядра пиразола и бензола (по два примера). Назовите их. Предложите реакции, позволяющие отличить эти вещества.
4. Напишите схемы реакций, назовите все соединения:

5. Напишите уравнения реакций бромирования, нитрования и сульфирования 2-метилфурана. Обоснуйте выбор реагентов для этих реакций.
6. 1,2-Диаминобензол ввели в реакцию циклизации с фенилуксусной кислотой, полученный продукт обработали хлороводородом. Напишите уравнения реакций, назовите соединения по систематической номенклатуре. Под каким названием и для каких целей применяется конечный продукт превращения?
Вариант 9
1. Назовите следующие соединения:

2. Сравните электронное строение и химические свойства пиррола и имидазола. Для какого гетероцикла и почему характерно образование ассоциатов?
3. Приведите схемы превращений: а) фурана в тиофен, б) a-метил-пиррола в a-метилфуран, в) тиазола в 2-аминотиазол.
4. Расположите следующие соединения в ряд по возрастанию легкости протекания реакций электрофильного замещения, ответ поясните: а) пиррол, б) бензол, в) толуол, г) тиофен. Приведите примеры указанных реакций для каждого из них.
5. Предложите способ получения фурацилина из пентоз, назовите все промежуточные продукты.
6. Укажите в молекуле фурацилина гидролитически неустойчивые группировки и приведите уравнение реакций гидролиза в щелочной среде. Объясните, какой газ будет выделяться при подкислении продуктов гидролиза.
Вариант 10
1. Напишите структурные формулы следующих соединений: а) 1,4-диметилпиррол, б) 4-гидроксипиразол, в) a-амино-b-(3-индолил) пропионовая кислота г) 2-[4(5)-имидазолил]этанамин Дайте тривиальные названия соединениям «в» и «г», укажите их биологическую роль.
2. Какими структурными особенностями обусловлен ароматический характер тиофена и фурана? Какой из этих гетероциклов более ароматичен и почему?
3. Приведите уравнения реакций, приводящих к исчезновению ароматических свойств пиррола. Объясните, как при этом изменяются кислотно-основные свойства.
4. Напишите уравнения реакций. Определите тип каждой реакции:

5. Заполните схему превращений, назовите продукты:

6. Проанализировав строение норсульфазола, объясните, почему он:
а) растворяется в кислотах и щелочах, б) гидролизуется, в) диазотируется. Подтвердите уравнениями реакций.
Вариант 11
1. Назовите приведенные соединения:

2. Сравните электронное строение и химические свойства пиразола и бензола.
3. Предложите способ получения 2-бромфурана из рибозы (путем последовательных реакций).
4. Приведите уравнения известных Вам реакций электрофильного замещения для имидазола. Назовите продукты реакций.
|
|
5. Заполните схему превращений:

6. Укажите в молекуле пенициллинов гидролитически неустойчивые группировки и приведите схемы гидролиза в кислой и щелочной средах.
Вариант 12
1. Приведите структурные формулы следующих соединений:
а) 1,4-диэтилимидазол, б) 5-гидроксиизооксазол, в) 2-амино-тиазолидин, г) гетероауксин.
2. Сравните электронное строение пиррола, бензола и пиразола. Объясните, какой из приведенных гетероциклов будет p‑избыточным, а какой p-амфотерным.
3. Напишите уравнения реакций и назовите соединения, в которые превратится пиррол под действием: а) амида натрия в жидком аммиаке, б) диоксандибромида, в) пиридинсульфотриоксида.
4. Заполните схемы превращений, назовите реагенты и продукты реакций. Укажите тип каждой реакции:
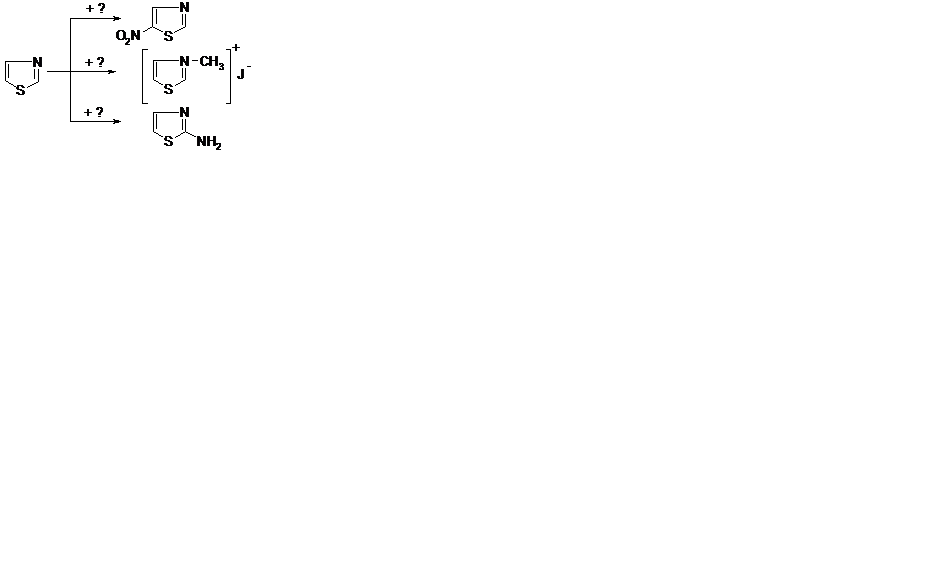
5. Напишите структурные формулы продуктов А, Б, В, Г в схеме превращений:

6. В состав каких лекарственных препаратов входит ядро тиазола и тиазолидина? Приведите формулы этих препаратов и укажите их применение в медицине. Объясните, в ИК-спектрах каких из этих препаратов и почему будет наблюдаться поглощение в области 1700-1800 см-1, в области 3400-3500 см-1(2 полосы).
Вариант 13
1. Назовите приведенные соединения:

2. Объясните различия в электронном строении гетероатомов пиррольного и пиридинового типов. Напишите формулы тиофена, оксазола, пирролина, тиазолидина и укажите, в каких из этих соединениях данные атомы отсутствуют.
3. Предложите способ получения 2-нитротиофена из ксилозы (путем последовательных реакций).
4. Напишите структурные формулы и названия соединений, в которые превратится пиразол под действием: а) метилмагнийиодида, б) иодистого метила, в) концентрированной серной кислоты при нагревании.
5. Заполните схему превращений, назовите соединения А и Б:

6. Напишите формулы и назовите пятичленные гетероциклы, входящие в состав дибазола, антипирина, норсульфазола. Обясните, для каких из них характерны; а) основные свойства, б) кислотные свойства, в) прототропная таутомерия. Подтвердите уравнениями реакций.
Вариант 14
1. Приведите структурные формулы следующих соединений: а) 5‑изопропилфурфурол б) (3-индолил)уксусная кислота, в) 2‑аминотиазол, г) a-амино-b-[4(5)-имидазолил] пропионовая кислота. Объясните значение цифр 4, 5 в названии соединения «г».
2. Какое соединение из задания 1 и почему может существовать в виде пары энантиомеров (поясните этот термин). Постройте для этого вещества проекционные формулы Фишера, соответствующие R- и S-стереоизомерам.
3. Приведите реакции получения из арабинозы пиррола, а затем его сульфопроизводного.
4. Напишите уравнения реакций сульфирования, нитрования, бромирования, аминирования тиазола. Укажите тип реакций.
5. Запишите формулами, заполните схему:

6. Напишите формулу гетероцикла, входящего в антипирин и амидопирин, пронумеруйте его. Опишите ход выполнения и аналитические эффекты цветных реакций на эти вещества.
Вариант 15
1. Назовите приведенные соединения:

2. Сравните электронное строение и химические свойстве пиразола и бензола.
3. Приведите реакции превращения: а) a-этилпиррола в a-этилфуран, б) тиофена в пиррол, в) b-изопропилфурана в b-изопропилтиофен.
4. Заполните схемы превращений, назовите реагенты и продукты реакций. Укажите тип каждой реакции:

5. Используя структурные формулы, заполните схему превращений:

6. Приведите формулы антипирина, дибазола, норсульфазола и предложите метод анализа, позволяющий различить эти препараты. Напишите уравнения реакций, укажите аналитические эффекты.
Вопросы для самоконтроля:
В заданиях 1-16 для каждого незаконченного утверждения напишите букву, соответствующую правильному ответу, учитывая, что ответ может быть использован один раз, несколько раз или не использован совсем.
| 1.Соединение, имеющее формулу называется… 2.Соединение, имеющее формулу называется… | 

| а) имидазол б) пиразол в) тиазол г) тиазолидин д) пиразолин |
| 3.Взаимодействие тиофена с хлорангидридом уксусной кислоты относится к реакциям… 4. Взаимодействие имидазола с хлорангидридом уксусной кислоты относится к реакциям… 5. Превращение фурана в тетрагидрофуран происходит в результате реакции… | а) присоединения б) отщепления в) замещения | |
| 6. При взаимодействии антипирина с хлоридом железа (III) образуется раствор… 7. При взаимодействии амидопирина с хлоридом железа (III) образуется раствор… 8. При взаимодействии амидопирина с азотистой кислотой образуется раствор… | а) бесцветный б) голубой в) красный г) зеленый д) фиолетовый | |
| 9. Продукт полного гидрирования пиразола называется… 10. В основе дибазола лежит гетероцикл, который называется… 11. При взаимодействии фурана и аммиака в присутствии оксида алюминия образуется… | а) пиррол б) пиразолон в) пиразолидин г) индол д) бензимидазол | |
| 12. Фурацилин обладает следующим действием… 13. Амидопирин используют как средство… 14. Дибазол применяют как средство… | а) коронарорасширяющее б) гипотензивное в) жаропонижающее г) антимикробное | |
| 15. Гетероатом пиррольного типа дает в общую p-электронную систему… 16. Гетероатом пиридинового типа имеет на свободной sp2-гибридной орбитали… | а) ноль электронов б)1 электрон в) 2 электрона 3) 3 электрона |
В заданиях 17-20 для каждого незаконченного утверждения один или несколько ответов являются верными. Напишите букву, соответствующую правильной комбинации ответов:
А - если верно 1,2,3
В - если верно 1 3
С- если верно 2,4
Д - если верно 3
Е- если верно все
17. Одновременно гетероатомы пиррольного и пиридинового типов содержат: 1) пирразол, 2) имидазол 3) тиазол, 4) индол, 5) пиразолин.
18. Прототропная изомеризация характерна для: 1) фурана, 2) тиазола, 3) имидазола, 4) пиррола, 5) оксазола.
19. Ацидофобными являются: 1) тиофен, 2) пиррол, 3) пиразол, 4) фуран, 5) тетрагидрофуран.
20. В реакцию присоединения тиазол вступает со следующими реагентами: 1) соляная кислота, 2) иодистый этил, 3) ацетилхлорид, 4) амид калия, 5) гидроксид калия.
В заданиях 21-25 каждое предложение представляет собой два утверждения, связанных словами "потому что". Определите достоверность каждого утверждения и причинно-следственную связь между ними. Напишите букву, соответствующую правильному ответу:
| Ответ | Утверждение 1 | Утверждение 2 | Связь |
| А | верно | верно | верно |
| В | верно | верно | неверно |
| С | верно | неверно | неверно |
| Д | неверно | верно | неверно |
| Е | неверно | неверно | неверно |
21. Норсульфазол вступает в реакцию диазотирования, потому что содержит ядро тиазола.
22. Пиррол является p-избыточным гетероциклом, потому что содержит гетероатом пиррольного типа.
23. Пиразол обладает NН-кислотностью, потому что содержит гетероатом пиридинового типа.
24. Имидазол является ацидофобным гетероциклом, потому что при взаимодействии с кислотами разрушается.
25. Фурфурол реагирует с семикарбазидом, потому что является производным азотсодержащего гетероцикла.
В заданиях 26-30 закончить ответы.
26. Фуран обработали диоксандибромидом, а затем смесью азотной и уксусной кислот. Конечный продукт называется...
27. Соединение «А» в следующей схеме называется..

28. Сероводород и фуран ввели в реакцию Юрьева, полученное органическое вещество нагрели с концентрированной серной кислотой. Конечный продукт превращения имеет формулу...
29. Фурацилин получают из пентоз с помощью последовательных реакций по схеме...
30. Получение амидопирина из антипирина выражается схемой...
Ответы
| 1. а 2. в 3. в 4. а 5. а | 6. в 7. д 8. д 9. в 10. д | 11. а 12. г 13. в 14. б 15. в | 16. в 17. А 18. Д 19. С 20. А | 21. В 22. А 23. В 24. Е 25. С |
26. 2-бром-5-нитрофуран
27. пирролнатрий.
| 28. | 
|
| 29. | 
|
| 30. | 
|
|
|
|

Архитектура электронного правительства: Единая архитектура – это методологический подход при создании системы управления государства, который строится...

История развития пистолетов-пулеметов: Предпосылкой для возникновения пистолетов-пулеметов послужила давняя тенденция тяготения винтовок...

История развития хранилищ для нефти: Первые склады нефти появились в XVII веке. Они представляли собой землянные ямы-амбара глубиной 4…5 м...

Индивидуальные очистные сооружения: К классу индивидуальных очистных сооружений относят сооружения, пропускная способность которых...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!