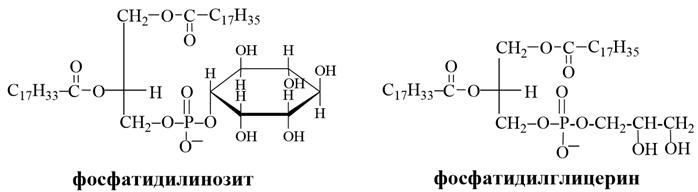
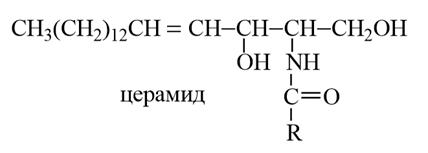 R = остаток ВЖК
R = остаток ВЖК
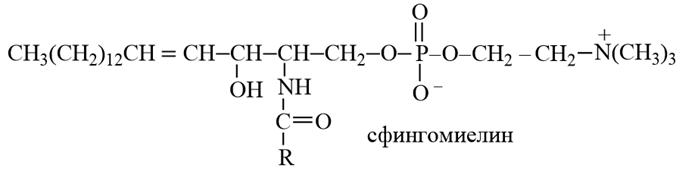
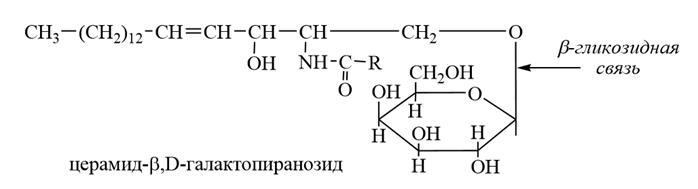
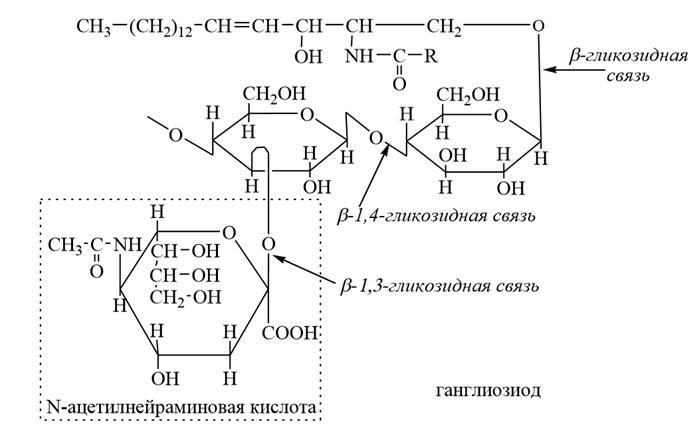
(Вроде, прям молекулу заучивать не надо, а лишь общие структурные элементы и связи).
Фосфолипиды:
1. Кефалины – фосфатидилколамины, аминоспирт – коламин (2аминоэтанол). Содержатся в тканях животных и растений, являются основным компонентом многих бактериальных клеток, впервые были выделены из тканей головного мозга (отсюда и название от греч. kephale голова). В условиях организма (рН~7,4) фосфоглицериды образуют внутренние соли.
2. Лецитины – фосфатидилхолины, аминоспирт – холин (гидроксид 2гидрокситриметиламмония, является витамином, регулирующим жировой обмен). Содержатся в соевых бобах, которые в промышленности служат сырьем для их получения, семянах подсолнечника, впервые были выделены из яичного желтка (отсюда и название от греч. lekithos - желток). Лецитин служит источником для синтеза ацетилхолина – нейромедиатора парасимпатической нервной системы.
3. Серилкефалины – фосфатидилсерины, аминоспирт – серин (аминокислота: 2-амино-3-гидроксипропановая кислота). Содержатся в мозге млекопитающих и других органах (печень, почки, сердце).
4. Фосфатидилинозиты и фосфатидилглицерины, содержат шестиатомный циклический спирт – инозит и трёхатомный спирт глицерин соответственно. Найдены во всех типах организмов.
Биологическая роль фосфолипидов, как веществ, действующих на границе раздела фаз, обусловлена наличием в молекуле гидрофильных и гидрофобных групп. Гидрофильный конец молекулы или «голова» обычно состоит из глицерина, фосфорной кислоты и спирта (многоатомного или аминоспирта). Гидрофобный конец или «хвост» образован алифатическими цепями жирных кислот. На границе раздела фаз такие соединения действуют как превосходные эмульгаторы. В водной среде бифильные фосфолипиды образуют мицеллы, внутренняя часть которой состоит из гидрофобных «хвостов», а полярные гидрофильные группы («голова») расположены на внешней поверхности мембраны.
Сфинголипиды
Это структурные аналоги глицеридов, в которых вместо глицерина используется основание сфингозин – длинноцепочечный двухатомный аминоспирт.
1) Церамиды – N-ацильные производные сфингозина, аминогруппа в которых ацилирована жирной кислотой. Встречаются в природе как в свободном виде (в липидах печени, селезёнки, эритроцитов), так и в составе сфинголипидов. Церамиды восстанавливают поверхностный слой кожи, снижают её проницаемость, уменьшают потерю воды и улучшают упругость, поэтому широко используются для приготовления мазей и кремов.
2) Сфингомиелины содержатся в клетках нервной ткани у организмов более высокой ступени эволюции. В сфингомиелинах гидроксил у С–1 церамида ацилирован фосфорилхолиновой группировкой.
Гликолипиды
Включают в свой состав спирт сфингозин и углеводные остатки, чаще всего глюкозу и галактозу, не содержат фосфорной кислоты и связанных с ней аминоспиртов. Гликолипиды входят в состав оболочек нервных клеток, плазматических мембран клеток, ганглиев, регулируют рост клеток и формируют их иммунные свойства.
1. Цереброзиды - остаток церамида связан β-гликозидной связью с β,Dгалактопиранозой или β,D-глюкопиранозой, в связи с чем выделяют: галактоцереброзиды и глюкоцереброзиды.
2. Ганглиозиды являются церамидолигосахаридами. Отличаются от цереброзидов тем, что содержат вместо моносахаридовного остатка сложный олигосахарид, в состав которого входит N-ацетилнейраминовая кислота. Молекулы ганглиозидов имеют большую молекулярную массу (до 3000).
Терпены (простые неомыляемые липиды)
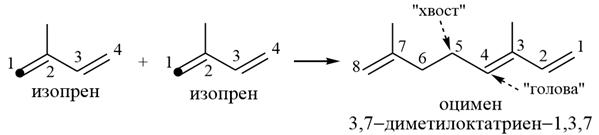
Ациклические монотерпены:
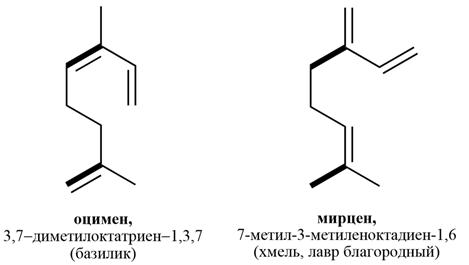
Моноциклические монотерпены:
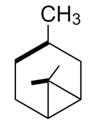
Бициклические монотерпены:
(нет, блин, беблия)
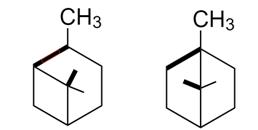
(То же самое, но комфортнее; на первой выделены терпеновые фрагменты):
Синтез камфоры из α-пинена по Тищенко:
Дитерпен:
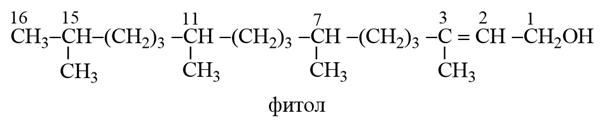
Тетратерпены:
Монотерпены – содержат два изопреновых звена, это бесцветные легко летучие жидкости с приятным запахом, содержатся в эфирных маслах растений, используются в парфюмерии.
Эфирными маслами называют нерастворимые в воде маслообразные продукты, которые в отличие от жирных масел полностью испаряются и не оставляют на бумаге жирных пятен. Они применяются в промышленности в качестве душистых веществ для ароматизации мыла и других косметических средств.
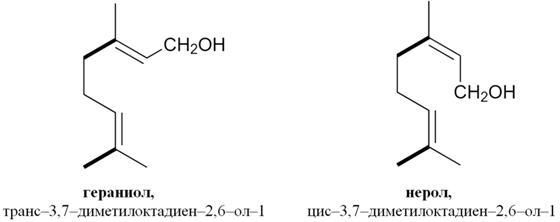
Ациклические монотерпены:
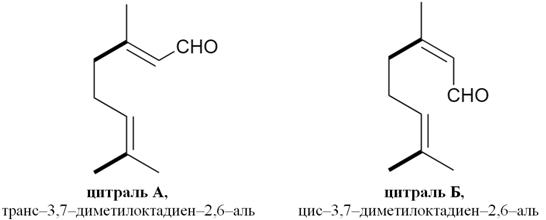
1) Гераниол и нерол содержатся в гераниевом, розовом и других маслах в свободном виде и в виде сложных эфиров. Применяются как душистые вещества в парфюмерной промышленности. При осторожном окислении гераниола и нерола получаются альдегиды цитраль А и цитраль Б.
2) Цитраль А и цитраль Б получаются при осторожном окислении гераниола и нерола. Природныйцитральявляется смесью обеих форм и находится в эфирных маслах растений, особенно в лимонном, эвкалиптовом, лемонграссовом проявляет антисептическое, болеутоляющее и противовоспалительное действие, применяется в медицине в глазной практике. Используется в пищевой и парфюмерной промышленности, а также в качестве сырья для синтеза ретинола (витамина А).
Моноциклические монотерпены:
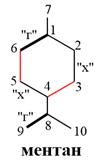
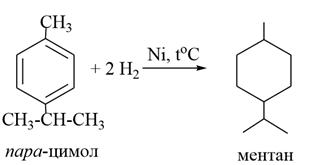
1) Ментан лежит в основе моноциклических монотерпенов – производное циклогексана: 1-изопропил-4-метилциклогексан. В природе ментан не встечается, его получают гидрированием пара–цимола (п–изопропилтолуола).
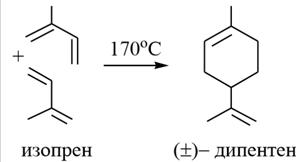
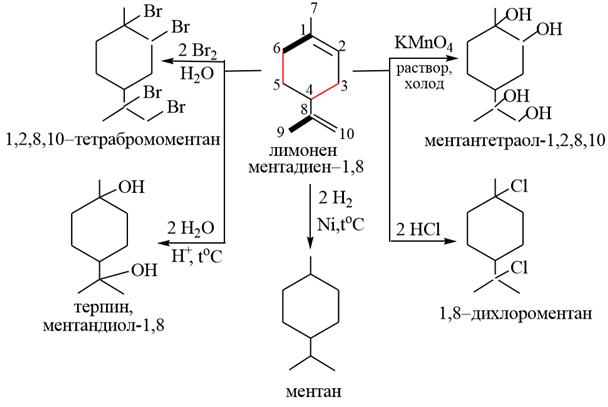
2) Лимонен – один из самых распространенных терпенов. Молекула лимонена содержит один асимметрический атом углерода и существует в виде пары энантиомеров. Так, лимонен (+) содержится в лимонном и апельсиновом маслах, а также в маслах укропа, тмина, сельдерея, бергамота. Лимонен (-) является основной составной частью масла хвойных игл. Рацемическую смесь лимоненов называют дипентеном. Дипентен может быть получен из димеризацией изопрена.
Алкилзамещенные дипентены являются психоактивным действующим началом гашиша (марихуана). Лимонен является изолированным диеном, поэтому в химическом отношении ведет себя как алкен, и может присоединять водород, галогеноводороды, обесцвечивать бромную воду, окисляться в условиях реакции Вагнера.
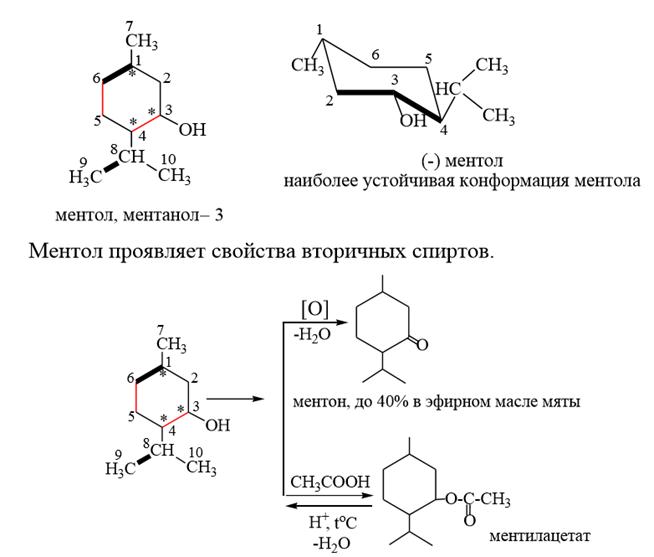
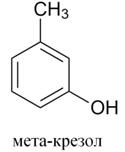
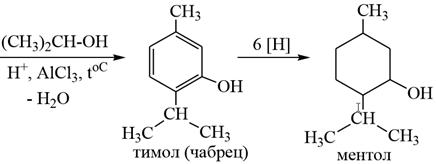
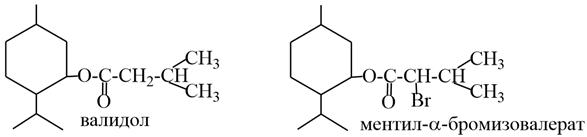
3) Ментол – терпеноид, относится к кислородсодержащим производным ментана. Ментол – белое кристаллическое вещество с приятным запахом и холодящим вкусом (т. пл.=42оС), основной компонент мяты перечной. Ментол плохо растворяется в воде, хорошо в спирте и других органических растворителях. Ментол имеет в молекуле три асимметрических атома углерода (С*) и может существовать в виде восьми оптических изомеров. Наиболее важным и устойчивым является изомер, у которого все заместители располагаются экваториально. В промышленности рацемический D,L – ментол получают из мета– крезола алкилированием его по Фриделю – Крафтсу изопропиловым спиртом в присутствии концентрированной серной кислоты. Ментол используется в пищевой и парфюмерной промышленности, обладает бактерицидными свойствами и спазмолитическим действием, входит в состав ингаляций и мазей, применяемых при насморке. В виде сложного эфира α-бромизовалериановой кислоты входит в состав лекарственных препаратов: валокордин, валосердин, корвалол. Препарат «Валидол» (успокаивающее средство) является сложным эфиром ментола и изовалериановой кислоты.
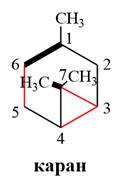
Бициклические монотерпены:
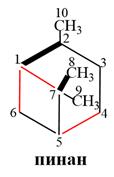
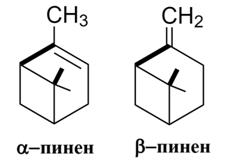
Ряд пинана:
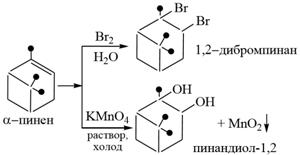
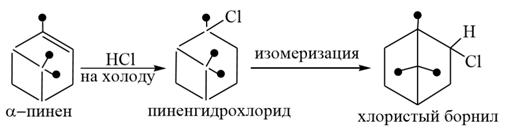
1) α–пинен – жидкость с запахом хвои, его левовращающий изомер является основной составной частью скипидара (до 70-75 %). Применяется для получения камфоры, терпингидрата, инсектицидов, и в качестве растворителя. Скипидар извлекают из живицы, которая вытекает из надрезов на стволах сосны. Живица – раствор канифоли (смесь смоляных кислот с формулой С19Н29СООН) в скипидаре. Скипидар состоит из разных терпенов. Получают скипидар из живицы отгонкой с водяным паром. Скипидар – бесцветная жидкость, легче воды, применяется в текстильной промышленности, лакокрасочной промышленности для приготовления лаков, в парфюмерии, для синтеза камфоры.
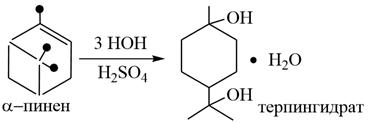
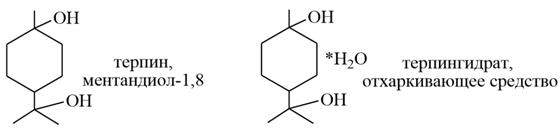
При действии воды в присутствии серной кислоты пинен дает терпингидрат. В медицинской практике применяется моногидрат терпина под названием терпингидрат в качестве отхаркивающего средства. Получают терпингидрат из α-пинена
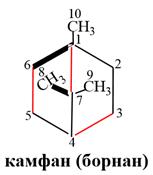
Ряд камфана:
2) Борнеол содержится в эфирном масле валерианы, тимьяна, его получают из эфирного масла камфорного лавра, произрастающего в Японии и на острове Борнео. В масле сибирской пихты содержится борнилацетат, омылением которого получают борнеол.
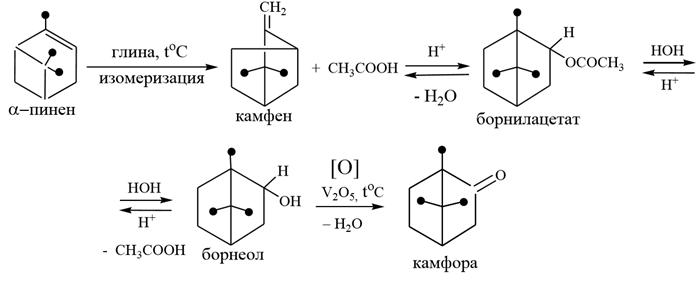
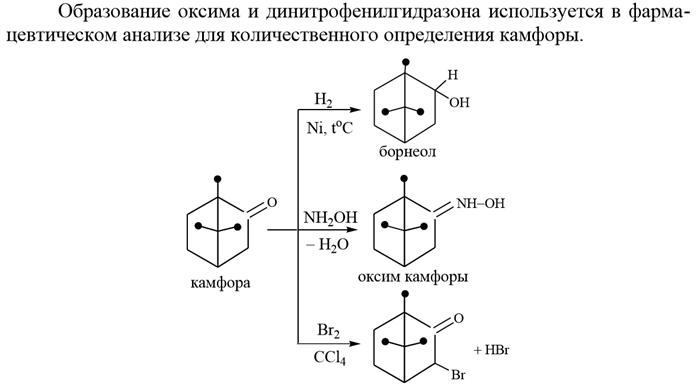
3) Камфора (борнано-2) представляет собой бесцветные кристаллы с характерным запахом. Правовращающая камфора получается из камфорного дерева (Япония, Тайвань) отгонкой из измельченной древесины с водяным паром. Левовращающая камфора в настоящее время получается из борнилацетата, рацемическая камфора – из α–пинена. Камфора издавна применяется в медицине в качестве антисептического средства и как стимулятор сердечной деятельности. Синтез камфоры из α–пинена по методу Тищенко В.Е
Образование оксима и динитрофенилгидразона камфоры используется в фармацевтическом анализе для количественного определения камфоры. При действии брома на камфору бромируется α–положение к карбонильной группе с образованием 3–бромокамфоры. Бромокамфора улучшает деятельность сердца, оказывает успокаивающее действие на центральную нервную систему.
Дитерпен:
Фитол - самый распространенный представитель ациклических дитерпеноидов, непредельный спирт, входящий в состав хлорофилла и витамина К.
Тетратерпены:
Каротиноиды составляют особую группу терпенов, которые являются растительными пигментами. Некоторые из них играют роль витаминов или предшественников витаминов, а также участвуют в фотосинтезе. Их молекулы содержат значительное число сопряженных двойных связей и поэтому окрашены. Их окраска меняется от желтого до ярко–красного цвета. Каротиноиды содержат 40 атомов углерода в молекуле. Они растворимы в растительных и животных жирах, многие из них легко окисляются кислородом воздуха. Каротиноиды широко распространены в природе; вместе с хлорофиллом содержатся не только в зеленых частях растений, но и в семенах. В организм животных они попадают с пищей.
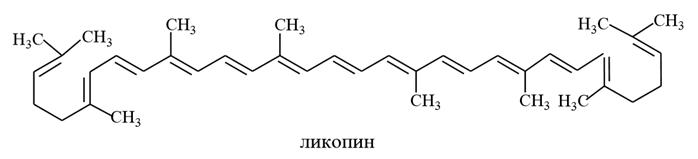
1) Природные каротиноиды можно рассматривать как производные ликопина, содержащегося в плодах томата, шиповника, ягодах и фруктах. При замыкании одного или двух колец на концах молекулы ликопина образуются α-, β-, или γ–каротины, отличающиеся количеством и строением боковых колец.
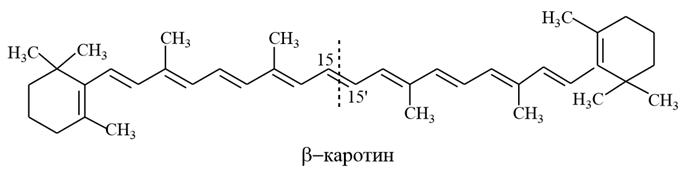
2) Каротин – пигмент желто–красного цвета, содержащийся в большом количестве в моркови, а также в молоке, сливочном масле, листьях растений и многих плодах. Каротин не индивидуальное вещество, а состоит из трех изомеров - α-, β- и γ – каротинов. Наиболее важным является β- каротин.
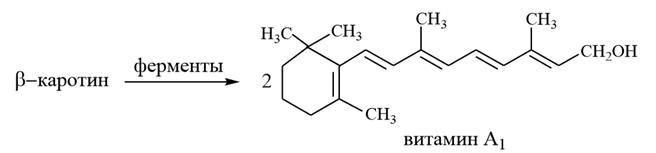
Все изомеры каротина являются предшественниками витаминов группы А, т.е. провитаминами группы А. Каждая из них in vivo дает молекулу витамина А1. Молекула β–каротина симметрична и состоит из двух одинаковых частей. Под влиянием ферментов в организме молекулы β – каротина разрываются по связи С15 – С16 с образованием двух молекул витамина А1.
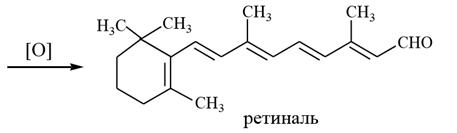
3) Витамин А1 – ретинол, содержится только в продуктах животного происхождения (сливочное масло, яичный желток, печень животных и морских рыб). Витамин А считается фактором роста. При его недостатке в пище наблюдается задержка роста, исхудание, высыхание роговицы глаз (ксерофтальмия), понижается сопротивляемость организма к инфекционным заболеваниям. В организме ретинол окисляется в ретиналь. Ретинол и ретиналь участвуют в зрительном цикле, в процессе зрительного цветовосприятия.
Стероиды (сложные неомыляемые липиды)
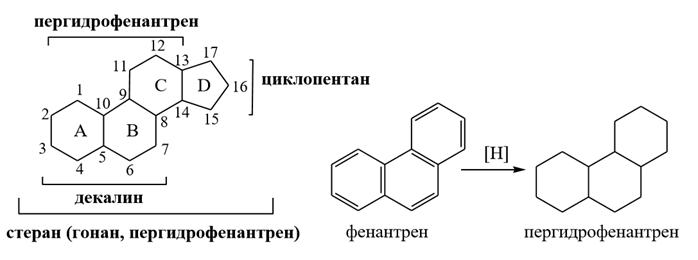
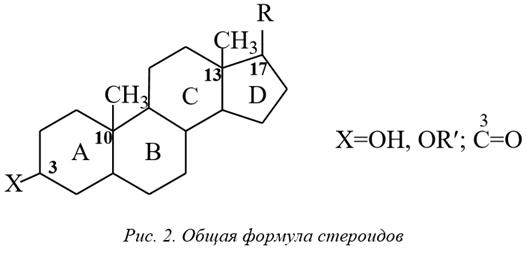

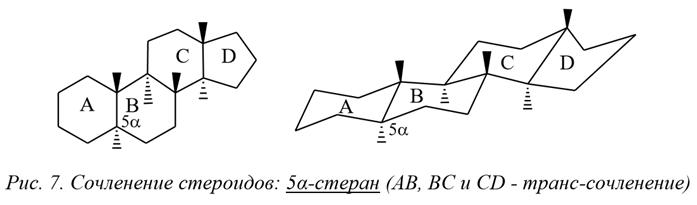
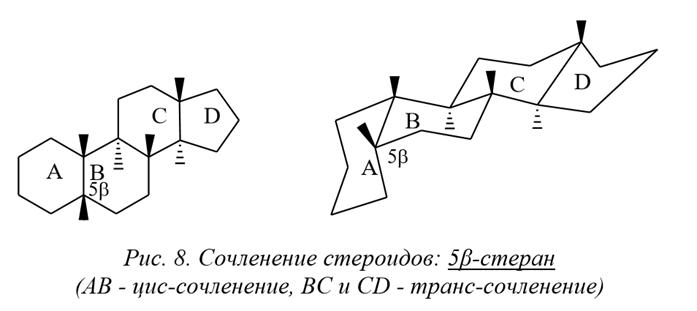
I. Стерины
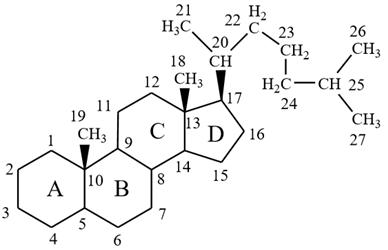
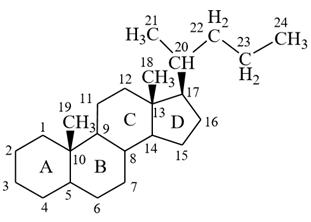
холестан (в основе)
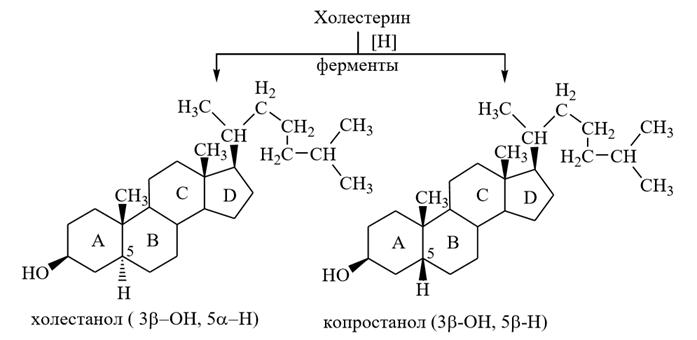
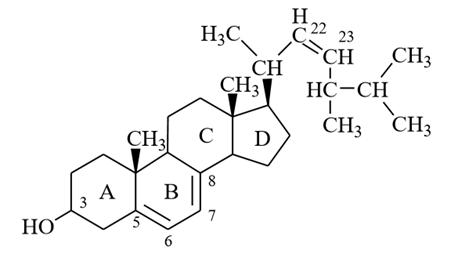
эргостерин (тип микостеринов)
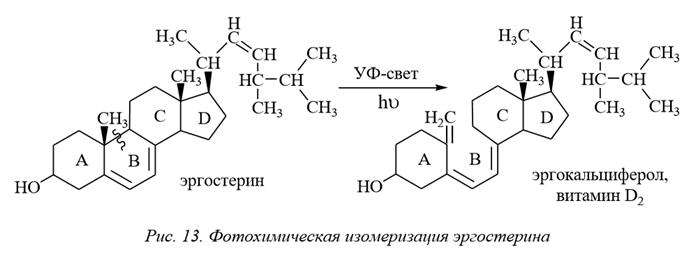
 7-дегидрохолестерина холекальциферол
7-дегидрохолестерина холекальциферол
(холестадиен-5,7-ола-3β) (витамин D3)
I. Стерины:
Холестан в основе.
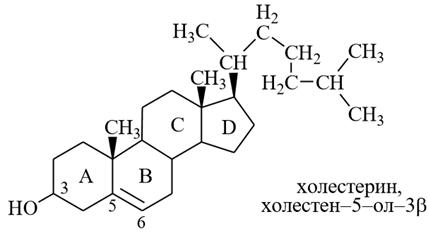
Зоостерины встречаются в организмах животных и человека. Наиболее важным является холестерин (холестерол) или холестен–5–ол–3β.
1) Холестерин – бесцветное кристаллическое вещество, присутствует практически во всех животных клетках, особенно много в нервной и мозговой ткани, участвует в построении клеточных мембран. В животных организмах холестерин содержит в свободном виде или в виде сложных эфиров с карбоновыми кислотами, в том числе и с ВЖК. Холестерин используется организмом для синтеза желчных кислот и стероидных гормонов. Основное количество холестерина (80 %) синтезируется в организме из ацетилкофермента А, остальное (20 %) поступает в организм с пищей. Излишки холестерина выводятся из организма в основном через пищеварительный тракт, и небольшое количество – сальными железами. При нарушении обмена веществ в организме человека холестерин откладывается на стенках сосудов в виде бляшек, стенки сосудов суживаются, что является одной из причин возникновения атеросклероза. Кроме того, холестерин может накапливаться в виде желчных камней. Получают холестерин из спинного мозга животных и из ланолина (жироподобного вещества, смываемого с овечьей шерсти), используют для синтеза стероидных гормонов и витамина D3 (антирахитического).
2) Э ргостерин (эргостерол; представитель микостеринов) или 24–метилхолестатриен–5,7,22–ол–3β (рис. 12) в больших количествах содержится в дрожжах, откуда его и получают. Эргостерин является предшественником эргокальциферола (витамина D2), который образуется из эргостерина в результате фотохимической изомеризации. Изомеризация провитаминов D2 происходит в коже человека под действием солнечных лучей. В результате реакции раскрывается кольцо В (связь разрывается между С-9 и С-10) и образуется дополнительная двойная связь. Аналогичным образом из 7-дегидрохолестерина (холестадиен-5,7-ола-3β) синтезируется холекальциферол (витамин D3).
3) Витамин D2 – белое кристаллическое вещество, содержится в молоке, рыбьем жире, сливочном масле, яичном желтке. Витамины группы D регулируют фосфорнокальциевый обмен, недостаток витамина D вызывает нарушение усвоения кальция и включения его в костную ткань, что является причиной возникновения рахита у детей. Избыточные дозы витамина D обладают токсическим действием – отложение кальция в почках и на стенках кровеносных сосудов. Кальциферолы в промышленности получают облучением провитаминов D УФ-светом в органическом растворителе. Непосредственно эргостерин получают в промышленности из дрожжей экстракцией органическим растворителем.
II. Желчные кислоты


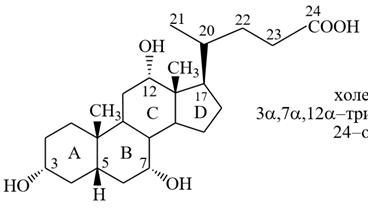
холан (в основе)
Доп.: урсодезоксихолевая кислота – 3α,7β-дигидрокси-5βхолан-24-овая кислота.
II. Желчные кислоты:
Холан в основе.
Из желчи было выделено 4 желчные кислоты. Они получили название холевых кислот. Структурные особенности: цис-сочленение колец А и В; алифатическая боковая цепь в состоит из пяти атомов углерода и включает концевую карбоксильную группу.
1) Холевая кислота (3α,7α,12α −тригидрокси−5β−холан− 24−овая кислота) – наиболее частая, α-конфигурация.
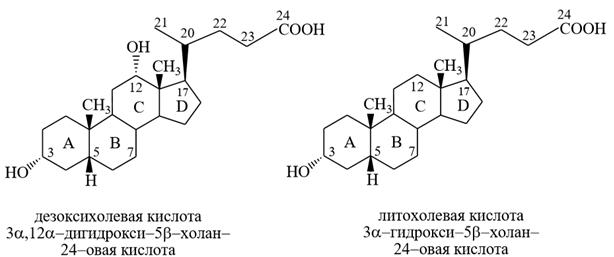
2) Дезоксихолевая кислота (3α, 12α-дигидрокси-5β-холан-24-овая кислота) отличаются от холевой кислоты отсутствием гидроксильной группы в положении С–7.
3) Литохолевая кислота (3-гидрокси-5β-холан-24-овая кислота) отличаются от холевой кислоты отсутствием гидроксильных групп в положениях С–7 и С–12.
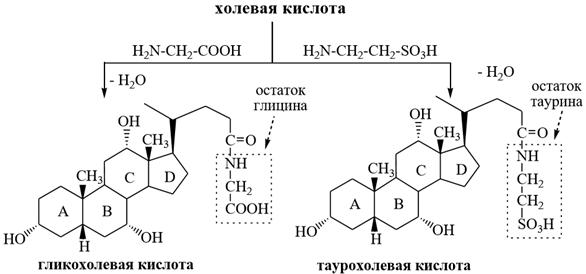
В желчи желчные кислоты находятся обычно не в свободном состоянии, а в виде амидов аминокислот: глицина (аминоуксусной кислоты) – гликохолевая кислота и таурина (2–аминоэтансульфокислоты) – таурохолевая кислота.
В форме ацильных производных желчные кислоты имеют гидрофобную часть (гонановый скелет) и гидрофильную часть (ионизированную карбоксильную или сульфогруппу), поэтому обладают поверхностно-активными свойствами, т.н. способностью располагаться на границе раздела фаз. Соли гликохолевой и таурохолевой кислот со щелочными металлами также обладают поверхностно-активными свойствами, поэтому способны эмульгировать жиры пищи, улучшая её усвоение в кишечнике. Кроме того, они активируют фермент липазу, катализирующий гидролиз жиров.
Из медвежьей желчи выделена урсодезоксихолевая кислота (3α, 7β-дигидрокси-5β-холан-24-овая кислота), которая способствует растворению других желчных кислот и используется для лечения желчекаменной болезни.
III. Половые гормоны (стероидные гормоны)
Андрогены
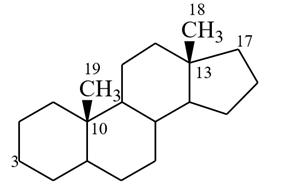
андростан (в основе)
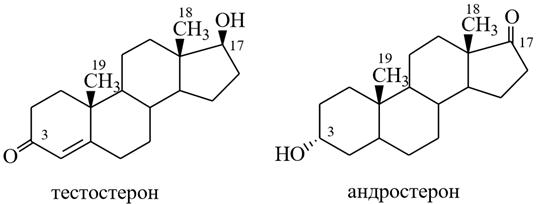
17β– гидроксиандростен–4–он–3 3α–гидрокси–5α–андростанон–17
Синтетический андроген:
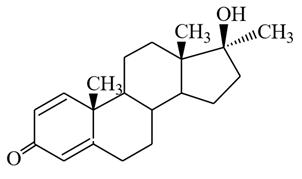
метандростенол
Эстрогены
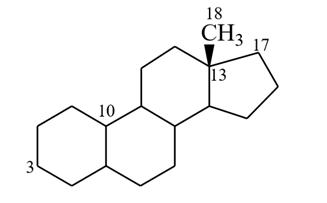
эстран (в основе)
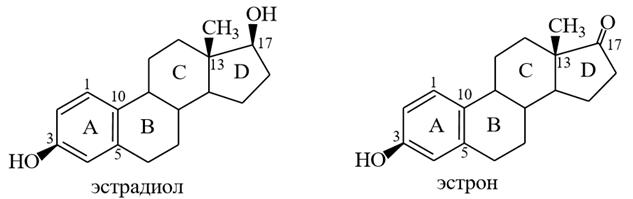
эстратриен–1,3,5 (10)–диол–3, 17β 3–гидроксиэстратриен–1,3,5 (10)–он–17
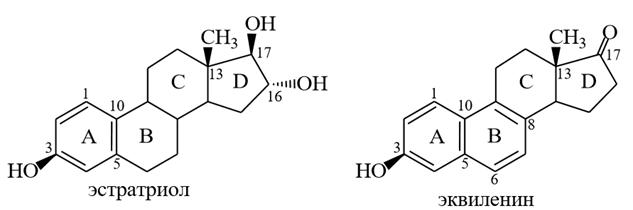
эстратриен–1,3,5 (10)–триол–3, 16α, 17β 3–гидроксиэстрапентаенен–1,3,5 (10),6,8–он–17
Синтетические эстрогены:
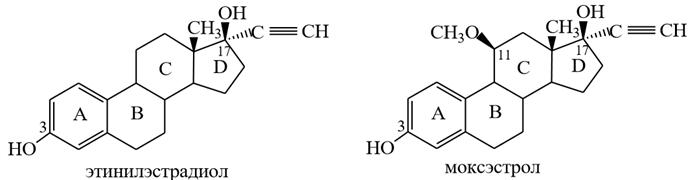
17α-этинилэстрадиол 11β-метокси-17α-этинилэстрадиол
Синтетические эстрогены нестероидной природы:

1,2-дифенилэтилен 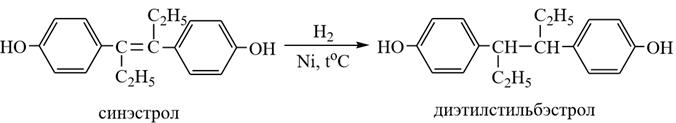
транс–3,4–ди(пара–гидроксифенил)гексен–3 мезо–3,4–ди(пара–гидроксифенил)гексан
Гестагены
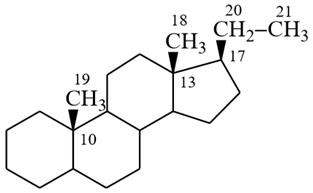
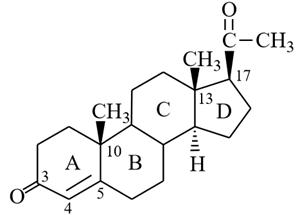
прегнан (в основе) прогестерон
III. Половые гормоны (стероидные гормоны):
Андрогены
Андростан в основе.
Для андрогенов характерно: отсутствие алкильного заместителя у С-17 и наличие кислородсодержащих (вторичного спиртового гидроксила или кетонной) функциональных групп у атомов С-3 и С-17.
Андрогенные гормоны вырабатываются мужскими половыми железами, они регулируют развитие и функционирование репродуктивной деятельности мужчин (самцов): возникновение вторичных половых признаков, работу половых желез, сперматогенез, рост организма в целом. Андрогены применяют при мужской климактерии и связанных с ней нервных и вазомоторных расстройствах, при импотенции. У женщин андрогены применяются при климактерических расстройствах. Важнейшими андрогенами являются тестостерон (17β– гидроксиандростен– 4–он–3) и андростерон (3α–гидрокси–5α–андростанон–17).
1) Тестостерон проявляет наибольшую гормональную активность, у взрослого мужчины в сутки вырабатывается 4-9 мг тестостерона, он содержит в положении С–3 кетонную и у С–17 гидроксильную группы, в положении С–4 двойную связь.
2) Андростерон обладает меньшей гормональной активностью, которая составляет ~10 % от активности тестостерона, имеет в положении С–3 гидроксильную, а в положении С–17 карбонильную группы.
Оба гормона имеют две ангулярные (угловые) метильные группы, кольца А и В транс–сочленены.
В проявлении гормональной активности у андрогенов большая роль отводится АВ-транс-соединению колец (АВ-цис-соединения не обладают гормональной активностью, например, метаболит андрогенов тестанолон). Изменения же у С-3 и С-17 не влияют на это. Сложные эфиры андрогенов обладают более высокой активностью, чем сами гормоны за счет того, что ацилированные («защищенные») группы более медленно метаболизируют в организме. В медицине в таблетках тестостерон и андростерон применяют в виде сложных эфиров. Андрогенные гормоны обладают также анаболической активностью, т.е. усиливают белковый обмен, рост мышечной ткани, кальцификацию костей.
Синтетические стероиды, обладающие анаболической активностью (метандростенолон, станозолол, силаболил), используются при нарушениях белкового обмена, дистрофии, после длительных инфекционных заболеваний, в послеоперационный период при ожогах и тяжелых травмах. За счет параллельного андрогенного действия вызывают ряд нежелательных побочных эффектов (рост волос по всему телу и на лице, огрубление голоса и др.). Применяют анаболические стероиды также в сельском хозяйстве для ускорения роста скота. Очень серьёзной проблемой является использование анаболических стероидов спортсменами для ускорения наращивания мышечной массы, т.к. их длительное применение приводит к выпадению волос на голове, поражению печени, гипертрофии миокарда, гипертонической болезни, атрофии яичек, акне, маскулинизации (накопление вторичных мужских половых признаков у женщин) или феминизации (накопление вторичных женских половых признаков у мужчин).
Рибоксин – нестероидное анаболическое (метаболическое) средство.
Эстрогены
Эстран в основе.
Для эстрогенов характерно: отсутствие алкильных заместителей у С-10 и С-17, а также наличие ароматического характера кольца А, наличие фенольного гидроксила у С-3 и вторичной спиртовой или кетонной группы у С-17.
1) Эстрадиол (эстратриен–1,3,5 (10)–диол–3, 17β) – вырабатывается в яичниках, является наиболее активным эстрогенным гормоном, выделен также из цветков ивы.
2) Эстрон (3–гидроксиэстратриен–1,3,5 (10)–он–17) – образуется при окислении эстрадиола, его активность составляет примерно 1/3 от активности эстрадиола, найден также в косточках фиников, семечках яблок и граната.
Эстрадиол и эстрон в организме превращаются друг в друга в результате окислительно-восстановительных реакций.
3) Эстриол (эстратриен–1,3,5 (10)–триол–3, 16α, 17β) – один из главных метаболитов эстрогенных гормонов, его активность очень низкая (1,5-2 % от активности эстрадиола).
4) Эквиленин (3–гидроксиэстрапентаенен–1,3,5 (10),6,8–он–17) – в его структуре ароматическим является не только кольцо А, но и кольцо В – обладает высокой эстрогенной активностью.
Эстрогенные гормоны управляют женской репродуктивной функцией, контролируют менструальный цикл. Применяются в медицине для лечения заболеваний, связанных с недостаточной функцией половых желез, бесплодием, при слабой родовой деятельности, для лечения некоторых онкологических заболеваний (например, рака предстательной железы), при лечении язвенной болезни, а также вместе с гестагенными гормонами входят в состав комплексных оральных контрацептивов.
Природные эстрогены не активны при пероральном применении, поэтому более широко используются синтетические эстрогены, имеющие алкильный радикал при С-17, за счет которого нивелируется недостаток природных, т.к. третичные спирты не способны окисляться в менее активные карбонильные соединения. К таким препаратам относятся: 17α-этинилэстрадиол и моксэстрол (11β-метокси-17αэтинилэстрадиол), обладающие очень высокой эстрогенной активностью.
Синтетические эстрогены нестероидной структуры: синэстрол (транс–3,4–ди (пара–гидроксифенил)гексен-3); диэтилстильбэстрол (мезо–3,4–ди (пара–гидроксифенил)гексан). Они являются производными стильбена (симметричного дифенилэтилена). Диэтилстилбэстрол и синэстрол применяют при лечении различных онкологических заболеваний (рака предстательной железы, молочной железы), а также в ветеринарии.
Гестагены
Прегнан в основе.
Для гестагенов характерно наличие винилкетонного фрагмента при С-3–С-5 и кетонных групп у атомов С-3 и С-20.
1) Прогестерон (гормон желтого тела; прегнен–4–дион–3, 20) по химической структуре схож с мужским половым гормоном тестостероном. Прогестерон способствует протеканию беременности, для медицинского применения он получается синтетическим путем. Прогестерон и его аналоги применяют при аменорее, кровотечениях, бесплодии, невынашивании беременности, а также вместе с эстрогенными гормонами входят в состав комплексных оральных контрацептивов. Некоторые гестагены (дроспиренон, диеногест, ципростерона ацетат) обладают антиандрогенной активностью, что используется также в лечении акне, в составе таких современных оральных контрацептивов как: диане-35, жанин, ярина и др.
IV. Кортикостероиды (стероидные гормоны)
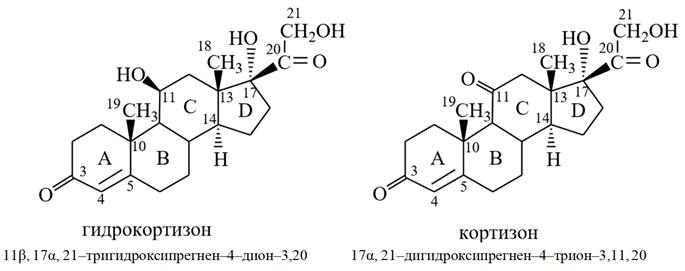
Глюкокортикоиды
 2. Минералокортикоиды
2. Минералокортикоиды
 Синтетические аналоги кортизона и гидрокортизона:
Синтетические аналоги кортизона и гидрокортизона:
IV. Кортикостероиды (стероидные гормоны):
Прегнан в основе.
Кортикостероиды вырабатываются в коре надпочечников.
Всего из коры надпочечников выделено 46 кортикостероидов. По характеру воздействия на процессы обмена в организме кортикостероиды делят на 2 группы.
Глюкокортикостероиды: регулирующие обмен углеводов, белков, жиров и нуклеиновых кислот;
1) Гидрокортизон (11β, 17α, 21–тригидроксипрегнен–4–дион–3,20).
2) Кортизон (17α, 21–дигидроксипрегнен–4–трион–3,11, 20).
Глюкокортикостероиды оказывают активное влияние на углеводный и белковый обмен. Они повышают содержание глюкозы в крови, способствуют накоплению гликогена в печени, вызывают увеличение выделения азота с мочой. Недостаток глюкокортикоидов сопровождается падением уровня глюкозы в крови и гликогена в печени. Глюкокортикостероиды проявляют противовоспалительное и антиаллергическое действие.
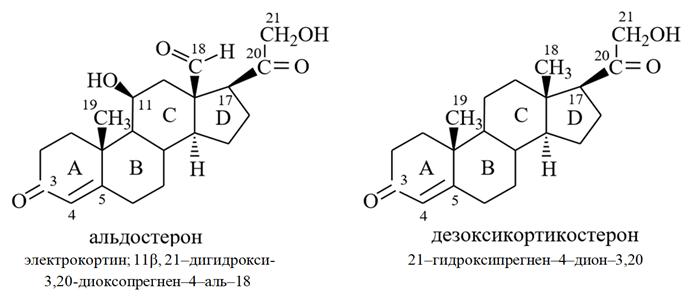
Минералокортикостероиды: влияют на солевой обмен (обмен Na+, K+ и воды).
3) Альдостерон (электрокортин, 11β, 21–дигидрокси-3, 20-диоксопрегнен–4–аль–18);
4) Дезоксикортикостерон (21–гидроксипрегнен–4–дион–3,20).
Минералокортикостероиды регулируют главным образом обмен натрия, калия, хлора и воды. Они способствуют удерживанию ионов натрия и хлора в организме и выведению с мочой ионов калия. Нехватка минералокортикоидов приводит к потере ионов Na+ и воды при одновременном росте содержания ионов К+.
Гормоны коры надпочечников необходимы для жизнедеятельности организма. Острая недостаточность надпочечников сопровождается сгущением крови, понижением артериального давления, астенией, желудочно-кишечными расстройствами и др. При введении кортикостероидов наблюдается увеличение уровня липидов в крови, подавление роста лимфоидной ткани (тимуса, селезёнки, лимфатических узлов), подавлению воспалительной реакции. Из природных кортикоидов в качестве лекарственных препаратов применяются: гидрокортизон, кортизон и дезоксикортикостеронацетат. Данные препараты обладают противовоспалительной, антиаллергической, иммунодепрессивной и др. видами фармакологической активности, благодаря чему широко применяются в медицине для лечения артритов, артрозов, ревматизма, бронхиальной астмы, некоторых воспалительных заболеваний кожи (розовые угри). Более широкое применение данных препаратов ограничивают их побочные эффекты, связанные с минералокортикоидной активностью, поскольку задержка в организме ионов натрия и воды приводит к гипертонии и отёкам. Поэтому, разработано большое число синтетических аналогов кортикостероидов, обладающих меньшим количеством побочных эффектов.
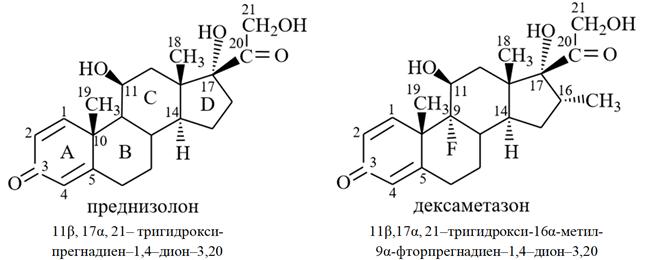
Синтетические аналоги кортизона и гидрокортизона: препараты преднизолон (11β, 17α, 21– тригидроксипрегнадиен–1,4–дион–3,20) и дексаметазон (11β, 17α, 21–тригидрокси-16αметил-9α-фторпрегнадиен–1,4–дион–3,20).
Эти соединения более активны, чем природные кортикоиды, действуют в меньших дозах, оказывают меньшее влияние на минеральный обмен: • введение двойной связи в положение С-1 значительно повышает противовоспалительную и глюкокортикоидную активность; • заместители в положении С-16 (16α-гидрокси-, 16α- или 16β-метил) существенно снижают минералокортикоидную активность (не развиваются отёки и гипертония); • атом фтора или хлора в положении С-9α также способствуют усилению глюкокортикоидной активности (индуктивный эффект атома галогена усиливает кислотные свойства средней 11βОН-группы, из-за чего она образует более прочную водородную связь с рецептором; 9α-фторостероиды труднее окисляются за счёт 11β-спиртовой группы в менее активные 11-кетостероиды).
Синтетические кортикостероиды применяют также для лечении ревматизма, бронхиальной астмы, воспалительных процессов кожи. Дексаметазон широко применяется в глазной практике для лечения конъюктивитов различной этиологии.
Те аналоги кортикостероидов, которые не имеют 11β-ОН-группы – не обладают гормональной активностью, потому, что не могут связываться с клеточным рецептором. Например, калийсберегающий диуретик (мочегонное средство) спиронолактон (верошпирон), который не имеет 11β-ОН-группы, является антагонистом альдостерона, т.е. оказывает противоположный альдостерону эффект – наоборот выводит воду и ионы натрия и задерживает иона калия.
V. Агликоны сердечных гликозидов
Группы агликонов:
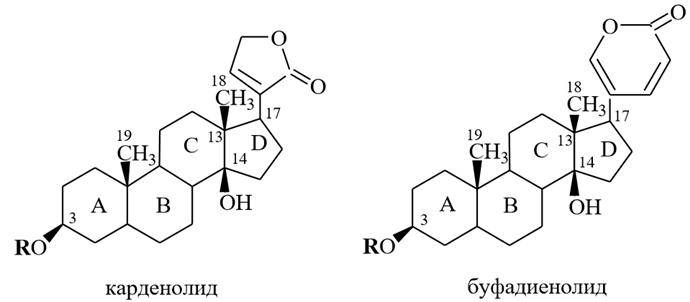
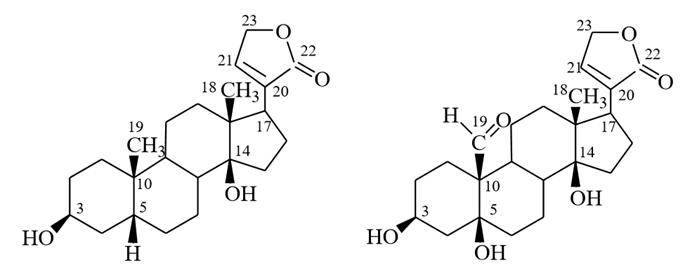
дигитоксигенин (карденолид) строфантидин (буфадиенолид)
3β,14βдигидрокси-5β-карден-20(22)-олид; 3β,5β,4β-тригидрокси-19-оксо-5β-карден-20(22)-олид
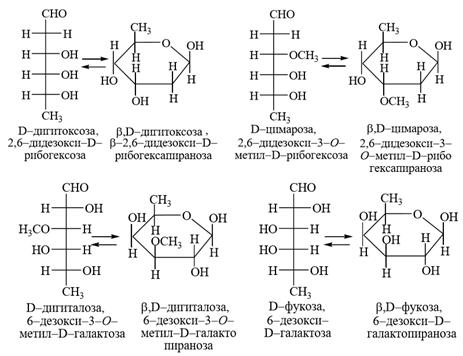
Метилентозы сердечных гликозидов:
Получение сердечного гликозида – Лантанозида А.
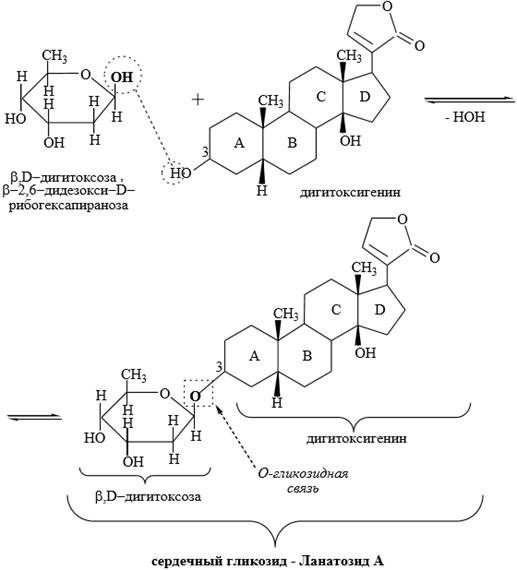
V. Агликоны сердечных гликозидов
Сердечные гликозиды – это стероиды растительного происхождения – содержатся в некоторых растениях, таких, как различные виды наперстянки, лютики, майский ландыш, строфант, олеандр, горицвет весенний и др. Представляют собой О- гликозиды, в молекулах которых несахарная часть агликон (генин) имеет стероидную структуру, а углеводный фрагмент представлен остатками моно-, ди-, три- или тетрасахарида.
Связь между углеводом и агликоном является β–гликозидной и осуществляется за счет гидроксильной группы у С–3 циклопентанопергидрофенантренового ядра. Кроме того, агликоны (генины) содержат также у С–14 гидроксильную, у С–13 метильную группы, а у С–17 – ненасыщенное лактонное кольцо. Кольца АВ и СD имеют циссочленение. Наличие ненасыщенных лактонных колец обусловливает неустойчивость сердечных гликозидов в щелочных растворах, легко гидролизующих лактоны. По характеру лактонного кольца агликоны сердечных гликозидов (рис. 30) делят на две группы: - карденолиды, содержащие у С–17 пятичленное ненасыщенное лактонное кольцо; - буфадиенолиды, имеющие у С–17 шестичленное ненасыщенное лактонное кольцо (найдены в растениях семейств лютиковых и лилейных).
Важнейшими карденолидами (рис. 31) являются дигитоксигенин (3β, 14βдигидрокси-5β-карден-20(22)-олид) и строфантидин (ангулярная группа С-19 окислена до альдегидной - 3β, 5β, 4β-тригидрокси-19-оксо-5β-карден-20(22)-олид).
Дигитоксигенин – агликон (генин) гликозида наперстянки дигитоксина, строфантидин – агликон строфантина – гликозида строфанта. Отмечена фармакологическая особенность, заключающаяся в том, что строоение заместителя у атома С-10 стероидного агликона существенно влияет на продолжительность действия сердечного гликозида. Те гликозиды, агликоны которых у атома С-10 имеют метильную группу (тип наперстянки, например, дигитоксигенин), действуют медленно и имеют свойство накапливаться в организме. Если у атома С-10 гликозида находится альдегидная группа или гидроксиметильная группа (СН2ОН) (тип строфанта, например, строфантидин, строфантидол), то действует быстро и так же быстро выводится из организма.
В состав углеводной компоненты гликозидов входят широко распространенные в растительном мире D–глюкоза, D–фруктоза, D–ксилоза, D-рамноза. Кроме того, входят в основном необычные специфические моносахариды, встречающиеся только в сердечных гликозидах, на сегодняшний день выделено около 35 различных моносахаридов. Большинство из них являются 6-дезокси- или 2,6-дидезоксисахарами: D-дигитоксоза, D-цимароза, D-дигиталоза, D-фукоза (рис. 32).
Сердечные гликозиды обладают выраженным кардиотоническим действием и широко используются при лечении сердечно-сосудистых заболеваний в виде настоек, экстрактов и т.д., в больших дозах являются сердечными ядами. Сердечные гликозиды действуют непосредственно на сердечную мышцу, увеличивая силу ее сокращения, они также оказывают сосудосуживающее действие. Многие сердечные гликозиды обладают цитотоксическим действием и используются в качестве противоопухолевых средств.
Гетероциклы
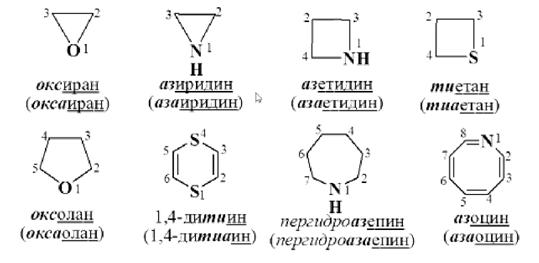
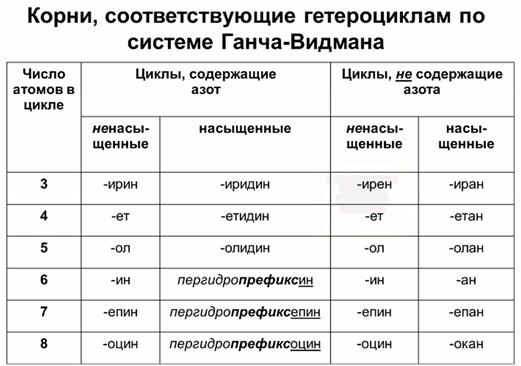
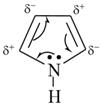
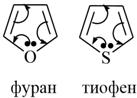
<




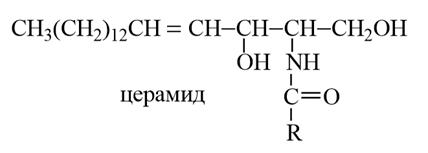 R = остаток ВЖК
R = остаток ВЖК


























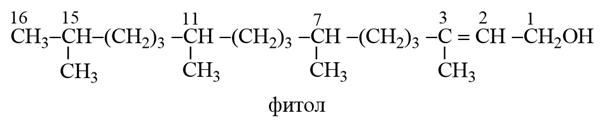














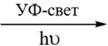 7-дегидрохолестерина холекальциферол
7-дегидрохолестерина холекальциферол
















 2. Минералокортикоиды
2. Минералокортикоиды Синтетические аналоги кортизона и гидрокортизона:
Синтетические аналоги кортизона и гидрокортизона:











