На сегодняшний день существует несколько технологий применения ингибиторов коррозии, это:
· непрерывное дозирование,
· непрерывное дозирование с предварительной ударной дозировкой,
· пробковые технологии,
· периодическая подача,
· закачка в пласт.
На Арланском месторождении (Вятская площадь) были проведены испытания ввода 4–х ингибиторов коррозии по различным технологиям. В табл. 2 в качестве примера приведена сравнительная эффективность некоторых предлагаемых технологий.
Таблица 2
Сравнительная эффективность предлагаемых технологий использования ингибиторов коррозии
Предлагаемое
Мероприятие
Экономический эффект, млн.руб.
Защитный эффект, %
| | Рекорд-608
| ХПК-002В*
| Сонкор-9801
| Азимут
14 Б
|
| Постоянная
дозировка в системе нефтесбора и системе ППД
| -
10,1
| 2,957
61,8
| 1,670
66,3
| 1,584
70,8
|
| Периодическая дозировка через каждые две недели в течении двух суток
| 18,298
10,1
| 17,909
61,8
| 18,078
66,3
| 18,089
70,8
|
| Периодическая дозировка + магнитная обработка
| 15,498
67,4
| 15,109
85,4
| 15,278
71,9
| 15,289
78,7
|
| Постоянная дозировка в системе нефтесбора
| 10,595
10,1
| 8,542
61,8
| 9,213
66,3
| 9,257
70,8
|
| Постоянная дозировка только в системе нефтесбора +
магнитная обработка
| 7,795
67,4
| 5,742
85,4
| 6,413
71,9
| 6,457
78,7
|
Типовые задачи по теме «Осложнения, связанные с внутренней коррозией промысловых трубопроводов»
Коррозия железа обуславливается наличием в воде кислорода, агрессивной углекислоты и сероводорода.
В пластовых водах существует равновесие:
 . (19)
. (19)
Из этого уравнения равновесия следует, что для поддержания определенной концентрации бикарбонат-ионов HCO3–, требуется, чтобы в воде присутствовало соответствующее этой концентрации количество свободного углекислого газа CO2, которое называют равновесным.
Если фактически присутствующее в воде количество CO2 больше равновесной концентрации, то избыток его способен вызвать растворение СаСО3, т.е. сдвинуть равновесие влево и довести рН воды до 3,5, при котором металл сильно корродирует. Такую воду называют агрессивной. При недостатке в воде CO2по сравнению с равновесной концентрацией бикарбонат-ионы HCO3- распадаются, т.е. равновесие сдвигается вправо, что приводит к выделению из воды осадка карбоната кальция СаСО3.
Если фактическое содержание в воде углекислого газа совпадает с равновесной концентрацией, из воды не будет выделяться осадок карбоната кальция и она не способна растворять СаСО3. Такая вода называется стабильной (рН=7).
Задача 1. Определение агрессивной углекислоты в пластовой води и определение типа воды.
По химическому составу воды (табл. 3) определить тип воды и наличие в ней агрессивной углекислоты.
Таблица 3
Состав минерализованной воды
Содержание ионов, мг/л
Свободная СО2, мг/л
| | Na+
| K+
| Ca2+
| Mg2+
| Cl-
| SO42-
| HCO 3 -
|
| 26,3
| 7
| 25,9
| 17
| 18
| 11,5
| 195,2
| 17,6
|
Решение.
1. Количество агрессивной углекислоты определяют по графикам, составленным Лаптевым Ф.Ф., в которых используется содержание связанной и свободной углекислоты. Для этого необходимо определить соотношение:
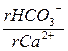 , (20)
, (20)
где ri – содержание иона в эквивалентной форме:
 (21)
(21)
где qi - содержание иона, мг/л, Э i - эквивалент иона (табл. 4), М i – молекулярная масса иона; В i - валентность иона..
Таблица 4
Эквиваленты ионов
| Ион
| Na+
| Mg2+
| Ca2+
| K+
| Fe3+
| Cl-
| SO42-
| HCO3-
| CO32-
|
| М i
| 23
| 24
| 40
| 39
| 56
| 35,5
| 96
| 61
| 60
|
| В i
| 23
| 12
| 20
| 39
| 18,6
| 35,5
| 48
| 61
| 30
|
Графиком №1 пользуются, если выполняется условие 22. В других случаях используют график №2.
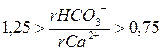 . (22)
. (22)
Для нашего случаявеличина отношения 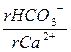 : составила:
: составила:
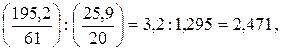
т.к. полученная величина больше 1,25 то для дальнейших расчетов воспользуемся графиком Б.
2. Находим суммы эквивалентов Са2+ (а) и НСО3- (в) и удвоенного содержания свободной углекислоты СО2 (с):
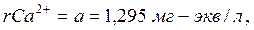 (23)
(23)
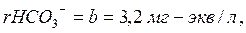 (24)
(24)
 (25)
(25)
 (26)
(26)
На графике №2 этим суммам отвечает точка, лежащая на кривой, соответствующей эквивалентному содержанию равновесной НСО3- 3,7 мг-экв/л.
В нашем варианте фактически в воде содержится 3,2 мг-экв/л НСО3- (см. формулу 24) т.е. равновесное эквивалентное содержание НСО3- выше имеющегося на 0,5 мг-экв/л (3,7 – 3,2 = 0,5). Это свидетельствует о том, что в пластовой воде недостаточно НСО3- относительно имеющегося СО2. Другими словами, избыток СО2 будет придавать воде коррозионную активность.
3. Далее по нижней шкале графика №2 находим, чтонедостаток НСО3- в количестве 0,5 мг-экв/л соответствует избытку СО2 в количестве 11 мг/л.
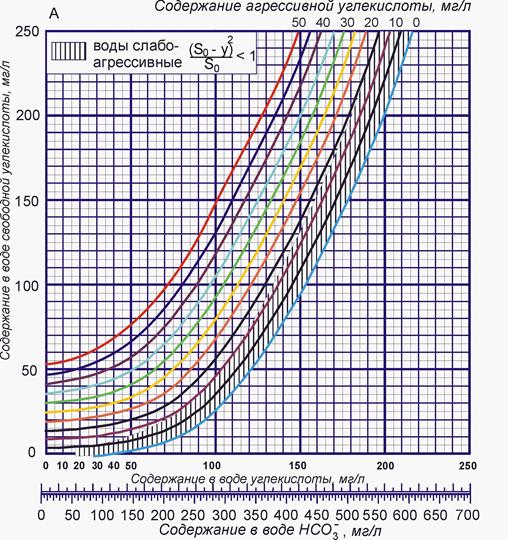
Рис. 11 – График Лаптева № 2 для определения количества агрессивной углекислоты

Рис. 11 – График Лаптева № 2 для определения количества агрессивной углекислоты
4. Зная содержание шести основных ионов в эквивалентной форме, можно, пользуясь классификацией Сулина (табл. 5), определить тип воды.
Таблица 5



 . (19)
. (19)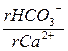 , (20)
, (20) (21)
(21)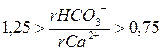 . (22)
. (22)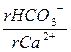 : составила:
: составила: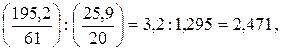
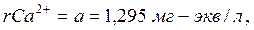 (23)
(23)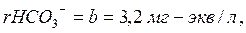 (24)
(24) (25)
(25) (26)
(26)




