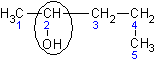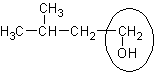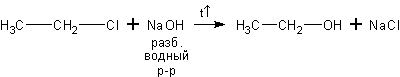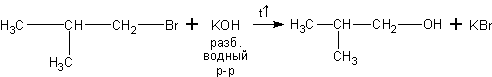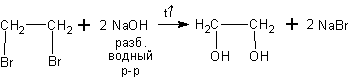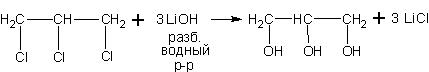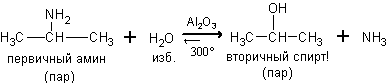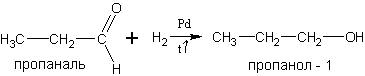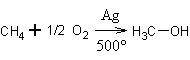По номенклатуре ИЮПАК в структурной формуле спирта находится самая длинная цепь из атомов углерода, обязательно включающая атом углерода, связанный с гидроксильной группой. Эта цепь нумеруется с той стороны, к которой ближе гидроксильная группа. Сначала называются алкильные радикалы с указанием их места положения в цепи, затем название углеводорода, соответствующего длине выбранной цепи, после чего добавляется окончание спиртов – «ол».
По рациональной номенклатуре атом углерода и связанный с ним гидроксил получают название «карбинол». Сначала называются алкильные радикалы, соединённые с упомянутым выше атомом углерода, а затем слитно слово «карбинол».
Также используется тривиальная номенклатура.
Таблица 4. Примеры названий изомерных спиртов.
| C5H12O
| Название по ИЮПАК
| Рациональное
название
| Тривиальное название
|
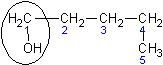
| Пентанол - 1
| н - Бутилкарбинол
| Амиловый спирт
|
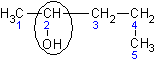
| Пентанол - 2
| Метилпропил-карбинол
| -
|

| Пентанол - 3
| Диэтилкарбинол
| -
|
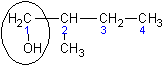
| 2 – метилбутанол - 1
| Втор - бутилкарбинол
| -
|
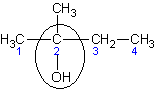
| 2 - метилбутанол - 2
| Диметилэтилкарбинол
| Трет – амиловый спирт
|
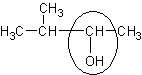
| 3 – метилбутанол - 2
| Метилизопропил-карбинол
| -
|
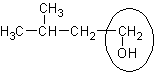
| 3 – метилбутанол - 1
| Изобутилкарбинол
| Изоамиловый спирт
|
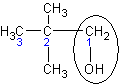
| 2,2 – диметил-
пропанол - 1
| Трет - бутилкарбинол
| Нео-пентиловый спирт
|
Способы получения спиртов
1. Гидратация алкенов: электрофильное присоединение воды к алкенам в присутствии каталитических количеств минеральных кислот. Присоединение воды к несимметричным алкенам протекает по правилу Марковникова: преимущественно (90%) водород присоединяется к наиболее гидрогенизинованному атому:

2. Гидратация алкадиенов. Алкадиены аналогично алкенам присоединяют в присутствии кислот воду.
Присоединение первого моля воды идёт преимущественно в положения 1 – 4. При присоединении второго моля воды образуются диолы. Ниже представлены примеры обоих случаев: 
3. Щелочной гидролиз галогеналканов. Галогеналканы вступают с водными растворами [2] щелочей в реакцию нуклеофильного замещения галогена на гидроксил:
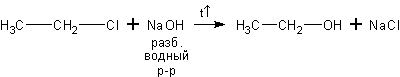
хлорэтан этанол
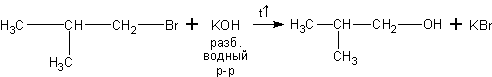
1-бром-2-метилпропан 2-метилпропанол-1
При действии водныхрастворов щелочей на дигалогеналканы получаются двухатомные спирты (или диолы):
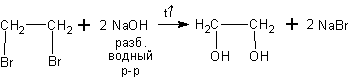
Как показано выше из 1,2-дибромэтана получается 1,2-этандиол (этиленгликоль).
Из 1,2,3-трихлорпропана, например, получают широко используемый глицерин (пропантриол - 1,2,3).
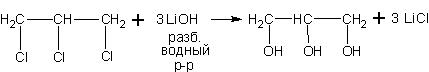
4. Гидролиз аминов. При нагревании с парами воды в присутствии катализатора протекает обратимая реакция, в которой конечными продуктами являются спирт с тем же строением углеродного скелета и аммиак.
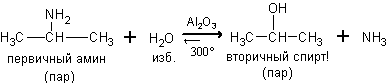
Первичные амины можно перевести в спирты так же действием нитританатрия в соляной кислоте при охлаждении до 2 – 5оС:

5. Гидрирование альдегидов и кетонов. Реакция гидрирования обратимо протекает на катализаторах – металлах платиновой группы: Ni, Pd, Pt:
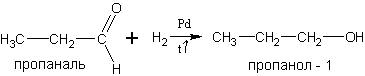
 пентандион-2,4 пентандиол-2,4
пентандион-2,4 пентандиол-2,4
6. Гидролиз алкоголятов. Алкоголяты практически нацело гидролизуются в воде при комнатной температуре:


7. Гидролиз сложных эфиров. Из сложных эфиров спирты наряду с карбоновыми кислотами могут быть получены путём кислотного гидролиза:

В щелочной среде реакция гидролиза сложных эфиров необратима:

8. Получение метанола. Специфический способ получения метанола – окисление метана на гетерогенном катализаторе – серебре – расчётным количеством кислорода до метанола:
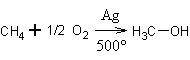
Современный промышленный метод получения метанола – каталитический синтез из оксида углерода (II) и водорода:

9. Получение этанола. Промышленный способ получения этанола – гидратация этилена (260-300оС, 10Мпа, в присутствии сильных кислот, на алюмосиликате с добавками солей кадмия, меди, кобальта), см. п.1.
Этанол образуется при брожении сахаров в присутствии дрожжей:
С6Н12О6 → 2С2Н5ОН + 2СО2