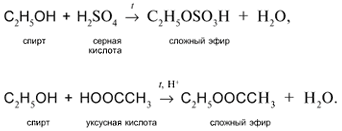Система уроков по теме: "Предельные одноатомные спирты"
Пояснительная записка.
Все классы органических соединений преподаю блоками. Блок состоит из трех частей:
1. урок-лекция,
2. тренировочные домашние упражнения,
3. урок-коррекция.
Урок-лекция (объяснение нового материала).
Цели:
- ввести понятие предельных одноатомных спиртов, свойств;
- развитие интереса, умения выделять главное, научить сравнивать и анализировать.
1. Определение.
Органические соединения, которые состоят из предельного углеводородного радикала и содержат одну функциональную гидроксильную группу (-ОН), называются насыщенными одноатомными спиртами.
Общая формула СnН2n+1ОН (где n 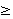 1) или R – ОН
1) или R – ОН
2. Гомологический ряд и номенклатура
СН3 ОН – метиловый спирт (метанол),
СН3 СН2ОН – этиловый спирт (этанол)….
- СН2 - гомологическая разница
Пример: 3-метилгексанол – 1
2. Изомерия положения функциональной группы (-ОН)
Пример: бутанол-1 -> бутанол-2
3. Изомерия между классами (предельные одноатомные спирты изомерны простым эфирам)
4. Физические свойства
1) Спирты от С1 до С11 – жидкости, от С12 до С - твердые.
2) Легче воды, бесцветны, жидкие имеют резкий запах, твердые запаха не имеют.
3) Низшие спирты (до пропилового) смешиваются с водой в любых отношениях. Высшие спирты практически нерастворимы в воде.
Межмолекулярная водородная связь возможна между отдельными молекулами спирта и между молекулами спирта и воды. Это влияет на физические свойства спиртов: повышает температуру кипения, снижает летучесть, способствует хорошей растворимости в воде, не позволяет перегонкой получить 100% спирт из его водного раствора.
5. Химические свойства (с примерами):
1) горение,
2) взаимодействие с активными металлами;
3) взаимодействие с органическими кислотами, с неорганическими кислотами;
4) с галогеноводородами;
5) окисление
- первичный спирт -> альдегид,
- вторичный спирт -> кетон,
- третичный спирт: тяжело окисляется с разрывом С-С связи;
6) дегидратация:
- внутримолекулярная,
- межмолекулярная с образованием простых эфиров;
7) дегидратация и дегидрирование (реакция Лебедева).
6. Получение одноатомных спиртов (с примерами).
В промышленности:
1) получение СН3 ОН
- из синтез-газа
- во время сухой перегонки древесины (древесный спирт),
2) гидратация алкенов,
3) брожение сахаристых веществ.
В лаборатории:
1) из алканов через галогенопроизводные,
2) восстановление альдегидов.
Физиологическое действие спиртов на организм негативно.
СН3 ОН – сильный яд! В малых количествах вызывает слепоту, в больших – приводит к смерти.
С2Н5ОН – наркотик. Под влиянием этанола у человека ослабляется внимание, затормаживается реакция, нарушается корреляция движений. При продолжительном употреблении вызывает глубокие нарушения нервной системы, заболевания сердечно-сосудистой системы, пищеварительного тракта, наступает тяжелая болезнь – алкоголизм.
7. Применение спиртов.
1) Метанол:
- в промышленном органическом синтезе (производство формальдегида),
- как растворитель,
- как добавка к бензину.
2) Этанол:
- производство уксусной кислоты,
- как растворитель,
- в парфюмерии,
- в медицине,
- как топливо,
- в пищевой промышленности.
8. Связь между ациклическими углеводородами и спиртами (показать на примерах).
Домашнее задание: пар. 17 (учебник О.С. Габриелян), тренировочные упражнения.
Приложение 1. Закрепление (если позволяет время)
1. Назвать по международной номенклатуре (2-4 примера).
2. Написать структурные формулы изомерных спиртов С4Н9 ОН и назвать их.
Приложение 2. Тренировочные домашние упражнения.
Тема: “Одноатомные спирты”.
Сложность 1 (оценка “удовлетворительно”).
1. Написать структурные формулы следующих соединений: 2-метилпентанол-1; 2,3-диметилбутанол-2; 2-метилпентен-1-ол-3.
2. Назвать вещество и написать два его гомолога и два изомера
1. Какой объем водорода выделится при взаимодействии 19,5 г калия с этанолом.
Сложность 2 (оценка “хорошо”).
1. Чем объясняется изомерия спиртов? Пояснить это на примере спирта, в молекуле которого четыре атома углерода. Назвать каждый изомер.
2. Написать реакции получения метанола.
3. Осуществить превращения:
Этан -> бромэтан-> этен-> этанол-> метилэтиловый эфир. Где происходит дегиратация?
4. При сжигании 4,8 г органического вещества образовалось 3,36 л оксида углерода (IV) и 5,4 г воды. Плотность паров этого вещества по метану 2. Определить формулу вещества.
Сложность 3 (оценка “отлично”).
1. Чем отличаются первичные, вторичные и третичные спирты? (Привести примеры каждого и назвать их)
2. Предложить схему получения из пропана пропанол-1.
3. Осуществить превращения (предложить две цепочки).
4. При межмолекулярной дегидратации 100г одноатомного предельного спирта неизвестного строения выделилось 21,09 г воды и выход продукта реакции составил 75% от теоретического. Определить строение спирта.
Урок-коррекция.
1 этап. 10-15 минут. Учащиеся задают вопросы по тренировочным упражнениям.
2 этап. 20-30 минут. Самостоятельная работа. Работа разноуровневая. Учащиеся выбирают любой вариант.
Самостоятельная работа (тема: “Одноатомные спирты”).
Оценка “удовлетворительно”
| Вариант 1
| Вариант 2
|
| 1. Какие вещества называют спиртами? (привести примеры).
2. Какие спирты образуются в результате гидратации следующих веществ: этена, бутена-2.
3. Осуществить превращения:
1)С2Н 5 ОН->С2Н 4 ->С2Н 5 Cl->С2Н5 ОН
2)ацетилен- >А-> этанол
4. При взаимодействии 12,8 г спирта с натрием образовалось 4,48 л водорода. Какой это спирт?
| 1. Написать общую формулу спиртов. Что такое функциональная группа?
2. Написать уравнение гидролиза водным раствором щелочи следующих соединений: хлорэтана, 2-хлорбутана.
3. Осуществить превращения:
1)СН 4 -> С2Н 2 -> С2Н 4 -> С2Н 5 ОН
2)этанол -> А-> этан
4. При дегидратации 12 г спирта образовался алкен и 3,6 г воды. Какой это спирт?
|
Оценка “хорошо”
| Вариант 3
| Вариант 4
|
| 1. Объяснить образование водородных связей между молекулами спирта и влияние на физические свойства.
2. Как получить спирты из алкенов (привести два примера).
3. Осуществить превращение: оксид углерода (IV) – метанол – хлорметан – этан – углекислый газ.
4. Найти молекулярную массу вещества А: пропанол-1 – А - пропанол-2
5. 0,5 моль метанола нагрели с KBr и H2SO4 и получили 38 г бромметана. Найти выход бромметана
| 1. Как доказать, что спирты отравляюще и пагубно действуют на организм человека.
2. Дописать уравнения и назвать вещества.
1. СН 3 – CHCl - СН 2 - СН 3 + КОН(водн)
2. СН 3 – CHCl - СН 2 - СН 3 + КОН(спирт)
1. Осуществить превращения: метан – этан – этен – этанол – углекислый газ
2. Определить молекулярную массу вещества А: этанол – А – 1,2-дихлорэтан.
3. Какая масса этилата натрия получится при взаимодействии этанола массой 11,5 г с натрием массой 9,2 г?
|
Оценка “отлично”
| Вариант 5
| Вариант 6
|
| 1. Почему температура кипения спиртов намного выше, чем соответствующих углеводородов?
2. Сколько изомерных бутиловых спиртов может образоваться из изомерных алкенов С4Н 8 при их гидратации?
3. Написать уравнения реакций, в результате которых можно получить из метана бутадиен-1,3.
4. Метанол массой 2,04 кг получили взаимодействием оксида углерода (11) объемом 2 м3 с водородом объемом 5 м3 (ну). Найти выход продукта реакции.
5. Определить массу пропанола-2, взятого для реакции, если во время дегидратации пропанола-2 получили пропен, который обесцветил бромную воду массой 200 г. Массовая доля брома в бромной воде равна 3,2%.
| 1. Почему нельзя физическими методами получить 100%-ный этанол из его водного раствора?
2. Сколько изомерных третичных спиртов имеют состав.С6Н13 ОН? Написать формулы и назвать.
3. Написать уравнения реакций, в результате которых можно получить из метана диэтиловый эфир.
4. Какую массу бутадиена-1,3 можно получить из спирта объемом 230 л и плотностью 0,8 кг/л, если массовая доля этанола в спирте 95%? Выход продукта реакции составляет 60%.
5. Вычислить массу добытого продукта, если выход на обеих стадиях синтеза составляет по 60%, если известно, что из пропанола-2 массой 24 г добыт 2-бромпропан, из которого синтезировали 2,3-диметилбутан.
|
Химические свойства спиртов
Одноатомные спирты не обладают ни щелочными, ни кислотными свойствами. Водные растворы спиртов на индикаторы не действуют.
Рассмотрим химические свойства спиртов на примере этанола. В молекуле этилового спирта СН3–СН2–ОН имеется четыре типа химических связей, различающихся полярностью: 1) Н–О;
2) С–О; 3) С–Н; 4) С–С. В результате химических превращений разрываются наиболее полярные связи Н–О, С–О и С–Н. Неполярная связь С–С в реакциях спиртов не разрывается.
1. Разрыв связи Н–О в реакции с натрием:
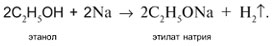
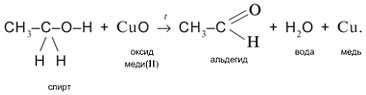
2. Одновременный разрыв связей Н–О и С–Н, находящихся при спиртовом атоме углерода, под действием окислителя (CuO) с отщеплением молекулы Н2О и образованием альдегида (СН3СНО):
2. Разрыв связи 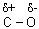 под действием нуклеофильных реагентов (ионов В– или молекул с неравномерным распределением заряда в молекуле
под действием нуклеофильных реагентов (ионов В– или молекул с неравномерным распределением заряда в молекуле 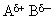 ) в кислой среде.
) в кислой среде.
3. а) Действие кислот НСl или НВr с образованием галогеналканов:
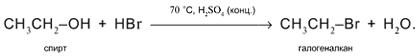
б) Действие кислородсодержащих кислот – неорганических и органических – с образованием сложных эфиров (подробнее см. урок 29):
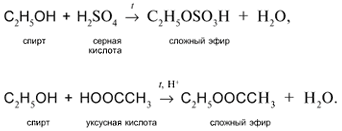
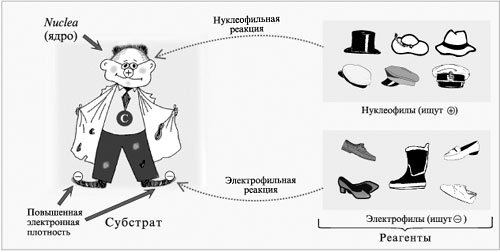



 1) или R – ОН
1) или R – ОН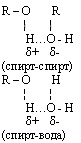

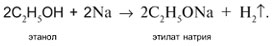

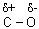 под действием нуклеофильных реагентов (ионов В– или молекул с неравномерным распределением заряда в молекуле
под действием нуклеофильных реагентов (ионов В– или молекул с неравномерным распределением заряда в молекуле 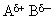 ) в кислой среде.
) в кислой среде.