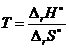Б2.В.1 ОСНОВЫ ОБЩЕЙ И НЕОРГАНИЧЕСКОЙ ХИМИИ
Модуль 1 Теоретические основы общей химии
направление подготовки бакалавра
Продукты питания животного происхождения
Уфа - 2013
УДК
Рекомендовано к изданию методической комиссией
факультета пищевых технологий
(протокол №_______ от «______» ________________________ 2013 г.)
\
Составитель: доцент Ганиева Е.С.
Рецензент:
доцент кафедры химии Шабаева Г.Б.
Ответственный за выпуск:
заведующий кафедрой химии профессор Исламова Р.М.
ВВЕДЕНИЕ
Данное методическое указание составлено для студентов 1 курса факультета пищевых технологий направления подготовки 260200 Продукты питания животного происхождения для выполнения домашней работы (эссе) по дисциплине Б2.В.1 Основы общей и неорганической химии. Оно включает в себя теоретический материал и контрольные задачи по темам «Эквивалент. Моль - эквивалент. Молярная масса эквивалента» и «Основные закономерности химических процессов», которые входят в «Модуль 1. Теоретические основы общей химии». Данные задания помогут усвоить теоретический материал и подготовиться к рубежной контрольной работе по модулю 1.
Для выполнения этих заданий необходимо проработать лекционный материал и учебные пособия. Студент выполняет задания своего варианта, номер которого укажет преподаватель. Работа оформляется на бумаге формата А4, причем приводится условие задачи и подробное решение задачи. В конце работы необходимо привести список использованной литературы.
Модуль 1 Теоретические основы общей химии
СОДЕРЖАНИЕ
Эквивалент. Моль - эквивалент. Молярная масса эквивалента.
Закон эквивалентов. с.5
Основные закономерности химических процессов с.14
Основы химической термодинамики с.14
Основы химической кинетики с.21
Основы химического равновесия с.24
Основы фазового равновесия с.27
ПРИЛОЖЕНИЕ с.35
ЛИТЕРАТУРА с.37
Эквивалент. Моль - эквивалент. Молярная масса эквивалента.
Закон эквивалентов.
Эквивалент - одно из стехиометрических понятий химии, указывает на равноценность количественных отношений исходных и образующихся веществ в химической реакции. Такая равноценность обуславливается равенством числа разрывающихся химических связей в исходных веществах и образующихся - в продуктах реакции.
Пример:
Fe(OH)3 + 3HCl → FeCl3 + 3H2O
1 моль 3 моль 1 моль 3 моль
В графической форме:

1Fe(OH)3, 1HCl, 1FeCl3, 1HOН содержат различное число реакционно-способных химических связей и в этом смысле указанные количества этих веществ не равноценны, не эквивалентны.
Реакция произойдет, если на 3 разрывающиеся химические связи в Fe(OH)3 будет приходиться 3 связи в HCl, что соответствует 3HCl. Как показывает приведенное выше уравнение, равноценными (другими словами, эквивалентными) по числу связей будут 1Fe(OH)3, 3HCl, 1FeCl3, 3HOН. Эквивалентными будут и такие доли молекул веществ, которые соответствуют возможности образования одной химической связи. Для 1 моля сложного вещества эта доля определит 1 моль-экв.

Масса одного моль – эквивалента сложного вещества, называемая молярной массой эквивалента, равна:

Число реакционноспособных химических связей в зависимости от состава и строения вещества можно выразить более конкретно:
| Типы соединений
| nх. св.
|
| Кислоты
| nH+
|
| Основания
| nOH-
|
| Соли
| nkt · Zkt = nAn · ZAn
|
| Оксиды
| nэлем. · Zэлем. = nO · ZO
|
В рассматриваемой реакции:
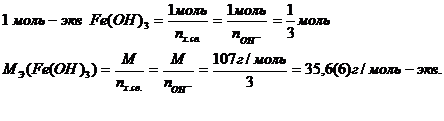

Значения масс эквивалентов сложных веществ можно выразить через массы эквивалентов, элементов или ионов его составляющих. Заменив в выражении  молярную массу на численно равную относительную молекулярную (Мr), молярную массу эквивалента – на эквивалентную (Э), получим:
молярную массу на численно равную относительную молекулярную (Мr), молярную массу эквивалента – на эквивалентную (Э), получим:

Эквивалентность реагирующих и образующихся веществ отражает закон эквивалентов, которому можно придать различные математические выражения:
1) nЭ,1 = nЭ,2 = nэ,3 = …
nЭ – число моль-эквивалентов

m – масса;
V – объем;
VЭ – объем одного моль-эквивалента газообразного вещества.
2) 
3) 
Объем 1 моль - эквивалента газов имеет различные значения:


 1 моль Н2 22,4 л х = 11,2 л
1 моль Н2 22,4 л х = 11,2 л
 1 моль-экв→ ½ моль х л
1 моль-экв→ ½ моль х л


 1 моль О2 22,4л х = 5,6 л
1 моль О2 22,4л х = 5,6 л
 1 моль-экв → ¼ моль х л
1 моль-экв → ¼ моль х л

Перед решением задач необходимо вспомнить:
1) простое и сложное вещество;
2) валентность элемента;
3) основные классы неорганических соединений;
4) номенклатура неорганических соединений;
5) графические формулы неорганических соединений;
6) понятие основность кислоты;
7) понятие кислотность основания;
8) электролитическая диссоциация неорганических соединений;
9) относительная атомная масса элемента;
10) относительная молекулярная масса вещества;
11) молярная масса вещества;
12) эквивалент;
13) моль – эквивалент,
14) молярная масса эквивалента;
15) закон эквивалентов.
Контрольные задания
Задание 1.
1 – 30. A: Назовите вещество, укажите к какому классу неорганических соединений оно относится. Вычислите молярную массу эквивалента.
В: Сколько моль – эквивалентов содержится в образце.
С: Какой объем занимает газ (н.у.)?
| Номер варианта
| A
| B
| C
|
| 1,16
| Fe в Fe2O3, Cl2O7, NaAlO2, Mg(OH)2, H2SO4
| 30 г Mg(OH)2
15 г K2CO3
| 0,5 моль – эквивалентов H2,
1,5 моль – эквивалентов Cl2
|
| 2,17
| Cl в Cl2O5, KOH, H3PO4, K2CO3, CaO
| 1,5 г H3PO4
3,7 г Ba(OH)2
| 3,8 моль – эквивалентов F2,
1,5 моль – эквивалентов O2
|
| 3,18
| P в P2O3, Al2(SO4)3, Fe(OH)2, H3PO4, Al2O3
| 8,7 г K2HPO4
10 г Pb(OH)2
| 9,7 моль – эквивалентов N2,
3,5 моль – эквивалентов Br2
|
| 4,19
| N в N2O3, H3PO4, Ba(OH)2, NaNO2, P2O5
| 10 г K2Cr2O7
2,3 г Zn(OH)2
| 3,2 моль – эквивалентов Ar,
6,6 моль – эквивалентов H2
|
| 5,20
| Si в SiO, H2SiO3, Fe(OH)3, K2HPO4, Na2O
| 6,1 г Ca3(PO4)2,
2,1 г HCl
| 2,1 моль – эквивалентов O2,
7,6 моль – эквивалентов H2
|
| 6,21
| C в СO2, K2Cr2O7, Zn(OH)2, H4P2O7, P2O5
| 8,1 г Mg(OH)2
3,4 г HNO3
| 9,3 моль – эквивалентов Ar,
6,6 моль – эквивалентов Cl2
|
| 7,22
| Ca3(PO4)2, MnO2, Pb(OH)2, V в V2O7, V2O7
| 15 г Na2S
67 г Na2SO3
| 6,8 моль – эквивалентов H2,
9,5 моль – эквивалентов F2
|
| 8,23
| CuOHNO3, Cu(OH)2, KMnO7, CrO, Сr в CrO
| 33 г Fe2O3
27 г H2CrO4
| 1,8 моль – эквивалентов O2,
13,5 моль – эквивалентов F2
|
| 9,24
| NaHSO4, Fe(OH)3, HCl, As2O3, As в As2O3
| 5 г CrO3,
3,3 г NaBiO3
| 13,7 моль – эквивалентов N2,
28,8 моль – эквивалентов H2
|
| 10,25
| CrCl3, Sn(OH)2, H3AlO3, CO, C в СO
| 1,7 г Cu(OH)2
5,2 г Ca3(PO4)2
| 4,5 моль – эквивалентов O2,
11,5 моль – эквивалентов F2
|
| 11,26
| Cr2(SO4)3, H2SnO2, Mg(OH)2, SO2, S в SO2
| 7 г As2O3
7,8 г NaHSO4
| 23,5 моль – эквивалентов Cl 2,
13,5 моль – эквивалентов H2
|
| 12,27
| Na2S, H2S, S в SO3, Ni(OH)2, SO3
| 6,3 г Mg(OH)2,
1,3 г HCl
| 7,8 моль – эквивалентов О2,
4,7 моль – эквивалентов Cl2
|
| 13,28
| Na2SO3, KOH, H2CrO4, CrO3, Cr в CrO3
| 9 г Fe(OH)3
8,3 г MnO2
| 17,8 моль – эквивалентов N 2,
4,7 моль – эквивалентов Ar
|
| 14,29
| KI, NH4OH, HNO2, Fe2O3, Fe в Fe2O3
| 5,8 г CuOHNO3,
4,3 г KOH
| 23,5 моль – эквивалентов О2,
14,7 моль – эквивалентов Ar
|
| 15,30
| NaBiO3, Fe(OH)3, Al2O3, Al в Al2O3, HNO3
| 9,8 г H3PO4,
15 г K2CO3
| 44,5 моль – эквивалентов О2,
64,7 моль – эквивалентов H2
|
Задание 2. Эквивалент вещества в химической реакции
1-30. Определите, чему равен 1 моль-экв исходных веществ, как доля от 1 моля.
| Номер варианта
| Уравнения реакций
|
|
|
|
|
| Fe(OH)3 + HCl → Fe(OH)2Cl + H2O
|
|
| Fe(OH)3 + 2HCl → FeOHCl2 + 2H2O
|
|
| 2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 6H2O
|
|
| CuOHNO3 + H2S → CuS + HNO3 + H2O
|
|
| Na2HPO4 + AlCl3 → AlPO4 + 2NaCl + HCl
|
|
| Ca(HCO3)2 + 2HCl → CaCl2 + 2H2O + 2CO2
|
|
| Al(OH)2Cl + KOH → Al(OH)3 + KCl
|
|
| H3PO4 + 3NaOH → Na3PO4 + 3H2O
|
|
| H3PO4 + 2NaOH → Na2HPO4 + 2H2O
|
|
| H3PO4 + NaOH → NaH2PO4 + H2O
|
|
| Fe(OH)2CH3COO + 3HNO3 → Fe(NO3)3 + CH3COOH + 2H2O
|
|
| KH2PO4 + KOH → K2HPO4 + H2O
|
|
| KH2PO4 + 2KOH → K3PO4 + 2H2O
|
|
| Bi(OH)2NO3 + KOH → Bi(OH)3 + KNO3
|
|
| Fe(OH)2Cl + 2HCl → FeCl3 + 2H2O
|
|
|
|
|
| K2HPO4 + KOH → K3PO4 + H2O
|
|
| Na2HPO4 + CaCl2 → CaHPO4 + 2NaCl
|
|
| K2CO3 + 2HNO3 → 2KNO3 + H2O + CO2
|
|
| 2FeSO4 + 2KOH → (FeOH)2SO4 + K2SO4
|
|
| FeSO4 + 2KOH → Fe(OH)2 + K2SO4
|
|
| H3PO4 + KOH → K3PO4 + 3H2O
|
|
| Al(OH)Cl2 + 2KOH → Al(OH)3 + 2KCl
|
|
| Bi(OH)(NO3)2 + 2KOH → Bi(OH)3 + 2KNO3
|
|
| PbCl2 + H2O → Pb(OH)Cl + HCl
|
|
| H2SO4 + PbCl2 → PbSO4 + 2HCl
|
|
| H2SO4 + KOH → KHSO4 + H2O
|
|
| Fe(OH)2NO3 + 2HNO3 → Fe(NO3)3 + 2H2O
|
|
| Al(OH)3 + KOH ® K[Al(OH)4]
|
|
| Al(OH)3 + HNO3 ® Al(OH)2NO3 + H2O
|
|
| Al(OH)3 + 2HNO3 ® Al(OH)(NO3)2 + 2H2O
|
Задание 2. Закон эквивалентов.
Задание 2.1. 1 – 30.Решите задачу.
1. На нейтрализацию 7,330 г фосфорноватистой кислоты Н3РО2 пошло 4,444 г NaOH. Вычислите эквивалентную массу кислоты, ее основность (nН+) и напишите уравнение реакции нейтрализации.
2. При восстановлении 6,50 г оксида образовалось 4,45 г металла. Вычислите молярные массы эквивалентов металла и его оксида.
3. При нейтрализации 9,8 г ортофосфорной кислоты израсходовано 8 г NaOH. Вычислите эквивалентную массу и основность (nН+) кислоты в этой реакции. На основании расчета напишите уравнение реакции.
4. В какой массе NaOH содержится столько же моль – эквивалентов, что и в 140 г КОН?
5. При взаимодействии 2,5 г карбоната металла с азотной кислотой образовалось 4,1 г нитрата этого же металла. Вычислите эквивалентную массу металла.
6. Из 3,31 г нитрата металла получается 2,78 г его хлорида. Вычислите молярную массу эквивалента этого металла.
7. Некоторый элемент образует кислородное соединение, содержащее 31,58 % кислорода. Вычислите эквивалентную и атомную массу этого элемента, если в данном оксиде он трехвалентен. Составьте формулу оксида.
8. Чему равен при н.у. эквивалентный объем кислорода? На сжигание 1,5 г двухвалентного металла требуется 0,69 л кислорода (н.у.). Вычислите массу эквивалента металла; чему равна его атомная масса?
9. Какой объем (н.у.) занимает 1 моль – эквивалент водорода? Сколько литров водорода (н.у.) выделилось при растворении в кислоте 0,45 г металла, молярная масса эквивалента которого равна 20 г/моль-экв?
10. В 2,48 г оксида одновалентного металла содержится 1,84 г металла. Вычислите молярную массу эквивалента металла; чему равна его атомная масса?
11. Является ли эквивалент элемента постоянной величиной? Чему равны эквивалентные массы хрома в его оксидах, содержащих 68,42 % и 52,00 % хрома. Определите валентность хрома в каждом из этих оксидов и составьте их формулы.
12. Трехвалентный элемент образует оксид, содержащий 31,58 % кислорода. Вычислите эквивалентную и атомную массу этого элемента. Составьте формулу оксида.
13. При окислении 8,37 г двухвалентного металла образовалось 10,77 г оксида. Вычислите молярную массу эквивалента металла; чему равна его атомная масса?
14. При взаимодействии 1,62 г трехвалентного металла с кислотой выделяется 2,015 л водорода (н.у.).Вычислите молярную массу эквивалента металла; чему равна его атомная масса?
15. Из 1,35 г оксида металла получается 3,15 г его нитрата. Вычислите молярную массу эквивалента этого металла.
16. При окислении 1,674 г двухвалентного металла образовалось 2,154 г оксида. Вычислите молярную массу эквивалента металла; чему равна его атомная масса?
17. Для растворения 16,8 г металла потребовалось 14,7 г серной кислоты. Определите эквивалентную массу металла и объем выделившегося водорода (н.у.).
18. Сколько моль – эквивалентов извести Ca(OH)2 потребуется для нейтрализации 196 г фосфорной кислоты для получения одно-, двух- и трехзамещенного фосфата кальция?
19. По реакциям нейтрализации серной кислоты и ортофосфорной одинаковым количеством щелочи образовались соответственно сульфат и дигидрофосфат. Каково отношение масс этих кислот, пошедших на нейтрализацию.
20. Оксид металла содержит 28,65% кислорода, а соединение того же металла с галогеном – 48,72 % галогена. Рассчитайте молярную массу эквивалента галогена.
21. Некоторое количество металла, эквивалентная масса которого равна 27,9 г/моль-экв, вытесняет из кислоты 700 мл водорода, измеренного при н.у. Определить массу металла.
22. 1,6 г кальция и 2,61 г цинка вытесняют из кислоты одинаковые количества водорода. Вычислить эквивалентную массу цинка, зная, что эквивалентная масса кальция равна 20 г/моль-экв.
23. Вычислите молярную массу эквивалента карбоната магния, если на растворение 8,4 г этой соли было израсходовано 33,2 мл 20% - ного раствора HCl (r = 1,1 г/моль).
24. Вычислите молярную массу эквивалента серной кислоты, если 98,08 г ее реагируют с 24, 32 г магния.
25. При восстановлении 2,4 г оксида двухвалентного металла водородом получено 0,54 г воды. Вычислите молярную массу эквивалента металла и его оксида и назовите металл.
26. Сколько литров кислорода, измеренного при н.у., расходуется при сгорании 2,4 г металла, молярная масса эквивалента которого равна 12 г/моль – экв..
27. При нагревании 20,06 г металла получено 21,55 г оксида. Вычислите молярную массу эквивалента металла.
28. Металл массой 16,8 г взаимодействует с 14,7 г серной кислоты. Рассчитайте молярную массу эквивалента металла и объем выделившегося водорода. (н.у.)
29. При взаимодействии 5,95 г некоторого вещества с 2,75 г хлороводорода получилось 4,40 г соли. Вычислить эквивалентные массы вещества и образовавшейся соли.
30. Эквивалентная масса металла в 2 раза больше, чем эквивалентная масса кислорода. Во сколько раз масса оксида больше массы металла?
Задание 2.2
1 – 30. Рассчитайте массу (или объем) продуктов реакции, если прореагировано указанное количество моль эквивалентов одного из веществ при нормальных условиях.
| Номер варианта
| Реакция
| Количество моль эквивалентов исходного вещества
|
|
| Zn + H2SO4 → ZnSO4 + H2
| 0,2 моль - экв Zn
|
|
| H2O2 + O3 → H2O + 2O2
| 0,3 моль - экв O3
|
|
| 4FeS2 + 11O2 → 2Fe2O3 + 8 SO2
| 1 моль - экв O2
|
|
| Cu(OH)2 + HCl → CuOHCl + H2O
| 0,5 моль - экв HCl
|
|
| Cu(OH)2 + 2HCl → CuCl2 + 2H2O
| 0,5 моль - экв HCl
|
|
| H2SO4 + 2KOH → K2SO4 + 2H2O
| 4 моль - экв KOH
|
|
| SO2 + 1/2O2 → SO3
| 0,1 моль - экв O2
|
|
| CO + H2O → CO2 + H2
| 2 моль - экв H2O
|
|
| N2 + O2 → 2NO
| 3 моль - экв N2
|
|
| 2H2 + O2 → 2H2O
| 0,6 моль - экв H2
|
|
| Fe2O3 + 3H2 → 2Fe + 3H2O
| 0,4 моль - экв H2
|
|
| 2H2O2 → 2H2O + O2
| 0,1 моль - экв H2O2
|
|
| 3H2 + N2 →2NH3
| 3 моль - экв H2
|
|
| N2O4 → 2NO2
| 1 моль - экв N2O4
|
|
| 2NH4NO3 → 4H2O + O2 + 2N2
| 0,2 моль - экв NH4NO3
|
|
| 4HCl + O2 → 2Cl2 + 2H2O
| 0,4 моль - экв O2
|
|
| SO2 + 2H2 → S + 2H2O
| 0,5 моль - экв H2
|
|
| CH4 + 2O2 → 2H2O + CO2
| 2 моль - экв O2
|
|
| 4NH3 + 3O2 → 2N2 + 6H2O
| 3 моль - экв O2
|
|
| 4NH3 + 5O2 → 4NO + 6H2O
| 5 моль - экв O2
|
|
| Fe2O3 + 3H2 → 2Fe + 3H2O
| 0,4 моль - экв Fe2O3
|
|
| 4FeS2 + 11O2 → 2Fe2O3 + 8 SO2
| 1,5 моль - экв FeS
|
|
| 4NH3 + 3O2 → 2N2 + 6H2O
| 3,5 моль - экв NH3
|
|
| SO2 + 2H2 → S + 2H2O
| 0,5 моль - экв SO2
|
|
| N2 + O2 → 2NO
| 1,5 моль - экв O2
|
|
| 4HCl + O2 → 2Cl2 + 2H2O
| 0,6 моль - экв HCl
|
|
| CO + H2O → CO2 + H2
| 2,5 моль - экв CO
|
|
| N2O4 → 2NO2
| 1 моль - экв NO2
|
|
| 3H2 + N2 →2NH3
| 3 моль - экв N2
|
|
| CH4 + 2O2 → 2H2O + CO2
| 2 моль - экв CH4
|
Основы химической кинетики
С помощью химической термодинамики можно определить направление любой химической реакции при заданных условиях, однако она ничего не может сказать о том, осуществима ли данная реакция и за какое время она закончится. Понятие время в химию вводит химическая кинетика.
Химическая кинетика изучает скорости химических реакций, их механизмы и закономерности протекания.
Основные различия между химической термодинамикой и кинетикой:
1) в химической термодинамики нет времени, она предсказывает только конечный результат процесса. Химическая кинетика изучает только изменяющиеся (динамические) системы.
2) Равновесные свойства определяются состоянием как исходных веществ, так и продуктов реакции. Для термодинамики важны левая и правая части химического уравнения. Скорость реакции определяется только состоянием исходных веществ. Для кинетики важна только левая часть уравнения реакции.
3) Термодинамические свойства определяются термодинамической активностью веществ, кинетические свойства - их концентрацией.
Скорость химической реакции в газовой фазе или растворе определяется изменением числа молекул (или числа молей n) вещества в единицу времени в единице объема:
 ,
,
Где «+» - скорость определяется по продукту реакции;
«-» - скорость определяется по исходному веществу;
Если реакция протекает при постоянном объеме, то скорость выражают через молярную концентрацию:  , которая имеет размерность моль/л.
, которая имеет размерность моль/л.

Для реакций, протекающих в газовой фазе, скорость реакции можно определять также через парциальные давления веществ. Скорость реакции выражают в различных единицах: моль/л с, Па/с.
Большинство химических реакций состоит из нескольких стадий, называемых элементарными реакциями. Под элементарной реакцией обычно понимают образование или разрыв химической связи, протекающий через образование переходного комплекса.
Переходный или активированный комплекс – конфигурация ядер, соответствующая переходу от реагентов к продуктам. Обычно переходному комплексу отвечает область вблизи максимума на энергетической кривой химической реакции.

Число частиц, участвующих в элементарной реакции, называют молекулярностью реакции. Элементарные реакции бывают трех типов.
1. Мономолеклярные реакции – элементарные реакции распада и изомеризации, в которых участвует только одна молекула:
Разрыв связей в исходной молекуле происходит под действием света или при нагревании, например:
CH3Br  CH3 + Br.
CH3 + Br.
2. В бимолекулярных реакциях происходит стокновение двух частиц:
При этом одни связи разрываются, а другие образуются, например:
H + Cl2 ® HCl + Cl
Бимолекулярные реакции - самый распространенный тип элементарной реакции.
3. В тримолекулярных реакциях одновременно сталкиваются три молекулы:
2 NO + O2 ® 2NO2
.
По характеру разрыва химической связи элементарные реакции подразделяются на гомолитические и гетеролитические. В гомолитической реакции электронная пара разрывается. В гетеролитической реакции оба электрона двухэлектронной химической связи переходят к одному из атомов.
В зависимости от фазового состояния компонентов различают гомогенные и гетерогенные реакции. Гомогенные реакции – реакции, протекающие в одной фазе, к гетерогенным реакциям – реакции, протекающие на границе двух фаз. Гомофазные реакции – все компоненты находятся в одной фазе, гетерофазные реакции – компоненты реакции находятся в разных фазах.
Сложная реакция состоит из нескольких элементарных реакций. Совокупность элементарных реакций называют механизмом сложной реакции. Скорость сложной реакции определяется скоростью самой медленной ее стадии – лимитирующей.
Скорость реакции зависит от природы реагирующих веществ, их концентрации, температуры и наличия катализатора. Зависимость скорости реакции от концентрации описывается основным постулатом химической кинетики - законом действующих масс (Гульдберг, Вааге, 1864 - 1867).
Для элементарных или простых реакций скорость химической реакции в каждый момент времени пропорциональна текущим концентрациям реагирующих веществ, возведенных в степени, равные стехиометрическим коэффициентам.
Для химической реакции аА + bВ → продукты
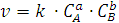 ,
,
Где k – константа скорости химической реакции; СА и СВ– молярные концентрации реагирующих веществ,
а и b – стехиометрические коэффициенты.
а – порядок реакции по веществу А;
b – порядок реакции по веществу В.
n = a + b – общий порядок реакции.
При CA = CB = 1 моль/л, v = k. Следовательно, константа скорости реакции - это удельная скорость (т.е. она равна скорости реакции при концентрации реагирующих веществ, равной единице).
Скорость большинства реакций увеличивается с ростом температуры, т.к. при этом возрастает энергия сталкивающихся частиц и повышается вероятность того, что при столкновении произойдет химическое превращение.
Для количественного описания температурных эффектов в химической кинетике используют два основных соотношения – правило Вант – Гоффа и уравнение Аррениуса.
Правило Вант – Гоффа (1884). При увеличении температуры на 10 градусов скорость химической реакции возрастает в 2 – 4 раза.
 ,
,
Где g = 2 ¸ 4 - температурный коэффициент скорости – коэффициент Вант – Гоффа;
 . и
. и  - скорость реакции при температуре Т1 и Т2.
- скорость реакции при температуре Т1 и Т2.
По закону действующих масс скорость реакции и константа скорости пропорциональны друг другу, поэтому правило Вант – Гоффа можно записать так:
 ,
,
Где  . и
. и 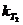 - константы скорости реакции при температуре Т1 и Т2.
- константы скорости реакции при температуре Т1 и Т2.
Правило Вант – Гоффа приближенно описывает экспериментальные данные и применимо только в очень ограниченном интервале температур.
Гораздо более точным является уравнение Аррениуса, описывающее температурную зависимость константы скорости:
 ,
,
Где Еакт – энергия активации, кДж;
А – предэкспоненциальный множитель;
R = 8,31 Дж/моль × К – универсальная газовая постоянная;
Т, К – температура.
В логарифмическом виде уравнение Аррениуса имеет вид:

Зная  и
и 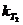 , можно рассчитать энергию активации:
, можно рассчитать энергию активации:

Гетерогенные реакции идут на поверхности раздела фаз, которая и служит реакционным пространством. Поэтому первой особенностью кинетики этих реакций является влияние площади реакционной поверхности на скорость реакции

Где с – концентрация реагента (газообразного или жидкого).
Если в реакции непосредственно участвует твердое вещество, то в кинетическое уравнение не входит его концентрация
Например, для реакции CaO (т) + CO2 (г) «CaCO3 (т) по закону действующих масс  .
.
Химическое равновесие
Для многих химических реакций при определенных внешних условиях наступает такое состояние, когда соотношение между концентрациями продуктов реакции и исходных веществ становится постоянным. Подобное состояние соответствует состоянию устойчивого химического равновесия, а концентрации реагентов называются равновесными.
При достижении химически равновесного состояния число молекул веществ перестает меняться и остается постоянным во времени. Для химического равновесия характерны следующие признаки:
1) равенство скоростей прямой и обратной реакций;
2) постоянство концентраций (парциальных давлений) компонентов при постоянстве внешних условий;
3) подвижность, то есть способность самопроизвольно восстанавливаться при небольших смещениях;
4) при р, Т=const величина G достигает минимального значения (dG =0 или ΔG =0);
5) равновесие достигается как прямым, так и обратным течением реакции.
Состояние химического равновесия характеризуется константой химического равновесия. Для химической реакции aA + bB  dD + eE, протекающей в жидкой фазе
dD + eE, протекающей в жидкой фазе
 ,
,
где Kc – константа химического равновесия, выраженная через концентрации
компонентов;
 – концентрации компонентов, определенные в состоянии равновесия.
– концентрации компонентов, определенные в состоянии равновесия.
Если указанная реакция является газофазной, то вместо концентрации компонентов используют их равновесные парциальные давления:

Если все реагенты газообразные и их поведение подчиняется законам идеальных газов, то связь между Kp и Kc можно выразить уравнением:
Kp = Kc (RT) Dn,
Где Dn - изменение числа молей газов в результате реакции:
Dn = (d + e) – (a + b).
Если изменить концентрацию хотя бы одного из компонентов равновесной системы, то концентрации всех остальных компонентов (реагентов и продуктов) будут изменяться до тех пор, пока не будут выполнены все приведенные выше 5 условий. То же самое происходит, если изменить температуру. Подобные изменения свидетельствуют о подвижном характере химического равновесия. При этом говорят о смещении равновесия в сторону образования либо исходных веществ (влево), либо продуктов реакции (вправо). Суть смещения состояния равновесия заключается в том, что при изменении концентрации и температуры претерпевают резкие изменения скорости прямой и обратной реакций. Это нарушает условие их равенства. Изменение скоростей вызывает изменение соотношения концентраций компонентов, а это в свою очередь снова приводит к выравниванию скоростей прямой и обратной реакций – возникает новое равновесное состояние.
Введение в систему других веществ, например, катализатора, не меняет постоянства соотношения равновесных концентраций реагентов, так как приводит к изменению в одинаковое число раз скорости прямой и обратной реакций.
Направление смещения равновесия в качественной форме определяется принципом Ле Шателье: если на систему, находящуюся в равновесии, оказывается внешнее воздействие, то равновесие смещается в том направлении, которое ослабляет влияние этого воздействия.
О влиянии изменения концентрации можно судит из уравнения изотермы химической реакции. Для приведенной выше реакции оно имеет следующий вид:
 ,
,
где  – неравновесные концентрации компонентов, моль/л;
– неравновесные концентрации компонентов, моль/л;
 – разница между свободными энергиями данного состояния и равновесного состояния системы;
– разница между свободными энергиями данного состояния и равновесного состояния системы;
Т – температура системы, К;
R – универсальная газовая постоянная;
Кс – константа равновесия при данной температуре Т;
DG° = -RT×lnKc – стандартная энергия Гиббса химической реакции.
Если система находится в состоянии равновесия, то в уравнении 4.3 первый член внутри скобки становится равным lnKc и DG = 0. Последний параметр является термодинамическим условием состояния равновесия.
После введения в равновесную систему исходных реагентов концентрация их возрастает и DG< 0, то есть смещение равновесия происходит в направлении протекания прямой реакции (слева направо). Такой же результат дает удаление из равновесной системы продуктов реакции. Последним методом смещения равновесия нередко пользуются в технологических процессах для увеличения выхода продуктов равновесных процессов.
Температура также влияет на направление смещения химического равновесия (изобара химической реакции):
 ,
,
где DН – тепловой эффект прямой реакции, Дж/моль;
R – универсальная газовая постоянная, Дж/(моль×К);
K1 и K2 – константы равновесия данной реакционной системы при температурах Т1 и Т2.
Действительно, если прямая реакция является экзотермическим (DН<0), то повышение температуры от Т1 до Т2 предполагает образование соотношения  < 0. Это свидетельствует о том, что в новом равновесном состоянии концентрация продуктов становится меньше, а исходных больше. Следовательно, повышение температуры приводит к смещению равновесия в сторону обратной эндотермической реакции (справа налево).
< 0. Это свидетельствует о том, что в новом равновесном состоянии концентрация продуктов становится меньше, а исходных больше. Следовательно, повышение температуры приводит к смещению равновесия в сторону обратной эндотермической реакции (справа налево).
Температура, при которой наступает химическое равновесие, равна:
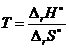
Основной особенностью константы гетерогенного равновесия является то, что в уравнение константы гетерогенного равновесия не входят никакие члены, относящиеся к твердым веществам, участвующим в прямой и обратной реакциях. Так как прямая и обратная реакции протекают на одной же поверхности раздела фаз, то площадь поверхности раздела фаз также не входит в уравнение константы химического равновевсия.
Фазовое равновесие
Равновесие процесса перехода вещества из одной фазы в другую без изменения химического состава называется фазовым равновесием. Примерами фазового равновесия могут быть следующие процессы:
Твердое вещество при плавлении превращается в жидкость;
Жидкость при кристаллизации превращается в твердое вещество;
Жидкость при испарении превращается в пар;
Пар при конденсации превращается в жидкость.
Твердое вещество при возгонке превращается в газ;
Газ при сублимации превращается в твердое вещество.
Фазовое равновесие является динамическим, т.е скорость прямого процесса равна скорости обратного процесса. Как и в случае химического равновесия, условием фазового равновесия является равенство энергии Гиббса процесса нулю: D G° = 0.
К наиболее общим законам гетерогенного равновесия (химического и фазового) относится правило фаз Гиббса, согласно которому числа степеней свободы С, фаз Ф, независимых компонентов К и внешних условий n, влияющих на равновесие, взаимосвязаны соотношением
С + Ф = К + n,
где С – число степеней свободы, число внешних условий, которые можно изменять в определенных пределах без изменения числа и вида фаз,
n – число внешних параметров, которые оказывают влияние на систему,
К – количество компонентов – химически однородная составная часть вещества, которая может быть выведена из системы.
Ф – число фаз – часть системы, однородная во всех ее точках по химическому составу и свойствам и отделенная от других фаз системы поверхностью раздела.
Перед решением задач необходимо усвоить сл<






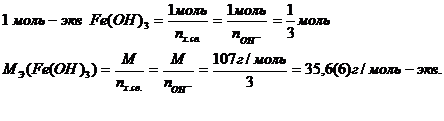

 молярную массу на численно равную относительную молекулярную (Мr), молярную массу эквивалента – на эквивалентную (Э), получим:
молярную массу на численно равную относительную молекулярную (Мr), молярную массу эквивалента – на эквивалентную (Э), получим:





 1 моль Н2 22,4 л х = 11,2 л
1 моль Н2 22,4 л х = 11,2 л 1 моль-экв→ ½ моль х л
1 моль-экв→ ½ моль х л

 1 моль-экв → ¼ моль х л
1 моль-экв → ¼ моль х л
 ,
, , которая имеет размерность моль/л.
, которая имеет размерность моль/л.

 CH3 + Br.
CH3 + Br.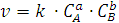 ,
, ,
, . и
. и  - скорость реакции при температуре Т1 и Т2.
- скорость реакции при температуре Т1 и Т2. ,
, . и
. и 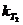 - константы скорости реакции при температуре Т1 и Т2.
- константы скорости реакции при температуре Т1 и Т2. ,
,


 .
. dD + eE, протекающей в жидкой фазе
dD + eE, протекающей в жидкой фазе ,
, – концентрации компонентов, определенные в состоянии равновесия.
– концентрации компонентов, определенные в состоянии равновесия.
 ,
, – неравновесные концентрации компонентов, моль/л;
– неравновесные концентрации компонентов, моль/л; – разница между свободными энергиями данного состояния и равновесного состояния системы;
– разница между свободными энергиями данного состояния и равновесного состояния системы; ,
, < 0. Это свидетельствует о том, что в новом равновесном состоянии концентрация продуктов становится меньше, а исходных больше. Следовательно, повышение температуры приводит к смещению равновесия в сторону обратной эндотермической реакции (справа налево).
< 0. Это свидетельствует о том, что в новом равновесном состоянии концентрация продуктов становится меньше, а исходных больше. Следовательно, повышение температуры приводит к смещению равновесия в сторону обратной эндотермической реакции (справа налево).