

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Таксономические единицы (категории) растений: Каждая система классификации состоит из определённых соподчиненных друг другу...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Таксономические единицы (категории) растений: Каждая система классификации состоит из определённых соподчиненных друг другу...
Топ:
Выпускная квалификационная работа: Основная часть ВКР, как правило, состоит из двух-трех глав, каждая из которых, в свою очередь...
Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов...
Генеалогическое древо Султанов Османской империи: Османские правители, вначале, будучи еще бейлербеями Анатолии, женились на дочерях византийских императоров...
Интересное:
Средства для ингаляционного наркоза: Наркоз наступает в результате вдыхания (ингаляции) средств, которое осуществляют или с помощью маски...
Аура как энергетическое поле: многослойную ауру человека можно представить себе подобным...
Принципы управления денежными потоками: одним из методов контроля за состоянием денежной наличности является...
Дисциплины:
|
из
5.00
|
Заказать работу |
Содержание книги
Поиск на нашем сайте
|
|
|
|
Восстановление оксидов металлов оксидом углерода принято описывать уравнением реакции (6.6), согласно которому для восстановления 1 моля оксида необходим 1 моль СО. Однако такая запись уравнения реакции не совсем корректна, так как после полного восстановления оксида газовая фаза содержит 100% СО2 и является окислительной по отношению к любому металлу.
Окисления восстановленного металла можно избежать, если образовавшаяся в результате реакции газовая фаза по отношению к металлу будет восстановительной. Для этого СО потребуется в большем количестве, а процесс восстановления будет описываться уравнением реакции
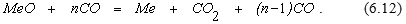
Расход восстановителя будет минимальным, если газовая фаза из 1 моля СО2 и (n-1) моля СО будет равновесной для реакции (6.6), то есть

Из уравнения (6.13) получим

Для легковосстановимых оксидов константы равновесия реакции (6.6) имеют большие значения, поэтому минимальный расход восстановителя близок к стехиометрическому.
Для оксидов второй группы константы равновесия реакции (6.6) близки к единице. При этом минимальный расход газообразного восстановителя существенно отличается от стехиометрического. Например, константа равновесия реакции восстановления FeO при 1000К равна 0,624. Согласно уравнению (6.14) для восстановления 1 моля оксида потребуется 2,6 моля СО.
Для трудно восстановимых оксидов константы равновесия реакции (6.6) очень малы. Поэтому минимальный расход восстановителя является очень высоким.
Например, для полного восстановления 1 моля MnO при 1000К потребуется 1,4•106 молей СО. Такой большой расход восстановителя обычно обеспечить не удается, поэтому на практике процесс восстановления с использованием газообразных восстановителей может быть реализован только для оксидов первой и второй групп.
Полученные выше выводы справедливы также при восстановлении оксидов металлов водородом и другими газами.
ВОССТАНОВЛЕНИЕ ОКСИДОВ МЕТАЛЛОВ УГЛЕРОДОМ.
Общая характеристика реакций восстановления оксидов углеродом. В научно-технической литературе восстановление оксидов углеродом принято называть прямым восстановлением, а восстановление оксидом углерода – косвенным или не прямым восстановлением.
В связи с несовершенством контакта между кусковыми материалами возможность непосредственного взаимодействия между углеродом и твердыми оксидами ограничена. Поэтому реакции прямого восстановления протекают преимущественно с участием газовой фазы и представляют собой результат последовательного протекания реакций косвенного восстановления
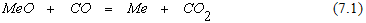
и взаимодействия углекислого газа с углеродом

Результат последовательного протекания реакций (7.1) и (7.2) можно описать уравнением
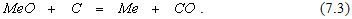
Согласно закону Гесса
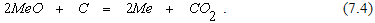
Изменение энтальпии реакции (7.1) может быть как отрицательной, так и положительной величиной. В первом случае оно обычно не велико и не превышает 172130 Дж/моль. Поэтому реакции прямого восстановления обычно являются эндотермическими.
При низких температурах восстановление оксидов углеродом может также протекать по реакции
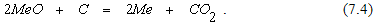
Однако при температурах более 950 – 1000оС углекислый газ взаимодействует с углеродом по реакции (7.2) и практически полностью превращается в СО.
Температура начала восстановления оксида. Система, в которой протекают реакции (7.1) и (7.2) состоит из пяти веществ, связанных между собой двумя уравнениями реакций. Следовательно, количество независимых компонентов системы k = 3. При отсутствии растворов количество находящихся в равновесии фаз f = 4, а число степеней свободы системы
C = k + n – f = 3 + 2 – 4 = 1.
Это означает, что однозначно охарактеризовать систему можно, указав температуру или давление.
При постоянном давлении количество степеней свободы системы становится равным нулю. Это означает, что система из чистых металла, оксида, углерода, СО и СО2 может находиться в состоянии равновесия только при одной температуре, которая определяется составом газовой фазы.
Сказанное выше показано на рисунке 7.1. Из рисунка видно, что при постоянном давлении реакции (7.1) и (7.2) могут одновременно находиться в равновесном состоянии только при одной температуре Тр.
Рассмотрим процессы, которые протекают в системе при температурах отличных от Тр.
Из рисунка 7.1 видно, что при Т >Тр в системе нет газовой фазы, которая удовлетворяла бы условиям равновесия реакций (7.1) и (7.2) одновременно.
Допустим, что при температуре Т1 реакция (7.1) находится в состоянии равновесия. При этом состав равновесной газовой фазы для реакции (7.1) отвечает точке б. Но газовая смесь такого состава не является равновесной по отношению к углероду, так как содержание СО2 в газовой фазе выше равновесного для реакции (7.2), которое соответствует точке в на рисунке.
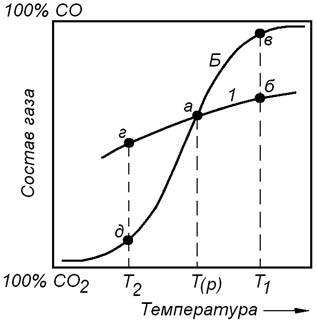
Рисунок 7.1 – Зависимость состава равновесной газовой фазы от температуры для экзотермической реакции косвенного восстановления и реакции С + СО2 = 2СО при постоянном давлении
В этих условиях реакция (7.2) протекает в направлении образования дополнительного количества оксида углерода и (%СО) в общей для двух реакций газовой фазе увеличивается. При этом газовая фаза перестанет отвечать условиям равновесия реакции косвенного восстановления, которая будет протекать в направлении восстановления оксида и образования дополнительного количества СО2. Результатом одновременного протекания реакций (7.1) и (7.2) будет процесс, который описывается уравнением реакции прямого восстановления (7.3).
Сказанное выше можно представить следующей схемой
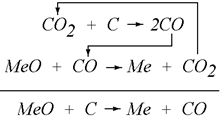
При наличии в исходном состоянии избытка углерода оксид металла будет полностью восстановлен и часть углерода останется не использованной. При этом равновесие в системе будет достигнуто, когда состав газовой фазы будет соответствовать точке в на рисунке 7.1.
При умеренных температурах в составе равновесного газа может находиться существенное количество СО2. Это означает, что восстановление оксида протекает как по реакции (7.3), так и по реакции (7.4).
При недостатке углерода он будет полностью израсходован и часть оксида останется не восстановленной. При этом равновесие в системе будет достигнуто, когда состав газовой будет соответствовать точке б.
При Т <Тр в системе также нет газовой фазы, которая одновременно удовлетворяла бы условиям равновесия реакций (7.1) и (7.2).
Допустим, что при температуре Т2 реакция (7.1) находится в состоянии равновесия. При этом состав равновесной газовой фазы для реакции (7.1) отвечает точке г. Но газовая смесь такого состава не является равновесной по отношению к углероду, так как содержание СО в газовой фазе выше равновесного для реакции (7.2), которое соответствует точке д на рисунке 7.1.
В этих условиях реакция (7.2) протекает в направлении разложения оксида углерода на углекислый газ и углерод. При этом (%СО2) в общей для двух реакций газовой фазе увеличивается, и она становится окислительной по отношению к металлу.
Протекающие при этом процессы можно представить следующей схемой
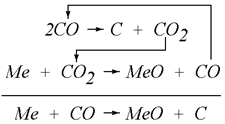
Таким образом, в присутствии углерода при Т <Тр оксид углерода по отношению к металлу может выступать в роли окислителя. Но окисление протекает не в результате непосредственного взаимодействия металла с СО, а при взаимодействии с СО2, который образуется в результате распада СО при наличии в системе углерода.
Если в исходном состоянии над металлом будет избыток газа, произойдет полное окисление металла. При этом состав равновесной газовой фазы будет соответствовать точке д.
Из рассмотренных примеров следует, что при постоянном давлении в системе возможны следующие процессы:
1. Равновесие при одной единственной температуре Тр характерной для каждого оксида.
2. Восстановление оксидов при температурах выше Тр, в связи с чем эту температуру называют также температурой начала восстановления.
3. Распад оксида углерода и окисление металла при температурах ниже Тр.
|
|
|

Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций...

Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим...

Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни...

Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ - конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой...
© cyberpedia.su 2017-2026 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!