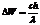Энергия рассеянного фотона  , энергия падающего фотона
, энергия падающего фотона 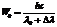 ,Найдем часть энергии
,Найдем часть энергии 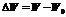
Фотон с энергией 0,25 МэВ рассеялся на свободном электроне. Энергия рассеянного фотона 0,2 МэВ. Определить угол рассеяния.
Энергия рассеянного фотона  , энергия падающего фотона
, энергия падающего фотона  , =>
, =>  ,
, 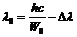 ,
,
отсюда находим изменение  , используя выражение
, используя выражение 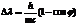 , получаем
, получаем 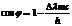
32. Фотон с энергией 1,2 МэВ был рассеян в результате эффекта Комптона на угол 90°. Найти энергию и длину волны рассеянного фотона.
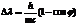 , энергия падающего фотона
, энергия падающего фотона 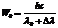 ,
, 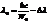 , тогда энергия рассеян. фотона
, тогда энергия рассеян. фотона 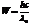 ,
, 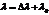
Что характерно для атомных спектров?
Атомные спектры, спектры оптические, получающиеся при испускании или поглощении света (электромагнитных волн) свободными или слабо связанными атомами; такими спектрами обладают, в частности, одноатомные газы и пары. Они являются линейчатыми — состоят из отдельных спектральных линий. Они наблюдаются в виде ярких цветных линий при свечении газов или паров в электрической дуге или разряде (спектры испускания) и в виде тёмных линий (спектров поглощения).
Что характерно для молекулярных спектров?
Молекулярные спектры, оптические спектры испускания и поглощения, а также комбинационного рассеяния света, принадлежащие свободным или слабо связанным между собой молекулам. М. с. имеют сложную структуру. Типичные М. с. — полосатые, они наблюдаются в испускании и поглощении и в комбинационном рассеянии в виде совокупности более или менее узких полос в ультрафиолетовой, видимой и близкой инфракрасной областях, распадающихся при достаточной разрешающей силе применяемых спектральных приборов на совокупность тесно расположенных линий.
Постулаты Бора.
1) В атоме существуют стационарные круговые орбиты, по которым электрон движется без излучения. Стационарными орбитами будут те, для которых момент количества движения 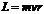 электрона может принимать значения, кратные
электрона может принимать значения, кратные 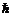 . То есть
. То есть 
2) При переходе атома из состояния с энергией 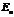 в состояние с энергией
в состояние с энергией 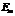 (
( ) излучается один фотон (квант), энергия которого равна
) излучается один фотон (квант), энергия которого равна 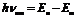
Какие опыты лежат в основе ядерной модели Резерфорда?
Опыты по рассеянию α-частиц в веществе, затем опыт по прохождению α-частиц в веществе через золотую фольгу.
В чем заключалось противоречие модели атома Резерфорда с классической теорией?
Согласно электродинамике, ускоренно движущиеся электроны должны излучать электромагнитные волны и вследствие этого непрерывно терять энергию. В результате электроны будут приближаться к ядру и в конце концов упадут на него. Таким образом, атом Резерфорда оказывается неустойчивой системой, что опять-таки противоречит действительности.
38. Правило частот Бора. Это и есть 2-ой постулат Бора.
2-й постулат Бора: При переходе атома из состояния с энергией E n в состояние с энергией E m (E n > E m) излучается один фотон (квант), энергия которого равна: h nm = En – Em
Правило квантования орбит.
Правило квантования, приводящее к правильным, согласующимся с опытом значениям энергий стационарных состояний атома водорода, было угадано Бором. Бор предположил, что выполняется следующее соотношение между скоростью движения электрона и радиусом орбиты: 
Здесь m – масса электрона, v– его скорость, rn – радиус стационарной круговой орбиты. Правило квантования Бора позволяет вычислить радиусы стационарных орбит электрона в атоме водорода и определить значения энергий.
Найти длину волны фотона при переходе электрона из состояния с энергией (–5 эВ) в состояние с энергией (–9 эВ).
2-ой постулат Бора  , отсюда
, отсюда 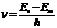 ,
,
так как 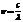 , тогда
, тогда  , длина волны
, длина волны 
41. Энергия электрона в водородоподобном атоме определяется соотношением  Выразить через эти обозначения энергию фотона, испускаемого при переходе электрона в атоме водорода с третьего энергетического уровня на первый.
Выразить через эти обозначения энергию фотона, испускаемого при переходе электрона в атоме водорода с третьего энергетического уровня на первый.

 подставить значения констант в уравнение. Ответ в Дж или в эВ.
подставить значения констант в уравнение. Ответ в Дж или в эВ.
42. Атом водорода в основном состоянии с энергией  поглотил квант света с длиной волны 121,5 нм. Определить энергию возбуждённого атома.
поглотил квант света с длиной волны 121,5 нм. Определить энергию возбуждённого атома.
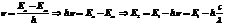
43. Энергия электрона в водородоподобном атоме определяется соотношением 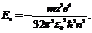 Выразить через эти обозначения энергию фотона, который испускает ион гелия He+ при переходе со второго энергетического уровня на первый.
Выразить через эти обозначения энергию фотона, который испускает ион гелия He+ при переходе со второго энергетического уровня на первый.
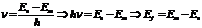
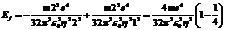 подставить значения констант в уравнение. Ответ в Дж или в эВ.
подставить значения констант в уравнение. Ответ в Дж или в эВ.
44. На сколько изменится энергия электрона в атоме водорода при излучении атомом фотона с длиной волны 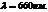 ?
?
Согласно второму постулату Бора частота излучения, соответствующая переходу электрона с одной орбиты на другую, определяется формулой 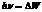 или
или  - (1). С другой стороны
- (1). С другой стороны 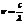 - (2),
- (2),
где с=3*108 м/с – скорость света,  -длина волны излученного атомом фотона. Приравнивая равные части уравнений (1) и (2). Получаем
-длина волны излученного атомом фотона. Приравнивая равные части уравнений (1) и (2). Получаем 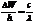 , откуда изменение кинетической энергии электрона
, откуда изменение кинетической энергии электрона 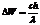



 , энергия падающего фотона
, энергия падающего фотона 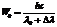 ,Найдем часть энергии
,Найдем часть энергии 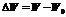
 , =>
, =>  ,
, 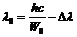 ,
, , используя выражение
, используя выражение 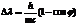 , получаем
, получаем 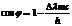
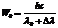 ,
, 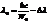 , тогда энергия рассеян. фотона
, тогда энергия рассеян. фотона 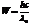 ,
, 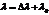
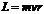 электрона может принимать значения, кратные
электрона может принимать значения, кратные 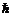 . То есть
. То есть 
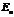 в состояние с энергией
в состояние с энергией 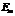 (
( ) излучается один фотон (квант), энергия которого равна
) излучается один фотон (квант), энергия которого равна 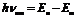

 , отсюда
, отсюда 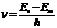 ,
,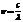 , тогда
, тогда  , длина волны
, длина волны 
 Выразить через эти обозначения энергию фотона, испускаемого при переходе электрона в атоме водорода с третьего энергетического уровня на первый.
Выразить через эти обозначения энергию фотона, испускаемого при переходе электрона в атоме водорода с третьего энергетического уровня на первый.
 подставить значения констант в уравнение. Ответ в Дж или в эВ.
подставить значения констант в уравнение. Ответ в Дж или в эВ. поглотил квант света с длиной волны 121,5 нм. Определить энергию возбуждённого атома.
поглотил квант света с длиной волны 121,5 нм. Определить энергию возбуждённого атома.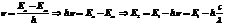
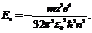 Выразить через эти обозначения энергию фотона, который испускает ион гелия He+ при переходе со второго энергетического уровня на первый.
Выразить через эти обозначения энергию фотона, который испускает ион гелия He+ при переходе со второго энергетического уровня на первый.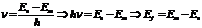
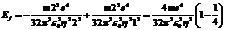 подставить значения констант в уравнение. Ответ в Дж или в эВ.
подставить значения констант в уравнение. Ответ в Дж или в эВ.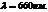 ?
?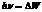 или
или  - (1). С другой стороны
- (1). С другой стороны 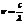 - (2),
- (2), -длина волны излученного атомом фотона. Приравнивая равные части уравнений (1) и (2). Получаем
-длина волны излученного атомом фотона. Приравнивая равные части уравнений (1) и (2). Получаем 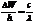 , откуда изменение кинетической энергии электрона
, откуда изменение кинетической энергии электрона