

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Своеобразие русской архитектуры: Основной материал – дерево – быстрота постройки, но недолговечность и необходимость деления...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Своеобразие русской архитектуры: Основной материал – дерево – быстрота постройки, но недолговечность и необходимость деления...
Топ:
Генеалогическое древо Султанов Османской империи: Османские правители, вначале, будучи еще бейлербеями Анатолии, женились на дочерях византийских императоров...
Когда производится ограждение поезда, остановившегося на перегоне: Во всех случаях немедленно должно быть ограждено место препятствия для движения поездов на смежном пути двухпутного...
Интересное:
Распространение рака на другие отдаленные от желудка органы: Характерных симптомов рака желудка не существует. Выраженные симптомы появляются, когда опухоль...
Финансовый рынок и его значение в управлении денежными потоками на современном этапе: любому предприятию для расширения производства и увеличения прибыли нужны...
Национальное богатство страны и его составляющие: для оценки элементов национального богатства используются...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Клееная фанера
Фанера (англ. plywood) производится путем склеивания листов натурального деревянного шпона толщиной 0,8 - 3, преимущественного лущеного, в горячих плоских прессах. Фанера является универсальным конструкционным материалом, используемым в самых различных областях. В мебельном производстве имеют важное значение плоскокленые элементы, получаемые в плоских прессах и гнутоклееные - получаемые в фасонных прессформах. Для строительных целей используются высокопрочные фанерные балки.
При изготовления декоративной фанеры в качестве наружных слоев используют высококачественный строганый шпон или декоративные синтетические материалы (пленки). Последние имеют также отличные защитные свойства. В бакелитовой фанере в качестве полимерной матрицы используют готовые бакелитовые пленки, получаемые на основе бумаг, пропитанных бакелитовыми (фенолоформальдегидными) смолами.
Ламинированная фанера, облицованная бумажными пленками на основе термореактивных полимеров, обладает улучшенными физико-химическими свойствами. Она используется, например, в качестве многоразовой опалубки в производстве бетонных работ, при изготовлении железнодорожных контейнеров и т.п.
Металлопласты
Металлопласт (англ. metal-based laminate) листовой конструкционный материал, состоящий из листового металла и полимерной плёнки, нанесенной с одной или двух сторон. Толщина металла (сталь, алюминий и его сплавы, титан и др.)обычно 0,3—1,2 мм, полимерной плёнки 0,05—1 мм. Плёнка может быть из фторопластов, пластифицированного и др. полимеров. Металлопласт получают путём нанесения на полосу заранее изготовленной плёнки, погружением полосы в расплав полимера, нанесением полимерной пасты или напылением полимера в порошкообразном состоянии. Покрытие может быть одно- или многоцветным, гладким или рельефным, имитировать ценные породы дерева, мрамор и др. материалы. Металлопласт не расслаивается в процессе деформации металла при штамповке или вырубке. Изделия не нуждаются в антикоррозионной защите и декоративной отделке.
|
|
 Металлопласты применяют в качестве кровельных материалов, для отделки зданий, перил балконов, в качестве водосточных желобов, внутренней обшивки стен, для изготовления дверных и оконных рам, корпусов автомобилей, холодильников, стиральных машин, радиоприёмников, телевизоров, тары для хранения агрессивных материалов, для внутренней отделки салонов пассажирских самолётов, вагонов, автофургонов и т.д.
Металлопласты применяют в качестве кровельных материалов, для отделки зданий, перил балконов, в качестве водосточных желобов, внутренней обшивки стен, для изготовления дверных и оконных рам, корпусов автомобилей, холодильников, стиральных машин, радиоприёмников, телевизоров, тары для хранения агрессивных материалов, для внутренней отделки салонов пассажирских самолётов, вагонов, автофургонов и т.д.
Текстолиты
(англ. textolite) изготавливают горячим прессованием нескольких слоев ткани, пропитанной термореактивными смолами. Текстолит - хороший диэлектрик, стоек к действию слабых кислот и щелочей, имеет низкий коэффициент трения (0,02 со смазкой и 0,32 без смазки), небольшую плотность (1,3- 1,4 г/см), легко поддается механической обработке (фрезерование, распиловка, сверление, штамповка, шлифование, строгание). Текстолит используется в качестве конструкционного материала в приборо- и станкостроении, машиностроении, в том числе химическом и нефтехимическом, в автоматических системах управления, судо- и тракторостроении и других отраслях. Из текстолитов изготавливают: шестерни; сепараторы для подшипников, обеспечивающих высокие скорости; кулачки, обладающие малой инерцией для различных станков, венцы червячных колес, втулки, амортизирующие прокладки, уплотнительные кольца и т.д.
Стеклотекстолиты
представляют собой прессованные слоистые материалы, состоящие из нескольких слоев стеклоткани, пропитанной связующим на основе эпоксидных или эпоксидно-фенольных смол. Они используется в качестве электроизоляционного и теплоизолирующего материала в радиотехнике, приборостроении, применяется в электрических высоковольтных машинах и аппаратах
|
|
Миканиты
представляют собой слоистые композиционные материалы получаемые на основе слюды с применением различных видов связующих (глифталевых, масляно-глифталевых, кремнийорганических и др.), используемые в качестве изоляционных материалов в электрических машинах и аппаратах.
Многослойные стекла
 (англ. laminated glass) состоят из одного или более листов силикатного или органического стекла и одного или более слоев полимера (пленки). Трехслойные стекла обычно называют триплексами. Многослойные стекла
(англ. laminated glass) состоят из одного или более листов силикатного или органического стекла и одного или более слоев полимера (пленки). Трехслойные стекла обычно называют триплексами. Многослойные стекла
применяется для остекления автомобилей, самолётов, вертолётов, судов, подвижного состава железнодорожного транспорта, в строительстве и т.д. Входящие в состав многослойных стекол полимерные пленки поглощают энергию удара и препятствую разлетанию осколков. Многослойные стекла используются для антивандальных и пуленепробиваемых остеклений. В многослойных стеклах могут быть реализованы различные декоративные приемы и в последнее время они активно используются в художественныз целях (витражи и т.п.).
Линолеум
(от лат. linum — лён, полотно и oleum — масло), полимерный рулонный материал для покрытия полов.
Первоначально линолеум получали на тканевой (джутовой) основе из растительных масел (льняного, подсолнечного, тунгового), пробковой муки и др. — так называемый глифталевый линолеум. Глифталевый линолеум с 50-х гг. уступил место поливинилхлоридному лионолеуму, который получил наибольшее распространение. В зависимости от основного исходного сырья (связующего) линолеум подразделяется на поливинилхлоридный, глифталевый (алкидный), коллоксилиновый (нитролинолеум) и резиновый (релин). Линолеум может быть безосновный (одно- и многослойный) и на упрочняющей (тканевой, пергаминовой) или теплозвукоизоляционной основе. Линолеум выпускается одно- и многоцветный (мраморовидный, крапчатый, узорчатый).
Рубероид,
(англ. ruberoid, asphalted paper) многослойный рулонный кровельный и гидроизоляционный материал, изготовляемый путём пропитки кровельного картона мягкими нефтяными битумами с последующим покрытием обеих поверхностей слоем тугоплавкого битума. Рубероид применяется для устройства верхнего слоя кровельного ковра; лицевая поверхность рубероида покрыта сплошным слоем крупнозернистой или чешуйчатой посыпки (крупный песок, слюда и др.), защищающим рубероид от воздействия солнечных лучей. Стеклорубероид изготовляется на основе стеклотканей.
|
|
Спеченные цветные металлы
Спеченный титан и его сплавы используют в виде полуфабрикатов (лист, трубы, пруток). Титановый каркас пропитывают магнием. Такие материалы хорошо обрабатываются давлением.
Широко используются материалы на основе меди, например, изготавливают бронзо – графитные шестерни. Свойства спеченных латуней выше, чем литых, из-за большей однородности химического состава и отсутствия посторонних включений.
Спеченные алюминиевые сплавы используют для изготовления поршней тяжело нагруженных двигателей внутреннего сгорания и других изделий, длительное время работающих при повышенных температурах, благодаря их повышенной жаропрочности и коррозионной стойкости.
Керамикометаллические материалы (керметы) содержат более 50 % керамической фазы. В качестве керамической фазы используют тугоплавкие бориды, карбиды, оксиды и нитриды, в качестве металлической фазы – кобальт, никель, тугоплавкие металлы, стали.
Керметы отличаются высокими жаростойкостью, износостойкостью, твердостью, прочностью. Они используются для изготовления деталей конструкций, работающих в агрессивных средах при высоких температурах, например, лопаток турбин, чехлов термопар. Частным случаем керметов являются твердые сплавы.
Неорганическое стекло
 Править
Править 
 Cтекло естественное метеоритного происхождения
Cтекло естественное метеоритного происхождения
 Добавил Moisey
Добавил Moisey
 Лампа неоновая вместо накальной (13ватт с освещением в 65 свечей)
Лампа неоновая вместо накальной (13ватт с освещением в 65 свечей)
 Добавил Moisey
Добавил Moisey
Неорганическое стекло́ или стекло, отличающееся составом стеклообразующих веществ: оксидов, фторидов и др. — твёрдый, хрупкий,аморфный материал, разновидности которого формируются при определённых условиях в процессе переохлаждения без кристаллизации расплава, но при определённых температурных и технологических условиях способное к кристаллизации (например, неорганический материал ситаллы).
Содержание
[показать]
|
Виды стекол  Править
Править
|
|
В зависимости от основного используемого стеклообразующего вещества, стекла можно рзделить на:
Стеклообразующие вещества  Править
Править
К стеклообразующим веществам относятся:
Оксиды:
Фториды:
и др.
Базовый метод получения силикатного стекла заключается в плавлении смеси кварцевого песка (SiO2), соды (Na2CO3) и извести (CaO). В результате получается химический комплекс с составом Na2O*CaO*6SiO2.
Технологии  Править
Править
Различаются три главных вида стекла:
В качестве главной составной части в стекле содержится 70 — 75 % двуокиси кремния (SiO2), получаемой из кварцевого песка при условии соответствующей грануляции и свободы от всяких загрязнений. Венецианцы для этого применяли чистый песок из реки По или даже завозили его из Истрии, тогда как богемские стеклоделы получали песок из чистого кварца.
Второй компонент — окись кальция (CaO) — делает стекло химически стойким и усиливает его блеск. На стекло она идёт в виде извести. Древние египтяне получали её из щебня морских раковин, а в средние века она приготовлялась из золы деревьев или морских водорослей, так как известняк в качестве сырья для приготовления стекла был ещё не известен. Первым подмешивать к стеклянной массе мел, как тогда назывался известняк, стали богемские стеклоделы в XVII веке.
Следующей составной частью стекла являются окиси щелочных металлов, вроде окиси натрия (Na2O) или окиси калия (K2O), нужные для плавки и выделки стекла. Их доля составляет примерно 16-17 %. На стекло они идут в виде соды (Na2CO3) или поташа (K2CO3), которые при температуре легко разлагаются на окиси. Соду сначала получали выщелачиванием золы морских водорослей, а в местности, удалённой от моря, применяли содержащий калий поташ, получая его выщелачиванием золы буковых или хвойных деревьев.
|
|
Содовое стекло можно с лёгкостью плавить, оно мягкое и потому легко поддаётся обработке, а кроме того, чистое и светлое.
Поташное стекло, напротив, более тугоплавкое, твёрдое и не такое пластичное и способное к формовке, но обладает зато сильным блеском. Оттого что раньше его получали непосредственно из золы, в которой много железа, стекло было зеленоватого цвета, и в XVI веке для его обесцвечивания начали применять перекись марганца. А так как именно лес давал сырьё для изготовления этого стекла, его называли ещё лесным стеклом. На килограмм поташа шла тонна древесины.
Свинцовое стекло (или хрусталь), получается заменой окиси кальция окисью свинца. Оно довольно мягкое и плавкое, но весьма тяжёлое, отличается сильным блеском и высоким коэффициентом светопреломления, разлагая световые лучи на все цвета радуги и вызывая игру света.
Основные свойства неорганического стекла  Править
Править
физико-химические характеристики  Править
Править
Обратимость прессов и свойств указывает на то, что стеклообразующие расплавы и затвердевшее стекло являются растворами в чистом виде. Обратимость — признак настоящего раствора. Определение неорганического стекла как переохлаждённой жидкости вытекает из способа получения стекла. Для перевода кристаллического тела в стеклообразное состояние его необходимо расплавить и затем переохладить снова. Переход вещества из жидкого состояния в твердое при понижении температуры происходит двумя путями: вещество кристаллизуется либо застывает в виде стекла. По первому пути могут следовать почти все вещества. Однако кристаллизация присутствует только в тех веществах, которые будучи в жидком состоянии, обладают малой вязкостью и вязкость которых возрастает сравнительно медленно, почти до момента кристаллизации. К таким веществам относится и оксид висмута, который в чистом состоянии практически не образует стекол.
Свойства стекла сопоставимы с понятием “свойство-состав” стеклообразных систем и показывает, что свойства можно разделить на две группы в зависимости от молярного состава — на простые и сложные.
Ко второй группе относятся свойства, которые более чувствительные к изменению состава. Зависимость их от состава сложна и часто не поддается количественным обобщениям. Например: вязкость, электропроводность, скорость диффузии ионов, диэлектрические потери, химическая стойкость, светопропускание, твёрдость, поверхностное натяжение, кристаллизационная способность и др. Расчёт этих свойств возможен лишь в конкретных случаях.
Физические свойства неорганического стекла  Править
Править
Физические свойства неорганического стекла (НС) и самое главное — прозрачность его, а таже механическая прочность, деформация, теплопроводность и др. одинаковы (изотропны) по всем направлениям. С течением времени стекло мутнеет. Помутнение вызвано появлением внутри стекла мелких кристаллов, оптические свойства которых иные, чем окружающей их аморфной среды в связи с неустойчивым состоянием аморфного вещества. Со временем аморфные вещества переходят в кристаллические. Центрами кристаллизации могут быть пылинки, вокруг которых начинается перегруппировка молекул, постепенно образующих кристаллическую решётку. Как говорят стекло "стареет".
Стекло (оптическое стекло), обладая важными характеристиками: высокой прозрачностью, дисперсией, изотропностью, термостойкостью, твёрдостью и т.д., прозрачно к свету (определённый диапазон электромагнитных лучей) и широко применяется в науке и технике:
Обычное НС как прозрачный материал — занимает достойное место в нашей жизни: в строительстве, науке, медицине, искусстве и т.д.

| Таблица физических свойств основных видов стекла | |||||||
| Свойства | Кальциево-натриевое стекло (1Na2O: 1CaO: 6SiO2)[1] | Боросиликатное стекло | Изоляционное стекло | Оптическое стекло | Кварцевое стекло | Германиевое стекло | Германий-кремниевое стекло |
| Химсостав, в % | 74 SiO2, 13 Na2O, 10.5 CaO, 1.3 Al2O3, 0.3 K2O, 0.2 SO3, 0.2 MgO, 0.01 TiO2, 0.04 Fe2O3 | 81 SiO2, 12.5 B2O3, 4 Na2O, 2.2 Al2O3, 0.02 CaO, 0.06 K2O | 63 SiO2, 16 Na2O, 8 CaO, 3.3 B2O3, 5 Al2O3, 3.5 MgO, 0.8 K2O, 0.3 Fe2O3, 0.2 SO3 | 41.2 SiO2, 34.1 PbO, 12.4 BaO, 6.3 ZnO, 3.0 K2O, 2.5 CaO, 0.35 Sb2O3, 0.2 As2O3 | SiO2 | GeO2 | GeSe2 |
| Вязкость log(η, в Па·с) = A + B / (T в °C - To) | 550-1450°C: A = -2.309 B = 3922 To = 291 | 550-1450°C: A = -2.834 B = 6668 To = 108 | 550-1400°C: A = -2.323 B = 3232 To = 318 | 500-690°C: A = -35.59 B = 60930 To = -741 | 1140-2320°C: A = -7.766 B = 27913 To = -271.7 | 515-1540°C: A = -11.044 B = 30979 To = -837 | |
| Температуратурная стойкость, Tg, °C | ~540 | 526 ± 27[2][3][4] | 395 [5] | ||||
| Коэффциент теплового расширения, ppm/K ~100-300°C | 3.5 | 0.55 | 7.3 | ||||
| Плотность при 20°C, г/см³ | 2.52 | 2.235 | 2.550 | 3.86 | 2.203 | 3.65 [6] | 4.16 [5] |
| Коэффициент преломления nD[7] при 20°C | 1.518 | 1.473 | 1.531 | 1.650 | 1.459 | 1.608 | 1.7 |
| Дисперсия (света) при 20°C, 104×(nF-nC)[7] | 86.7 | 72.3 | 89.5 | 67.8 | |||
| Модуль упругости E, при 20°C, МПа | 72 | 65 | 75 | 43.3 [8] | |||
| Модуль среза (жёсткости) при 20°C, МПа | 29.8 | 28.2 | 26.8 | 31.3 | |||
| Температура плавления, в °C | 1040 | 1070[9] | |||||
| Теплоёмкость при 20°C, Дж/(K·моль) | 49 | 50 | 50 | ||||
| Поверхностное напряжение, при ~1300°C, мДж/м2 | |||||||
| Химическая стойкость, Гидролитический класс, по ISO 719[10] | 3 | 1 | 3 |
Химическая устойчивость неорганического стекла  Править
Править
Химическая устойчивость НС видна по устойчивому отношению его к различным агрессивным средам. Это одно из важных свойсттв стекол. Но весь диапазон возможных стеклообразных систем, их химическая устойчивость различаться - от предельно устойчивого кварцевого стекла до растворимого (жидкого) стекла. Прцесс разрушения стекла в агрессивных жидкостях различают в двух видах:
При растворении компоненты стекла переходят в раствор в одинаковых пропорциях, в каких они находятся в стекле. Многие стеклообразные стекольные системы растворяются с некоторой скоростью в плавиковой кислоте и в концентрированных горячих растворах щелочей.
При выщелачивани наблюдается механизм взаимодействия стекла с водой и кислотами, кроме плавиковой. При выщелачивании в расвор переходят в основном избранные компоненты - оксиды щелочных и щелочноземельных металлов. В результате перехода на поверхности стекла образуется зещитная пленка, которая по своему составу максимально приближена к составу стекла. Переход от выщелачивания к растворению возможен при взаимодействии стекла с водой или с HCl, H2SO4, HNO3 и. т. п. только в том случае, если стекло сильно обогащено щелочами.
Химической устойчивости НС определяется по потере массы образца после обработки в агрессивной среде в течении заданного промежутка времени. Потери выражаются в мг/см². Наиболее подходит метод выборочного определения компонентов, перешедших в раствор. В данном случае потери выражают числом молей каждого из оксидов, перешедших в раствор с единицы поверхности стекла.
Для определения химической устойчивости НС в растворах в условиях высоких температур и давлений кроме потерь веса надо определять глубину разрушенного слоя и характер разрушенной поверхности.
Цвет неорганического стекла  Править
Править
Основная статья: Цвет стекла
Стекло — это сплавленная из обычных сырых материалов стеклянная масса бесцветна, с лёгким желтовато-зелёным или голубовато-зелёным отливом, вызываемым различными минеральными примесями. Для того, чтобы эту массу внутри стекла окрасить, чаще всего применяют окислы металлов, добавляя их в шихту до или после плавки.
История  Править
Править
Основная статья: История стекла
 Мюнхенская Чашка Клетки из Кёльна, 4-ое столетие нашей эры
Мюнхенская Чашка Клетки из Кёльна, 4-ое столетие нашей эры
 Добавил Moisey
Добавил Moisey
Неорганическому стеклу более четырёх тысяч лет, открыли его случайно, в Египте.
Графит
[править]
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 20 февраля 2011; проверки требуют 25 правок.


Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 20 февраля 2011; проверки требуют 25 правок.
Перейти к: навигация, поиск
| Графит | |

| |
| Формула | C (углерод) |
| Сингония | Гексагональная (планаксиальная) |
| Цвет | Серый, чёрный стальной |
| Цвет черты | Чёрная |
| Блеск | Металловидный |
| Прозрачность | Непрозрачный |
| Твёрдость | 1—2 |
| Спайность | Совершенная по {0001} |
| Плотность | 2,09—2,23 г/см³ |
| Графит |
| Фазы железоуглеродистых сплавов |
| Феррит (твердый раствор внедрения C в α-железе с объемно-центрированной кубической решеткой) Аустенит (твердый раствор внедрения C в γ-железе с гранецентрированной кубической решеткой) Цементит (карбид железа; Fe3C метастабильная высокоуглеродистая фаза) Графит стабильная высокоуглеродистая фаза |
| Структуры железоуглеродистых сплавов |
| Ледебурит (эвтектическая смесь кристаллов цементита и аустенита, превращающегося при охлаждении в перлит) Мартенсит (сильно пересыщенный твердый раствор углерода в α-железе с объемно-центрированной терагональной решеткой) Перлит (эвтектоидная смесь, состоящая из тонких чередующихся пластинок феррита и цементита) Сорбит (дисперсный перлит) Троостит (высокодисперсный перлит) Бейнит (устар: игольчатый троостит) — ультрадисперсная смесь кристаллов низкоуглеродистого мартенсита и карбидов железа |
| Стали |
| Конструкционная сталь (до 0,8 % C) Инструментальная сталь (до ~2 % C) Нержавеющая сталь (легированная хромом) Жаростойкая сталь Жаропрочная сталь Высокопрочная сталь |
| Чугуны |
| Белый чугун (хрупкий, содержит ледебурит и не содержит графит) Серый чугун (графит в форме пластин) Ковкий чугун (графит в хлопьях) Высокопрочный чугун (графит в форме сфероидов) Половинчатый чугун (содержит и графит, и ледебурит) |
Графит (от др.-греч. γράφω — пишу) — минерал из класса самородных элементов, одна из аллотропных модификаций углерода. Структура слоистая. Слои кристаллической решётки могут по-разному располагаться относительно друг друга, образуя целый ряд политипов, с симметрией от гексагональной сингонии (дигексагонально-дипирамидальный), до тригональной (дитригонально-скаленоэдрический). Слои слабоволнистые, почти плоские, состоят из шестиугольных слоёв атомов углерода. Кристаллы пластинчатые, чешуйчатые. Образует листоватые и округлые радиально-лучистые агрегаты, реже — агрегаты концентрически-зонального строения. У крупнокристаллических выделений часто треугольная штриховка на плоскостях (0001).
Содержание
[убрать]
|
[править] Свойства
Хорошо проводит электрический ток. В отличие от алмаза обладает низкой твёрдостью (1—2 по шкале Мооса). Плотность 2,08—2,23 г/см³. Цвет тёмно-серый, блеск металлический. Неплавкий, устойчив при нагревании в отсутствие воздуха. В кислотах не растворяется. Жирный (скользкий) на ощупь. Природный графит содержит 10—12 % примесей глин и окислов железа. При трении расслаивается на отдельные чешуйки (это свойство используется в карандашах).
Электрическая проводимость монокристаллов графита анизотропна, в направлении, параллельном базисной плоскости, близка к металлической, в перпендикулярном - в сотни раз меньше. Минимальное значение проводимости наблюдается в интервале 300-1300 К, причем положение минимума смещается в область низких температур для совершенных кристаллических структур. Наивысшую электрическую проводимость имеет рекристаллизованный графит.
Коэффициент теплового расширения графита до 700 К отрицателен в направлении базисных плоскостей (графит сжимается при нагревании), его абсолютное значение с повышением температуры уменьшается. Выше 700 К коэффициент теплового расширения становится положительным. В направлении, перпендикулярном базисным плоскостям, коэффициент теплового расширения положителен, практически не зависит от температуры и более чем в 20 раз выше среднего абсолютного значения для базисных плоскостей.
Монокристаллы графита диамагнитны, магнитная восприимчивость незначительна в базисной плоскости и велика в ортогональных базисным плоскостях. Коэффициента Холла меняется с положительного на отрицательный при 2400 К.
[править] Химические свойства
Со многими веществами (щелочными металлами, солями) образует соединения включения.
Реагирует при высокой температуре с воздухом сгорая до углекислого газа. Фторированием в контролируемых условиях можно получить (CF)x.
[править] Структура
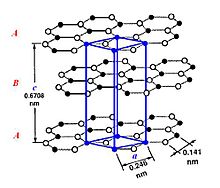

α-графит
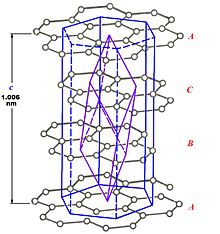

β-графит
Каждый атом углерода ковалентно связан с тремя другими окружающими его атомами углерода.
Различают две модификации графита: α-графит (гексагональный P63/mmc) и β-графит (ромбоэдрический R(-3)m). Различаются упаковкой слоёв. У α-графита половина атомов каждого слоя располагается над и под центрами шестиугольника (укладка …АВАВАВА…), а у β-графита каждый четвёртый слой повторяет первый. Ромбоэдрический графит удобно представлять в гексагональных осях, чтоб показать его слоистую структуру.
β-графит в чистом виде не наблюдается, так как является метастабильной фазой. Однако, в природных графитах содержание ромбоэдрической фазы может достигать 30 %. При температуре 2500-3300 К ромбоэдрический графит полностью переходит в гексагональный.
[править] Условия нахождения в природе
Сопутствующие минералы: пирит, гранаты, шпинель. Образуется при высокой температуре в вулканических и магматических горных породах, в пегматитах и скарнах. Встречается в кварцевых жилах с вольфрамитом и др. минералами в среднетемпературных гидротермальных полиметаллических месторождениях. Широко распространён в метаморфических породах — кристаллических сланцах, гнейсах, мраморах. Крупные залежи образуются в результате пиролиза каменного угля под воздействием траппов на каменноугольные отложения (Тунгусский бассейн). Акцессорный минерал метеоритов. С помощью ионной масс-спектрометрии российским учёным удалось обнаружить в составе графита золото, серебро и платиноиды (платина, палладий, иридий, осмий и проч.)в форме металлоорганических нанокластеров.
[править] Искусственный синтез
Искусственный графит получают разными способами:
[править] Переработка

| Этот раздел статьи следует викифицировать. Пожалуйста, оформите его согласно правилам оформления статей. |

| В этом разделе не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка стоит на статье с 12 мая 2011 |
Переработкой графита, получают различные марки графита и изделия из них.
Товарные сорта графита получают обогащением графитовых руд. В зависимости от степени очистки графитовые концентраты классифицируют на промышленные марки по областям применения, каждая из которых выдвигает специфические требования к физико-химическим и технологическим свойствам графитов.
В свете последних открытий российских учёных появилась перспектива получения из графитовых руд золота и платиноидов.
[править] Переработка графита в терморасширенный графит
На первом этапе исходный кристаллический графит окисляют. Окисление сводится к внедрению молекул и ионов серной или азотной кислоты в присутствии окислителя (перекись водорода, перманганат калия и др.) между слоями кристаллической решетки графита. Окисленный графит отмывают и сушат. Затем окисленный графит подвергают термообработке до Т=1000 °C со скоростью 400-600 °C/с. Благодаря чрезвычайно высокой скорости нагрева происходит резкое выделение газообразных продуктов разложения внедренной серной кислоты из кристаллической решетки графита. В результате межслойное расстояние увеличивается примерно в 300 раз, а число маленьких частиц графита и объём пробы увеличивается в 60-400 раз. В полученном материале остается некоторое количество оксидов серы или азота в зависимости от применяемой технологии. Далее полученный терморасширенный графит прокатывают, иногда армируют, добавляют присадки и прессуют для получения изделий.
[править] Переработка графита для получения различных марок искусственного графита
Для производства искусственного графита используют в основном нефтяной кокс как наполнитель и каменноугольный пек как связующее. Для конструкционных марок графита в качестве добавок к наполнителю применяют природный графит и сажу. Взамен каменноугольного пека как связующего или пропитывающего вещества используют некоторые синтетические смолы, например, фурановые или фенольные.
Производство искусственного графита складывается из следующих основных технологических этапов:
Кокс дробят до величин кусков 30-40 мм, затем прокаливают в специальных прокалочных печах при 1300 °C. При прокаливании достигается термическая стабильность кокса, уменьшается содержание в нем летучих веществ, увеличиваются его плотность, электро — и теплопроводность. После прокаливания кокс размалывают до необходимой крупности. Порошки кокса дозируют и смешивают с пеком в смесильных машинах при 90-130 °C.
В смесильную машину вначале загружают сухие компоненты, а затем добавляют жидкий пек. После смешивания массу равномерно охлаждают до температуры прессования (80-100 °C). Заготовки прессуют или методом выдавливания массы через мундштук, или в пресс-форме. При прессовании холодных порошков изменяют технологию подготовки помола и смешения.
Для карбонизации связующего и скрепления отдельных зёрен в монолитный материал заготовки обжигают в многокамерных газовых печах при температуре 800—1200 °C. Продолжительность цикла обжига (нагрев и охлаждение) составляет 3-5 недель в зависимости от размера и плотности заготовок. Графитация — окончательная термическая обработка — превращает углеродный материал в графит. Графитацию проводят в печах сопротивления Ачесона или в печах прямого нагрева Кастнера при температурах 2400-3000 °C. При графитировании углеродистых нефтяных заготовок идет процесс укрупнения кристаллов углерода. Из мелкокристаллического «амфорного» углерода получается крупнокристаллический графит, атомная решетка которого ничем не отличается от атомной решетки природного графита.
Некоторые изменения технологического процесса получения искусственного графита зависят от требуемых свойств конечного материала. Так, для получения более плотного материала углеродные заготовки пропитывают (после обжига) в автоклавах один или несколько раз пеком с последующим обжигом после каждой пропитки и графитацией в конце всего технологического процесса. Для получения особо чистых материалов графитацию проводят одно<
|
|
|

История развития пистолетов-пулеметов: Предпосылкой для возникновения пистолетов-пулеметов послужила давняя тенденция тяготения винтовок...

Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим...

Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни...

Особенности сооружения опор в сложных условиях: Сооружение ВЛ в районах с суровыми климатическими и тяжелыми геологическими условиями...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!