Механизм процесса гомополимеризации пропилена достаточно сложен и еще не до конца изучен.
Механизм гомополимеризации пропилена
Истинный механизм реакции роста и фактор, определяющий образование стереорегулярного полимера, многие годы были предметом широких дискуссий. Среди обсуждавшихся механизмов полимеризации наибольшее признание получили так называемые биметталлический механизм Натта и монометаллический механизм Косси.
Механизм Косси, по-видимому, наиболее признанный в настоящее время. Однако здесь будут представлены оба механизма.
Натта предположил следующий механизм полимеризации. При смешении катализатора и сокатализатора происходит хемосорбция алкилатов алюминия на твердой поверхности хлоридов титана, в результате образуется координационный мостичный комплекс, имеющий дефицит электронов со следующей структурой:

Этот комплекс теперь уже является активным центром. Молекула мономера притягивается к Ti—С-связи (С атом из алкильной группировки R) активного центра и образует π-комплекс с ионом Ti:

C-связь между R и Ti открывается, в результате возрастает дефицит электронов Ti и образуется карбанион на R:

Ион Ti притягивает π-электроны мономера и образует с ним σ – связь, противоион притягивает к себе углеродный атом с меньшей электронной плотностью. Таким образом, мономер внедряется в переходный комплекс замкнутой структуры:
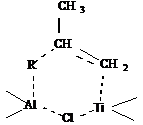
Это переходное состояние начинает рост цепи по связи металл-углерод, регенерируя исходный активный центр:

Повторив всю цепочку событий со второй присоединяющейся молекулой мономера, можно представить структуру роста цепи двух звеньев:

В дальнейшем повторяется внедрение следующих мономерных звеньев в этот переходный комплекс с одинаковой ориентацией заместителя в мономере в сторону от иона металла, что и приводит к эффекту стереорегулирования.
Монометаллический механизм, предложенный Косси, предполагает в отличие от механизма Натта, что активным компонентом катализатора является только группировка Ti—R, а функция алюминиевого компонента сводится только к алкилированию TiCl3. При смешении катализатора и сокатализатора алюминий хемосорбируется на поверхности твердого TiCl3. На поверхности катализатора у иона Ti пять координационных связей занято атомами С1, кроме того, ион Ti имеет еще одну вакантную d-орбиталь в положении (6) в соответствии со схемой:

Атомы Cl в позициях (1) и (2) связаны также с другими ионами Ti в кристаллической решетке TiCl3 и, за исключением С1, в позиции (5), который способен к обмену с алкильной группой, все остальные четыре С1 не склонны к такому обмену. Вслед за стадией хемосорбции алюминийорганического соединения на поверхности кристалла TiCl3 ион Ti3+ алкилируется путем обмена в соответствии со схемой:

Согласно этой схеме образуется активный каталитический центр октаэдрической структуры, в котором четыре атома С1 расположены в узлах кристаллической решетки, этильный радикал связан с Ti σ-связью, кроме того, ион Ti имеет еще одну вакантную орбиталь в положении, где первоначально находился пятый атом С1. После образования активного центра катализатора молекулы мономера могут занимать вакантную d-орбиталь, связываясь в переходный π-комплекс с Ti:

переходное состояние
Этот переходный комплекс быстро перестраивается, приводя к началу роста полимерной цепи за счет внедрения мономера по связи Ti—Et. Одновременно с внедрением мономерного звена и ростом цепи происходит регенерация вакантной d-орбитали либо в исходном положении, либо в положении, где первоначально находился Et-радикал:

В первом случае, т.е. при постоянной регенерации вакантной d-орбитали в исходном положении, мономерное звено внедряется в переходный комплекс в одном и том же пространственном расположении, что приводит в конечном счете к изотактической конфигурации полимерной цепи. Во втором случае, т.е. при регулярном изменении расположения вакантной d-орбитали, присоединяющееся мономерное звено чередует способ подхода к активному центру. Это приводит к образованию синдиотактическогополимера. Способ регенерации вакантной орбитали зависит от ряда факторов, и в первую очередь от невалентных взаимодействий между заместителями X подходящего к активному центру мономерного звена и последнего звена, уже вошедшего в полимерную цепь, а также этого заместителя с атомами Сl активного центра.
Ряд других факторов, таких, как тип каталитической системы, структура кристаллической решетки, мольное отношение компонентов катализатора, температура реакции, влияют на способность миграции вакантной d-орбитали и, следовательно, на стереорегулярность образующегося полимера.
Реакция полимеризации пропилена с использованием каталитической системы четвертого поколения CDi может быть описана путем ее разделения на четыре основных этапа:
1. Активация: Сокатализатор (ТЭА) вступает в реакцию с TiCl4 на поверхности катализатора на подложке и снижает степень окисления Ti с (+4) до (+3), активируя, таким образом, Ti для полимеризации. Между триэтилалюминием и активным центром происходит реакция алкилирования с образованием связи Ti-C.
2. Инициирование: молекула пропилена встраивается в связь Ti-C на активном центре, формируя, таким образом, начало полипропиленовой цепи.
3. Рост цепи: молекулы пропилена успешно встраиваются в активный центр, полимерная цепь начинает расти наружу (т.е. разрастаться) с поверхности частицы катализатора. Такое встраивание в связь Ti-C может осуществляться двумя путями:
 Ti-CH2-CH(CH3)-P (1,2 или первичное встраивание)
Ti-CH2-CH(CH3)-P (1,2 или первичное встраивание)
Ti-P + CH2=CH-CH3
 Ti-CH(CH3)-CH2-P (2,1 или вторичное встраивание)
Ti-CH(CH3)-CH2-P (2,1 или вторичное встраивание)
где Ti и P обозначают активный центр металла и полимерную цепь, соответственно.
Если вслед за одним первичным встраиванием (1,2) происходит другое первичное встраивание (1,2), то соединение молекул осуществляется по принципу «голова к хвосту». Если вслед за первичным встраиванием (1,2) происходит вторичное встраивание (2,1), то соединение молекул осуществляется по принципу «хвост к хвосту». Если вслед за вторичным встраиванием (2,1) происходит первичное встраивание (1,2), то соединение молекул осуществляется по принципу «голова к голове».
При обрыве полимерной цепи под действием водорода после первичного (1,2) или вторичного (2,1) встраивания образуются соответственно изопропиловая и н-бутиловая концевые группы:
 Ti-CH2-CH(CH3)-CH2-CH(CH3)-P + H2 Ti-H + CH3-CH(CH3)-CH2-CH(CH3)-P
Ti-CH2-CH(CH3)-CH2-CH(CH3)-P + H2 Ti-H + CH3-CH(CH3)-CH2-CH(CH3)-P
(изопропиловая концевая группа)
 Ti-CH(CH3)-CH2-CH2-CH(CH3)-P + H2 Ti-H + CH3(CH2)3-CH(CH3)-P
Ti-CH(CH3)-CH2-CH2-CH(CH3)-P + H2 Ti-H + CH3(CH2)3-CH(CH3)-P
(н-бутиловая концевая группа)
Если вслед за вторичным встраиванием (2,1) дальнейший рост происходит за счет первичного встраивания (1,2), то образующаяся полимерная цепь разрастается по принципу «голова к голове».
Поскольку случаи встраивания по принципам «голова к голове» и «хвост к хвосту» настолько редки, что практически не фиксируются методами ИК- или ЯМР-спектроскопии, и при этом н-бутиловые концевые группы наблюдаются достаточно часто, можно сделать вывод, что случайное вторичное (2,1) встраивание возможно, но такое нестандартное расположение препятствует дальнейшему встраиванию мономерных звеньев.
4. Обрыв цепи: Ниже приведены наиболее значимые реакции обрыва полимерной цепи при производстве полипропилена с применением катализаторов на подложке MgCl2:
a. передача цепи с помощью мономера:
 Ti-CH2-CH(CH3)-P + CH2=CH-CH3 Ti-CH2-CH2-CH3 + CH2=C(CH3)-P
Ti-CH2-CH(CH3)-P + CH2=CH-CH3 Ti-CH2-CH2-CH3 + CH2=C(CH3)-P
b. передача цепи с помощью сокатализатора:
 Ti-CH2-CH(CH3)-P + AlR3 Ti-R + R2Al-CH2-CH(CH3)-P
Ti-CH2-CH(CH3)-P + AlR3 Ti-R + R2Al-CH2-CH(CH3)-P
с. передача цепи с помощью водорода:
 Ti-CH2-CH(CH3)-P + H2 Ti-H + CH3-CH(CH3)-P
Ti-CH2-CH(CH3)-P + H2 Ti-H + CH3-CH(CH3)-P
Молекула водорода самостоятельно встраивается в активный центр и обрывает цепь за счет образования на ее конце метильной группы («—CH3»).
Из всех трех вышеуказанных реакций передача цепи с помощью водорода является наиболее эффективным процессом обрыва полимерной цепи. Реакция «a» важна только при отсутствии водорода и при протекании полимеризации в обычных условиях. Передача цепи с помощью алкилалюминиевого сокатализатора играет вторичную роль.
Таким образом, водород используется для контроля молекулярной массы полимера. Увеличение концентрации водорода приводит к повышению скорости реакции обрыва полимерной цепи, вследствие чего образуются более короткие полимерные цепи, имеющие меньшую молекулярную массу. Аналогичным образом, снижение концентрации водорода ведет к снижению скорости реакции обрыва полимерной цепи, вследствие чего образуются более длинные полимерные цепи, имеющие большую молекулярную массу.
Обрыв полимерной цепи может также происходить вследствие протекания реакций с каталитическими ядами; в этом случае активный центр необратимо деактивируется и не участвует в дельнейшей полимеризации.






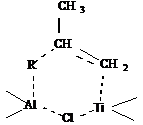






 Ti-CH2-CH(CH3)-P (1,2 или первичное встраивание)
Ti-CH2-CH(CH3)-P (1,2 или первичное встраивание) Ti-CH(CH3)-CH2-P (2,1 или вторичное встраивание)
Ti-CH(CH3)-CH2-P (2,1 или вторичное встраивание) Ti-CH2-CH(CH3)-CH2-CH(CH3)-P + H2 Ti-H + CH3-CH(CH3)-CH2-CH(CH3)-P
Ti-CH2-CH(CH3)-CH2-CH(CH3)-P + H2 Ti-H + CH3-CH(CH3)-CH2-CH(CH3)-P Ti-CH2-CH(CH3)-P + AlR3 Ti-R + R2Al-CH2-CH(CH3)-P
Ti-CH2-CH(CH3)-P + AlR3 Ti-R + R2Al-CH2-CH(CH3)-P Ti-CH2-CH(CH3)-P + H2 Ti-H + CH3-CH(CH3)-P
Ti-CH2-CH(CH3)-P + H2 Ti-H + CH3-CH(CH3)-P

