Гомогенные процессы
Гомогенными называются процессы, осуществляемые в объеме какой-либо фазы (жидкой или газовой).
Гомогенные процессы в газовой фазе особенно характерны для органической технологии. В ряде случаев они реализуются испарением органических веществ с последующей обработкой паров газообразными реагентами - хлором, кислородом, диоксидом серы, оксидами азота; соответственно происходят химические реакции хлорирования, окисления, сульфирования, нитрования и т. д. Часто применяют парофазный пиролиз, т. е. нагревание паров органических веществ без доступа воздуха с целью получения новых продуктов; при пиролизе происходит расщепление сложных молекул с образованием свободных радикалов, предельных и непредельных углеводородов, которые вступают в реакции полимеризации, конденсации, изомеризации и др. Пиролиз жидких и газообразных веществ называется также крекингом. Примером промышленных газофазных процессов может служить термическое и фотохимическое хлорирование углеводородов для получения органических растворителей, ядохимикатов и других продуктов органического синтеза.
Парофазный пиролиз углеводородов - метана (природного газа), нефтепродуктов, каменноугольной смолы - происходит по радикально-цепному механизму. Вначале молекулы расщепляются, образуя, свободные радикалы, которые затем продолжают цепь, заимствуя атомы водорода и образуя новые радикалы. Заданный состав продуктов реакции можно получить, изменяя температуру и время пребывания продуктов расщепления в реакционной зоне. В технологии неорганических веществ газофазные гомогенные процессы осуществляются, например, в производстве серной,
азотной и соляной кислот. Так, в парах сжигают серу в печах камерного типа для получения диоксида серы; получают оксид азота из воздуха в условиях низкотемпературной плазмы (103 — 105 К) по реакции
 кДж
кДж
В низкотемпературной плазме осуществляется также электрокрекинг углеводородов, например метана с целью получения ацетилена, синтез озона из кислорода и др.
В производстве азотной кислоты в газовой фазе идет окисление оксида азота в диоксид по суммарному уравнению
 кДж
кДж
В газовой фазе идет синтез хлороводорода из водорода и хлора в производстве соляной кислоты по экзотермической реакции
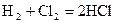
Гомогенные процессы в жидкой фазе применяют в промышленности чаще, чем газофазные. Скорость химических реакций в жидкой фазе, как правило, в тысячи раз выше, чем в газах (при той же температуре), но скорость диффузии в жидкостях значительно меньше, чем в газах, вследствие высокой вязкости жидкости. Коэффициент диффузии в газах составляет 0,1- 1 см2/с, а в жидкостях  см2/с.
см2/с.
К гомогенным процессам в жидкой фазе относятся, например, реакции нейтрализации и обменного разложения в технологии минеральных солей. В жидкой фазе осуществляют ряд процессов в технологии органических веществ: получение простых и сложных эфиров, полимеризация в растворах и расплавах, щелочное плавление бензолсульфокислот в производстве фенола, отдельные стадии сернокислотной гидратации этилена в производстве этилового |спирта и др.
В гомогенных средах (газовой и жидкой) - многие процессы идут по цепному механизму: окисление, полимеризация и пиролиз углеводородов, галогенирование углеводородов, синтез хлороводорода из элементов и др.
На скорость гомогенных процессов в газовой и жидкой фазах влияют концентрации реагирующих компонентов, давление, температура и перемешивание.
Подавляющее большинство реакций протекает в несколько стадий. Скорость всей реакции обычно лимитируется скоростью самой медленной стадией, которая и определяет порядок реакции. Поэтому, как правило, порядок реакции не совпадает с ее молекулярностью, т. е. суммой числа молекул, вступающих во взаимодействие стехиометрии суммарного уравнения реакции.
Гомогенные процессы
Гомогенными называются процессы, осуществляемые в объеме какой-либо фазы (жидкой или газовой).
Гомогенные процессы в газовой фазе особенно характерны для органической технологии. В ряде случаев они реализуются испарением органических веществ с последующей обработкой паров газообразными реагентами - хлором, кислородом, диоксидом серы, оксидами азота; соответственно происходят химические реакции хлорирования, окисления, сульфирования, нитрования и т. д. Часто применяют парофазный пиролиз, т. е. нагревание паров органических веществ без доступа воздуха с целью получения новых продуктов; при пиролизе происходит расщепление сложных молекул с образованием свободных радикалов, предельных и непредельных углеводородов, которые вступают в реакции полимеризации, конденсации, изомеризации и др. Пиролиз жидких и газообразных веществ называется также крекингом. Примером промышленных газофазных процессов может служить термическое и фотохимическое хлорирование углеводородов для получения органических растворителей, ядохимикатов и других продуктов органического синтеза.
Парофазный пиролиз углеводородов - метана (природного газа), нефтепродуктов, каменноугольной смолы - происходит по радикально-цепному механизму. Вначале молекулы расщепляются, образуя, свободные радикалы, которые затем продолжают цепь, заимствуя атомы водорода и образуя новые радикалы. Заданный состав продуктов реакции можно получить, изменяя температуру и время пребывания продуктов расщепления в реакционной зоне. В технологии неорганических веществ газофазные гомогенные процессы осуществляются, например, в производстве серной,
азотной и соляной кислот. Так, в парах сжигают серу в печах камерного типа для получения диоксида серы; получают оксид азота из воздуха в условиях низкотемпературной плазмы (103 — 105 К) по реакции
 кДж
кДж
В низкотемпературной плазме осуществляется также электрокрекинг углеводородов, например метана с целью получения ацетилена, синтез озона из кислорода и др.
В производстве азотной кислоты в газовой фазе идет окисление оксида азота в диоксид по суммарному уравнению
 кДж
кДж
В газовой фазе идет синтез хлороводорода из водорода и хлора в производстве соляной кислоты по экзотермической реакции
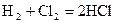
Гомогенные процессы в жидкой фазе применяют в промышленности чаще, чем газофазные. Скорость химических реакций в жидкой фазе, как правило, в тысячи раз выше, чем в газах (при той же температуре), но скорость диффузии в жидкостях значительно меньше, чем в газах, вследствие высокой вязкости жидкости. Коэффициент диффузии в газах составляет 0,1- 1 см2/с, а в жидкостях  см2/с.
см2/с.
К гомогенным процессам в жидкой фазе относятся, например, реакции нейтрализации и обменного разложения в технологии минеральных солей. В жидкой фазе осуществляют ряд процессов в технологии органических веществ: получение простых и сложных эфиров, полимеризация в растворах и расплавах, щелочное плавление бензолсульфокислот в производстве фенола, отдельные стадии сернокислотной гидратации этилена в производстве этилового |спирта и др.
В гомогенных средах (газовой и жидкой) - многие процессы идут по цепному механизму: окисление, полимеризация и пиролиз углеводородов, галогенирование углеводородов, синтез хлороводорода из элементов и др.
На скорость гомогенных процессов в газовой и жидкой фазах влияют концентрации реагирующих компонентов, давление, температура и перемешивание.
Подавляющее большинство реакций протекает в несколько стадий. Скорость всей реакции обычно лимитируется скоростью самой медленной стадией, которая и определяет порядок реакции. Поэтому, как правило, порядок реакции не совпадает с ее молекулярностью, т. е. суммой числа молекул, вступающих во взаимодействие стехиометрии суммарного уравнения реакции.
Факторы, влияющие на протекание гомогенных процессов
Влияние концентрации реагирующих веществ. С увеличением концентрации реагирующих веществ скорость гомогенной реакции увеличивается.
Влияние давления. Повышение давления ускоряет газовые реакции, так как с ростом давления увеличиваются концентрации компонентов. Всегда благоприятно применение давления для процессов, протекающих с уменьшением газового объема, так как согласно принципу Ле Шателье, повышение давления вызывает увеличение выхода продукта.
Влияние температуры. Повышение температуры вызывает ускорение гомогенных реакций в соответствии с уравнением Аррениуса.
Влияние перемешивания. Перемешивание имеет наибольшее значение для жидкостных процессов, поскольку скорости диффузии в жидкостях в десятки и сотни раз меньше, чем в газах. Перемешивание растворов позволяет сильно увеличить общую скорость процесса за счет снятия диффузионных торможений. Перемешивание жидкости наиболее часто проводится в резервуарах с механическими и пневматическими мешалками.
Для газовых реакций перемешивание необходимо для начального смешения компонентов и для выравнивания концентраций и температур в ходе процесса. начальное смешение осуществляется при помощи разнообразных форсунок или сопл, через которые подводятся газы. с таким расчетом, чтобы они смешались в общем турбулентном потоке.



 кДж
кДж кДж
кДж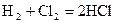
 см2/с.
см2/с.

