1) 2 гр. ксилемы заливаем 100 гр. 1% оксалата аммония.
2) Эту колбу с смесью кипятим на водяной бане 60 минут при 970С, при этом колба закрыта.
3) Охлаждаем колбу.
4) Эту смесь центрифугируем 10 мин на 4000 об/мин и сливаем надосадочную жидкость.
5) Еще раз заливаем 1% оксалатом аммония нашу смесь и кипятим на водяной бане 30 мин., также центрифугируем.
6) Вымываем оксалат аммония водой: заливаем дисцилированную воду в центрифужные стаканчики тщательно перемешиваем и центрифугируем на 4000 об/мин.
7) Так еще три раза. Проверяем рН универсальной лакмусовой бумажкой.
8) Готовим раствор 4Н КОН и 3% борной кислоты: 44,888 гр. КОН и 6 гр. Н3ВО3 на 200 мл. дисцилированной воды.
9) Заливаем 100 мл раствора к ксилеме и отстаиваем 1 час, затем центрифугируем и выливаем надосадочную жидкость.
10) Промываем водой: заливаем дисцилированную воду в центрифужные стаканчики тщательно перемешиваем и центрифугируем на 4000 об/мин. промываем до тех пор пока рН среды не будет нейтральным.
Растворение целлюлозы
Получение раствора хлорида лития в N, N – диметилацетамиде
1) N, N-диметилацетамид (ДМА) сушили над молекулярными ситами 4А.
2) В колбу присыпали 8 гр. хлорида лития и нагревали в термостате до 1800 в течение 4–5 часов, затем охлаждали и приливали 100 мл. высушенного над молекулярным ситом ДМА.
3) Колбу закрывали стеклянной пробкой и раствор перемешивали на шейкере до растворения хлорида лития (оставляли на ночь).
Выделение прочно связанных полисахаридов из растворенной целлюлозы клеточной стенки ксилемы льна
1) 1 гр. «целлюлозы» суспензировали в 10 мл. воды 40–60 мин.
2) Отделяли на воронке Шота со вставленным нейлоновым фильтром.
3) Осадок промывали на фильтре ацетоном.
4) Выдерживали в ацетоне (10 мл., 60 мин.)
5) Осадок промывали на фильтре ДМА
6) Выдерживали в ДМА (10 мл., 40–60 мин.)
7) Оставляли на ночь в свежей порции ДМА
8) На воронке шота отделяли «целлюлозу»
9) Суспензировали ее в 100 мл раствора хлорида лития в N, N – диметилацетамиде.
10) Колбу закрывали стеклянной пробкой и перемешивали до растворения целлюлозы на шейкере (1–2 дня).
11) Раствор целлюлозы по каплям добавляли к 100 мл. дисцилированной воды при перемешивание на магнитной мешалке. Раствор оставляли на ночь.
12) Отделяли выпавшую целлюлозу на воронке Шота с нейлоновым фильтром и промывали ее два – три раза дисцилированной водой (по 50 мл.) Получили Фильтрат 1
13) Фильтрат 1 Заливали в диалезный мешок 12 – 14 тысяч Дальтон.
14) Диалезный мешок клали в 3-х литровую банк с дисцилированной водой и ставили на магнитную мешалку, воду в банке меняли 4 раза.
15) На роторном испарителе концентрировали раствор.
16) Хроматографируем концентрированный раствор. Готовим 40 пробирок, моем их хромкой и сушим в сушильном шкафу при 1200С.
17) На хроматографе задаем программу (по каплям, 40 пробирок, в одну пробирку 40 капель ≈ 1,8 мл.)
18) В эпиндорф вливаем концентрированный раствор и центрифугируем 5 мин. при 6 000 об/мин.
19) Хроматографирование на Sepharose CL-4B элюент 0,02% NaN3 и АсNa 10 mM pH 5,5, разделение по молекулярным массам.
20) Определяем количество сахаров методом Дюбуа (фенольным методом). 200 мкл образца+200 мкл 5% раствора фенола, помещаем пробирки в холодную воду и добавляем 1 мл. концентрированной серной кислоты. Кипятим на водяной бане 10 минут и охлаждаем. Измеряем оптическую плотность при 490 нм. (Смотри гафик1)
21) Выпавшую целлюлозу суспензировали в 50 мл 0,01 М растворе NaAc, рН 4,5 + 0,05% NaN3, содержавший 0,1 мл раствора целлюлазы и инкубировали в течение ночи.
22) Раствор фильтровали на воронке Шота и осадок заново суспезировали в новой порции раствора фермента. Мы получили фильтрат 2.
23) Фильтрат 2 обессоливали на колонке Sephadex G-25, элюент 0,02% NaN3. 0,005 гр. Blue Dextran 2000 кД и 0,250 гр. СоCl2 растворяли в 5 мл дисцилированной воды и хроматографируем. Blue Dextran 2000 кД начало 25 мл конец 30 мл. СоCl2 начало 60 мл. конец 73 мл.
24) Хроматографирование на Sepharose CL-4B элюент 0,02% NaN3 и АсNa 10 mM pH 5,5, разделение по молекулярным массам.
25) Определяем количество сахаров методом Дюбуа (фенольным методом). 200 мкл образца+200 мкл 5% раствора фенола, помещаем пробирки в холодную воду и добавляем 1 мл. концентрированной серной кислоты. Кипятим на водяной бане 10 минут и охлаждаем. Измеряем оптическую плотность при 490 нм (Смотри график2).
Моносахаридный анализ
1) Фильтрат 1 и Фильтрат 2 обессоливаем на колонке Sepharose G250, элюент 10мМ пиридин и 10мМ уксусная кислота рН 4,5.
2) Высушиваем при 600С до полного отсутствия воды.
3) Добавляем 400 мл ТФУ (Трифторуксусная кислота), помещаем в сушильный шкаф на 1 час при температуре 1200С.
4) Затем опять сушим при 600С
5) Растворяем водой и определяем моносахаридный соcтав на Daionex (Данные моносахаридного состава смотри в таблице 1).
6) Мы объединили наши пробирки в следующие фракции до целлюлазной обработки: фракция 1 5–10; фракция 2 11–16; фракция 3 17–23; фракция 4 24–26; фракция 5 27–35.
Фракции после целлюлазной обработки: фракция 1 6–10; фракция 2 11–16; фракция 3 17–19; фракция 4 20–24; фракция 5 25–26; фракция 6 27–31.
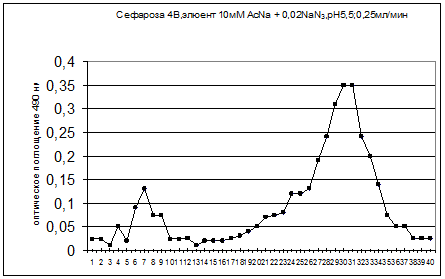
Рисунок 1 – Распределение прочносвязанных полисахаридов во фракциях после растворения целлюлозы до ферментативной обработки.

Рисунок 2 – Распределение прочносвязанных полисахаридов после растворения после ферментативной обработки
Таблица 1. Моносахаридный состав во фракциях
|
| Рамноза
| Арабиноза
| Галактоза
| Глюкоза
| Ксилоза
| Галактуроновая кислота
| Глюкуроновая кислота
|
| Фракция 1, после целлюлазы
| 49.290
| 33.680
| 68.173
| 7.624
| 5.855
| 254.246
| 1.166
|
| Фракция 2, после целлюлазы
| 61.981
| 43.261
| 99.500
| 6.804
| 13.317
| 311.360
| 3.365
|
| Фракция 3, после целлюлазы
| 25.478
| 17.145
| 79.425
| 6.605
| 31.317
| 161.033
| 10.089
|
| Фракция 4, после целлюлазы
| 6.349
| 7.295
| 48.161
| 25.828
| 86.452
| 67.533
| 10.577
|
| Фракция 5, после целлюлазы
| 4.020
| 14.716
| 40.078
| 40.401
| 210.336
| 3.171
| 5.546
|
| Фракция 6, после целлюлазы
| 1.678
| 4.407
| 13.217
| 28.017
| 136.191
| 6.781
| 1.291
|
| Фракция 1, до целлюлазы
| 0
| 0
| 0
| 0
| 0.535
| 358.507
| 0
|
| Фракция 2, до целлюлазы
| 0.556
| 0.481
| 2.689
| 5.364
| 1.107
| 0.476
| 0
|
| Фракция 3, до целлюлазы
| 12.596
| 15.664
| 39.576
| 12.444
| 0
| 21.317
| 1.393
|
| Фракция 4, до целлюлазы
| 20.762
| 24.131
| 54.572
| 11.218
| 54.753
| 67.032
| 2.955
|
| Фракция 5, до целлюлазы
| 82.195
| 151.536
| 325.976
| 131.493
| 0
| 426.007
| 19.982
|
Результаты и их обсуждение
При подготовке ксилемы в первую очередь надо было остановить все процессы происходящие в ней поэтому фиксировали ее. Обработка ксилемы включала два основных этапов. Первое – механическое растирание на мельнице для того что бы получит муку, так как так лучше будет удаляться не прочно связанные вещества с целлюлозой и лучше растворяться. Второе – экстракция пектина и гемицеллюлозы с хелатирующими и щёлочными растворами.
Удаление пектиновых веществ с мы осуществили с помощью оксалата аммония, как известно пектиновые вещества связаны между собой ионами Са, а оксалат аммония является хелатирующим веществом которое связывается с ионами Са и пектиновые вещества отделяются от целлюлозы. Для удаление оксалата аммония и пектиновых веществ из нашей колбы мы центрифугируем их 3 раза с водой.
Обработка клеточной стенки ксилемы льна 4% NaOH позволяла извлекать гемицеллюлозные вещества, которые не извлекаются оксалатом аммония, нужен более сильный раствор. Мы применяли 4% NaOH который высвобождает целлюлозу от гемицеллюлозных веществ. Затем мы снова удаляли щелочь и гемицеллюлозные вещества с помощью метода центрифугирования при этом проверяли рН универсальной лакмусовой бумажкой, промывали до нейтрального.
Выдерживание в воде «отчищенной» ксилемы необходимо для так называемой активации, без этого этапа целлюлоза не растворяется. Выдерживание в ацетоне и ДМА необходимо для полного удаления воды, так как при наличие воды целлюлоза выподает в осадок. Клеточную стенку волокна растворяли в» 8% растворе LiCl в ДМА, и заново осаждали целлюлозу путём добавления воды. Осаждение в воде необходимо для того что бы фермент полностью расщепил целлюлозу, если опустить этот этап то целлюлоза плохо будет подвергаться гидролизу. 8% раствор LiCl в ДМА мы используем так как они вместе являются хорошими растворителями целлюлозы и не реагируют с ней, к тому от них легко избавиться с помощью хроматографии. Раствор отделяли от целлюлозы (Фильтрат 1). Целлюлозу суспензировали в содержащем целлюлазу ацетатном буфере. В течение 1–2 суток фермент растворял осаждённую целлюлозу (Фильтрат 2). Мы получили раствор прочно связанных полисахаридов с целлюлозой. Далее с помощью ТФУ мы разрушаем все гликозидные связи и при высушивание весь ТФУ испаряется, и остаются мономеры сахаров. Dionex эта ионно-обменная хроматография, на ней мы и определяем моносахаридный состав, заранее вкалываются стандарты моносахоров по которым мы и опознаем конкретный моносахар.
В дальнейшем планируется провести ЯМР анализ и определить тип связующих гликанов.
Выводы
1. Отчистили клеточную стенку от пектиновых и гемицеллюлозных веществ.
2. Получили раствор прочносвязанных с целлюлозой полисахаридов.
3. Разделили фракции по молекулярным массам.
4. Определили моносахаридный состав во фракциях.
Литература
1. Керне, А. Жизнь растений. / А. Керне // СПб.: Просвещение, – 1906. – Т. 2. – 838 с.
2. Полевой, В.В. Физиология растений. / В.В. Полевой // М.: Высшая школа, – 1989. – 464 с.
3. Brett, C.T. Cellulose microfibrils in plants: biosynthesis, deposition, and integration into the cell wall / C.T. Brett // Int. Rev. Cytol. – 2000. – V. 199. – P. 61–99.
4. Chivasa, S., Proteomic analysis of the Arabidopsis thaliana cell wall / S. Chivasa, B.K. Ndimba, W.J. Simon, D. Robertson, X.L. Yu, J.P. Knox, P. Bolwell, A.R. Slabas // Electrophoresis. – 2002. – V. 23. – P. 1754–1765.
5. Cosgrove, D.J. Group I allergens of grass pollen as cell wall-loosening agents / D.J. Cosgrove, P.A. Bedinger, D.M. Durachko // Proc. Natl. Acad. Sci. USA. – 1997. – V. 94. – P. 6559–6564.
6. Delmer, D. Cellulose biosynthesis: exciting times for a difficult field of study / D. Delmer // Plant Physiol. Plant Mol. Biol. – 1999. – V. 50. – P. 245–276.
7. DeWitt, G. Comparative compositional analysis of walls with two different morphologies: archetypical versus transfer-cell-like / G. DeWitt, J. Richards, D. Mohnen, A.M. Jones / Protoplasma. – 1999. – V. 209. – №3/4. – P. 238–245.
8. Frey-Wissling, A. Submicroscopic morphology of protoplasm and its derivatives. / A. Frey-Wissling. // N.Y.: Elsevier. – 1948. – 47 p.
9. Fry, S.C. The growing plant cell wall: chemical and metabolic analysis. / S.C. Fry // London: Longman Sci. and Technic. – 1988. – 333 p.
10. Fry, S.C., Xyloglucan endotransglucosylase, a new wall-loosening enzyme activity from plants / S.C. Fry, R.C. Smith, K.F. Renwick, D.J. Martin, S.K. Hodge, K.J. Matthews // Biochem. J. – 1992. – V. 282. – P. 821–828.
11. Gaspar, T., Peroxidases 1970–1980: A survey of their biochemical and physiologic roles in higher plants. / T. Gaspar, C. Penel, T. Thorpe, H. Greppin. // Switzerland: University of Geneva Press. – 1982. – P. 60–121.
12. Gaspar, Y., The complex structures of arabinogalactan-proteins and the journey towards understanding function / Y. Gaspar, K.L. Johnson, J.A. McKenna, A. Bacic, C.J. Schultz // Plant Mol. Biol. – 2001. – V. 47. – P. 161–176.
13. Jarvis, M.C. Control of thickness of collenchyma cell walls by pectins / M.C. Jarvis // Planta. – 1992. – V. 187. – P. 218–220.
14. Jose-Estaniol, M., Plant cell wall glycoproteins and their genes / M. Jose-Estaniol, P. Puigdomenech // Plant Physiol. Biochem. – 2000. – V. 38. – №1/2. – P. 97–108.
15. Lamport, D.T.A. The protein component of primary cell walls / D.T.A. Lamport // Adv. Bot. Res. – 1965. – V. 2. – P. 151–218.
16. Lamport, D.T.A., The use of tissue cultures for the study of plant cell walls / D.T.A. Lamport, D.H. Northcote // Biochem. J. – 1960. – V. 76. – P. 52.
17. Mohnen, D. Biosynthesis of pectins and galactomannans / D. Mohnen // Comprehensive Natural Products Chemistry / Eds Pinto B.M., Barton D.H.R., Meth-Cohn O. Oxford: Elsevier. – 1999. – P. 497–527.
18. Mohnen, D. Biosynthesis of pectins and galactomannans / D. Mohnen // Comprehensive Natural Products Chemistry / Eds Pinto B.M., Barton D.H.R., Meth-Cohn O. Oxford: Elsevier. – 1999. – P. 497–527.
19. Nishitani, K., Endo-xyloglucan transferase, a novel class of glycosyltransferase that catalyzes transfer of a segment of xyloglucan molecule to another xyloglucan molecule / K. Nishitani, R. Tominaga // J. of Biol. Chem. – 1992. – V. 267. – P. 21058–21064.
20. Saxena, I.M., Cellulose biosynthesis: current views and evolving concepts / I.M. Saxena, R.M. Brown // Ann. Bot. – 2005. – V. 96. – №1. – P. 9–21.
21. Schroder, R., Mannan transglycosylase: a novel enzyme activity in cell walls of higher plants / R. Schroder, T.F. Wegrzyn, K.M. Bolitho, R.J. Redgwell // Planta. – 2004. – V. 219. – P. 590–600.
22. Schroder, R., LeMAN4 endo-beta-mannanase from ripe tomato fruit can act as a mannan transglycosylase or hydrolase / R. Schroder, T.F. Wegrzyn, N.N. Sharma, R.G. Atkinson // Planta. – 2006. – V. 224. – P. 1091–1102.








