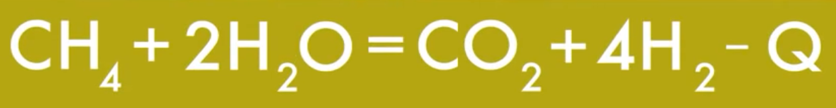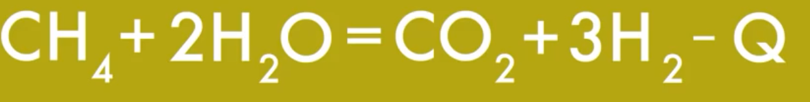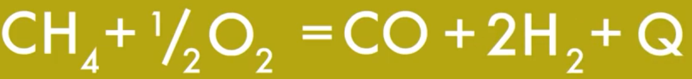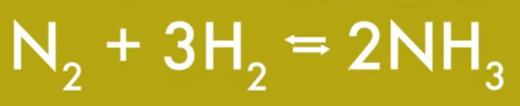(конусная дробилка, шаровая мельница, высокочастотный грохот, вращающиеся валки)
Экстракция – физико-химический процесс разделения веществ (преим. жидких) с помощью избирательных (селективных) растворителей.
Раствор/смесь в-ва + экстрагент = экстракт + раствор в-ва + рафинат
2) Основная химия (N, P, K-удобрения и производство H2SO4)
Можно делать моноудобрения (проще, но менее эффективные) или комплексные (гомогенизированные или гранулированные — снаружи K «всхожесть», посередине N «урожайность», ядрышком является P «за качество».)
3) Химия органического синтеза (каучук, шины, пластмассы, синт. волокна)
Калийные удобрения
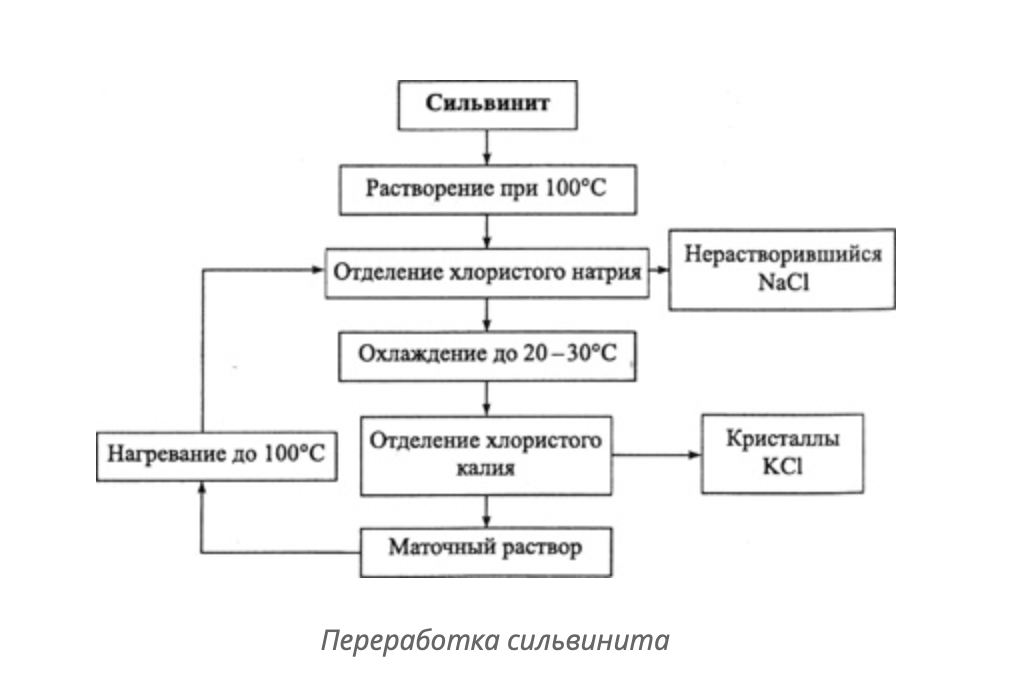
Есть 2 способа получения калия из калийных солей (сильвинита: NaCl + KCl):
· Галургия (растворимы при разной температуре: поэтому растворяем KCl, таким образом NaCl остается в осадке, от него избавляемся фильтрацией; при охлаждении хлористый калий кристаллизуется из маточного раствора)
Щёлок — водный настой древесной золы, состоящий в растворе в основном из карбонатов калия (поташ) и натрия (сода). Обладает сильнощелочной реакцией.
· Флотация (берем флотационный реагент, который смачивает KCl и не смачивает NaCl)
Азотные удобрения
К аммиачным удобрениям относятся: жидкий аммиак (82% N), аммиачная вода (20–22% N), сульфат аммония (21% N), хлорид аммония (26% азота).
Нитратными удобрениями являются: нитрат натрия (16% N), нитрат калия (14% N), нитрат кальция (16% N).
Аммиачно-нитратные удобрения – нитрат аммония (34% N); амидные удобрения – цианамид кальция (35% N, технический продукт 19–22% N); мочевина, или карбамид (47% N).
Наряду с указанными азотными удобрениями применяются смешанные удобрения, также содержащие азот (аммофосы, нитрофоска).
Аммиачная селитра (нитрат аммония) NH4NO3 — безбалластное удобрение в аммиачной и нитратной форме, содержащее около 35% азота. Этапы производства аммиачной селитры:
1) Нейтрализация слабой азотной кислоты (50–55%) газообразным аммиаком (в нейтрализатор непрерывно подводится аммиак и через разбрызгиватель подается азотная кислота):
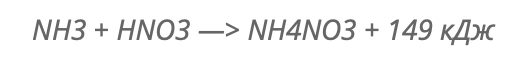
2) Выпаривание воды в вакуум-выпарном аппарате доводим концентрацию раствора аммиачной селитры с 70–80 % до 98–99 %.
3) Гранулирование через сепаратор: плав селитры разбрызгивается вращающимся диском, капли застывают, попадая в ток холодного воздуха, образуются гранулы.
4) Сушка и упаковка.
Карбамид. Реакция Базарова. Превращение раствора карбамида в гранулы происходит за счёт охлаждения восходящим воздушным потоком за время падения со 100 м до 7 м (от 137°С до 50°С)
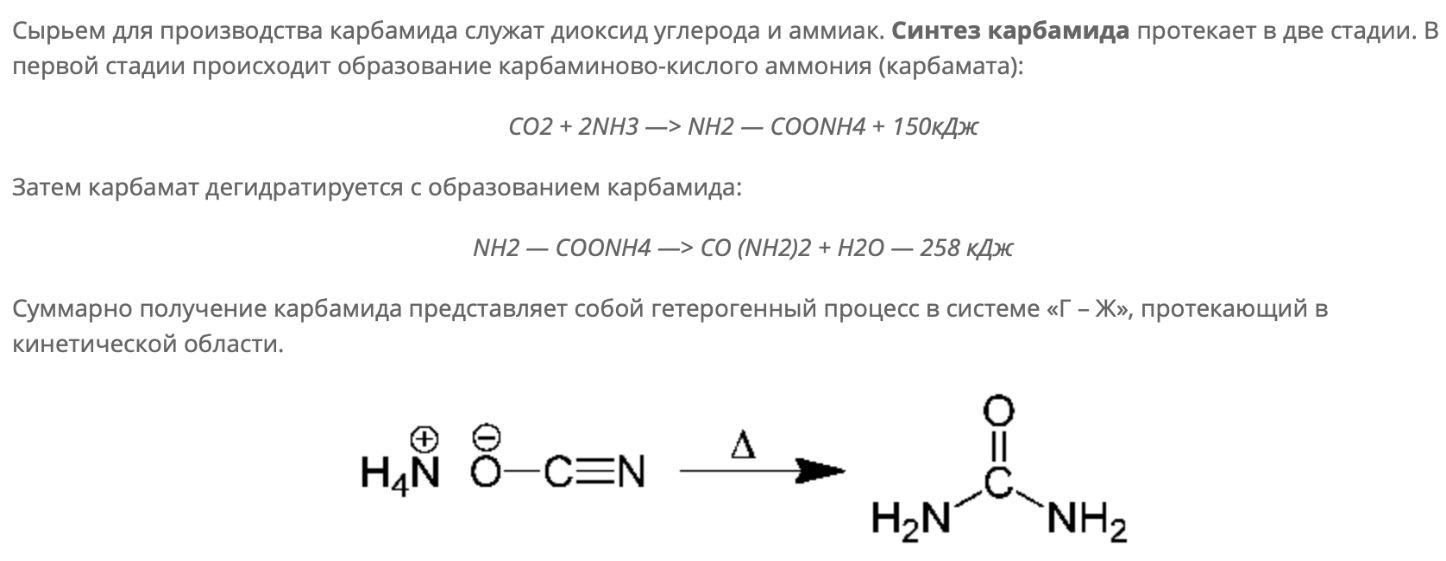
Производство аммиака
Аммиак — бесцветный газ, хорошо растворимый в воде.
Подготовка реагентов (природный газ, вода, воздух). В печь первичного риформинга поступает смесь природного газа и паров воды, где частично превращается в смесь водорода, угарного и углекислого газа (здесь оксид никеля — в роли катализатора):
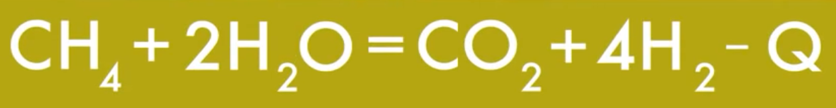
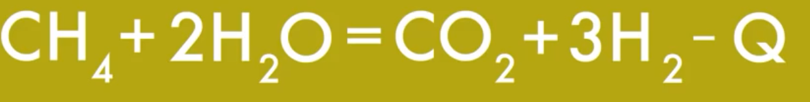
В печи первичного риформинга (огромная камера сгорания) протекает единственный эндотермический процесс: снизу подаётся воздух, с боков по трубам идет природный газ, температура внутри печи —> 1000°С; реакционная смесь вместе с катализатором циркулирует по трубам внутри камеры сгорания, получает тепло от стенок (т. к. важно обогревать равномерно). На выходе получаем: H2, CO2, CO и непрореагировавший CH4 под температурой 800°С.
Смесь поступает в реактор вторичного риформинга, куда также подается воздух (берется необходимое количество азота N), там остатки метана реагируют с кислородом…
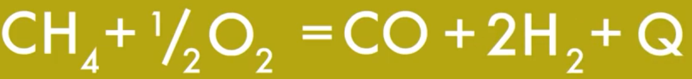
… но часть всё равно сгорает до паров воды, от которых потом придётся избавляться, теперь смесь газа содержит в основном азот, водород, оксиды углерода и пары воды (от двух последних необходимо избавиться, а то они потом будут реагировать с аммиаком и мешать синтезу либо травить катализатор)

Смесь последовательно проходит через 2 конвектора, где угарный газ, реагируя с водой, образует углекислый газ и необходимый нам водород. Содержание угарного газа упало с 15 % до 0,3 %.

Теперь в блоке поглощения CO2 избавимся от всего углекислого газа с помощью абсорберов. Раствор метилдиэтаноламина (основание) реагирует с CO2 под давлением, образуя карбонат. Далее в стрипинг-колонне давление сбрасывается и карбонат распадается на исходные продукты: метилдиэтаноламин возвращается в блок поглощения, а углекислый газ улавливают и передают на производство мочевины. Всё же доли угарного и углекислого газа остаются в смеси и после очистки, окончательно от них избавляются в метанаторе => образуется метан и воду. В итоге в КСА поступают азот, водород, метан, аргон и немного водяных паров.


Сердце всего производства — колонна синтеза аммиака, в которой N2 взаимодействует с Н2 под давлением 157 атм. И температурой 436°С:
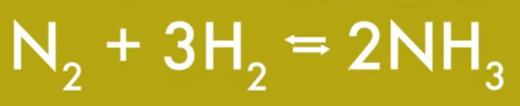
Реакция синтеза аммиака обратима, чтоб сместить равновесие вправо, надо либо увеличить давление, либо понизить температуру, но при понижении температуры замедляется скорость протекания реакции => используют катализатор (мелкораздробленное железо, чтоб была большая площадь соприкосновения). Чтобы нагнать столь большое давление используют трёхступенчатый компрессор на паровой турбине (электричество слишком дорого).
При выходе из колонны синтеза газ охлаждают до 0°С, часть его сжижается и отделяется в сепараторе, а непрореагировавший газ с остатками аммиака возвращается в колонну. Первичный аммиак очищают путем нескольких процедур сжижения—сжатия и поступает в изотермическое хранилище («огромный термос»).
Фосфорные удобрения
• Ca3(PO4)2 – фосфоритная мука (<20% P2O5)
• Ca(H2PO4)2+2CaSO4 – суперфосфат простой (ок. 20% P2O5)
Технологическая схема производства суперфосфата складывается из следующих операций:
1. измельчение природных фосфатов,
2. дозировка серной кислоты и природных фосфатов,
3. смешивание реагентов в смесителе с получением пульпы,
4. схватывание и затвердевание суперфосфатной массы в реакционной камере,
5. дозревание суперфосфата на складе.
• CaHPO4*2H2O – преципитат (27–31% P2O5)
Производство преципитата СаНРO4—2Н20 заключается в нейтрализации фосфорной кислоты известняком, а затем известковым молоком. Образовавшийся осадок преципитата отфильтровывают от раствора и сушат.
• Ca(HPO4)2 *2H2O – суперфосфат двойной (45% P2O5)
Простой и двойной суперфосфат производят путем разложения природных фосфатов кислотами (серной, азотной, фосфорной, реже соляной). Суть производства – перевод нерастворимых, плохо усваиваемых соединений в растворимые, разложение природных фосфатов путем спекания или сплавления их при высокой температуре с солями натрия, калия, магния