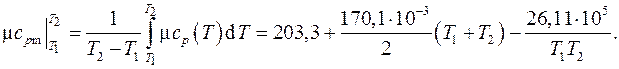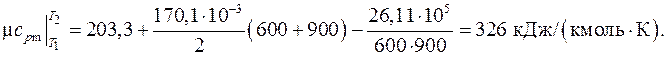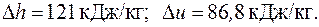Идеального газа
Удельной теплоемкостью называется количество теплоты Q, которое необходимо сообщить единице количества вещества, чтобы изменить его температуру на один градус. В зависимости от способа измерения количества вещества различают:
– удельную массовую теплоемкость, Дж/(кг∙К):
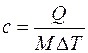 , (3.1)
, (3.1)
где М, кг – масса вещества;
– удельную объемную теплоемкость, Дж/(м3∙К):
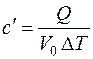 , (3.2)
, (3.2)
где V 0, м3 – объем вещества при нормальных физических условиях (см. разд.1);
– удельную мольную теплоемкость, Дж/(кмоль∙К):
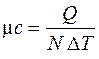 , (3.3)
, (3.3)
где N, кмоль – количество киломолей вещества.
Различные виды удельных теплоемкостей связаны между собой простыми соотношениями:
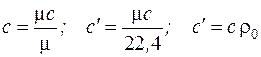 , (3.4)
, (3.4)
где 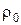 , кг/м3 – плотность газа при н.ф.у;
, кг/м3 – плотность газа при н.ф.у;
μ, кг/кмоль – молекулярная масса газа.
В зависимости от характера термодинамического процесса подвода тепла различают теплоемкости при постоянном объеме сv и при постоянном давлении сp, связанные между собой формулой Майера
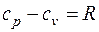 , (3.5)
, (3.5)
где R, Дж/(кг ∙К) – газовая постоянная.
По классической (молекулярно-кинетической) теории теплоемкость газов не зависит от температуры, а определяется только количеством атомов в молекуле (числом степеней свободы молекулы f): 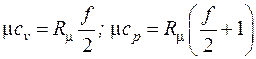 . Определенные таким образом мольные теплоемкости газов приводятся в табл. 3.1, массовые и объемные теплоемкости рассчитываются по выражениям (3.4). Полученные значения хорошо совпадают с экспериментальными данными в области комнатных температур.
. Определенные таким образом мольные теплоемкости газов приводятся в табл. 3.1, массовые и объемные теплоемкости рассчитываются по выражениям (3.4). Полученные значения хорошо совпадают с экспериментальными данными в области комнатных температур.
Отношение теплоемкостей
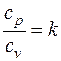 (3.6)
(3.6)
называется показателем адиабаты, который для идеального газа также зависит только от количества атомов в молекуле (табл. 3.1).
Таблица 3.1
Значения мольных теплоемкостей газов по классической теории
| Вид газа
| Число степеней свободы
| Показатель адиабаты
| Мольные теплоемкости, кДж/(кмоль∙К)
|
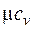
| 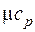
|
| 1-атомный
| 3
| 1,67
| 12,47
| 20,79
|
| 2-атомный
| 5
| 1,40
| 20,79
| 29,10
|
| 3-х и более атомный
| 6
| 1,33
| 24,94
| 33,26
|
Эксперимент показывает, что теплоемкости газов заметно изменяются с температурой. Истинной теплоемкостью газа при данной температуре является величина 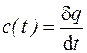 . Тогда средняя теплоемкость газа в интервале температур (
. Тогда средняя теплоемкость газа в интервале температур (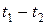 ) находится по формуле
) находится по формуле
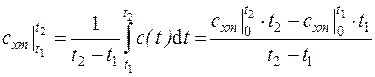 , (3.7)
, (3.7)
где 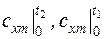 – средние теплоемкости в интервалах температур
– средние теплоемкости в интервалах температур 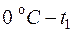 ,
, 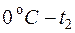 соответственно (берутся из таблиц – см. прил.1);
соответственно (берутся из таблиц – см. прил.1);
индекс x – обозначает характер процесса (p = const или v = const).
Средние массовая и объемная теплоемкости смеси газов находятся как
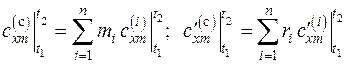 , (3.8)
, (3.8)
где 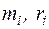 – соответственно массовые и объемные доли компонентов смеси.
– соответственно массовые и объемные доли компонентов смеси.
Внутренняя энергия термодинамической системы U, Дж – это энергия, связанная с различными формами движения и взаимодействия ее структурных частиц (кинетическая энергия движения молекул, потенциальная энергия взаимодействия молекул и др.). Удельная внутренняя энергия – это энергия, отнесенная к единице массы системы 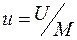 , Дж/кг.
, Дж/кг.
Внутренняя энергия является однозначной функцией состояния системы, т. е. зависит только от параметров термодинамической системы, например 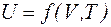 .
.
Для идеального газа внутренняя энергия зависит только от температуры и находится как:
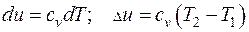 . (3.9)
. (3.9)
Энтальпия – это энергия расширенной термодинамической системы, включающей в себя саму систему и окружающую среду (оболочку, удерживающую систему в заданном объеме). Энтальпия H, Дж, и удельная энтальпия 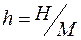 , Дж/кг, определяются как:
, Дж/кг, определяются как:
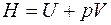 ; (3.10)
; (3.10)
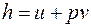 . (3.11)
. (3.11)
Энтальпия является однозначной функцией состояния системы, т. е. зависит только от параметров термодинамической системы, например 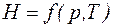 .
.
Энтальпия идеального газа зависит только от температуры:
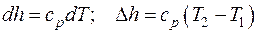 . (3.12)
. (3.12)
В формулах (3.9), (3.12) теплоемкости газа при постоянном давлении ср и при постоянном объеме сv определяются либо методами молекулярно-кинетической теории по табл. 3.1, либо как средние теплоемкости в интервале температур от Т 1 до Т 2 по уравнению (3.7).
Задачи
3.1. Найти среднюю удельную теплоемкость cp азота в интервале температур от 1000 оС до 2000 оС, если известно, что 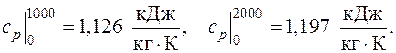
Решение
Средняя теплоемкость в интервале температур от t 1 до t 2 вычисляется согласно формуле (3.7):
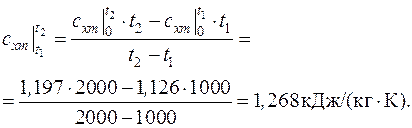
3.2. Найти объемную и массовую теплоемкости кислорода при постоянном объеме и постоянном давлении с использованием молекулярно-кинетической теории газов.
Решение
Согласно табл. 3.1 мольные теплоемкости двухатомных газов:
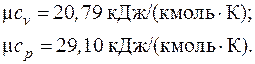
Тогда значения объемных и массовыхтеплоемкостей для кислорода с учетом (3.4):
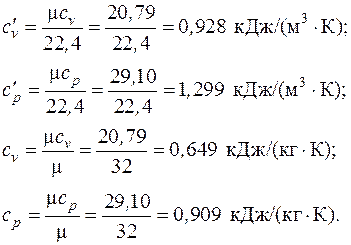
3.3. Определить теплоту, необходимую для нагрева смеси газов массой 5 кг при постоянном давлении от температуры 40 оС до температуры 800 оС, если смесь газов имеет следующий массовый состав:. 20 % – азот N2; 80 % – углекислый газ CO2. При расчетах:
а) учесть зависимость теплоемкости от температуры;
б) теплоемкости cv и cp вычислить методами молекулярно- кинетической теории.
Сравнить полученные результаты, определив относительную погрешность в вычислении теплоты.
Решение
Количество теплоты для смеси идеальных газов находится по формуле
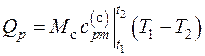 , где
, где 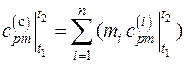 .
.
а) Найдем среднюю удельную теплоемкость каждого компонента смеси в интервале температур (40–800 оС) по формуле 3.7. Для этого необходимо определить средние теплоемкости в интервалах температур (0–40 оС) и (0–800 оС), используя таблицу прил.1.
Поскольку в таблице значения удельных теплоемкостей даются с интервалом 100 оС, теплоемкости  в интервале температур (0–40 оС) определяем путем интерполирования. Тогда:
в интервале температур (0–40 оС) определяем путем интерполирования. Тогда:
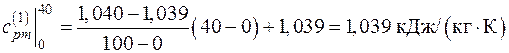 ;
;
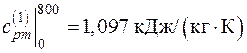 ;
;
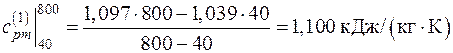 ;
;
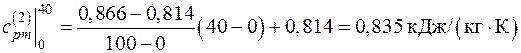 ;
;
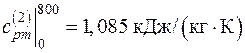 ;
;
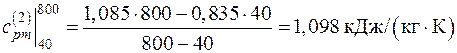 .
.
Смесь газов задана массовым составом, следовательно, массовые доли компонентов: m 1 = 0,2 (азот); m 2 = 0,8 (углекислый газ).
Тогда средняя удельная теплоемкость смеси газов при постоянном давлении в заданном интервале температур будет равна
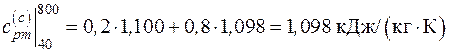 ,
,
а количество теплоты, необходимой для нагрева смеси газов,
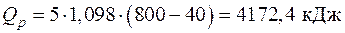 .
.
б) Для нахождения удельных массовых теплоемкостей компонентов смеси с помощью молекулярно-кинетической теории газов используем табл. 3.1. При этом учтем, что азот – двухатомный газ, а углекислый газ – трехатомный. Массовые теплоемкости:
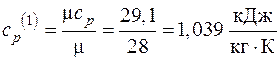 ;
;
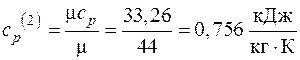 .
.
Средняя теплоемкость смеси и количество необходимой для нагрева теплоты в этом случае будут равны
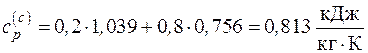 ;
;
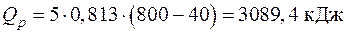 .
.
Относительная погрешность в вычислении количества теплоты
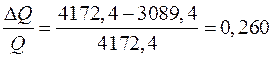 или 26 %.
или 26 %.
3.4. В объеме V1 = 200 м3 при температуре t 1 =100 оС и давлении p 1 = 3 бар находится смесь идеальных газов заданного объемного состава: 60 % – азот; 40 % – кислород.
Определить теплоту, необходимую для нагрева смеси газов при постоянном объеме до температуры 500 оС.
Ответ: 173,5 МДж.
3.5. Воздух с температурой 80 оС образуется в результате смешения при постоянном давлении двух потоков: холодного воздуха с температурой 0 оС и горячего воздуха с температурой 900 оС. Определить, сколько горячего и холодного воздуха необходимо взять для получения 1 кг смеси. При расчете теплоемкостей не учитывать их зависимость от температуры.
Ответ: 0,917 кг холодного воздуха и 0,083 кг горячего воздуха.
3.6. Определить средние массовые и объемные теплоемкости при постоянном давлении и постоянном объеме смеси газов в интервале температур от 0 до 1300 оС, если смесь имеет следующий объемный состав: 8 % – двуокись углерода СО2; 2 % – окись углерода СО; 85 % – азот N2; 5 % – водород Н2. 
Ответ:

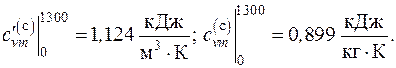
3.7. Определить количество тепла, воспринятого воздухом в регенераторе газовой турбины от смеси газов заданного состава: СО – 2,1 %; СО2 – 12,3 %; SO2 – 1,8 %; N2 – 83,8 % (по массе). Смесь газов охлаждается в регенераторе при постоянном давлении p = 1,2 бар от температуры 427 оС до 120 оС. Расход газов при начальных условиях 12500 м3/ч. КПД регенератора 0,95.
Ответ: Q = 2,36 ГДж/ч.
3.8. Определить удельный объем и массовую теплоемкость при постоянном объеме пара натрия при давлении p = 10 бар и температуре t = 927 оС, если известно, что при этих параметрах пар натрия является смесью одно- и двухатомных молекул следующего мольного состава: r Na = 0,8628, 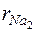 = 0,1372. Найти парциальные давления одно- и двухатомных паров натрия. Теплоемкости газов, составляющих смесь, рассчитать согласно молекулярно-кинетической теории. Молекулярная масса натрия μNa = 23 кг/кмоль.
= 0,1372. Найти парциальные давления одно- и двухатомных паров натрия. Теплоемкости газов, составляющих смесь, рассчитать согласно молекулярно-кинетической теории. Молекулярная масса натрия μNa = 23 кг/кмоль.
Ответ: v = 0,381 м3/кг; сv = 520,44 Дж/(кг×К );
p Na = 8,628 бар; 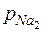 = 1,372 бар.
= 1,372 бар.
3.9. Определить мольную изобарную теплоемкость воздуха при температурах t 1 = 287 oC и t 2 = 560 oC, если известна интерполяционная формула для истинной мольной теплоемкости воздуха
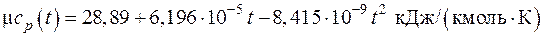
и среднюю мольную изобарную теплоемкость воздуха в интервале температур (t 1 – t 2).
Результаты сравнить с табличными данными.
Решение
Подставив значения температур t 1 = 287 oC и t 2 = 560 oC в интерполяционную формулу, получим значения истинных мольных теплоемкостей при данных температурах:
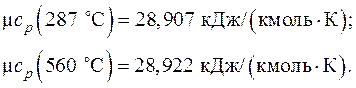
Тогда средняя мольная изобарная теплоемкость воздуха в интервале температур (t 1 – t 2) определится как
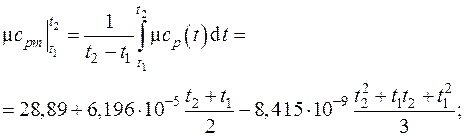
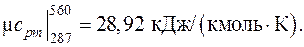
Рассчитанная с использованием таблиц прил.1 средняя теплоемкость воздуха в том же интервале температур, определяемая по формуле (3.7), оказывается равной
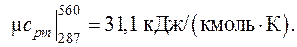
Расхождение результатов составляет 7,3 %.
3.10. Определить тепловую мощность 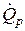 , необходимую для нагрева при постоянном давлении p = 1,2 бар смеси газов состава:
, необходимую для нагрева при постоянном давлении p = 1,2 бар смеси газов состава:
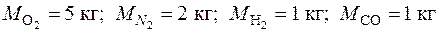
от t 1 = 325 оС до t 2 = 800 оС. Расход смеси по параметрам на входе равен 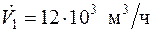 . Вычислить также массовый расход смеси.
. Вычислить также массовый расход смеси.
Ответ: 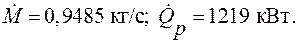
3.11. Определить истинную изобарную массовую теплоемкость кислорода при температуре t = 1000 оС, если средняя теплоемкость в интервале температур (0– t оС) задается интерполяционной формулой 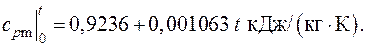
Решение
Из определения средней теплоемкости в каком-либо интервале температур (3.8) следует, что
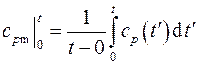
или
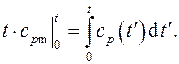

Используя правила дифференцирования определенного интеграла по переменному верхнему пределу, получаем
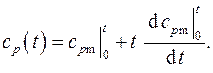
Вычисления дают:
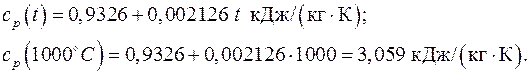
3.12. Зависимость мольной изобарной теплоемкости газообразного фосфата кальция Ca3(PO4)2 от температуры выражается уравнением
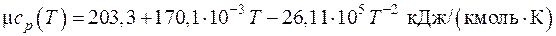 .
.
Найти значение мольной изобарной теплоемкости этого газа в интервале температур от 600 К до 900 К.
Решение
В соответствии с понятием определенного интеграла среднее значение теплоемкости в заданном интервале температур вычисляется как
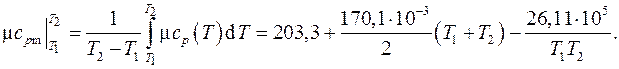
Вычисления дают
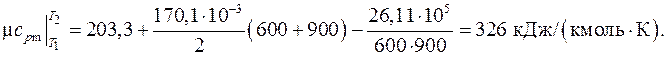
3.13. В компрессоре газовой турбины сжимается воздух. Начальная температура воздуха t 1 = 30 oC, температура после сжатия t 2 = 150 oC. Определить изменение энтальпии и внутренней энергии воздуха в процессе сжатия, учитывая зависимость теплоемкости от температуры.
Ответ: 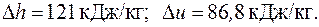



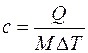 , (3.1)
, (3.1)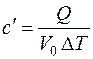 , (3.2)
, (3.2)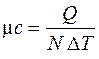 , (3.3)
, (3.3)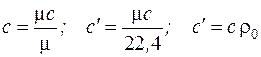 , (3.4)
, (3.4)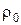 , кг/м3 – плотность газа при н.ф.у;
, кг/м3 – плотность газа при н.ф.у;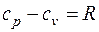 , (3.5)
, (3.5)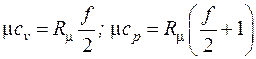 . Определенные таким образом мольные теплоемкости газов приводятся в табл. 3.1, массовые и объемные теплоемкости рассчитываются по выражениям (3.4). Полученные значения хорошо совпадают с экспериментальными данными в области комнатных температур.
. Определенные таким образом мольные теплоемкости газов приводятся в табл. 3.1, массовые и объемные теплоемкости рассчитываются по выражениям (3.4). Полученные значения хорошо совпадают с экспериментальными данными в области комнатных температур.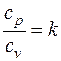 (3.6)
(3.6)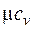
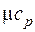
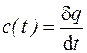 . Тогда средняя теплоемкость газа в интервале температур (
. Тогда средняя теплоемкость газа в интервале температур (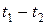 ) находится по формуле
) находится по формуле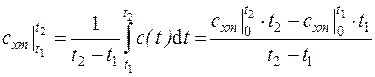 , (3.7)
, (3.7)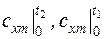 – средние теплоемкости в интервалах температур
– средние теплоемкости в интервалах температур 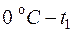 ,
, 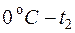 соответственно (берутся из таблиц – см. прил.1);
соответственно (берутся из таблиц – см. прил.1);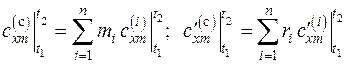 , (3.8)
, (3.8)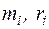 – соответственно массовые и объемные доли компонентов смеси.
– соответственно массовые и объемные доли компонентов смеси.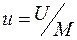 , Дж/кг.
, Дж/кг.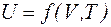 .
.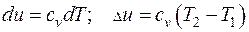 . (3.9)
. (3.9)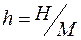 , Дж/кг, определяются как:
, Дж/кг, определяются как: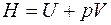 ; (3.10)
; (3.10)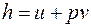 . (3.11)
. (3.11)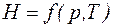 .
.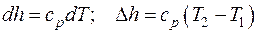 . (3.12)
. (3.12)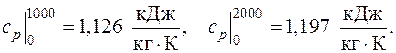
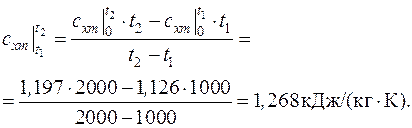
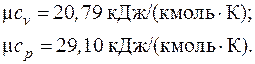
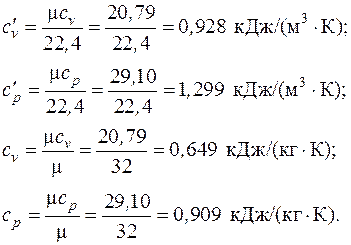
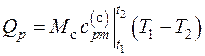 , где
, где 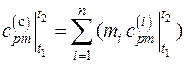 .
. в интервале температур (0–40 оС) определяем путем интерполирования. Тогда:
в интервале температур (0–40 оС) определяем путем интерполирования. Тогда: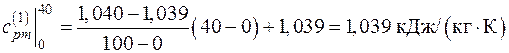 ;
;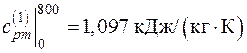 ;
;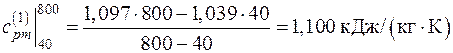 ;
;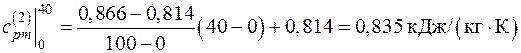 ;
;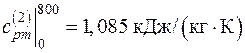 ;
;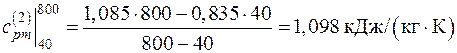 .
.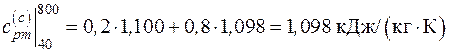 ,
,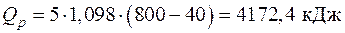 .
.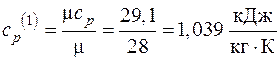 ;
;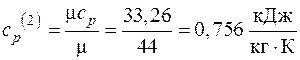 .
.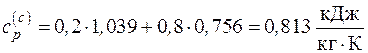 ;
;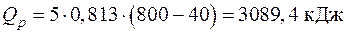 .
.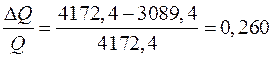 или 26 %.
или 26 %.
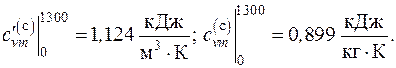
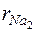 = 0,1372. Найти парциальные давления одно- и двухатомных паров натрия. Теплоемкости газов, составляющих смесь, рассчитать согласно молекулярно-кинетической теории. Молекулярная масса натрия μNa = 23 кг/кмоль.
= 0,1372. Найти парциальные давления одно- и двухатомных паров натрия. Теплоемкости газов, составляющих смесь, рассчитать согласно молекулярно-кинетической теории. Молекулярная масса натрия μNa = 23 кг/кмоль.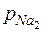 = 1,372 бар.
= 1,372 бар.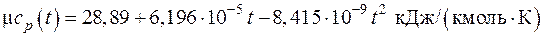
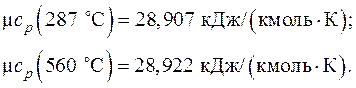
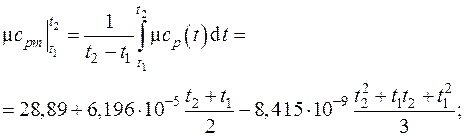
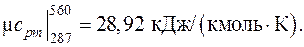
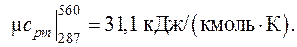
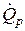 , необходимую для нагрева при постоянном давлении p = 1,2 бар смеси газов состава:
, необходимую для нагрева при постоянном давлении p = 1,2 бар смеси газов состава: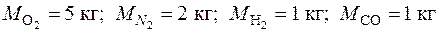
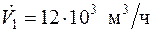 . Вычислить также массовый расход смеси.
. Вычислить также массовый расход смеси.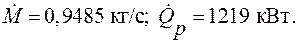
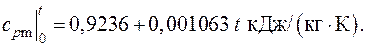
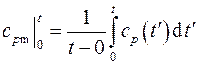
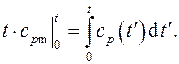

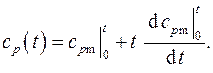
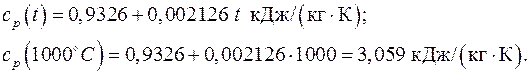
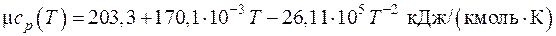 .
.