Лиотропный ряд адсорбции однозарядных катионов:
катион Cs+ Rb+ NH4+ K+ Na+ Li+
радиус, Å 1,68 1,48 1,43 1,33 0,95 0,6
Увеличение радиуса гидратированных катионов
Уменьшение адсорбции
Лиотропный ряд адсорбции однозарядных анионов:
анион NO3– I– Br– Cl– F–
радиус, Å 2,5 2,16 1,36 1,81 1,36
Увеличение радиуса гидратированных анионов
Уменьшение адсорбции
2.2.5. Ионообменная адсорбция
Адсорбенты, способные к обмену ионами, называются ионитами.
Иониты — твердые адсорбенты, нерастворимые в воде и органических растворителях, имеющие общие формулы RMx и RAy, содержащие катион M или анион А, способные к обмену с катионом M1 и анионом A1.
Иониты имеют сетчатую структуру. С сеткой ковалентно связаны группы атомов R±, несущие положительный или отрицательный заряд (фиксированные ионы). Этот заряд компенсируется противоионами (М+ или А–). Фиксированные ионы вместе с противоионами (R–M+ или R+А–) называют ионогенными группировками.
По типу ионогенных групп иониты делят на катиониты R– M+ (кислотные иониты, обменивающие катионы) и аниониты R+А– (основные иониты, обменивающие анионы).
Сильнокислотные катиониты содержат остатки серной, фосфорной и других кислот, слабокислотные — карбоксильные, сульфгидрильные группы.
Сильноосновные аниониты содержат аммониевые или сульфониевые основания, а слабоосновные — аминогруппы и остатки других органических азотистых оснований.
Ионообменные реакции:
для катионита: R–H+ + Na+ 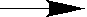 R–Na+ + H+
R–Na+ + H+
для анионита: R+OH– + Cl– 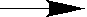 R+Cl– + OH–
R+Cl– + OH–
Активность ионитов — поглощающая способность характеризуется обменной емкостью (ОЕ) — количеством ионов (ммоль), связываемых одним граммом сухого ионита из раствора в равновесных условиях.
Иониты нашли широкое применение в медицине: как средства для регулирования водно-солевого баланса, для детоксикации при отравлениях токсичными электролитами, для предотвращения ацидозов и т. д. В хирургии, например, монокарбоксицеллюлоза используется в качестве гемостатического бактерицидного и рассасывающего средства, а также как носитель лекарственных препаратов.
Применение в фармации: умягчение жесткой, опреснение засоленной воды, для извлечения из анализируемых смесей различных компонентов.
2.2.6. Смачивание
Смачивание — это поверхностное явление, заключающееся во взаимодействии жидкости с твердым или другим жидким телом при наличии одновременного контакта этих двух несмешивающихся фаз с третьей фазой — газом (чаще всего воздухом).
Если на поверхность твердого тела нанесена капля жидкости, то в системе имеются три поверхности раздела фаз: твердое тело—газ, жидкость—газ, жидкость—твердое тело с соответствующими поверхностными натяжениями: σтг, σтж, σгж. Линия пересечения всех трех поверхностей раздела –– линия смачивания; замкнутая линия смачивания образует периметр смачивания. Угол  между поверхностями жидкость—газ и твердое тело—жидкость –– краевой угол смачивания.
между поверхностями жидкость—газ и твердое тело—жидкость –– краевой угол смачивания.
Смачивание

Несмачивание

Если рассматривать поверхностные натяжения как силы, приложенные перпендикулярно к единице длины периметра смачивания и действующие по касательной к соответствующим поверхностям, то условие равновесия этих сил выражается уравнением Юнга:
σтг = σтж + σжг cosθ или 
· если краевой угол острый (θ < 900), т. е. cosθ > 0, то поверхность смачивается жидкостью («ограниченное смачивание»);
· если краевой угол тупой (θ > 900),  т. е. cos θ < 0; то поверхность не смачивается («плохое смачивание»)
т. е. cos θ < 0; то поверхность не смачивается («плохое смачивание»)
· если равновесный краевой угол не устанавливается, капля растекается в тонкую пленку — «полное смачивание» или растекание.
Если молекулярная природа жидкости и твердого тела близки, а σ жидкости мало — смачивание и растекание (органические жидкости с малым σ смачивают твердые тела). Жидкие металлы (высокие значения σ) смачивают только поверхности твердых металлов. Вода смачивает оксиды и растекается на некоторых силикатах, но не смачивает парафин.
Характеристика явления — энтальпия смачивания:
Δ Н = Hтг –Нтж
Отношение энтальпий смачивания твердых поверхностей водой (Нв) и углеводородом (H у) — характеристика гидрофильности поверхности — коэффициент гидрофильности. Для гидрофильных поверхностей  1, для гидрофобных — β < 1. Для активированного угля β
1, для гидрофобных — β < 1. Для активированного угля β  0,4 (гидрофобная поверхность), для кварца β
0,4 (гидрофобная поверхность), для кварца β 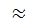 2 (гидрофильная поверхность), для крахмала β
2 (гидрофильная поверхность), для крахмала β 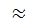 20 (сильно гидрофильная поверхность).
20 (сильно гидрофильная поверхность).



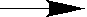 R–Na+ + H+
R–Na+ + H+ между поверхностями жидкость—газ и твердое тело—жидкость –– краевой угол смачивания.
между поверхностями жидкость—газ и твердое тело—жидкость –– краевой угол смачивания.


 т. е. cos θ < 0; то поверхность не смачивается («плохое смачивание»)
т. е. cos θ < 0; то поверхность не смачивается («плохое смачивание») 1, для гидрофобных — β < 1. Для активированного угля β
1, для гидрофобных — β < 1. Для активированного угля β  0,4 (гидрофобная поверхность), для кварца β
0,4 (гидрофобная поверхность), для кварца β 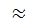 2 (гидрофильная поверхность), для крахмала β
2 (гидрофильная поверхность), для крахмала β 

