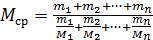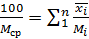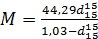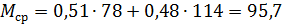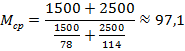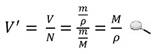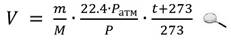Гетероатомные соединения(ГАС)–это химические соединения на основе углеводородов любой группы, содержащие один или несколько различных компонентов.
Основные гетероатомные соединения:
• Серосодержащие соединения
• Кислородосодержащие соединения
• Азотосодержащие соединения
• Металлосодержащие соединения
Содержание серы (S), кислорода (O) и азота (N) составляет:
• Сера (S) от 0,02 до 7%
• Кислород (O) от 0,05 до 3,6%
• Азот (N) до 1,7%
Общим на долю гетероатомных соединений присутствующих в нефтях приходится несколько процентов, но их нахождение нежелательно при переработке нефти, вызывает коррозию аппаратуры, отравляют дорогостоящие катализаторы, придавая товарным нефтепродуктам темный цвет и неприятный запах.
Распределение гетероатомных соединений в нефтях неравномерно. Основная их часть в тяжелых дестиллятных фракциях (ТНК=350-5000C).
Миллионная доля — единица измерения каких-либо относительных величин, равная 1·10 − 6 от базового показателя. Аналогична по смыслу проценту или промилле .
Обозначается млн − 1 [1] HYPERLINK "https://ru.wikipedia.org/wiki/%D0%9C%D0%B8%D0%BB%D0%BB%D0%B8%D0%BE%D0%BD%D0%BD%D0%B0%D1%8F_%D0%B4%D0%BE%D0%BB%D1%8F"[2] , мд [3] или сокращением ppm (от англ. parts per million, читается «пи-пи-эм» —«частей на миллион»). Английскую аббревиатуру ppm иногда путают с промилле HYPERLINK "https://ru.wikipedia.org/wiki/%D0%9C%D0%B8%D0%BB%D0%BB%D0%B8%D0%BE%D0%BD%D0%BD%D0%B0%D1%8F_%D0%B4%D0%BE%D0%BB%D1%8F"[3] и ошибочно расшифровывают как пропромилле и обозначают как «ппм».
Соотношения:
• 1 млн − 1 = 0,001 ‰ = 0,0001 % = 0,000 001 = 10 − 6 ;
• 1 % = 10 000 ppm;
• 1 ‰ = 1000 ppm.
Физико-химические свойства нефтепродуктов
Такие физико-химические показатели, как плотность, пределы выкипания, температура застывания, вязкость, дают определённую характеристику её товарных качеств. Некоторые из них входят в ГОСТы на товарные нефтепродукты, косвенно или непосредственно характеризуя их эксплуатационные свойства. Другие используются при расчёте и проектировании нефтепроводов, нефтеперерабатывающей аппаратуры и т.д.
Всякое вещество имеет свойство только ему одному присущее, по которому можно установить это вещество.
Например, если вещество, при давлении 760 мм ртутного столба кипит при 100 0C, при 0 0 C –переходит из жидкого состояния в твердое, а при 4 0C и объеме 1см3 имеет массу равную 1г, то это вещество –дистиллированная вода.
Точно также характеризуя нефти и нефтепродукты необходимо знать совокупность их физико-химических свойств, некоторых констант (const), которые используются для расчетов нефтезаводской аппаратуры, контроля производственных процессов, характеристике качества товарных нефтепродуктов и другие.
Плотность
Это один из важнейших и широко употребляемых показателей качества нефтей и нефтепродуктов.
Абсолютная плотность–масса вещества находящаяся в единице объема. В системе СИ она имеет размерность кг/м3.
В практике нефтяного дела определяют относительную плотность P (T2 к T1) - это безразмерная величина, показывающая отношение плотности нефтепродукта при температуре T2 к плотности дистиллированной воды при температуре T1.
Стандартные температуры приняты для воды - T1=40C, для нефтепродукта – T2=200C.
В ряде стран для воды и нефтепродукта стандартной является температура T1=T2=15,50C.
При определении плотности (T1=40C и T2=200C) численные значения абсолютной и относительной плотностей совпадают, поскольку плотность воды при 40C=1 (единице).
Плотность нефтепродуктов возрастает с увеличением их молекулярной массы (температуры кипения) и уменьшается для одного и того же нефтепродукта (или нефти) с повышением его температуры. Для определения плотности нефтей и нефтепродуктов при температуре t пользуются линейным законом Д.И. Меделеева по формуле:
Pt4 = P204 – a(t-20),
Где Pt4 –относительная плотность при температуре t, 0С;
P204- то же при стандартной температуре, 200С;
a –поправка на изменение плотности при изменении температуры на 10С.
Поправку используют так же при расчёте P204 в P15,515,5
P15,515,5 = P204 + 5a
Если смешение нескольких нефтепродуктов не приводит к расширению или сжатию объёма смеси по сравнению с суммой объёмов исходных компонентов, то среднюю плотность находят по правилу смешения:
Рср. =Р1 V1+ V2+…+ Рn Vn,
Где Р1, Р2, Рn –относительные плотности компонентов смеси, определённые при одной и той же температуре;
V1, V2,Vn –соответственно их объёмы при той же температуре.
Плотность жидких нефтепродуктов в заводской практике измеряют прибором, называемым ареометром (нефтеденсиметром).
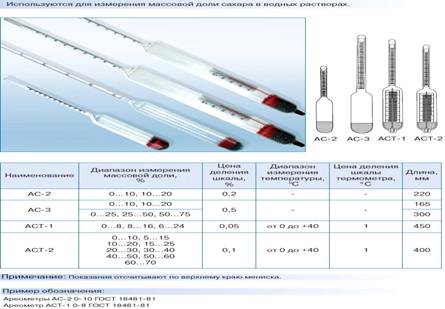
Он дает точность измерения до 0,001. Высоковязкие нефтепродукты измеряют методом разбавления керосином. Зная плотность керосина легко вычислить плотность смеси из высоковязкого нефтепродукта.
Плотность возрастает при одинаковых условиях и при равном числе атомов углерода в молекуле, в ряду: Парафины –Нафтены –Арены.
Величину обратную плотности (1/P, м3/кг) называют удельным объем и используют при расчете количества нефти и нефтепродуктов в резервуарах, при транспортировке.
На величину плотности нефти влияют много факторов. Главное из них –содержание растворённых газов и смол, фракционный, а для дистиллятов также и химический состав.
Плотность жидкостей определяют с помощью ареометров и пикнометров.
Плотность газа при стандартных условиях Pг (кг/нм3) может быть вычислена по формуле: Pг = М/22,4
Где М –молекулярная масса газа, кг/кмоль; 22,4 –объём 1 кмоля газа при стандартных условиях, нм3.
Для газообразных продуктов за стандартные условия приняты давление 0,101 МПа (760 мм.рт.ст.) и температура 273 К0 (00С)
|
Нефтепродукт
|
Плотность
|
| Бензин
| Не более 770
|
| Реактивное топливо
| Не менее 780
|
| Дизельное топливо (летнее)
| Не более 860
|
| Дизельное топливо (зимнее)
| Не более 840
|
| Мазут
| Не более 955
|
| Вакуумный газойль
| 870-950
|
| Гудрон
| 970-990
|
Характеризующий фактор
Это условный параметр, представляющий собой функцию плотности и средней молярной температуры кипения нефтепродукта (Тср.м., К), отражающий его химическую природу:
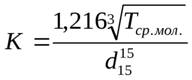
Где К - характеризующий фактор; Тср.м. –средняя малярнаятемпература кипения нефтепродукта, К; 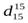 –относительная плотность воды и нефтепродукта при температуре 150С.
–относительная плотность воды и нефтепродукта при температуре 150С.
Под средней молярной температурой кипения нефтепродукта (Тср.м., К) понимают среднюю температуру между началом и концом кипения фракции.
Средние значения характеризующего фактора для некоторых нефтепродуктов:
Парафиновые нефтепродукты…………………………12,5-13,0
Нафтеноароматические………………………………...10-11
Ароматизированные…………………………………….10
Продукты крекинга………………………………………10-11
Значения характеризующего фактора применяются обычно для последующего расчёта молекулярной массы узких нефтяных фракций.
Молекулярная масса
Нефть и нефтепродукты представляют собой смеси индивидуальных углеводородов и других соединений, поэтому они характеризуются средней молекулярной массой. Средняя молекулярная масса многих нефтей 250-300 кг/кмоль. Первый представитель жидких углеводородов –пентан С5 Н12–имеет молярную массу 72кг/кмоль. У более высокомолекулярных гетероатомных соединений нефти и её высоковязких фракций масса составляет 1200 - 2000 кг/кмоль. Молекулярная масса тем больше, чем выше средняя температура кипения фракции.
Молекулярные массы фракций с одинаковыми пределами кипения, но выделенные из разных нефтей, близки между собой. Поэтому можно пользоваться экспериментальными данными по таблице:
| фракция
| Мср.
| фракция
| Мср.
| фракция
| Мср.
| фракция
| Мср.
|
| 50-100
| 90
| 200-250
| 155
| 350-400
| 250
| 500-550
| 412
|
| 100-150
| 110
| 250-300
| 187
| 400-450
| 305
| 550-600
| 480
|
| 150-200
| 130
| 300-350
| 220
| 450-500
| 350
|
|
|
Молекулярную массу можно рассчитать по формуле Б.П.Воинова:
Мср.= 60+0,3Тср.м.+0,001Т2ср.м.
Где Мср –молекулярная масса фракции; Тср.м. –средняя молекулярная температура кипения светлых нефтяных дистиллятов, определяемая экспериментально и по специальным графикам, К.
В расчетной практике молекулярную массу часто определяют по эмпирическим формулам. Наибольшее применение нашла формула Б. П. Воинова:
Мср.= 7К–21,5+(0,76-0,04К)Тср.м.+(0,00245)Т2ср.м.
Где Мср.- молекулярная масса фракции; Тср.м. –средняя молекулярная температура кипения нефтяных дистиллятов, К; К –характеризующий фактор.
| Наиболее распространенной эмпирической формулой для определения среднего значения молекулярной массы веществ, входящих в состав той или иной фракции, является зависимость Б.П. Воинова:
Мср. = а + dtср. + ct 2ср.
|
|
|
Где a, b, c - постоянные, различные для каждого класса углеводородов, tср - средняя температура кипения нефтепродуктов, определяемая по соответствующим графикам.
Например, для парафиновых углеводородов эта формула будет иметь вид:
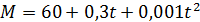
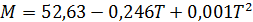
Данная формула применима и для узких бензиновых фракций.
Пример 1. Средняя температура кипения фракции 120 °С. Ее молекулярная масса равна
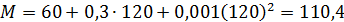
Формулу Б.М. Воинова уточнил А.С. Эйгенсон, введя характеризующий фактор K.
С введением характеризующего фактора формула принимает вид
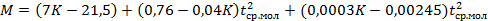
Формулой можно пользоваться для определения молекулярной массы фракций, выкипающих до 350 °С (точность ±2 ÷ 3%).
Молекулярную массу тяжелых фракций можно определить в зависимости от вязкости при 50 и 100 °С.
Пример 2. Определить молекулярную массу нефтепродукта с пределами кипения 82 – 110 °С, плотностью  Содержание узких фракций в этом продукте следующее (в мол.долях): (Hb – 90 °C) – 0,21; (90 – 95 °C) – 0,10; (95 – 100 °C) – 0,35; (100 – 105 °C) – 0,11.
Содержание узких фракций в этом продукте следующее (в мол.долях): (Hb – 90 °C) – 0,21; (90 – 95 °C) – 0,10; (95 – 100 °C) – 0,35; (100 – 105 °C) – 0,11.
Решение. Определяем среднюю температуру кипения каждой узкой фракции в °С
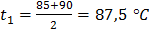
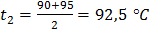
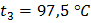

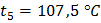
Подставляя полученные данные в формулу, получаем

Определяем значение 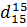


Молекулярная масса является свойством аддитивным.
Среднюю молекулярную массу смеси можно определить, зная мольную долю и молекулярную массу каждого компонента смеси:
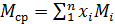
где  –содержание компонентов в смеси, мол.доли;
–содержание компонентов в смеси, мол.доли; 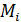 –молекулярная масса компонента смеси.
–молекулярная масса компонента смеси.
Молекулярную массу смеси нескольких нефтяных фракций можно определить по формуле
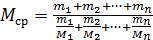
или
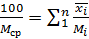
где m1, m2, … mn –масса компонентов смеси, кг; М1, М2, …, Мn –молекулярная масса компонентов смеси; - % масс.компонента.
Молекулярную массу нефтепродукта можно определить также по формуле Крэга
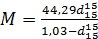
пример 3. Определить среднюю молекулярную массу смеси бензола с изооктаном, если мольная доля бензола составляет 0,51, изооктана 0,49.
Решение. Молекулярная масса бензола 78, изооктана 114. Подставляя эти значения в формулу, получаем
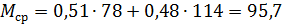
Пример 4. Смесь состоит из 1500 кг бензола и 2500 кг н-октана. Определить среднюю молекулярную массу смеси.
Решение. Используя формулу
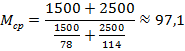
Расчет мольного объёма
В практических расчетах при определении размеров реакторов, испарительных и ректификационных колонн необходимо знать мольный объем жидких нефтепродуктов или их паров.
Мольный объем жидкостей V' (м3) вычисляют по формуле:
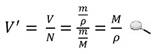
Объем паров можно определить из уравнения Клапейрона:
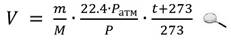




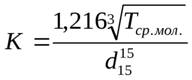
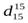 –относительная плотность воды и нефтепродукта при температуре 150С.
–относительная плотность воды и нефтепродукта при температуре 150С.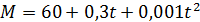
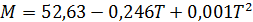
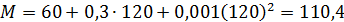
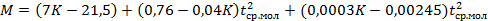
 Содержание узких фракций в этом продукте следующее (в мол.долях): (Hb – 90 °C) – 0,21; (90 – 95 °C) – 0,10; (95 – 100 °C) – 0,35; (100 – 105 °C) – 0,11.
Содержание узких фракций в этом продукте следующее (в мол.долях): (Hb – 90 °C) – 0,21; (90 – 95 °C) – 0,10; (95 – 100 °C) – 0,35; (100 – 105 °C) – 0,11.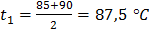
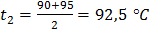
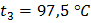

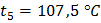

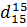


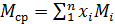
 –содержание компонентов в смеси, мол.доли;
–содержание компонентов в смеси, мол.доли; 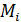 –молекулярная масса компонента смеси.
–молекулярная масса компонента смеси.