Бактерия | Бактериальный инвазин | Рецептор(ы) хозяина | Особенности
Yersinia | Инвазин | бета1-интегрин | «Зип-лайк» — фагоцитоз, инвазия опосредованная актином, но не разрушающая мембрану клетки, (активированная тирозинкиназой)
Yersinia | Yad A | бета1-интегрин | Менее эффективный чем инвазин
Yersinia | Ail |? | Инвазия неэффективна и менее специфична
L. monocytogenes | Интерналин | (Inl A) | Е-кадхерин | «Зип-лайк» — фагоцитоз, опосредованная актином, мембрана клетки не разрушается, активация тирозинкиназой
S. flexneri | Ipa-D | альфа5бета1-интегрин? | Разрушение мембраны, изменение клеточного цитоскелета без истечения кальция
S. typhimurium | SipB-D |? | «Рифление» мембраны, изменение клеточного цитоскелета, макропиноцитоз, ток кальция и некоторые другие сигналы (не ингибируемые киназными ингибиторами), формирование поверхностных отростков
Энтеропатогенная E. coli | Инвазин | Hp90 | Формирование «пьедестала» и тесная адгезия (зависимая от микротрубок и актина), опосредована тирозинкиназой
Pseudomonasaeruginosa. Возбудитель синегнойной инфекции продуцирует несколько внеклеточных белков, способствующих его инвазии и диссеминации (рис. 8).
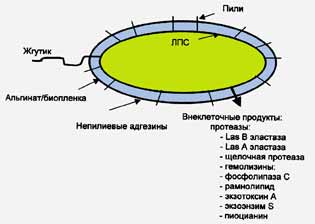
Рис. 8. Схематическое изображение факторов вирулентности Pseudomonas aeruginosa. P. aeruginosa имеет факторы вирулентности, связанные с клеткой (жгутики, пили, непилиевые адгезины, альгинат, ЛПС) и внеклеточные факторы вирулентности [Van Delden С., Iglewski В., 1998]
Прежде всего это экзотоксин А (является ADP-рибозилтрансферазой). Он способен инактивировать фактор элонгации 2 и тем самым ингибировать в клетке белковый синтез. Экзотоксин А ответственен за локальные повреждения тканей и иммуносупрессию. Экзоэнзим S также является ADP-рибозилтрансферазой, но преимущественно рибозилирут GTP-белки, такие как Ras. Он ответственен за непосредственное разрушение легочной ткани. Два гемолизина — фосфолипаза С и рамноллипид, могут действовать как синергисты при разрушении липидов и лектинов. Рамноллипид содержит детергент-подобную структуру и благодаря ей он растворяет фосфолипиды легочных тканей, делая их более доступными для разрушения фосфолипазой С. Протеазы (LasB-эластаза, LasA-эластаза и щелочная протеаза) играют основную роль во время острой фазы инфекции. Роль щелочной протеазы в инвазии P. aeruginosa, неизвестна. LasA-эластаза является сериновой протеазой и действует как синергист LasB-протеазы (цинк металлопротеаза) при деградации эластина легочной ткани. LasB-эластаза деградирует не только эластин, но и фибрин и коллаген, а также инактивирует человеческие иммуноглобулины G и А, компоненты комплемента и лизоцим, находящийся в воздушных путях, т. е., LasB-эластаза еще и препятствует действию механизмов защиты хозяина [Van Delden С, Iglewski В., 1998]. Система регуляции генов патогенности P. aeruginosa показана на рис. 9.
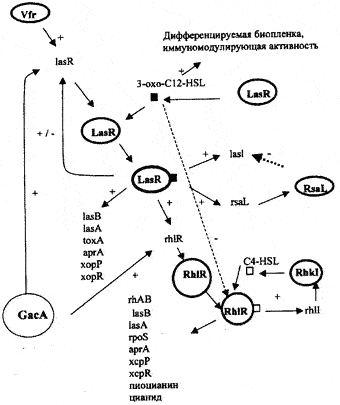
Рис. 9. Схематическое изображение регуляции генов патогенности Pseudomonas aeruginosa. Система сигналов las, передаваемых от «клетки к клетке», в иерархическом каскаде контролируется посредством сигнальной системы белка rhi Комплекс LasR/-3-oxo-C12-HSL активирует транскрипцию rhlR. 3-охо-12HSL блокирует активацию RhlR посредством C4-HSL. Сама las-система контролируется позитивно — посредством Vfr и GacA, и негативно — посредством RsaL. 3-oxo-C12-HSL требуется для дифференциации биопленки и обладает иммуномодуляторной активностью. Обе сигнальные системы регулируют экспрессию различных генов (lasB — LasB-эластаза; lasA — LasA-эластаза; toxA — экзотоксин А; аргА — щелочная протеаза хсрР и xcpR — гены хср-секреторного пути; rhlАВ — рамнозилтрансфераза, требуемая для продукции рамноллипида; rpoS — сигма-фактор стационарной фазы [Van Delden С, Iglewski В., 1998]
Shigella flexneri — возбудитель дизентерии у людей. Посредством эндоцитоза, через лимфатические фолликулы пейферовых бляшек тонкого кишечника, шигеллы проникают в слизистую оболочку ободочной кишки (рис. 10). Продуктами генов, которые инициируют процесс инвазии, являются три белка: IpaB (плазмидный антиген инвазии — 62 кд), IpaD (38 кд), IpaC (42 кд). В lamina prdpria они инфицируют макрофаги и вызывают запрограммированную гибель клеток. Цитокины высвобождаются и индуцируют воспаление. Вследствие притока полиморфно-ядерных фагоцитов разрушается базальная мембрана и разрывается эпителий. Клетки, теперь уже лишенные щеточной каемки, становятся уязвимыми и не защищенными от индуцируемого плазмидой проникновения шигелл. Детерминантой апоптической гибели макрофагов является белок IpaB. В течение короткого времени после проникновения шигелл в клетки, вакуоли лизируются под действием IpaB. Высвободившись, бактерии быстро размножаются внутри цитоплазмы. Шигеллы неподвижны и лишены жгутиков, но они перемещаются внутри клетки и распространяются от одной клетки к другой. Это обусловлено образованием у них «хвоста» из полимеризованного актина хозяина под влиянием гена ics (гена внутриклеточного распространения), который кодирует 120 кд белок. Перенос шигелл осуществляется через выступы на поверхности одной клетки, которые вставлены в инвагинации соседней клетки. Затем части, содержащие бактерии, отсекаются. Двойные мембраны лизируются продуктами плазмидного гена icsB, высвобождая бактерии для дальнейших циклов роста и переноса [Smith H., 1995; Finlay В Falkow S., 1997; Goosney D. et al., 1999].

Рис. 10. Механизм инвазии Shigella flexneri. A. Иммунофлюоресцентная фотография, показывающая Shigella (темноевключение), проникающую через цитоплазму посредством полимеризованного актина (светлые нити). B. Перестановки цитоскелета, обусловленные инвазией Shigella. Наружный мембранный белок IcsA используется шигеллой для продвижения вклетку хозяина. IcsA непосредственно соединяется с двумя белками клетке хозяина — винкулином и белком нейрального синдрома Вискота-Аль-Дрехта (N-WASP). Шигелла расщепляет винкулин, в результате образуется 90 кд фрагмент, который присоединяется к IcsA и к вазодилататорстимулирующему белку (VASP). VASP рекрутирует белки цитоскелета клетки хозяина (актин и профилин) к бактериальной поверхности и формирует актиновый «мотор» для продвижения шигеллы
Salmonella typhimurium — возбудитель энтероинфекции людей (рис. 11). Для проникновения возбудителя в нефагоцитирующий эпителий необходимы несколько хромосомных генов (inv/spa), кластированных на «острове патогенности», названном SPI1 (Salmonella pathogenicity island 1; более подробно см. «острова патогенности» и «системы секреции бактериальной клетки»). Подобно ЕРЕС, АРМ кодирует третий тип секреторной системы, активируемой посредством межклеточного контакта. Это позволяет экспортировать и клетку хозяина детерминанты вирулентности, необходимые для бактериальной инвазии [Goosney D. et al., 1999].

Рис. 11. Механизм инвазии Salmonella typhimurium. A. Трансмиссионная электронная микрофотография индуцированного Salmonella «рифления» мембраны поляризованных Сасо-2 эпителиальных клеток. B. Инвазия Salmonella в эпителиальные клетки хозяина. Salmonella секретирует белки вирулентности, включающие SopE и SptP с помощью секреторной системы III типа. SopE функционирует как фактор обмена гуанидина для небольших СТР(гуанидинтрифосфат) — связывающих белков, вероятно, вызывая обмен GDP на GTP белка CDC42, члена семейства Rho. SptR является фосфатазой, необходимой для инвазии. Предполагается, что она разрушает цитоскелет. Инвазия также стимулирует активность фосфолипазы С (PLC1, приводящей к истечению из клетки и иозитолтрифосфата (IP3) и Са2+. Последний, в свою очередь, «обратным ходом» может быть вовлечен в перестройку цитоскелета, что приводит к «рифлению» мембраны эукариотической клетки и интернализации Salmonella [Goosney D. et al., 1999]
Yersinia. Наиболее изучены системы инвазии у Yersinia enterocolitica и у Yersinia pseudotuberculosis. Первоначально они проникают в организм через посредничество М-клеток пейеровых бляшек подвздошной кишки. Дальнейшая диссеминация происходит благодаря выживанию внутри макрофагов, которые мигрируют через лимфатическую систему. Оба микроорганизма обладают хромосомными генами, кодирующими наружный мембранный белок инвазии, способствующий их адгезии и проникновению в нефагоцитирующие клетки. Показано, что инвазин эффективно присоединяется к белкам семейства (бета1-интегринов. После тесного связывания с интегринами, инвазин индуцирует проникновение бактерии во внутрь клетки с помощью механизма, подобного «застежке молнии» («zipper-like» mechanism — «зип-лайк» механизм). Он заключается в «расстегивании» мембраны вокруг бактерии в момент ее проникновения в клетку хозяина. Энтеропатогенные Yersinia обладают еще двумя инвазинами: Ail и YadA. Белок Ail способствует более эффективной адгезии к эпителиальным клеткам, но не участвует в их инвазии. Зато он способствует устойчивости Yersinia к действию сыворотки (такие белки широко распространены среди других инвазивных бактерий). YadA — это белок, закодированный на плазмиде. Подобно инвазину он связывается с (бета1-интегринами клеток хозяина. Присоединение Yersinia к бета1-интегрину клетки хозяина запускает механизм контакт-зависимой секреции плазмидных факторов вирулентности и последующей транслокации в ее цитоплазму отдельных бактериальных белков [Smith H., 1995; Finlay В, Falkow S., 1997].
Патогены, связывающие молекулы хозяина для осуществления инвазии. Механизмы инвазии отдельных патогенов не поддаются логике. Легионеллы и микобактерии связывают фрагменты комплемента СЗb и СЗbi, которые облегчают их проникновение в фагоцитирующие клетки, и тем самым, уменьшают для них риск подвергнуться воздействию окислительных радикалов [Schlesinger L.S., Haas R., 1994]. Другие микроорганизмы связывают фибронектин, который затем функционирует как мостик между бактерией и фибронектиновым рецептором клетки хозяина, способствуя их инвазии. Например, Mycobacterium leprae продуцирует фибронектинсвязывающий белок, который способствует ее проникновению в эпителий и шванновские клеточные линии [Schorey А.В. et al., 1995]. Интересно, что механизмы, используемые для инвазии в нефагоцитирующие клетки функционируют и в отношении фагоцитирующих клеток. Например, мутант S. typhimurium, утративший способность к инвазии эпителиальных клеток, одновременно значительно снижает свою способность проникать в фагоцитирующие клетки [Gahring L.C., 1990]. Это возможно потому, что использование бактериями путей активной инвазии, помогает им избежать антибактериальной активности фагосом, куда они неизбежно попадают при традиционном фагоцитозе [Finlay В., Falkow S., 1997].
Внутриклеточная жизнь бактериальных патогенов. Механизм блокирования активного фагоцитоза макрофагами теплокровных имеет аналоги в природе: легионеллы, проникая в амебы и инфузории, используют те же механизмы, предотвращающие их переваривание и позволяющие микробам активно размножаться в вакуолях простейших [Бухарин О.В., Литвин В.Ю., 1997]. Т. е. патогенность «новых» для человека бактерий может объясняться тем, что они уже были преадаптированы к такой встрече. С. Richmond (1987) считает, что проникновение легионелл в легочные макрофаги обусловлено их «ошибкой» (по определению В. Levin — это «недальновидная эволюция»), ставшей возможной из-за большого сходства этих клеток с их природными хозяевами — амебами. Любопытно и то, как легионеллы убивают человеческие фагоциты. Для этого они используют эволюционно очень древний прием — индуцирование апоптоза, видимо «отработанный» еще на амебах [Hagele S., et al., 1998]. В ряде исследований обнаружена прямая корреляция между успешным внутриклеточным ростом бактерии и ее вирулентностью |Finlay В., Falkow S., 1997].
Большинство фагоцитированных бактерий все же погибает в макрофагах и полиморфно-ядерных лейкоцитах. Однако некоторые применяют удачные стратегии собственного выживания. Например, S. flexneri и L. monocytogenes растворяют мембрану образовавшейся вокруг них вакуоли и таким образом получают доступ к богатой питательными веществами цитоплазме. Coxiella burnetii выживает и даже «процветает» среди бактерицидных агентов, доставляемых клеткой хозяина в фаголизосомы. Основным требованием Демона Дарвина к патогену является способность того приспособиться к температуре, осмолярности, концентрации кислорода и уровню питательных веществ внутри тканей хозяина. Это позволит ему достичь такой скорости размножения, которая в наибольшей степени способствует использованию ресурсов хозяина при данной стратегии паразитизма, а, следовательно, ведет к дальнейшему развитию болезни.
Жизнь внутри вакуоли. Патогены используют разнообразные механизмы, позволяющие им избежать гибели в вакуолях («непробиваемые» капсулы; ферменты, нейтрализующие кислородные радикалы и протеолитические ферменты и др.). Но удивительно то, что некоторые из них фактически зависят от факторов, обнаруженных в фаголизосомах! Например, С. burnetii и S. typhimurium нуждаются в кислых значениях рН в качестве сигнала для внутриклеточной репликации. При этом само проникновение именно в данную фаголизосому, тоже предопределено. Специфический рецептор, который патоген использует для вторжения в эпителиальную клетку или для поглощения фагоцитом, в значительной степени влияет на конечную внутриклеточную локализацию вакуоли, которая окружает патоген [Finlay В., Falkow S., 1997]. Вот уж действительно, паразитические микроорганизмы это не примитивные, а более древние формы жизни!
Взаимодействие бактериальных патогенов с иммунной системой хозяина. Локальное взаимодействие бактериального патогена с тканями, как правило, вызывает большое количество системных реакций, посредством которых организм хозяина пытается контролировать течение инфекции. Иммунная система млекопитающих способна узнавать многие компоненты бактерий, особенно ЛПС и пептидогликан. Однако на некоторые из них эта реакция чрезмерна. Staphylococcus aureus продуцирует токсин, названный «суперантигеном» из-за того, что он вызывает токсический шок. «Суперанти-генными» свойствами обладают отдельные антигены возбудителя псевдотуберкулеза и уропатогенных кишечных палочек. Их роль в инфекционном процессе не ясна. Предполагается, что «суперантигены» позволяют бактериям преодолевать локальные защитные системы хозяина [Finlay В., Falkow S., 1997], т. е. их синтез является следствием «недальновидной эволюции».
В результате длительного селекционного давления (в том числе и в окружающей среде), наиболее «удачливые» патогены вырабатывают стратегию, позволяющую либо избежать, либо вводить в заблуждение иммунную систему нового хозяина. О.В. Бухарин и Б.Я. Усвяцов (1996) выделяют 4 типовых механизма защиты бактерий от факторов иммунитета.
Экранирование клеточной стенки бактерий. Механизмы экранирования структур бактерий (пептидогликан, поверхностные белки клеточной стенки и др.), опознаваемых иммунной системой хозяина, могут иметь как специфический, так и неспецифический характер. Из неспецифических «экранов», наиболее изучены капсулы и капсулоподобные образования.
Создание бактериями капсульного материала полисахаридной и протеиновой природы представляет наиболее типичную тактику бактериального уклонения от фагоцитоза. Являясь по своей природе полимером N-ацетилнейраминовой кислоты, капсулы многих бактерий сходны не только в химическом, но и в биологическом отношении. Они покрывают основные компоненты клеточной стенки и препятствуют активации комплемента сыворотки [Бухарин О.В., Литвин В.Ю., 1997].
Капсулоподобные образования формируются за счет неспецифической сорбции поверхности бактериальной клетки сывороточных протеинов хозяина (иммуноглобулинов, фибриногена, 2-микроглобулина, гаптоглобулина, сывороточного альбумина, и др.). Такое иммуноглобулиновое покрытие может достигать толщины 100 нм. Оно помогает бактериям уйти от распознавания иммунной системой, придает устойчивость к фагоцитозу и прикрывает их поверхность от лиганд-рецепторных взаимодействий [Бухарин О.В., Литвин В.Ю., 1997].
Сходную функцию — экранирование петидогликана и воспрепятствование опсонизирующему действию системы комплемента, выполняет у стафилококков — белок А, у стрептококков — белок М [Езепчук Ю.В., 1985].
К специфическому механизму экранирования клеточной стенки бактерий, видимо, можно отнести их антигенную вариабельность.
Многие поверхностные структуры бактерий способны к антигенному варьированию — это жгутики, пили, ЛПС, капсулы, S-слой, секретируемые ферменты и отдельные белки клеточной стенки. Однако это не означает, что они все сразу варьируют у каждого патогена. Интенсивному варьированию подвержены только некоторые из них, как правило, это активно экспрессируемые (или экспонируемые) иммунодоминантные поверхностные белки патогенов, «проживающих» на поверхности слизистых оболочек. Примеров антигенной вариабельности среди внутриклеточных бактерий, значительно меньше. Видимо, это связано с тем, что основной иммунный ответ хозяина вызывают другие их антигены [Finlay В., Falkow S., 1997].
Наиболее хорошо механизм антигенной вариации изучен у Neisseria (N. gonorrhoeae, N. meningitidis). Основной варьирующей антигенной структурой у представителей этого семейства являются пили. Гонококки располагают потенциально большим набором серологически различных пилей, однако всегда экспрессируется ген только одного из них. Это вызвано тем, что в бактериальной клетке постоянно экспрессируется только один функционально активный пилиновый локус (pil E). Но одновременно с ним в хромосоме разбросаны еще более чем 50 усеченных нетранскрибируемых генов пилей. В случае генетической перестановки, происходящей по принципу «русской рулетки» (и посредством Rec А), экспрессируемый ген в pil Е заменяется одним из молчащих, с другими серологическими свойствами — антигенная структура гонококка меняется [Seifert H.S., 1992].
Другой варьирующей структурой семейства являются их поверхностные белки Ора. Экспрессия гена каждого такого белка независима от других и реализуется через «двухпозиционный переключатель». Каждый ора-ген в регионе, кодирующем гидрофобную сигнальную последовательность, имеет серию повторов последовательности СТСТТ. Количество СТСТТ определено рамкой трансляции гена и, в итоге, один из двух полных белков Ора экспрессируется. Рекомбинация между СТСТТ-последовательностями меняет количество СТСТТ-повторов и антигенную специфичность белка Ора [Stern A., Meyer T.F., 1987].
Borreliahermsii — возбудитель возвратной лихорадки, демонстрирует другой пример антигенных вариаций. Этот микроорганизм содержит линейную плазмиду, которая кодирует множество молчащих копий вариабельных основных белков. Подобно пилям Neisseria, через Перестановки ДНК в экспрессионные сайты на других линейных плазмидах, боррелией осуществляется экспрессия антигенно различных основных белков [Girons S., Barbour A.G., 1991].
Многие бактериальные поверхностные компоненты варьируют от штамма к штамму. Вот только несколько примеров: ЛПС сальмонелл — более 60 типов; капсула S. pneumoniae — более 80 типов; IgA-протеаза H. influenzae — более 30 вариантов; М-белок стрептококков — более 80 серотипов. Большинство вариаций вызвано маленькими нуклеотидными заменами, вставками и делециями генов, которые кодируют эти факторы вирулентности, а в результате этих процессов мы наблюдаем антигенный дрейф у возбудителя инфекции [Finlay В., Falkow S., 1997].
Продукция бактериями секретируемых факторов, инактивирующих защиту хозяина. Микробная клетка обладает средствами дистанционного действия, которые представляют многочисленную группу секретируемых бактериальных субстанций, направленных на инактивацию механизмов иммунной защиты.
Наиболее изучено образование трипсиноподобных ферментов, расщепляющих иммуноглобулины класса A (IgA). Продукция данных ферментов характерна для бактерий, инфицирующих слизистые оболочки бактерий. Протеазы данного типа некоторых микроорганизмов (P. aeruginosa и S. marcescens) действуют неспецифично и расщепляют другие гуморальные защитные протеины хозяина — лизоцим, фибронектин, и даже компоненты тканей, включая фибробласты. Бактерии также продуцируют ферменты, деградирующие комплемент, лизоцим, бактерицидный компонент лейкоцитарного интерферона, гистоны, дефенсины и др. Наши знания об этих факторах постоянно расширяются [Бухарин О.В., Усвяцов Б.Я., 1996]. Очень важным представляется их способность к полифункциональному действию (см., например, действие LasB-эластазы). Благодаря этому патоген может добиться «успехов» в новом для себя хозяине не нарушая «принципа экономии генов».
Антигенная мимикрия. Под антигенной мимикрией понимается наличие сходных структур у хозяина и паразита, представленных молекулами разного генетического набора (рис. 12). Сходство между протеинами, закодированными у микроорганизмов, и собственными протеинами хозяина — встречается достаточно широко. Данное явление оставляет отчетливые генетические следы в человеческих популяциях после глобальных эпидемических катастроф.

Рис. 12. Схема антигенной мимикрии между Kl. pneumoniae и HLA человека. Гомологичный участок Kl. pneumoniae и антигены гистосовместимости человека (HLA B-27) имеют 6 из 9 пар сходных аминокислот [Бухарин О.В., Усвяцов Б.Я., 1996]
Образование форм бактерий с отсутствием (дефектом) клеточной стенки. Невозможность «замаскировать» пептидогликан бактериальной клетки приводит к тому, что бактерия либо частично, либо полностью теряет его вместе с клеточной стенкой. С точки зрения паразита, это биологически оправданный шаг, так как возбудитель для организма становится неузнаваем и персистирование его в среде обитания продолжается [Бухарин О.В., Усвяцов Б.Я., 1996].
«Острова патогенности» и системы секреции бактериальной клетке. Так как инфекционная болезнь проявляется разнообразными патологическими процессами, протекающими в органах и тканях, то первоначально считалось, что патогенные свойства бактерий формируются с помощью каких-то редких и уникальных механизмов. Однако спектр таких механизмов оказался не так широк, как первоначально предполагалось. Была установлена общность ряда молекулярных инструментов, используемых бактериями для достижения разных целей [Finlay В., Falkow S., 1989]. Постепенно возникло и другое противоречие в представлениях о бактериальной патогенности. В ранних поисках генов вирулентности, исследователями была обнаружена локализация многих из них на плазмидах или Фагах [Брода П., 1982]. Позже стало ясно, что гены патогенности, переносимые фагами и плазмидами, не способны вызвать в организме хозяина все те патологические изменения, которые вызывают различные патогенные микроорганизмы [Mecsas J., Strauss E.J 1996], и их роль в эволюции патогенных бактерий явно преувеличена. Оба противоречия разрешились тогда, когда для исследователей интерес стали представлять хромосомы.
Было обнаружено, что большая часть так называемых факторов патогенности располагается на хромосомах отдельными кластерами из функционально связанных групп генов. Последовательности этих кластеров отличались от большей части генома, что позволили выдвинуть предположение об их «чужеродном» происхождении. Позже подобные структуры были найдены на плазмидах, однако они не охватывают всего многообразия таких структур, имеющихся на хромосомах. Эти наблюдения позволили выдвинуть концепцию «островов патогенности», расположенных на дискретных и часто имеющих чужеродное происхождение участках ДНК, кодирующих группы вирулентных признаков (табл. 2). Одновременно стали накапливаться сведения о механизме доставки синтезируемых факторов патогенности за пределы бактериальной клетки (рис. 13). В частности у вида Yersinia была обнаружена секреторная система (III типа), закодированная в одном из «островов патогенности» [Salmond G., Reeves PJ., 1993]. Механизм действия такой системы способствует продвижению эффекторных молекул в участки клетки хозяина, где они оказываются способными изменять его физиологию [Rosqvist R. et al., 1991; Rosqvist R., 1990].
Таблица 2











