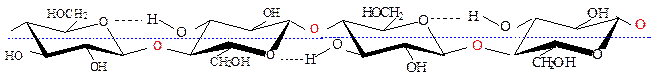Углеводы
Сыктывкар 2004
Утверждено на заседании кафедры биологической и общей химии КФ КГМА от «» 2004 года
Составители: Никитина Н.И., Цапок П.И., Казакова Е.И.
Содержание
| Введение
I. Моносахариды
I.1. Типы моносахаридов и их номенклатура
I.2. Стереохимия моносахаридов
I.3. Вывод конфигураций альдоз D-ряда
I.4. Доказательство конфигурации пентоз и гексоз D-ряда
I.5. Таутомерия моносахаридов
I.6. Мутаротация
I.7. Конформации моносахаридов
I.8. Химические свойства моносахаридов
а. Реакции нециклических форм
б. Реакции циклических форм
Тестовые задания
I.9. Производные моносахаридов
II. Олигосахариды
II.1. Строение дисахаридов
II.2. Свойства дисахаридов
II.3. Производные дисахаридов
Тестовые задания
III. Полисахариды
III.1. Гомополисахариды
III.2. Гетерополисахариды
III.3. Смешанные углеводсодержащие полимеры
Тестовые задания
Список литературы
| 3
5
5
6
8
10
14
18
19
20
20
25
28
32
37
37
41
43
43
45
46
53
55
59
60
|
ВВЕДЕНИЕ
Моно- и дисахариды – простейшие представители соединений, относящихся к классу углеводов, иногда называемых также сахарами. Уже давно они стали интенсивно изучаться химиками, биологами, медиками, учеными, работающими в области сельского хозяйства и пищевой промышленности. Углеводы играют громадную роль в обеспечении функционирования животных и растительных организмов на Земле.
В химии углеводов главная роль принадлежит моносахаридам – тем «кирпичикам», из которых построены полисахариды – биополимеры, составляющие основную массу органического вещества на Земле и играющие наряду с нуклеиновыми кислотами и белками важнейшую роль практически во всех процессах, протекающих в организмах.
Из моносахаридов же самое большое значение имеют полиоксиальдегиды и полиоксикетоны, именно они являются теми органическими веществами, которые первоначально образуются из диоксида углерода и воды в процессе фотосинтеза.
СО2 + Н2О ® Моносахариды + ½ О2
В биосфере Земли, по-видимому, нет другого пути биосинтеза органических веществ из неорганических. Этот процесс протекает в зеленых растениях. Масштабы его огромны. Достаточно сказать, что по самым приблизительным подсчетам ежегодно таким образом синтезируется порядка 5×1010 тонн углеводов.
Однако полиоксиальдегиды и полиоксикетоны являются не только первноначальными продуктами фотосинтеза. Раз образовавшись, они подвергаются далее многочисленным трансформациям, обеспечивая многие важнейшие процессы жизнедеятельности. Большая часть из них расходуется на образование полисахаридов, выполняющих помимо многих других функций роль строительных материалов и аккумуляторов энергии. Другая же часть подвергается после фосфорилирования ферментативному расщеплению. Выделяющаяся при этом энергия расходуется на образование макроэргических соединений, которые затем принимают активное участие в образовании более стабильных источников энергии – некоторых моносахаридов, резервных полисахаридов и жиров.
Например, в организме для глюкозы характерны три типа распада: анаэробный распад до молочной кислоты, аэробный распад до углекислого газа и воды и спиртовое брожение. Реакции в живых организмах традиционно делят на аэробные (в присутствии кислорода) и анаэробные (в отсутствие кислорода) процессы. Термин «анаэробные» реакции не следует понимать буквально, поскольку в живых тканях анаэробных условий не бывает, это лишь указывает, что в данных реакциях кислород не используется.
Реакции анаэробного распада происходят в мышцах и других тканях, если расход и доставка кислорода не скомпенсированы, например, при интенсивной работе. Накопление молочной кислоты в этом случае вызывает болезненные ощущения. В анаэробных условиях гликолиз – единственный процесс в животном организме, поставляющий энергию. Благодаря этому процессу организм человека и животных может функционировать определенный период времени в условиях недостатка кислорода.
Аэробный распад углеводов – это основной путь катаболизма углеводов и освобождения энергии в них запасенной. В результате этих процессов глюкоза распадается до СО2 и Н2О, а освобождающаяся энергия используется для синтеза АТФ. Аэробный распад глюкозы может происходить во всех органах и тканях. В наибольшей зависимости от этого процесса находится мозг. Он расходует около 100 г глюкозы в сутки.
Спиртовое брожение осуществляется дрожжеподобными организмами. Этот процесс имеет большое практическое значение для получения этанола в виноделии, пивоварении, хлебопекарной промышленности из природного сырья, даже из древесины (в конечном счете из глюкозы):
Многие доступные моносахариды легко расщепляются ферментами и вне организма, давая в ряде случаев практически полезные продукты ферментолиза. Известны уксуснокислое, лимоннокислое виды брожения, а также такие виды брожения, которые приводят к бутанолу, ацетону и бутандиолу-2,3. Известно также бактериальное разложение клетчатки, приводящее к метану.
Механизмы многих из этих ферментативных реакций расшифрованы. Все они изучаются биохимией, которая, однако, была бы бессильна понять суть явлений, если бы были неизвестны строение и химические свойства субстратов, т.е. в первую очередь моносахаридов.
I. Моносахариды
Среди моносахаридов наиболее распространены полиоксиальдегиды и полиоксикетоны. Однако встречаются также соединения, содержащие помимо карбонильной и гидроксильной и иные функции, и отличающиеся другими особенностями строения.
Таблица 1
Операции
| Уравнивание концов
| Укорочение цепи +
Уравнивание концов
|
| Рибоза
Арабиноза
Ксилоза
Ликсоза
| -
+
-
+
| -
-
+
+
|
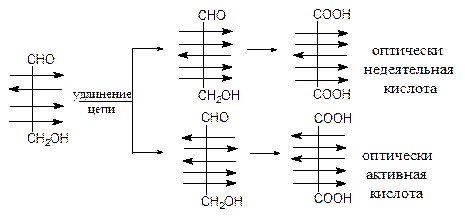 Рассмотрим на примере глюкозы как установить конфигурацию той или иной гексозы. Если в результате укорочения цепи получена арабиноза, то исходным веществом могли быть глюкоза или манноза. Уравнивание концов в применении к рассматриваемому случаю не поможет сделать выбор между указанными гексозами, т.к. обе они при этом дают оптически активные кислоты. Чтобы ответить на вопрос о том, какая из гексоз глюкоза или манноза перед нами, необходимо прибегнуть к последовательному удлинению цепи и уравниванию концов исследуемой гексозы. При этом, как видно из приведенной ниже схемы, глюкоза даст одну оптически деятельную двухосновную кислоту и одну – оптически недеятельную, а манноза - две оптически деятельные.
Рассмотрим на примере глюкозы как установить конфигурацию той или иной гексозы. Если в результате укорочения цепи получена арабиноза, то исходным веществом могли быть глюкоза или манноза. Уравнивание концов в применении к рассматриваемому случаю не поможет сделать выбор между указанными гексозами, т.к. обе они при этом дают оптически активные кислоты. Чтобы ответить на вопрос о том, какая из гексоз глюкоза или манноза перед нами, необходимо прибегнуть к последовательному удлинению цепи и уравниванию концов исследуемой гексозы. При этом, как видно из приведенной ниже схемы, глюкоза даст одну оптически деятельную двухосновную кислоту и одну – оптически недеятельную, а манноза - две оптически деятельные.
Аналогичным образом можно различить гексозы гулозу и идозу. Например, из гулозы получаются две оптически деятельные кислоты, а из идозы - одна оптически деятельная и одна оптически недеятельная кислоты.
Рассмотренным выше операциям Фишер подверг все известные альдозы D- и L-рядов и установил, таким образом, строение каждой из них. Это позволило сделать пространственное отнесение известных альдоз, имевших лишь тривиальные названия.
I.6. Мутаротация
| Вода Пиридин
a +52,50 b
+112,20 +17,50
| |
Приведенные выше равновесия между циклической и открытой формами моносахаридов реализуются в расплавах или растворах. Это подтверждается тем, что при растворении в воде каждого из чистых кристаллических аномеров первоначальное удельное вращение растворов [α]
D меняется во времени, таким образом, что постепенно становится одинаковым для растворов полученных как из α-, так и из β-аномеров.
Например, для чистой α-D-глюкозы угол вращения при растворении в воде уменьшается от +112,20 до +52,50, а для чистой β-D-глюкозы угол вращения увеличивается от +17,50 до +52,50.
Это убедительно подтвердило существование равновесий цикло-оксо-тауто-мерии. Явление изменения удельного вращения свежеприготовленных водных растворов моносахаридов называется мутаротацией. В растворе D-глюкозы после установления равновесия содержится 35% α- и 64% β-аномера; концентрация открытой формы, через которую и осуществляются взаимопревращения аномеров, составляет всего 0,024%. Количество фуранозной формы исчезающе мало. Следует отметить, что концентрация открытых форм в растворах пентоз и фруктозы существенно больше. Так, для D-рибозы, например, она равна около 8,5%, а в случае фруктозы ее наличие легко определяется спектроскопически.
Конформации моносахаридов
Молекулы моносахаридов, как и молекулы других органических соединений, могут существовать в различных конформациях. Умение выбрать из числа из бесчисленного множества конформаций, которые может принимать молекула данного вещества, наиболее устойчивую, часто позволяет объяснить свойства и реакционную способность органических соединений. Это относится также и к моносахаридам.
Большое значение конформационный анализ имеет в ряду пиранозных форм альдоз и кетоз и их производных. В перспективных формулах полуацетальных форм моносахаридов оксидное кольцо во всех случаях изображалось как плоское. Для фураноз такое изображение, в основном, правильно отражает реальную форму молекулы, поскольку валентные углы в плоском пятичленном цикле практически не искажены. В случае пираноз ситуация аналогична наблюдаемой для циклогексана, для которого наиболее характерными являются формы - кресла и ванны. Причем, кресло наиболее выгодно. В случае пираноз конформации кресла будут выглядеть следующим образом: в конформации С1 первый атом углерода находится под плоскостью, в которой расположены атомы С2, С3, С5 и О, а в конформации 1С – над ней.
Из всех конформаций наиболее устойчивой будет та, в которой нековалентные взаимодействия между отдельными заместителями (фрагментами) минимальны. Поэтому предпочтительной будет та конформация, в которой большая часть объемистых заместителей (гидроксильных и особенно оксиметильной групп) находится не в аксиальном, а в экваториальном положении.

Рассмотрим с этих позиций конформации D-глюкопиранозы, в молекуле которой имеется 4 гидроксильных и одна оксиметильная группы. В молекуле α–аномера в конформации С1 экваториальное положение занимают 3 гидроксильных группы и оксиметильная группы, а в конформации 1С в экваториальном положении находится только одна гидроксильная группа (при С1). В случае β-аномера глюкозы конформер 1С вообще не будет иметь в экваториальном положении ни гидроксильных, ни оксиметильной групп. Естественно поэтому, что оба аномера D-глюкозы существуют практически только в конформации С1.
Б. Реакции циклических форм
Рассмотренные выше свойства моносахаридов не противоречат их строению как полиоксиальдегидов и полиоксикетонов. Однако ряд свойств пентоз и гексоз приведенные формулы объяснить не могли. Так, оказалось, что пентозы и гексозы в отличие от обычных альдегидов не образуют бисульфитных производных. Кроме того, полные метиловые эфиры, приготовленные из пентоз и гексоз действием диметилсульфата и щелочи (или иодистого метила в присутствии оксида серебра), не давали характерного осадка с реактивом Фелинга, а также реакции серебряного зеркала, типичных для альдегидов.
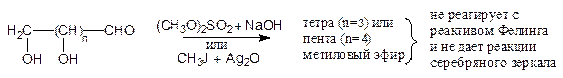
 В тоже время гидролиз этих эфиров разбавленным раствором кислоты, т.е. в условиях, в которых простые эфиры устойчивы, приводил к отщеплению одной метильной группы. Так, из тетраметилового эфира, приготовленного из пентоз, получался триметиловый эфир, а из пентаметилового, приготовленного из гексоз, – тетраметиловый:
В тоже время гидролиз этих эфиров разбавленным раствором кислоты, т.е. в условиях, в которых простые эфиры устойчивы, приводил к отщеплению одной метильной группы. Так, из тетраметилового эфира, приготовленного из пентоз, получался триметиловый эфир, а из пентаметилового, приготовленного из гексоз, – тетраметиловый:
Продукты такого «монодеметилирования» полных метиловых эфиров пентоз и гексоз уже давали реакцию серебряного зеркала.
Таким образом, было установлено, что какая-то одна из гидроксогрупп в молекулах пентоз и гексоз обладает особыми свойствами. Особые свойства этой гидроксогруппы явились следствием того, что она внутримолекулярно взаимодействует с карбонильной группой, образуя циклический полуацеталь (кольчато-цепная таутомерия). Эта гидроксогруппа также и называется, полуацетальной.
 С ее участием легко образуются метиловые эфиры. Для получения последних соответствующий моносахарид достаточно обработать метиловым спиртом в присутствии 3%-ного хлористого водорода:
С ее участием легко образуются метиловые эфиры. Для получения последних соответствующий моносахарид достаточно обработать метиловым спиртом в присутствии 3%-ного хлористого водорода:
Полученные таким образом производные пентоз и гексоз называют метилгликозидами; полуацетальный гидроксил, который легко замещается – гликозидным гидроксилом; атом углерода С1, у которого произошло замещение – гликозидным центром; вступающий заместитель – агликоном.
Легкость замещения гликозидного гидроксила используется для получения гликозидов самого разнообразного строения. Так, при обработке пентоз и гексоз аминами, не являющихся сильными основаниями (иначе пойдет эпимеризация), происходит образование соответствующих N-гликозидов. Например:
Фрагмент молекулы
моносахарида
Здесь агликонами являются аминная и фениламинная группы.
Остаток моносахарида сообщает связанному с ней агликону легкую растворимость в воде, делает его способным функционировать в живой (животной или растительной) клетке.
В связи с этим становится понятным чрезвычайно большая распространенность гликозидов в природе. Примерами могут служить компоненты нуклеиновых кислот – нуклеозиды; действующее начало горчичного масла – глюкоиберин, арбутин, используемые в цветной фотографии, и многие другие. В молекулы моносахаридов в качестве агликонов иногда вводят физиологически активные вещества, что облегчает их применение в медицине (усвояемость, возможность использования растворов).
Контрольные вопросы
1. Какими реакциями можно доказать наличие в молекуле глюкозы альдегидной и гидроксильных групп.
2. Что произойдет при нагревании пентаметилглюкозы и пентаацетилгалактозы при нагревании их с разбавленной серной кислотой.
3. Какие продукты образуются при окислении маннозы, при ее восстановлении, при взаимодействии с гидроксиламином, с избытком фенилгидразина.
4. Какиe два моносахарида дадут тот же озазон, что и L-галактоза.
5. Напишите схемы получения следующих гликозидов: а) метил-b-D-глюко-фуранозида; б) этил-a-D-галактопиранозида; в) изопропил-b-D-фруктопирано-зида, г) о-(оксиметил)фенил-b-D-глюкопиранозида (салицина), д) метил-b-D-рибофуранозида.
6. Нагревание пентоз с разбавленной серной кислотой приводит к образованию фурфурола. Напишите уравнение реакции.
7. Напишите проекционные формулы Фишера всех D-альдогексоз, которые при восстановлении образуют оптически неактивные многоатомные спирты.
8. Какой продукт получается при окислении азотной кислотой D-галактозы? Почему полученное соединение не обладает оптической активностью.
Тестовые задания
1. Какое из соединений является a-D-рибопиранозой?








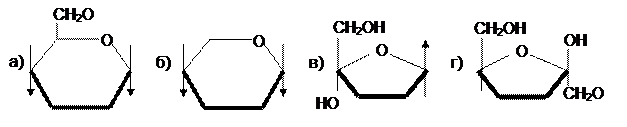
2. Образование соединения синего цвета при взаимодействии глюкозы (раствор) с гидроксидом меди (II) с образованием глюконата меди (II) обусловлено наличием в ее молекуле:
а) одной ОН-группы б) s- и p-связей
в) нескольких ОН-групп г) альдегидной группы
3. Какому моносахариду в открытой форме соответствует структура следующего циклического полуацеталя:

4. Углеводом, входящим в состав РНК, является:
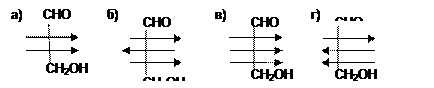
5. D-глюкоза и D-галактоза являются между собой:
а) эпимерами б) диастереомерами в) гомологами г) изомерами
6. Метилгликозид можно получить при взаимодействии:
а) глюкозы с ангидридом уксусной кислоты
б) галактозы с метиловым спиртом
в) крахмала с метилхлоридом
г) глюконовой кислоты с метанолом
7. Озазон – это продукт взаимодействия углевода с:
а) гидроксиамином б) гидразином в) вторичным амином г) HCN
8. Какая структура соответствует метил-a–D-глюкопиранозиду:
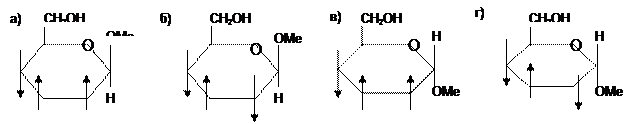
9. Какой из реагентов не вызывает ответной реакции у глюкозы?
а) NH2OH б) Cu(OH)2 в) NaHSO3 г) Ag(NH3)2OH
10. Какой из моносахаридов входит в состав нуклеиновых кислот?
а) a-D-глюкопираноза б) b-D-фруктофураноза
в) a-L-маннопираноза г) b-D-рибофураноза
11. Шестиатомный спирт сорбит образуется при взаимодействии глюкозы с?
а) уксусной кислотой б) Ag(NH3)2OH в) этанолом г) водородом
12. При растворении сахаров с течением времени происходит изменение угла вращения до определенной равновесной величины. Это явление называется:
а) поляризация б) конформационная изомерия
в) мутаротация г) ионизация
13. Как называются два оптических изомера по отношению друг к другу:

а) эпимеры б) цис-транс-изомеры
в) энантиомеры г) диастереомеры
14. Реакция с каким веществом используется для доказательства того, что глюкоза – пятиатомный спирт?
а) Cu(OH)2 б) CH3COOH в) Ag2O г) NaHSO3
15. Продуктом реакции является:


а) метил-a-D-галактопиранозид
б) метил-b-D-галактопиранозид
в) метил-2,3,4,6-тетра-О-метил-a-D-галактопиранозид
г) метил-2,3,4,6-тетра-О-метил-b-D-галактопиранозид
16. Названию 2,3,6-три-О-метил-a-D-глюкопиранозе соответствует структура:

17. Альдозу от изомерной ей кетозы можно отличить по реакции с:
а) Н2 б) NaHSO3 в) Ag(NH3)2OH г) C6H5NHNH2
18. Какое из приведенных соединений не является компонентом таутомерного равновесия D-рибозы:
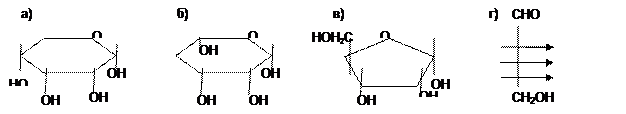
19. Фруктоза дает реакцию серебряного зеркала, так как:
а) возможна цикло-оксо-таутомерия б) возможна кето-енольная таутомерия в) содержится кето-группа г) содержится виц-диольный фрагмент
20. Фруктоза является:
а) кетогексозой б) кетопентозой в) альдогексозой г) дисахаридом
21. a– и b–глюкоза – это:
а) оптические изомеры б) структурные изомеры
в) олигосахариды г) цис-транс-изомеры
22. Какая функциональная группа присутствует в циклической форме глюкозы:
а) гидроксильная б) альдегидная в) карбоксильная г) карбонильная
23. Какая формула отвечает L-маннозе
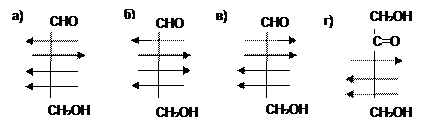
24. Изомерами являются:
а) 2-метилпропанол-1 и бутанол-1 б) D- и L-аланин
в) метанол и метаналь г) глюкоза и фруктоза
25. Какая характеристика не соответствует глюкозе:
а) имеет неразветвленный углеродный скелет
б) содержит кетонную группу
в) в циклической форме имеет 4 асимметрических центра
г) окисляется Cu(OH)2 при нагревании
26. Какая проекционная формула соответствует R-конфигурации глицеринового альдегида:
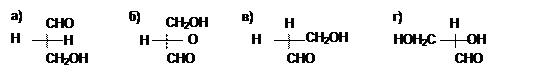
27. Конечным продуктом цепочки превращений является:
C6H5NHNH2 H2O Zn/CH3COOH


 D-глюкоза … ….
D-глюкоза … ….
(избыток) H+
а) крахмал б) фенилозазон D-глюкозы в) фруктоза г) сахароза
28. Какие схемы реакций показывают наличие в глюкозе альдегидной группы?
 а) С6Н12О6 + Cu(OH)2 (комн. t)
а) С6Н12О6 + Cu(OH)2 (комн. t)
 б) С6Н12О6 + HNO3
б) С6Н12О6 + HNO3
 в) С6Н12О6 + Ag(NH3)2OH
в) С6Н12О6 + Ag(NH3)2OH
 г) С6Н12О6 + Cu(OH)2 (высокая t)
г) С6Н12О6 + Cu(OH)2 (высокая t)
29. Какие моносахариды относятся к типу альдоз:
а) глюкоза б) рибоза в) дезоксирибоза г) сорбит
30. Сколько асимметрических атомов углерода в молекуле b-D-рибофуранозы:
а) один б) два в) три г) четыре
Рис.1. Схема синтеза аскорбиновой кислоты
Аскорбиновая кислота является g-лактоном 2-оксо-L-гулоновой кислоты. Существует в виде двух таутомерных форм (оксо-енольная таутомерия).
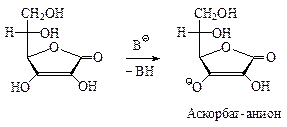 Из химических свойств аскорбиновой кислоты рассмотрим два – наиболее важных. Аскорбиновая кислота проявляет довольно сильные кислотные свойства, обусловленные диссоциацией одной из ОН-групп ендиольного фрагмента. Показатель кислотности рКа 4,2 (сравните, для уксусной кислоты рКа 4,76).
Из химических свойств аскорбиновой кислоты рассмотрим два – наиболее важных. Аскорбиновая кислота проявляет довольно сильные кислотные свойства, обусловленные диссоциацией одной из ОН-групп ендиольного фрагмента. Показатель кислотности рКа 4,2 (сравните, для уксусной кислоты рКа 4,76).
Аскорбиновая кислота обладает сильными восстановительными свойствами. Образующаяся при ее окислении дегидроаскорбиновая кислота легко восстанавливается обратно в аскорбиновую кислоту. Этот процесс обеспечивает некоторые окислительно-восстановительные реакции в организме, например гидроксилирование пролина и лизина – аминокислот, необходимых для синтеза прочного коллагена. При цинге – болезни, вызванной недостатком витамина С, синтез коллагена нарушен, образуются менее прочные коллагеновые волокна. С этим связана ломкость кровеносных сосудов и возникновение множественных точечных кровоизлияний.
II. Олигосахариды
Олигосахариды (oligos - «малый»)– продукты поликонденсации моносахаридов с числом звеньев 2-10. Олигосахариды подразделяют на:
- ди-, три-, тетрасахариды и т. д. (по количеству мономерных звеньев);
- восстанавливающие и невосстанавливающие (по отношению к реактивам Толленса или Фелинга).
Наиболее распространенной и изученной группой олигосахаридов являются дисахариды (биозы).
II. 1. Строение дисахаридов
II.2. Свойства дисахаридов
Дисахариды – кристаллические вещества, хорошо растворимые в воде, оптически активны. Наиболее важные свойства дисахаридов приведены в табл.2.
Таблица 2. Свойства дисахаридов.
| Вид процесса
| Восстанавливающие
дисахариды
| Невосстанавливающие
дисахариды
|
| Цикло-оксо-таутомерия
| +
| -
|
| Мутаротация
| +
| -
|
| Окисление:
- в щелочной среде
(р-вы Толленса, Фелинга)
- в кислой среде
|
+
+
|
-
+
|
| Гидролиз:
- в кислой среде
- в щелочной среде
- ферментативный
|
+
-
+
|
+
-
+
|
| Образование:
- простых эфиров
- сложных эфиров
|
+
+
|
+
+
|
Дисахариды вступают во многие реакции, характерные для моносахаридов, например, образуют простые и сложные эфиры, окисляются в кислой среде в гликобионовые кислоты и др. Дисахариды обладают способностью гидроли-зоваться в кислой (но не в щелочной) среде с образованием моносахаридов.
Некоторые химические свойства отличны у разных типов дисахаридов. В первую очередь, это разное отношение к действию окислителей в щелочной среде.
Контрольные вопросы
1. В чем заключается явление инверсии сахарозы? Напишите уравнение реакции.
2. Напишите уравнения реакций мальтозы с реактивами Толленса и Фелинга.
3. Напишите схему образования озазона лактозы. Можно ли получить озазон сахарозы?
4. Напишите структурную формулу b-D-глюкопиранозил-(1®6)-D-глюкопиранозы.
5. Является ли этот дисахарид восстанавливающим; как это можно доказать?

6. Что образуется при гидролизе:
а) хитобиозы
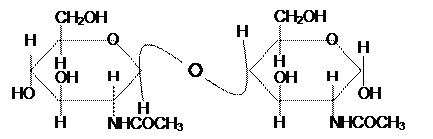
б) хондрозина
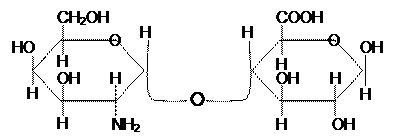
7. Какое систематическое название следует дать мелибиозе, имеющей строение:
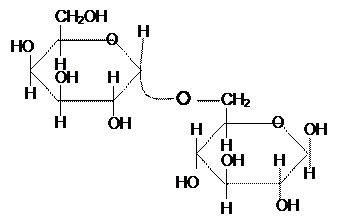
III.1. Гомополисахариды
Крахмал – основной запасной полисахарид растений, синтезируется в процессе фотосинтеза и откладывается в клетках в виде зерен. Крахмал содержится в клубнях картофеля (20%), зернах кукурузы (68%), пшеницы (70%), риса (80%). В организм человека и животных крахмал попадает с пищей и затем разлагается в желудочно-кишечном тракте при участии ферментов до глюкозы, которая используется как источник энергии и частично превращается в гликоген печени и мышц. Основной повторяющейся единицей, из которой синтезируется крахмал, являются остатки D- глюкозы, последовательно соединенные между собой a-(1,4)-гликозидными связями.
Известны две формы крахмала a-амилоза и амилопектин, которые встречаются в растениях как отдельно, так и в виде смесей. Обычный состав: амилоза – 20%, амилопектин – 80%. Амилоза растворима в горячей воде и может быть отделена. Амилопектин в горячей воде набухает и образует клейстер.
a -Амилоза имеет число звеньев 200-1000, a (1®4)-гликозидные связи, неразветвленную структуру. Молекулярная масса от нескольких тысяч до 500 тыс. Цепь амилозы начинается с невосстанавливающего конца и заканчивается восстанавливающим. Поскольку доля концевого остатка относительно всей молекулы невелика, то амилоза проявляет очень слабые восстановительные свойства.
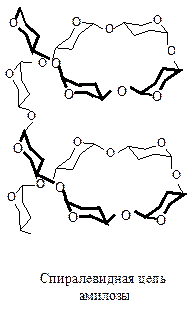 Для молекул амилозы характерна нитевидная форма, т.к. a-D-глюкопираноз-ные звенья имеют ваннообразные конформации, которые способствуют спирали-зации полиглюкозидной цепи. При этом молекулы амилозы свернуты в левую спираль. На каждый виток спирали приходится 6 углеводных звеньев (рис. 2).
Для молекул амилозы характерна нитевидная форма, т.к. a-D-глюкопираноз-ные звенья имеют ваннообразные конформации, которые способствуют спирали-зации полиглюкозидной цепи. При этом молекулы амилозы свернуты в левую спираль. На каждый виток спирали приходится 6 углеводных звеньев (рис. 2).
Рис. 2. Вторичная структура амилозы.
Внутри этой спирали есть пустоты, в которые могут входить молекулы других веществ с образованием соединений включения. Такое соединение включения амилоза образует с молекулами иода; оно окрашено в интенсивно синий цвет, что используется в аналитической химии для обнаружения как крахмала, так и йода (йодкрахмальная проба).
 Амилоза при ферментативном гидролизе образует сначала дисахарид – мальтозу (гидролиз начинается с невосстанавливающего конца амилозы и осуществляется последовательным отщеплением молекул мальтозы), а при полном гидролизе – D-глюкозу.
Амилоза при ферментативном гидролизе образует сначала дисахарид – мальтозу (гидролиз начинается с невосстанавливающего конца амилозы и осуществляется последовательным отщеплением молекул мальтозы), а при полном гидролизе – D-глюкозу.
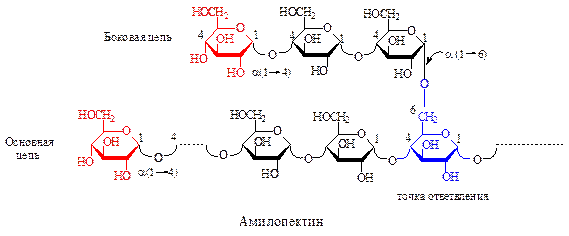 Амилопектин в отличие от амилозы имеет разветвленное строение. Главная и ответвленные цепи содержат a (1®4)-гликозидные связи, а в точках ответв-ления a-(1®6)-гликозидные связи. Между точками разветвления располагаются 20-25 гликозидных остатков. Молекулы амилопектина имеют сферическую фор-му и молекулярной массой от 100 тысяч до нескольких миллионов. Амилопектин – невосстанавливающий полисахарид, с йодом дает красно-фиолетовое окраши-вание, позволяющее отличить фракцию амилопектина от фракции амилозы.
Амилопектин в отличие от амилозы имеет разветвленное строение. Главная и ответвленные цепи содержат a (1®4)-гликозидные связи, а в точках ответв-ления a-(1®6)-гликозидные связи. Между точками разветвления располагаются 20-25 гликозидных остатков. Молекулы амилопектина имеют сферическую фор-му и молекулярной массой от 100 тысяч до нескольких миллионов. Амилопектин – невосстанавливающий полисахарид, с йодом дает красно-фиолетовое окраши-вание, позволяющее отличить фракцию амилопектина от фракции амилозы.
При частичном гидролизе амило-пектина происходит расщепление макромол-екулы на более мелкие осколки, называемые декстринами. Декстрины растворяются в
воде лучше, чем крахмал, и, следовательно,
легче усваиваются организмом.
Такой процесс расщепления, или декстринизация крахмала, осуществляется при хлебопечении или при глажке накрахмаленного белья.
Так называемый предельный декстрин образуется при ферментативном гидролизе крахмала ном гидролизе крахмала под действием b-амилазы. Водные растворы декстринов окрашиваются иодом в красный цвет.
При дальнейшем гидролизе с участием ферментов, расщепляющих a (1®4)- и a (1®6)- связи образуются дисахариды мальтоза и изомальтоза. Конечным продуктом гидролиза является глюкоза.
Гликоген – запасной полисахарид животного происхождения, встречается также в высших грибах, дрожжах и растений и даже некоторых бактериях. У животных он присутствует в клетках печени и мышцах. Структура гликогена аналогична структуре амилопектина с той разницей, что ответвления встречаются чаще (через 6-12 остатков). Молекулярная масса гликогена достигает 100 млн.
Гликоген растворяется в горячей воде, образуя коллоидный раствор, дающий с иодом желто-красную окраску, однако, гликоген, выделенный из животных клеток, дает с иодом красно-фиолетовый цвет (подобно амилопектину).
При кислотном гидролизе гликоген превращается в D-глюкозу, т.к.является полисахаридом, образованным за счет a (1®3)-, a (1®4)- и a (1®6)-гликозидных связей, причем (1®6)-связи возникают и в ветвях гликогена. Из-за большей степени разветвленности молекулы гликогена имеют более плотную, более компактную форму, чем молекулы амилопектина. Как и амилопектин, гликоген гидролизуется до мальтозы и изомальтозы; (1®6)-связи гликогена расщепляются бакториальным ферментом пуллуланазой.
Гликоген выполняет важные функции в организме. При недостатке глюкозы в крови происходит быстрый гидролиз гликогена в клетках печени и, наоборот, при избыточном содержании глюкозы начинается синтез гликогена.
Проблема тучности: при содержании гликогена 50-60 г на 1 кг ткани глюкоза перестает расходоваться на синтез гликогена, а идет на образование жира.
Декстраны – запасные полисахариды бактерий и дрожжей. Это поли-a-D-глюкопираноза, цепи которой образуются за счет a (1®6)-гликозидных связей, а многочисленные ответвления за счет a (1®2)-, a (1®3)- и a (1®4)-связей. Молекулярная масса декстранов достигает сотен миллионов. Степень полимеризации и разветвления декстранов зависит от вида продуцирующего их микроорганизма; сырьем для биосинтеза декстранов служит сахароза. Декстраны подобно белкам обладают антигенными свойствами. Используются как заменители плазмы крови после снижения молекулярной массы до 50-100 тыс. с помощью кислотного гидролиза или ультразвука. На основе декстранов производят молекулярные сита – сефадексы, применяемые в фармацевтической промышленности для разделения смесей веществ и очистки.
 Целлюлоза – структурный полисахарид растений, выполняет опорные функции, обладает большой механической прочностью. Целлюлоза содержится в древесине (50-70%), хлопке (до 100%). Целлюлоза – сырье для целлюлозно-бумажной, текстильной промышленности, используется при изготовлении взрывчатых веществ.
Целлюлоза – структурный полисахарид растений, выполняет опорные функции, обладает большой механической прочностью. Целлюлоза содержится в древесине (50-70%), хлопке (до 100%). Целлюлоза – сырье для целлюлозно-бумажной, текстильной промышленности, используется при изготовлении взрывчатых веществ.
Молекула целлюлозы линейна, не имеет разветвлений, состоит из b-D-глюкопиранозных звеньев, соединенных только b (1®4)-гликозидными связями, число звеньев 2,5-12 тыс., молекулярная масса достигает 1-2 млн. остатки D-глюкозы в целлюлозе находятся в кресловидной конформации, что исключает спирализацию полиглюкозидной цепи и предопределяет ее линейное строение:
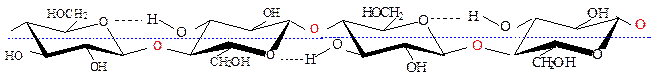
Линейное строение молекул целлюлозы связано в первую очередь с b-конфигурацией аномерного атома углерода. Этому способствует также образование внутримолекулярных водородных связей.
Кроме внутримолекулярных водородных связей молекулы целлюлозы образуют многочисленные межмолекулярные связи. Это приводит к возникновению параллельно расположенных жестких цепей – ленточных структур, похожих на b-слои белков. Это, так называемая, вторичная структура целлюлозы. Благодаря своему строению целлюлоза обладает большой механической прочностью, волокнистостью, нерастворимостью в воде и химической инертностью.
Любопытно, что целлюлоза растворяется в реактиве Швейцера (гидроксид меди (II) в концентрированной растворе аммиака), а также в солянокислом растворе ZnCl2 при нагревании или в концентрированной серной кислоте. Благодаря наличию свободных гидроксильных групп целлюлоза способна реагировать со спиртами и кислотами с образованием эфиров. Так, при нитровании целлюлоза HNO3 образуется нитрат целлюлозы, применяемый в изготовлении взрывчатых веществ, целлулоида, лаков. Ацилирование уксусным ангидридом приводит к образованию белой волокнистой массы, из которой изготавливают искусственный шелк.
Волокна целлюлозы модифицируют введением в ее молекулу карбокси-метильных групп –CH2COOH или диэтиламиноэтильных групп –C2H4N(C2H5)2; в результате получаются карбоксиметилцеллюлоза или диэтиламиноэтилцел-люлоза, которые применяют в хроматографии для разделения аминокислот, белков, нуклеиновых кислот в качестве ионообменных смол.
Целлюлоза при частичном гидролизе образует дисахарид – целлобиозу, а при полном гидролизе – глюкозу. Такой гидролизат используется для получения технического этилового спирта, для выращивания кормовых дрожжей и приготовления некоторых медицинских препаратов.






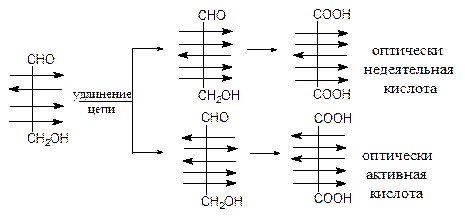 Рассмотрим на примере глюкозы как установить конфигурацию той или иной гексозы. Если в результате укорочения цепи получена арабиноза, то исходным веществом могли быть глюкоза или манноза. Уравнивание концов в применении к рассматриваемому случаю не поможет сделать выбор между указанными гексозами, т.к. обе они при этом дают оптически активные кислоты. Чтобы ответить на вопрос о том, какая из гексоз глюкоза или манноза перед нами, необходимо прибегнуть к последовательному удлинению цепи и уравниванию концов исследуемой гексозы. При этом, как видно из приведенной ниже схемы, глюкоза даст одну оптически деятельную двухосновную кислоту и одну – оптически недеятельную, а манноза - две оптически деятельные.
Рассмотрим на примере глюкозы как установить конфигурацию той или иной гексозы. Если в результате укорочения цепи получена арабиноза, то исходным веществом могли быть глюкоза или манноза. Уравнивание концов в применении к рассматриваемому случаю не поможет сделать выбор между указанными гексозами, т.к. обе они при этом дают оптически активные кислоты. Чтобы ответить на вопрос о том, какая из гексоз глюкоза или манноза перед нами, необходимо прибегнуть к последовательному удлинению цепи и уравниванию концов исследуемой гексозы. При этом, как видно из приведенной ниже схемы, глюкоза даст одну оптически деятельную двухосновную кислоту и одну – оптически недеятельную, а манноза - две оптически деятельные.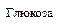





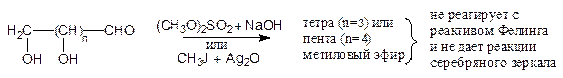
 В тоже время гидролиз этих эфиров разбавленным раствором кислоты, т.е. в условиях, в которых простые эфиры устойчивы, приводил к отщеплению одной метильной группы. Так, из тетраметилового эфира, приготовленного из пентоз, получался триметиловый эфир, а из пентаметилового, приготовленного из гексоз, – тетраметиловый:
В тоже время гидролиз этих эфиров разбавленным раствором кислоты, т.е. в условиях, в которых простые эфиры устойчивы, приводил к отщеплению одной метильной группы. Так, из тетраметилового эфира, приготовленного из пентоз, получался триметиловый эфир, а из пентаметилового, приготовленного из гексоз, – тетраметиловый: С ее участием легко образуются метиловые эфиры. Для получения последних соответствующий моносахарид достаточно обработать метиловым спиртом в присутствии 3%-ного хлористого водорода:
С ее участием легко образуются метиловые эфиры. Для получения последних соответствующий моносахарид достаточно обработать метиловым спиртом в присутствии 3%-ного хлористого водорода: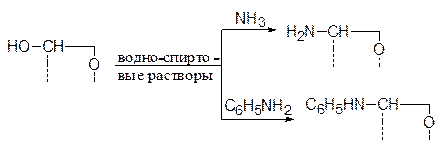



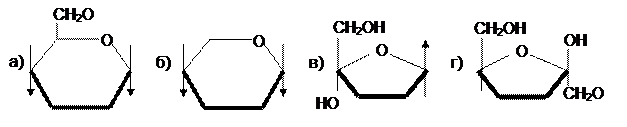

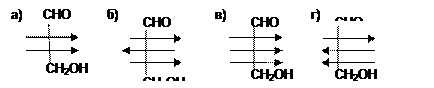
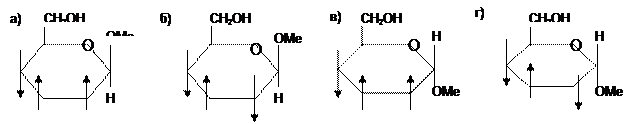
 а) эпимеры б) цис-транс-изомеры
а) эпимеры б) цис-транс-изомеры





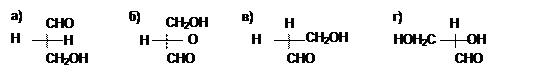


 D-глюкоза … ….
D-глюкоза … …. а) С6Н12О6 + Cu(OH)2 (комн. t)
а) С6Н12О6 + Cu(OH)2 (комн. t) б) С6Н12О6 + HNO3
б) С6Н12О6 + HNO3  в) С6Н12О6 + Ag(NH3)2OH
в) С6Н12О6 + Ag(NH3)2OH  г) С6Н12О6 + Cu(OH)2 (высокая t)
г) С6Н12О6 + Cu(OH)2 (высокая t)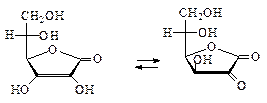
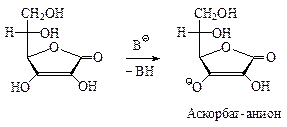 Из химических свойств аскорбиновой кислоты рассмотрим два – наиболее важных. Аскорбиновая кислота проявляет довольно сильные кислотные свойства, обусловленные диссоциацией одной из ОН-групп ендиольного фрагмента. Показатель кислотности рКа 4,2 (сравните, для уксусной кислоты рКа 4,76).
Из химических свойств аскорбиновой кислоты рассмотрим два – наиболее важных. Аскорбиновая кислота проявляет довольно сильные кислотные свойства, обусловленные диссоциацией одной из ОН-групп ендиольного фрагмента. Показатель кислотности рКа 4,2 (сравните, для уксусной кислоты рКа 4,76).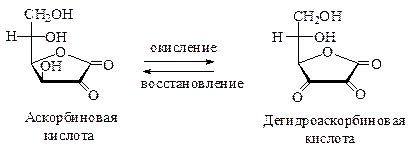

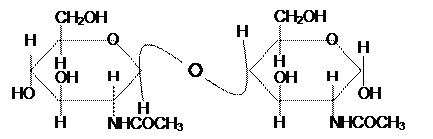

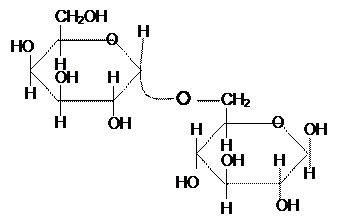
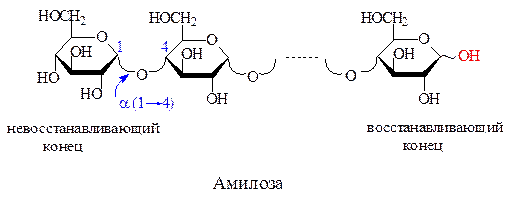
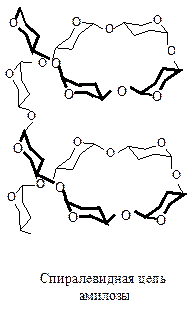 Для молекул амилозы характерна нитевидная форма, т.к. a-D-глюкопираноз-ные звенья имеют ваннообразные конформации, которые способствуют спирали-зации полиглюкозидной цепи. При этом молекулы амилозы свернуты в левую спираль. На каждый виток спирали приходится 6 углеводных звеньев (рис. 2).
Для молекул амилозы характерна нитевидная форма, т.к. a-D-глюкопираноз-ные звенья имеют ваннообразные конформации, которые способствуют спирали-зации полиглюкозидной цепи. При этом молекулы амилозы свернуты в левую спираль. На каждый виток спирали приходится 6 углеводных звеньев (рис. 2).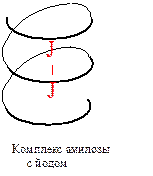

 Амилоза при ферментативном гидролизе образует сначала дисахарид – мальтозу (гидролиз начинается с невосстанавливающего конца амилозы и осуществляется последовательным отщеплением молекул мальтозы), а при полном гидролизе – D-глюкозу.
Амилоза при ферментативном гидролизе образует сначала дисахарид – мальтозу (гидролиз начинается с невосстанавливающего конца амилозы и осуществляется последовательным отщеплением молекул мальтозы), а при полном гидролизе – D-глюкозу.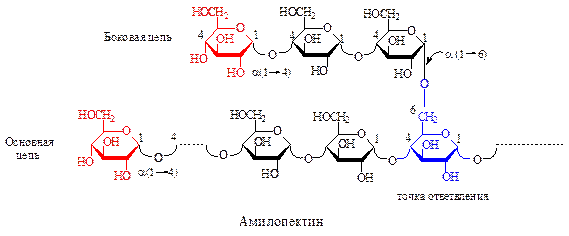 Амилопектин в отличие от амилозы имеет разветвленное строение. Главная и ответвленные цепи содержат a (1®4)-гликозидные связи, а в точках ответв-ления a-(1®6)-гликозидные связи. Между точками разветвления располагаются 20-25 гликозидных остатков. Молекулы амилопектина имеют сферическую фор-му и молекулярной массой от 100 тысяч до нескольких миллионов. Амилопектин – невосстанавливающий полисахарид, с йодом дает красно-фиолетовое окраши-вание, позволяющее отличить фракцию амилопектина от фракции амилозы.
Амилопектин в отличие от амилозы имеет разветвленное строение. Главная и ответвленные цепи содержат a (1®4)-гликозидные связи, а в точках ответв-ления a-(1®6)-гликозидные связи. Между точками разветвления располагаются 20-25 гликозидных остатков. Молекулы амилопектина имеют сферическую фор-му и молекулярной массой от 100 тысяч до нескольких миллионов. Амилопектин – невосстанавливающий полисахарид, с йодом дает красно-фиолетовое окраши-вание, позволяющее отличить фракцию амилопектина от фракции амилозы.

 Целлюлоза – структурный полисахарид растений, выполняет опорные функции, обладает большой механической прочностью. Целлюлоза содержится в древесине (50-70%), хлопке (до 100%). Целлюлоза – сырье для целлюлозно-бумажной, текстильной промышленности, используется при изготовлении взрывчатых веществ.
Целлюлоза – структурный полисахарид растений, выполняет опорные функции, обладает большой механической прочностью. Целлюлоза содержится в древесине (50-70%), хлопке (до 100%). Целлюлоза – сырье для целлюлозно-бумажной, текстильной промышленности, используется при изготовлении взрывчатых веществ.