Соединения включения применяются для разделения смесей. Мочевина, например, позволяет выделить углеводороды нормального строения, которые она связывает в виде соединений включения, а тиомочевина - углеводороды, имеющие разветвленные цепи.
Цеолиты, получаемые с различными заданными размерами полостей, находят промышленное применение для сушки газов, разделения веществ, в ионообменных процессах.
На способности многих газов и легкокипящих жидкостей образовывать соединения включения (клатраты) с водой основаны удобные способы их хранения и разделения.
Включение - метод защиты от окисления на воздухе некоторых нестойких молекул.
Соединения включения используются и в аналитических целях: в адсорбционной и распределительной хроматографии для разделения нитрофенолов, нитроаминов и т.п.
Основные характеристики графита
Углерод имеет несколько аллотропных модификаций, из которых наиболее известны графит и алмаз. Можно упомянуть также карбин - линейные полимерные цепочки (=С=С=С=)n, фуллерены - сферические и эллипсоидальные молекулы (например, С60 и С70), аморфный углерод (сажу, например).
Графит (от греч. γραφειν - пишу) - минерал из класса самородных элементов, одна из аллотропных модификаций углерода. Структура слоистая. Слои кристаллической решётки могут по-разному располагаться относительно друг друга, образуя целый ряд политипов, с симметрией от гексагональной сингонии (дигексагонально-дипирамидальный), до тригональной (дитригонально-скаленоэдрический). Слои слабоволнистые почти плоские, состоят из шестиугольных слоёв атомов углерода. Кристаллы пластинчатые, чешуйчатые.
Графит
|  <http://ru.wikipedia.org/wiki/%D0%A4%D0%B0%D0%B9%D0%BB:GraphiteUSGOV.jpg> <http://ru.wikipedia.org/wiki/%D0%A4%D0%B0%D0%B9%D0%BB:GraphiteUSGOV.jpg>
|
| Формула <http://ru.wikipedia.org/wiki/%D0%A5%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D1%84%D0%BE%D1%80%D0%BC%D1%83%D0%BB%D0%B0>C (углерод <http://ru.wikipedia.org/wiki/%D0%A3%D0%B3%D0%BB%D0%B5%D1%80%D0%BE%D0%B4>)
|
|
| Сингония <http://ru.wikipedia.org/wiki/%D0%A1%D0%B8%D0%BD%D0%B3%D0%BE%D0%BD%D0%B8%D1%8F>Гексагональная (планаксиальная) <http://ru.wikipedia.org/wiki/%D0%93%D0%B5%D0%BA%D1%81%D0%B0%D0%B3%D0%BE%D0%BD%D0%B0%D0%BB%D1%8C%D0%BD%D0%B0%D1%8F_%D1%81%D0%B8%D0%BD%D0%B3%D0%BE%D0%BD%D0%B8%D1%8F>
|
|
| Цвет <http://ru.wikipedia.org/wiki/%D0%A6%D0%B2%D0%B5%D1%82>Серый, чёрный стальной
|
|
| Цвет черты <http://ru.wikipedia.org/wiki/%D0%A6%D0%B2%D0%B5%D1%82_%D1%87%D0%B5%D1%80%D1%82%D1%8B>Чёрная
|
|
| Блеск <http://ru.wikipedia.org/wiki/%D0%91%D0%BB%D0%B5%D1%81%D0%BA>Металловидный
|
|
| Прозрачность <http://ru.wikipedia.org/wiki/%D0%9F%D1%80%D0%BE%D0%B7%D1%80%D0%B0%D1%87%D0%BD%D0%BE%D1%81%D1%82%D1%8C_%D1%81%D1%80%D0%B5%D0%B4%D1%8B>Непрозрачный
|
|
| Твёрдость <http://ru.wikipedia.org/wiki/%D0%A8%D0%BA%D0%B0%D0%BB%D0%B0_%D0%9C%D0%BE%D0%BE%D1%81%D0%B0>1 - 2
|
|
| Спайность <http://ru.wikipedia.org/wiki/%D0%A1%D0%BF%D0%B0%D0%B9%D0%BD%D0%BE%D1%81%D1%82%D1%8C>Совершенная по {0001}
|
|
| Плотность <http://ru.wikipedia.org/wiki/%D0%9F%D0%BB%D0%BE%D1%82%D0%BD%D0%BE%D1%81%D1%82%D1%8C>2,09 - 2,23 г/см³
|
|
Свойства
Хорошо проводит электрический ток <http://ru.wikipedia.org/wiki/%D0%AD%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B9_%D1%82%D0%BE%D0%BA>. В отличие от алмаза <http://ru.wikipedia.org/wiki/%D0%90%D0%BB%D0%BC%D0%B0%D0%B7> обладает низкой твёрдостью <http://ru.wikipedia.org/wiki/%D0%A2%D0%B2%D1%91%D1%80%D0%B4%D0%BE%D1%81%D1%82%D1%8C> (1-2 по шкале Мооса <http://ru.wikipedia.org/wiki/%D0%A8%D0%BA%D0%B0%D0%BB%D0%B0_%D0%9C%D0%BE%D0%BE%D1%81%D0%B0>). Плотность <http://ru.wikipedia.org/wiki/%D0%9F%D0%BB%D0%BE%D1%82%D0%BD%D0%BE%D1%81%D1%82%D1%8C_%D0%B2%D0%B5%D1%89%D0%B5%D1%81%D1%82%D0%B2%D0%B0> 2,08 - 2,23 г/см³. Цвет тёмно-серый, блеск <http://ru.wikipedia.org/wiki/%D0%91%D0%BB%D0%B5%D1%81%D0%BA> металлический. Неплавок, устойчив при нагревании в отсутствие воздуха. В кислотах <http://ru.wikipedia.org/wiki/%D0%9A%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D1%8B> не растворяется. Жирный (скользкий) на ощупь. Природный графит содержит 10-12 % примесей глин и окислов железа.
Графит - наиболее стабильная при обычных условиях модификация, имеет ярко выраженное слоистое строение. В слоях атом углерода прочно связан химической связью с тремя другими, слои связаны друг с другом фактически лишь слабыми ван-дер-ваальсовыми силами. Слои расположены таким образом, что половина атомов одного слоя находится под центрами гексагонов другого, а вторая половина - друг под другом, то есть в графите два вида кристаллографически разных атомов углерода. В обычном гексагональном графите слои расположены точно один под другим через один все четыре валентных электрона участвуют в образовании химических связей в слое. Поэтому кратность связи 1,33.
Однако очень малая часть электронов (примерно 1 на 18 000 атомов) находится в зоне проводимости, формируя металлическую связь между слоями. По этой причине металлическая связь вносит крайне небольшой вклад в энергетику взаимодействия между слоями, которая определяется в основном ван-дер-ваальсовыми силами, но существенным образом определяет свойства графита, такие, как:
· теплопроводность, которая в три раза превышает теплопроводность ртути,
· электропроводность, которая соизмерима с металлической (0,1 от электропроводности ртути),
· характерный металлический блеск графита.
Слоистость структуры определяет ярко выраженную анизотропию свойств:
· электропроводность вдоль направления слоев на два порядка выше, чем перпендикулярно им,
· теплопроводность также гораздо (в пять раз) выше в направлении параллельно слоям,
· коэффициент теплового расширения перпендикулярно слоям примерно в 20 раз больше, чем параллельно им.
Это объясняется тем, что слабая связь между слоями легче расшатывается тепловым движением, чем сильная химическая связь в слоях.
Относительно слабая связь между слоями позволяет широко использовать графит в качестве скользящих контактов для электрических машин, делает графит удобным твердым смазочным материалом для нагретых частей установок и двигателей (однако заметим, что при температурах порядка 25000С и выше графит в значительной мере теряет свои смазочные свойства).
С химической точки зрения графит достаточно инертен: заметное окисление на воздухе начинается лишь при температуре выше 500 0С и даже при воздействии такого агрессивного реагента, как фтор, при комнатной температуре не наблюдалось никаких изменений.
Однако, несмотря на свою достаточно высокую химическую инертность, графит довольно легко дает так называемые интеркалаты (слоистые соединения включения) и с гораздо менее химически активными реагентами.
Структура
 <http://ru.wikipedia.org/wiki/%D0%A4%D0%B0%D0%B9%D0%BB:Hex.jpg>
<http://ru.wikipedia.org/wiki/%D0%A4%D0%B0%D0%B9%D0%BB:Hex.jpg> 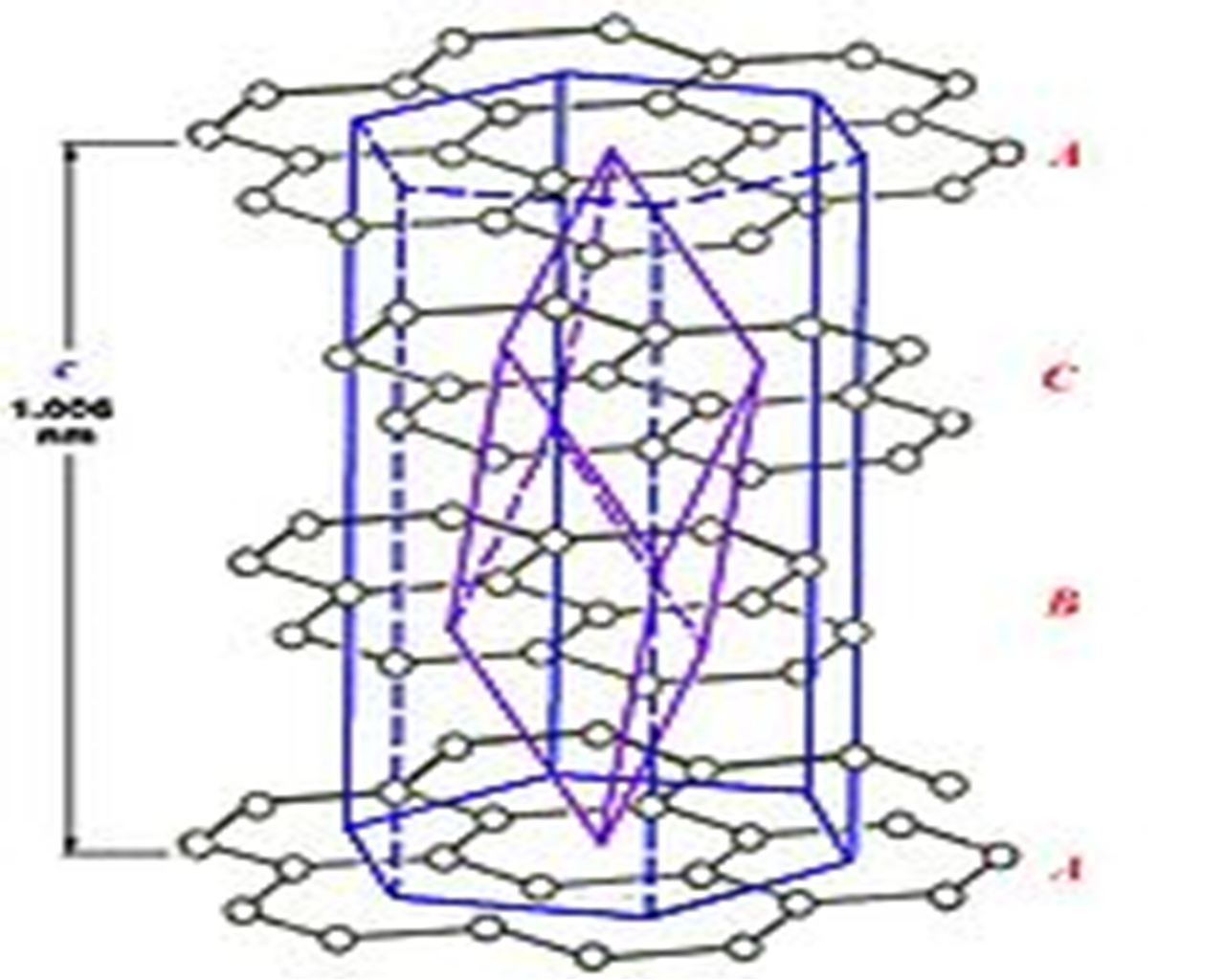 <http://ru.wikipedia.org/wiki/%D0%A4%D0%B0%D0%B9%D0%BB:3R.jpg>
<http://ru.wikipedia.org/wiki/%D0%A4%D0%B0%D0%B9%D0%BB:3R.jpg>
α-графит β-графит
Каждый атом <http://ru.wikipedia.org/wiki/%D0%90%D1%82%D0%BE%D0%BC> углерода <http://ru.wikipedia.org/wiki/%D0%A3%D0%B3%D0%BB%D0%B5%D1%80%D0%BE%D0%B4> ковалентно <http://ru.wikipedia.org/w/index.php?title=%D0%9A%D0%B2%D0%B0%D0%BB%D0%B5%D0%BD%D1%82%D0%BD%D0%BE%D1%81%D1%82%D1%8C&action=edit&redlink=1> связан <http://ru.wikipedia.org/wiki/%D0%A5%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D1%81%D0%B2%D1%8F%D0%B7%D1%8C> с тремя другими окружающими его атомами углерода.
Различают две модификации графита: α-графит и β-графит. Различаются упаковкой слоёв. У α-графита половина атомов каждого слоя располагается над и под центрами шестиугольника, а у β-графита каждый четвёртый слой повторяет первый. Ромбоэдрический графит удобно представлять в гексагональных осях, чтоб показать его слоистую структуру.
β-графит в чистом виде не наблюдается, так как является метастабильной фазой. Однако, в природных графитах содержание ромбоэдрической фазы может достигать 30 %.



 <http://ru.wikipedia.org/wiki/%D0%A4%D0%B0%D0%B9%D0%BB:GraphiteUSGOV.jpg>
<http://ru.wikipedia.org/wiki/%D0%A4%D0%B0%D0%B9%D0%BB:GraphiteUSGOV.jpg> <http://ru.wikipedia.org/wiki/%D0%A4%D0%B0%D0%B9%D0%BB:Hex.jpg>
<http://ru.wikipedia.org/wiki/%D0%A4%D0%B0%D0%B9%D0%BB:Hex.jpg>  <http://ru.wikipedia.org/wiki/%D0%A4%D0%B0%D0%B9%D0%BB:3R.jpg>
<http://ru.wikipedia.org/wiki/%D0%A4%D0%B0%D0%B9%D0%BB:3R.jpg>


