

Своеобразие русской архитектуры: Основной материал – дерево – быстрота постройки, но недолговечность и необходимость деления...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Своеобразие русской архитектуры: Основной материал – дерево – быстрота постройки, но недолговечность и необходимость деления...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...
Топ:
Генеалогическое древо Султанов Османской империи: Османские правители, вначале, будучи еще бейлербеями Анатолии, женились на дочерях византийских императоров...
Установка замедленного коксования: Чем выше температура и ниже давление, тем место разрыва углеродной цепи всё больше смещается к её концу и значительно возрастает...
Выпускная квалификационная работа: Основная часть ВКР, как правило, состоит из двух-трех глав, каждая из которых, в свою очередь...
Интересное:
Средства для ингаляционного наркоза: Наркоз наступает в результате вдыхания (ингаляции) средств, которое осуществляют или с помощью маски...
Инженерная защита территорий, зданий и сооружений от опасных геологических процессов: Изучение оползневых явлений, оценка устойчивости склонов и проектирование противооползневых сооружений — актуальнейшие задачи, стоящие перед отечественными...
Как мы говорим и как мы слушаем: общение можно сравнить с огромным зонтиком, под которым скрыто все...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Белки связи??
1. пептидная – аминокислоты явл амфотерными соединениями и могут взаимодействовать друг с другом. В реакцию вступают карбоксильная и амино группы в рез-те образуется пептидная связь. Соединения содержащие до 8 аминокислот в составе наз пептиды, 8-100 аминокислот – полипептиды, более 100 – белки. Пептидная связь явл очень прочной лежит в основе формирования структуры молекулы белка.
2. доп виды хим связей
В состав белков входят аминокислоты, радикал кот содержит разнообразные хим группы. Эти группы могут реагировать друг с другом и образуют так называемые доп-е виды хим связи.
Водородна я – она образуется при взаимодействии ковалентно-связанного атома кислорода, имеющего отриц заряд и ков связанного атома водорода, имеющего полож заряд. Водородная связь может образовываться при взаимодействии пептидных групп, гидроксильных групп, при взаимодействии гидроксильных и амино групп. Вод связи явл очень слабыми, они легко разрушаются, но легко образуются вновь, среди доп видов явл самой многочисленной.
Дисульфидная – образ при взаим-и сульфгидрильных групп –SH. Эта одна из самых прочных связей их доп-х видов.
Солевые или ионные – обусловлены взаимодействием аминокислот, имеющих основной и кислотный характер.
Гидрофобное взаимодействие – сближение неполярных гидрофильных частей молекулы за счет вытеснения молекул воды и ослабления взаимодействия с ОС.
Структура белковой молекулы
Молекула белка имеет сложную пространственную организацию, в кот различают 4 уровня: первичная, вторичная, третичная и четвертичная структуры.
Первичная структура – опред-ся порядком чередования аминокислотных остатков полипептидной цепи. Структура образована пептидными связями и явл очень прочной. Эта структура явл основной и определяет все остальные уровни структурной организации молекулы белка. Информация о первичной структуры белка заключается в молекулах ДНК в виде генов.
|
|
Вторичная – ориентация полипептидной цепи в пространстве, происходит образование спиралевидной или складчатой структуры. Различают 3 разновидности втор структуры: альфа-спираль(полипептидная цепь закручивается вокруг оси), бета-структура(складчатый слой, отдельные участки цепи располагаются параллельно друг другу), неупорядоченный клубок. Вторичная структура поддерживается водородными связями, кот образ-ся между аминокислотными остатками расположенными на небольшом расстоянии друг от друга в полипептидной цепи.
Третичная – это упаковка спирали в небольшом объеме пространства поддерживается всеми доп видами хим связей, причем связи обр-ся между остатками аминокислот, находящихся на значительном расстоянии друг от друга в полипептидной цепи. В зав-ти от формулы молекулы белки бывают глобулярные и фибриллярные.
Глобулярные(округлые) имеют соотношение длины и ширины менее 1/50. Многие из этих белков растворимы в воде, обладают ферментативной активностью.
Фибриллярные(нитевидные) соотношение длины и ширины более чем 1/50. Такие белки входят в состав волос, шерсти, выполняют сократительные ф-и.
Четвертичная – это ассоциация нескольких полипептидных цепей в одну молекулу. Структура поддерживается всеми доп видами хим связи. Белки, имеющие четвертичную структуру наз олигомерами, а отдельные полипептидные цепи – субъединицы или протомеры. Основной структурой явл вторичная, а свойства и ф-и белков зависят от третичной и четвертичной структур.
Строение молекулы ДНК.
При изучении состава ДНК было установлено, что количество пуриновых азотистых оснований соответствует количеству пиримидиновых: А+Г=Т+Ц. Эта закономерность получила название – правило Чаргаффа. На основании этой закономерности в 1953г была разработана модель строения ДНК. Согласно этой модели ДНК состоит из 2х полинуклеотидных цепей закрученных вокруг общей оси. Сахарофосфатные связи нах-ся снаружи, а азотистое основание внутри спирали перпендикулярно оси. Полинуклеотидные цепи поддерживаются водородными связями, кот возникают между строго определенными парами азотистых оснований. Против аденина одной цепи всегда располагается тимин другой цепи и между ними образуется две водородные связи А-Т. Против Г одной цепи нах-ся Ц др цепи и между ними образ 3 водородные связи Г-Ц. эта закономерность наз правилом комплиментарности.
|
|
Хим св-ва моносахаридов.
При восстановлении моносахаридов образуются соответствующие многоатомные спирты, так как восстановлению подвергается альдегидная или кетонная группа. В растениях сорбит, который образуется при восстановл.глюкозы или фруктозы,при восстан.рибозы-рибит.
Взаимодействие со спиртами. Сахара, являясь производными спиртов, могут взаимодействовать со спиртами с образованием простых эфиров типа R—О—R1 с выделением воды.Если реакция проходит только с участием гликозидного гидрооксила, то образовавшаяся структура носит название гликозида. В этом случае вновь образовавшаяся связь называется гликозидной.в растениях гликозиды выполняют защитную ф-ию, тк обладают горьким запахом/вкусом,токсичные. Взаимодействие с кислотами.Моносахариды, являясь производными спиртов, могут взаимодействовать с кислотами с образованием сложных эфиров. Наиболее важные производные — фосфорные эфиры сахаров – сахарофосфаты.Донор фосфорной кислоты — АТР, в молекуле которой расщепляется высокоэнергетическая связь. Под действием фермента гексокиназа остаток фосфорной кислоты переносится на глюкозу к первому углеродному. Окисление моносахаридов.при окисл.моносахариды образуют карбоновые к-ты.,в зависимости от усл.окисления образуются разные типы к-т,если окисл.альдегидная группа образуются альдоновые к-ты,если окисл.первичная спиртовая группа образ.уроновые к-ты,если окисл.и альдегидн.и первичн.спирт.группы,то образ. Дикарбоновые к-ты. полимеризация. взаим. друг с другом,образуя полисахариды,по хим природе полисахариды являются простыми эфирами,а образующаяся связь-гликозидной. восстанавливающие сахара.все монои полисахариды 1ого порядка,имеющие свободный гликозидный гидроксил,способны восстанавливать оксиды металлов до металла или до оксидов с меньшей степенью окисления-восстанавливающие или редуцирующие сахара. изомеризация. может протекать по типу альдоза-кетоза в этой р-ии учавствуют сахарофосфаты.фосфорные эфиры способны к мутаротации те перемещению фосфатной группы внутри молекулы.эпимеризация происходит изменение конформации при одном из ассиметрических атомов углерода,эти процессы протекают при участии сахарофосфатов. Взаимодействие моносахаридов с аминокислотами.Под влиянием повышенных температур, кислой или щелочной рН среды, высокой влажности, характерных для многих технологических процессов, например при выпечке хлеба, тепловой сушке, стерилизации консервов, ферментации табака и чая, старении коньяка моносахариды участвуют в реакциях неферментативного характера, вызывающих потемнение обрабатываемых продуктов. Эти реакции получили название реакций меланоидинообразования.
|
|
При меланоидинообразовании происходит взаимодействие восстанавливающих сахаров — моносахаридов, дисахаридов и продуктов гидролиза полисахаридов с аминокислотами, пептидами и белками с образованием темноокрашенных продуктов — меланоидинов, как правило, трудно или нерастворимых в воде.Химизм реакции до конца не установлен. Считают, что на первом этапе происходит разложение исходной аминокислоты и реагирующей с ней восстанавливающего сахара. Из аминокислоты образуется соответствующий альдегид, аммиак и углекислый газ, а из сахара фурфурол или оксиметилфурфурол. Альдегиды обладают определенным запахом и придают аромат пищевым продуктам. Фурфурол или оксиметилфурфурол далее реагируют с другой аминокислотой с образованием желто-коричневых пигментов.Из аминокислот легче всего вступает в эту реакцию самая дефицитная аминокислота лизин, из-за чего снижается биологическая ценность продукта.
26.полисахориды 1ого порядка.мальтоза целлобиоза лактоза. Мальтоза С12Н22О11 состоит из двух остатков -D-глюкопиранозы, соединенных гликозидной связью альфа1 -4.Мальтоза в свободном состоянии в растениях содержится в небольшом количестве, но появляется при прорастании, так как она образуется при гидролитическом расщеплении крахмала. В нормальном зерне и муке она отсутствует. Наличие ее в муке говорит о том, что эта мука получена из проросшего зерна. Большое количество мальтозы содержится в солоде, который применяется в пивоварении, поэтому мальтозу называют также солодовым сахаром. Под действием фермента -глюкозидазы (мальтазы) мальтоза подвергается гидролизу до D-глюкозы. Мальтоза сбраживается дрожжами. Лактоза С12Н22О11 построена из -D-галактопиранозы и D-глюкопиранозы, соединенных между собой бета1- 4 гликозидной связью. В растениях она встречается редко.В большом количестве (4…5 %) лактоза содержится в молоке, поэтому ее называют молочным сахаром. Это восстанавливающий сахар со слабым сладким вкусом. Сбраживается лактозными дрожжами до молочной кислоты.
|
|
Целлобиоза С12Н22О11 состоит из двух остатков бета-D-глюкопиранозы, соединенных между собой бета1- 4 гликозидной связью.
Она служит структурным компонентом полисахарида целлюлозы и образуется из нее при гидролизе под действием фермента целлюлазы. Этот фермент продуцируется рядом микроорганизмов, а также он активен в прорастающих семенах.
27.строение и св-ва сахарозы. Производная альфа глюкозы и бета фруктозы,соедненных альфа1-бета2 гликозидной связью. Широко распростр. В природе,много в корнеплодах сахарной свеклы от 14-20 прицентов. Сахарный тростник 14-25 проц.. сахароза не содержид гликозидного гидроксила является невосстан.сахаром и хим инертна,в растениях выполняет транспортную ф-ию,перенесит глюкозу из мест синтеза. по проводящим пучкам растения сахароза перемещается со скоростью 20-30см/ч, обладает сладким вкусом,ристворима в воде,при нагреве до 200 и выше дегитратация сахарозы с обаз карамели. При к-тном или ферментативном гидролизе сахароза распадается на глюкозу и фруктозу 1:1-инвертный сахар.
28. Полисахарариды 2-ого порядка. Характеристика запасных полисахаридов. Крахмал (С6Н10О5)n является важнейшим представителем полисахаридов в растениях. Этот запасной полисахарид используется растениями как энергетический материал. Крахмал в животном организме не синтезируется, аналогичным запасным углеводом у животных является гликоген.
Крахмал в больших количествах содержится в эндосперме злаков — 65…85 % его массы, в картофеле — до 20 %.
Крахмал не является химически индивидуальным веществом. В его состав кроме полисахаридов входят минеральные вещества, в основном представленные фосфорной кислотой, липиды и высокомолекулярные жирные кислоты — пальмитиновая, стеариновая и некоторые другие соединения, адсорбированные углеводной полисахаридной структурой крахмала.
|
|
В клетках эндосперма крахмал находится в виде крахмальных зерен, форма и размер которых характерны для данного вида растения. Форма крахмальных зерен дает возможность легко распознать крахмалы различных растений под микроскопом, что используется для обнаружения примеси одного крахмала в другом, например при добавлении кукурузной, овсяной или картофельной муки к пшеничной.
В запасающих тканях различных органов — клубнях, луковицах более крупные крахмальные зерна откладываются в запас в амилопластах как вторичный (запасной) крахмал. Крахмальные зерна имеют слоистую структуру.
Крахмал является сложным соед состоящим из углеводной и неуглеводной частей,неуглеводная составляет от 2 до 6 проц. И представлена фосфорной к-той\липидами,высокомолекулярными жирными к-тами. Углеводная часть состоит из полисахаридов 2х типов амилозы и амилопектина,которые являются полимерами альфа глюкозы,амилоза-линейная часть крахмала,состоит из остатков альфа глюкозы,сое.альфа1-4гликозидной связью,кол-во остатков глюкозы от 100 до нескольких тыс. молекула амилозы имеет 1 восстанавливающий и 1 не восстан.концы. при взаим с йодом амилоза окрашивается в синий цвет. Амилопектин разветленный компонент крахамла,содерж.до 50тыс остатков альфа глюкозы соединяется главным образом альфа 1-4гликозидн.связью.
Инулин запасной полисахарид растений,полимер бета фруктозы,образован связями бета 2-1. На концах молекулы присутствует сахароза. Накапливается в подземных частях растений, содерж.в клубнях топинамбура,корневищах георгина,артишок.
29. Полисахарариды 2-ого порядка. Характеристика структурных полисахаридов. Целлюлоза (С6Н10О5) – полисахарид второ-го порядка, является основным компонентом клеточных стенок. Целлюлоза состоит из остатков бета-D-глюкозы, соединенных между собой бета1- 4 гликозидной связью.Среди других полисахаридов, из которых состоит клеточная стенка растений, он относится к микрофибриллярным полисахаридам, так как в клеточных стенках молекулы целлюлозы соединены в структурные единицы, получившие название микрофибрилл. Последняя состоит из пучка молекул целлюлозы, расположенных по ее длине параллельно друг другу. Содержание целлюлозы в растениях колеблется в широких пределах: в волокнах хлопчатника 90 %, древесине 50, листьях табака 10, семенах злаковых культур 3…5, подсолнечника 2, ягодах винограда 1 %.
В среднем на одну молекулу целлюлозы приходится около 8000 остатков глюкозы. Гидроксилы у атомов углерода С2, С3 и С6 не замещены. Повторяющееся звено в молекуле целлюлозы — остаток дисахарида целлобиозы.Целлюлоза не растворяется в воде, но в ней набухает. Свободные гидроксильные группы способны замещаться на радикалы — метильный —СН3 или ацетальный с образованием простой или сложноэфирной связи. Это свойство играет большую роль при изучении строения целлюлозы, а также находит применение в промышленности при производстве искусственного волокна, лаков, искусственной кожи и взрывчатых веществ.
У большинства животных и человека целлюлоза не переваривается в желудочно-кишечном тракте, так как в их организме не вырабатывается целлюлаза — фермент, гидролизующий 4 гликозидную связь. Этот фермент синтезируется различного рода микроорганизмами, вызывающими гниение древесины. Целлюлозу хорошо переваривают термиты, потому что в их кишечнике живут симбиотические микроорганизмы, вырабатывающие целлюлазу.В кормовые рационы крупного рогатого скота включают целлюлозу (в составе соломы и других компонентов), так как в их желудке находятся микроорганизмы, синтезирующие фермент целлюлазу.
Значение целлюлозы
Промышленное значение целлюлозы огромно — производство хлопчатобумажных тканей, бумаги, деловой древесины и целый ряд химических продуктов, в основе которых лежит переработка целлюлозы.
Классификация липидов
В зависимости от способов и приемов обезжиривания, вида растворителя, характера подготовки материала к обезжириванию различают следующие группы липидов:
– свободные липиды, извлекаемые неполярными безводными растворителями;
– связанные липиды, извлекаемые гидрофильными полярными растворителями или их смесями (хлороформ, этанол, ацетон), разрушающими непрочные белково-липидные и гликолипидные соединения и высвобождающие липиды;
– прочносвязанные липиды, извлекаемые после обработки растительного материала спиртовым раствором щелочи при кипячении для разрушения прочных комплексов липидов с нелипидными соединениями; при этом происходят гидролиз и омыление липидов щелочью.
По строению и способности к гидролизу липиды подразделяют на омыляемые и неомыляемые (рис. 1).
Омыляемые липиды в результате гидролиза распадаются на несколько (обычно не более четырех) структурных компонентов, а при взаимодействии с щелочами образуют соли жирных кислот — мыла. Обязательной химической структурой омыляемых липидов служит сложноэфирная связь между спиртовой группой и ацилом — остатком жирной кислоты. Поэтому омыляемые липиды имеют второе название — ацильные липиды.
Ацильные липиды подразделяют на нейтральные и полярные.
Нейтральные липиды включают ацилглицеролы — три-, ди- и моноацилглицеролы, представляющие собой сложные эфиры жирных кислот и трехатомного спирта — глицерола, и воски — сложные эфиры жирных кислот и одно- или двухатомных спиртов с длинной углеродной цепью. Полярные липиды включают фосфолипиды и гликолипиды, сложные эфиры жирных кислот и спиртов с замещающими группами. В составе фосфолипидов один из ацилов замещен на ортофосфорную кислоту с присоединенной группой — чаще всего остатком холина, серина или этаноламина. В составе гликолипидов один из ацилов замещен одной или двумя молекулами галактозы или другими углеводами.
Неомыляемые липиды (или изопреноиды) представляют собой или короткие полимерные цепи, состоящие из звеньев изопрена, к которым присоединены простые органические молекулы, или производные изопрена. К группе неомыляемых липидов относят стеролы, каротиноиды, хлорофиллы, жирорастворимые витамины, госсипол и многие другие изопреноидные соединения. функции липидов
1Энергетическая функция. При окислении 1 г нейтральных жиров (триацилглицеролов) выделяется около 38 кДж энергии.
2Защитная функция. Липиды (воски) образуют защитные водоотталкивающие и термоизоляционные покровы растений, их семян и плодов. Высокая твердость восков и их химическая инертность защищают растения от механических повреждений и разрушения ферментами микроорганизмов, предотвращают избыточное испарение воды в листьях и плодах.
3Структурная функция. Липиды — главные структурные компоненты клеточных мембран, образуют двойные слои полярных липидов, в которые встраиваются белки-ферменты.
4 Регуляторная функция. Липидами являются жирорастворимые витамины и производные некоторых жирных кислот.
Строение и св-ва жира.
Триацилглицеролы ТАГ жиры являются сложными эфирами трехатомного спирта глицерола и высокомолекул.жирных к-т. В растениях преимущественно синтезируются не насыщенные жирные к-ты,в животных-насыщенные. В зависимости от жирнокислотного состава по консистенции жиры бывают жидкие и твердые. Жидкие-масла содерж.ненасыщ.жирные к-ты,в основном растительного происхожд. Животные жиры-твердые т к содерж.насыщ. жиные к-ты,могут накапливаться в растениях. Жидкое растит. Масло можно превратить в твердое путем насыщения двойных связщей водоодом-гидрогенизация. Св-ва ТАГ. Легче воды,нерастворимв в ней,на ее поверхности могут оразовывать пленки. Способны сорбировать газы,летучие в-ва,эфиры и масла,но сами не летучи,при кипячении с р-рами к-т распадаются по месту сложно эфирной связи с обазованием глицерола и жирных к-т. При щелочном гидролизе-омылении,образуется глицерол и соли жирных к-т-мыла.
Качество жиров и масел характеризуется следующими показателями или числами:
– кислотное число (к. ч.) — это количество миллиграммов едкого кали, необходимое для нейтрализации свободных жирных кислот, содержащихся в 1 г масла или жира. Кислотное число является гостированным показателем масла или жира и характеризует качество масел и жиров, оценивая степень гидролиза ТАГ ферментом липазой;
– число омыления (ч. о.) — это количество миллиграммов едкого кали, необходимое как для омыления жирных кислот в составе ТАГ, так и для нейтрализации свободных жирных кислот в 1 г исследуемого масла или жира;
– йодное число (й. ч.) — это количество граммов йода, эквивалентное галоиду, присоединившемуся по месту двойных связей к 100 г исследуемого масла или жира. Присоединение йода происходит по месту двойных связей, поэтому йодное число является показателем степени ненасыщенности жирных кислот. Чем выше йодное число, тем они ненасыщеннее и тем легче масло или жир будут высыхать и быть пригодными для изготовления лаков и красок.
Альфа окисление жирных к-т.
Углеродный скелет жирной к-ты уменьшается на 1 атом, в результате образуется жирная к-та,имеющая на 1 атом меньше,чем исходная,выделяется углекислый газ,и небольшое кол-во энергии. В этом процессе учавствует декарбоксилаза,особая пероксидаза и дегидрогиназы небелковой частью является НАД. В кач-ве промежуточного продукта образуется альдегид,который под действием дегидрогиназы превращается в к-ту. Биологич значение альфа окисления заключается в том,что образуется жирные к-ты с нечетным числом атомов углерода. Процесс альфа окисл происходит до образования лауриновой к-ты
Бета окисление жирных к-т
низкомолекулярн жирн к-ты имеющие С меньше 12 подвергаются бета окислению. Бета окисл. Спец форма окисления жирных к-т в этом процессе учавствует кофермент А. Со А и все промежуточные продукты являющиеся тиоэфирами Со А. процесс бета окисления сопровождается выделением большого кол-ва энергии. 1 стадия-активация жирной к-ты путем присоед Со А в рез-те образуется макроэргическая связь за счет исп-я 1 молекулы АТФ образуется ацил кофермент А. 2 стадия окисление активированной жирной к-ты под действием аэробной дегидрогеназы происходит отщепление 2х атомов в рез-те между альфа и бета углеродными атомами обр-тся 2 связь,это соед альфа,бета ненасыщенный кофермент А.
Фосфолипиды.
Фосфолипиды. Относятся к классу сложных липидов и являются производными ацилглицеролов, в которых одна из жирных кислот замещена фосфорной кислотой с присоединенным к ней азотистым основанием. Из азотистых оснований, входящих в состав фосфолипидов, наибольшее распространение получил аминоспирт холин – сильное основание, легкорастворимое в воде и спирте, но нерастворимое в эфире. Его можно рассматривать как производное NН4ОН, в молекуле которого три атома водорода замещены метильными группами —СН3, а четвертый атом — остатком этилового спирта. Холин играет важную роль в обмене веществ, так как под действием соответствующих ферментов он может передавать содержащиеся в нем метильные группы другим веществам. Фосфолипиды, содержащие холин, называются фосфатидилхолином (лецитином). Существуют также фосфатидилэтаноламины, которые вместо холина содержат этаноламин СН2ОН — СН2NН2, и фосфатидилсерины, содержащие аминокислоту серин. В семенах масличных растений обнаружены также фосфолипиды, у которых замещающая группа состоит из глицерола, из двух и более дисахаридов; известны фосфатидилинозитолы, содержащие спирт мио-инозит. Особую группу составляют фосфолипиды, у которых вместо глицерола содержится аминоспирт сфингозин (сфингофосфолипиды) Фосфолипиды, не содержащие азотистого основания, носят название фосфатидных кислот. Они содержатся в растениях в виде солей металлов (чаще всего кальциевых или магниевых).
Жирнокислотный состав фосфолипидов отличается большей насыщенностью по сравнению с жирнокислотным составом ТАГ соответствующего масла. Чистые фосфолипиды представляют собой белые воскообразные вещества, желтеющие на воздухе в результате окисления ненасыщенных жирных кислот. Они хорошо растворимы в большинстве неполярных органических растворителей и масле.
Молекулы фосфолипидов обладают выраженной полярностью. Тот конец молекулы, где расположен остаток азотистого основания и который обладает гидрофильными свойствами, называют «головой». Остальную часть молекулы, на которой располагаются остатки жирных кислот, называют «хвосты». «Хвосты» обладают гидрофобными свойствами (рис. 2, в).
Благодаря этому фосфолипиды в растворах образуют слоистые структуры, которые играют очень важную роль в построении структур протоплазмы — клеточных биомембран. Фосфолипиды — природные антиоксиданты, они предохраняют масла от окисления, легко окисляясь сами.
Наибольшее количество фосфолипидов содержится в семенах сои — 1,5...2,0 % массы семян. В промышленных растительных маслах содержание фосфолипидов колеблется в зависимости от условий, при которых было получено масло. Наибольшее их количество содержится в экстракционном масле. Для выделения фосфолипидов из растительных масел их подвергают гидратации — обработке небольшим количеством воды. Гидратируясь, фосфолипиды теряют способность растворяться в масле и выпадают в осадок.
Фосфолипиды как эмульгаторы широко применяются в пищевой промышленности при изготовлении шоколада, маргарина, майонеза и в качестве веществ, предохраняющих жиры от окисления и порчи.
ВОСКИ
Они представляют собой сложные смеси высокомолекулярных липидов, жирных кислот и спиртов. Они содержатся в кутикуле клеток. Состав смеси у разных растений различен. Преобладающим компонентом являются сложные эфиры жирных кислот с С20 — С24 атомами углерода в цепи и спиртов с С24 — С28 углеродными цепями. В восках высокое содержание неэтерифицированных спиртов жирного ряда и жирных кислот. Обычными компонентами восков являются также углеводороды С29 — С31 с нечетным числом атомов углерода, кетоны и другие окисленные продукты. Известно два типа восков — простые и сложные. К простым относятся эфиры нормальных первичных спиртов. Сложные воски представляют собой эфиры разветвленных одно- и двухатомных спиртов и разветвленных жирных или оксикислот. Известны также цветные воски — производные жирных кислот и двухатомных спиртов каротиноидной природы. Кроме жирных кислот и алифатических спиртов в восках присутствуют углеводороды парафинового ряда.
Как уже отмечалось, из-за высокой молекулярной массы составляющих их жирных кислот и спиртов при обычной температуре воски имеют твердую консистенцию. Они покрывают тонким слоем листья, стебли, стволы и плоды растений, предохраняя их от переувлажнения и высыхания, механических повреждений и неблагоприятного воздействия на них микробов.
Воски обнаружены в плодовых и семенных оболочках всех масличных растений. Так, в семянке подсолнечника содержание восков составляет 1,2…1,3 % от массы, в том числе в плодовой оболочке до 83 % от их общего содержания, в семенной оболочке — до 16 % и в ядре семян — до 1 %. Наличие восков затрудняет получение высококачественных растительных масел. Для получения прозрачного подсолнечного масла проводят трудоемкую обработку — вымораживание восков.
Дыхание и брожение
Для осуществления всех реакций в живых организмах требуется постоянный приток энергии. Основным источником энергии в живой клетке является дыхание.Дыхание — это окислительно-восстановительный процесс расщепления (диссимиляции) органических веществ (углеводов, липидов) с выделением энергии. При окислении высвобождается та энергия, которую аккумулировали зеленые растения в процессе фотосинтеза.
Общее ур-е дыхания:С6Н12О6 + 6О2 6СО2 + 6Н2О + 2780 кДж
Это уравнение аэробного дыхания. Наряду с этим существуют организмы более древние в эволюционном отношении, у которых процесс окисления органических веществ идет в анаэробных условиях. Этот тип окисления впервые был изучен у микроорганизмов и получил название «брожение».
Различают три основные типа брожения:
1 Спиртовое С6Н12О6 2С2Н5ОН + 2СО2 + Q кДж;
Лежит в основе производства вина, пива, хлеба
2 Молочнокислое. Играет большую роль при изготовлении молочнокислых продуктов, кваса, хлебных заквасок, квашении овощей, получении молочной кислоты..3 Маслянокислое
С6Н12О6 СН3СН2СН2СООН + 2Н2 + 2СО2 + Q кДж
Вследствие неприятного вкуса и запаха масляной кислоты не находит применения, но оно вызывает порчу пищевых продуктов: картофеля, овощей, вспучивание сыра, прогоркание масла.Кроме этих основных видов брожения в природе существуют пропионовокислое, уксуснокислое, ацетоновое и другие виды. Для растений, животных и человека характерен аэробный распад углеводов.
40 влияние различных факторов на интенсивность дыхания растительного сырья.
Чаще всего интенсивность дыхания оценивают по количеству диоксида углерода, выделенного растительным материалом в единицу времени. Размерность интенсивности дыхания — мг СО2 на 100 г материала в час или за сутки.
На интенсивность дыхания влияют следующие факторы:
1 Влияние влажности сырья.Интенсивность дыхания зависит в первую очередь от влажности хранящегося сырья. С увеличением влажности сырья интенсивность дыхания возрастает. Вначале это увеличение незначительно. Интенсивность дыхания резко возрастает при достижении влажности сырья выше критического значения. Это объясняется тем, что в растительных клетках от нуля W0 до Wкр влага находится в связанном с коллоидами (углеводами, белками) состоянии и не может активно участвовать в биохимических реакциях. После достижения Wкр в клетках появляется «свободная» влага, наличие которой приводит к резкому возрастанию активности гидролитических, окислительных и других ферментативных систем, вследствие чего интенсивность дыхания также резко увеличивается.
Величина критической влажности зависит главным образом от соотношения в растительном сырье гидрофильных и гидрофобных соединений, т. е. от содержания гидрофильных белков и углеводов и гидрофобных липидов. Именно поэтому Wкр семян масличных растений имеет более низкие значения по сравнению с зерном злаковых.
Уровень критической влажности для гидрофильной части семян или зерна любых растений будет находиться в относительно узких пределах, изменяясь от 13 до 15 %. Существует формула пересчета критической влажности для масличных семян в зависимости от величины массовой доли липидов — масличности семян:
Wкр = 14,5 (100 – М)/100,
где М — масличность семян, % на СВ.
2 Влияние температурыНа интенсивность дыхания влияет температура. С повышением температуры интенсивность дыхания возрастает до оптимальной температуры, которая лежит в пределах от 40 до 60 °С. При температуре выше оптимальной происходит денатурации белков ферментативных систем и, как следствие, снижается интенсивность дыхания.
Величина оптимальной температуры очень сильно зависит от влажности хранящегося сырья. С повышением влажности оптимум температуры, соответствующей максимуму интенсивности дыхания, смещается в сторону более низких температур.
3 Влияние газового состава атмосферы.Интенсивность дыхания зависит от газового состава атмосферы, окружающей хранящееся сырье. С повышением количества кислорода интенсивность дыхания возрастает. Большое количество азота и диоксида углерода угнетает дыхание, снижая скорость окисления органических веществ.
Для лучшей сохранности растительное сырье, особенно дорогостоящие тропические и субтропические плоды и фрукты, хранят в регулируемых средах (РГС). При применении РГС обязательным условием является отвод паров воды и диоксида углерода из массы хранящегося сырья. Это исключает возможность развития в сырье анаэробных процессов, в том числе брожения.
4 Влияние возраста.Интенсивность дыхания зависит от возраста организма. В молодом организме, например недозрелом зерне, с большей скоростью протекают обменные реакции и дыхание идет с большей интенсивностью.
ДЫХАТЕЛЬНЫЙ КОЭФФИЦИЕНТ — отношение объема выделенной углекислоты к объёму поглощенного кислорода.
Химизм спиртового брожения.
биохимический процесс превращения углеводов в этиловый спирт и углекислый газ.Спиртовое брожение вызывают дрожжи, а также некоторые плесневые грибы и бактерии. Типичное брожение с высоким выходом спирта наблюдается в результате жизнедеятельности культурных дрожжей (сахаромицес).В промышленном производстве спирта используют различные материалы: пшеницу, рожь, ячмень, кукурузу, картофель, свеклу, древесные опилки, солому и т. Клетчатку соломы и древесных опилок предварительно подвергают кисличному гидролизу, а крахмал зерновых злаков - осахариванию солодом.Химизм спиртового брожении зависит от характера субстрата, концентрации в нем сахара, реакции среды (pH), вида и расы дрожжей, окружающей температуры, Наибольший выход спирта отмечают в результате аппаратного брожения.В бродильной промышленности используются дрожжи верхового и низшего брожения. Верховое брожение лучше развивается при температуре 18-30°; протекает бурно, с обильным выделением углекислого газа, пенообразованием и появлением пленки на поверхности субстрата.Дрожжи верхового брожения применяют в спиртовой промышленности и хлебопечении. Низовое брожение совершается спокойно; его используют в пивоварении; развивается оно при низкой температуре (4 - 10°) с постепенным просветлением субстрата. Дрожжи обычно оседают на дно сосуда. Реакция спиртового брожения подобна гликолизу. Расхождение начинается только после образования пирувата. Конечный этап гликолиза заменяется двумя ферментативными реакциями. Сначала пируват подвергаетсядекарбоксилированию, продуктом которого является ацетальдегид. Данная реакция происходит при участии пируватдекарбоксилазы, ТПФ и ионов магния.
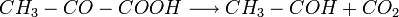
После ацетальдегид восстанавливается водородом, который отщепляется откофермента NADH. При этом ацетальдегид восстанавливается до этанола. Собственно, цель спиртового брожения — это окисление NADH, чтобы он мог снова принять участие в гликолизе. Катализатором являетсяалкогольдегидрогеназа.
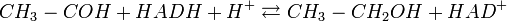
Таким образом, продуктами спиртового брожения являются этанол и со2, а не молочная кислота, как вмолочнокислом брожении.
В результате получается реакция:
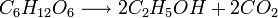
Спиртовое брожение сопровождается запасанием энергии в виде АТФ. Суммарно реакцию можно записать так:
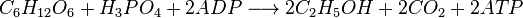
При введении специфических ингибиторов формы брожения спиртового изменяются.
Фотосинтез его значение
Происходящий за счет световой энергии процесс усвоения диоксида углерода зеленым растением и образования органического вещества получил название фотосинтеза. Этот процесс – основной источник органических соединений на нашей планете. В процессе фотосинтеза СО2 под влиянием солнечного света, поглощенного хлорофиллом, восстанавливается до гексозы и выделяется свободный кислород.
Суммарное уравнение фотосинтеза имеет следующий вид:
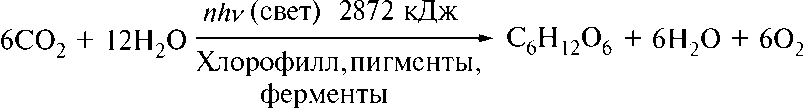
Количество световой энергии, затрачиваемой при фотосинтезе на образование одного моля гексозы, равно 2870 кДж (при дыхании эта энергия выделяется).
Значение фотосинтеза:
1 Является основным источником кислорода на нашей планете.
2 В результате фотосинтеза образуются все органические соединения: углеводы, белки, липиды и т.д.
3 В продуктах фотосинтеза накапливается огромное количество энергии. Ежегодно в результате фотосинтеза усваивается из атмосферы 3,5×1011 т диоксида углерода, выделяется в атмосферу 2,5×1011 т кислорода и образуется 2,3×1011 т органических веществ (в пересчете на сухое вещество).
4 Утилизирует диоксид углерода, предотвращая быстрое развитие парникового эффекта.
Фотосинтез свойственен не только зеленным растениям, но и низшим эукаротическим формам, таким, как водоросли. Обладают способностью к фотосинтезу и некоторые прокариоты (например цианобактерии и некоторые другие). Не менее половины всего фотосинтеза на Земле протекают в морях, озерах и реках, где его осуществляют множество самых разнообразных микроорганизмов, составляющих фитопланктон. Строение хлорофилла
Фотосинтез у высших зеленых растений протекает в специализированных внутриклеточных органеллах — хлоропластах, способных доставлять энергию для метаболических процессов только в дневные часы.
В молекуле хлорофилла, присутствующего в хлоропластах клеток
|
|
|

Автоматическое растормаживание колес: Тормозные устройства колес предназначены для уменьшения длины пробега и улучшения маневрирования ВС при...

Таксономические единицы (категории) растений: Каждая система классификации состоит из определённых соподчиненных друг другу...

Типы оградительных сооружений в морском порту: По расположению оградительных сооружений в плане различают волноломы, обе оконечности...

Наброски и зарисовки растений, плодов, цветов: Освоить конструктивное построение структуры дерева через зарисовки отдельных деревьев, группы деревьев...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!