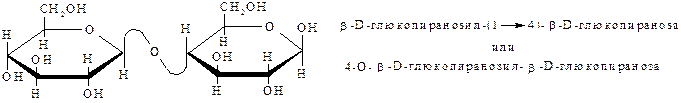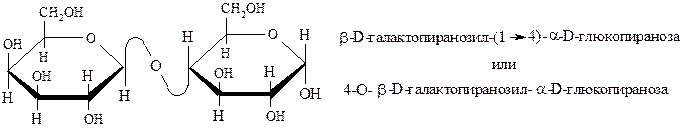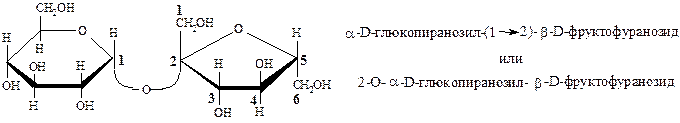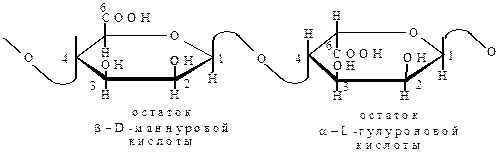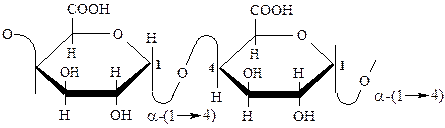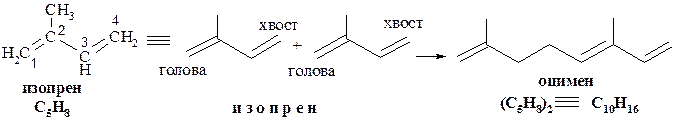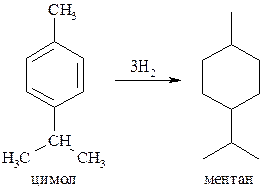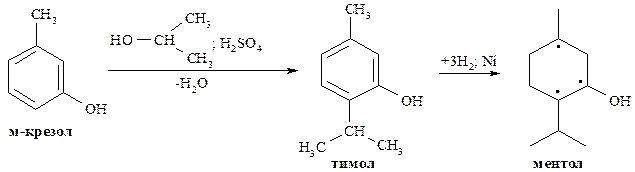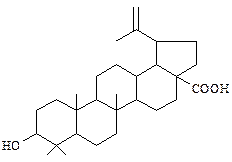Мальтоза (солодовый сахар).

Получают действием солода на крахмал. Содержащийся в солоде фермент амилаза расщепляет крахмал до этого дисахарида.
Как видно из структуры, мальтоза состоит из двух α-D-глюкозных остатков, связанных 1→4-гликозидной связью. Легко растворяется в воде, имеет сладкий вкус. Водные растворы мальтозы мутаротируют.
Целлобиоза.
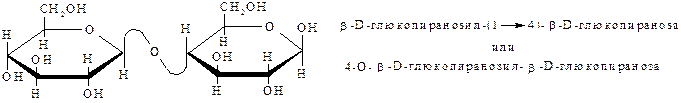
Целлобиоза является структурным фрагментом целлюлозы, откуда её и получают гидролизом.
Целлобиоза в отличие от мальтозы организмом не усваивается и в качестве пищевого продукта не используется.
Лактоза (молочный сахар).
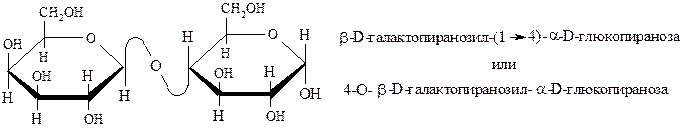
Содержится в молоке, менее растворима в воде по сравнению с другими дисахаридами, но не гигроскопична. Водные растворы мутаротируют.
Лактоза имеет особую биологическую значимость, поскольку является важнейшим питательным веществом для новорожденных.
Невосстанавливающие дисахариды.
Сахароза (тростниковый или свекловичный сахар).
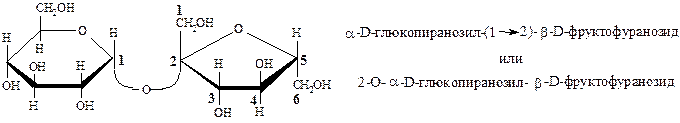
Растворы сахарозы не мутаротируют. Удельное вращение водного раствора сахарозы [α]D20= +66,5о. При гидролизе сахарозы образуется смесь равных количеств глюкозы и фруктозы и эта смесь уже характеризуется левым вращением, тогда как до гидролиза раствор имел правое вращение. Это объясняется тем, что фруктоза имеет левое вращение ([α]D20= -92о), а глюкоза – правое вращение ([α]D20= +52,5о).
Изменение в процессе гидролиза знака вращения раствора сахарозы (правое на левое) называется инверсией.
Смесь равных количеств глюкозы и фруктозы, образующаяся в процессе гидролиза сахарозы, называется инвертным сахаром.
Натуральный мёд является природным инвертным сахаром.
Полисахариды
Полисахариды должны рассматриваться как О-гликозиды, но в отличие от олигосахаридов они содержат от нескольких десятков до нескольких тысяч моносахаридных остатков.
Будучи поли-О-гликозидами, полисахариды легко подвергаются кислотному гидролизу. Если использовать разные ферменты, то можно осуществлять избирательный ферментативный гидролиз с целью получения ди-, три-, тетра- и т.д. сахаридов. Таким путём получают мальтозу из крахмала, целлобиозу из целлюлозы и т.д.
Полисахариды, состоящие из остатков только одного моносахарида, называются гликанами или гомополисахаридами. Если в построении полисахаридов участвуют разные моносахариды, то они называются гетерополисахаридами.
Полигликозидные цепи в молекуле полисахарида могут быть разветвлёнными и неразветвлёнными, что зависит от порядка связи между отдельными полимерными звеньями.
Гомополисахариды
Целлюлоза (клетчатка) – (С6Н10О5)n. Наиболее распространённое на земле органическое вещество. Древесина содержит от 45 до 70% клетчатки. Примером чистой целлюлозы является вата, фильтровальная бумага и т.д. Целлюлоза относится к β-гликанам(гомополисахаридам), мономерным звеном которых является β-D-глюкоза. Моносахаридные остатки соединены между собой β-1→4-гликозидной связью. Таких остатков в целлюлозе до 12000.
Характерная и отличительная особенность целлюлозы заключается в том, что макромолекулы этого линейного полимера располагаются параллельно друг другу и между ними возникают межмолекулярные водородные связи, что в свою очередь приводит к образованию волокон. Благодаря этому достигается высокая механическая прочность и жёсткость.
В отличие от крахмала, целлюлоза в воде не растворяется, но набухает в растворах щелочей, медноаммиачном комплексе. Целлюлоза находит широкое применение в производстве искусственных волокон, взрывчатых веществ, этанола и др. Для удобства изображения различных производных целлюлозы обычно используют упрощённую формулу [C6H7O2(OH)3]n.
Целлюлозу можно ацетилировать и получить триацетилцеллюлозу, которая далее используется для получения ацетатного шёлка и невоспламеняющихся кино-фотоматериалов:

Целлюлозу можно нитровать и в зависимости от стехиометрического соотношения реагентов получают моно-, ди- и тринитроклетчатки:

Смесь моно- и динитроклетчатки называется коллодийной ватой или коллоксилином и находит широкое применение. Из коллоксилина, камфоры и этилового спирта получают целлулоид.
Тринитрат клетчатки используется для получения бездымного пороха и изготовления взрывчатых устройств.
Метилированная целлюлоза или метилцеллюлоза может быть представлена общей формулой [C6H7O2(OH)3-X(OCH3)X. В каждом димерном фрагменте может содержаться в общей сложности до трёх-четырёх метоксигрупп:

Метилцеллюлоза растворяется в воде. Если водный раствор нагреть, то при температуре выше 50оС он переходит в гель. Это свойство метилцеллюлозы широко используется в фармации при изготовлении лекарственных форм наружного применения.
Крахмал – (C6H10О5)n продукт фотосинтеза. Относится к α-гликанам. Как гомополисахарид состоит из α-D-глюкозных остатков, соединенных между собой α-1→4 и α-1→6 гликозидными связями. Крахмал по своему составу неоднороден и представляет собой смесь двух полисахаридов – амилозы и амилопектина. Соотношение этих фракций в среднем равно 1:4, хотя в зависимости от растительного источника оно может сильно меняться.
Амилоза (C6H10O5)n. Здесь α-D-глюкозные остатки соединены между собой α(1→4)–глюкозидными связями. Полисахаридная цепь амилозы практически неразветвленна и состоит из 1000 – 6000 глюкозных остатков:

Макромолекула амилозы благодаря α-гликозидной связи может принимать спиралеобразную форму, где каждый виток сформирован шестью моносахаридными остатками.
Амилоза растворима в воде. С молекулярным йодом амилоза образует окрашенное в синий цвет соединение, что находит применение в качественном анализе (йодкрахмальная проба).
Амилопектин также состоит из α-глюкозных остатков, которые соединены между собой не только 1→4 - гликозидной связью, но и 1→6. Такой порядок глюкозидных связей приводит к разветвлению. Глюкозные остатки в неразветвленной цепи (линейный участок) связаны 1→4–глюкозидной связью. В местах же разветвления цепи глюкозный остаток одного линейного участка образует связь с атомом углерода С – 6 моносахаридного остатка второго линейного участка, что представлено ниже:

Чистый амилопектин в горячей воде растворяется лучше, чем амилоза. С йодом раствор амилопектина окрашивается в фиолетовый цвет.
В растениях крахмал откладывается в качестве запасного питательного продукта.
Гликоген (животный крахмал) (С6H10O5)n.
В организме животных этот полисахарид играет исключительную роль как запасной продукт. Он содержится во всех животных тканях, но больше всего в печени и мышцах. Является структурным аналогом амилопектина, но, в отличие от последнего, разветвлен в большей степени.
Декстраны – полисахариды бактериального происхождения общей формулы (C6H10O5)n и построенные из α-D-глюкозных остатков. Преобладающим типом связи между моносахаридами является α-1→6 глюкозидная связь, на долю которой приходится примерно 50 – 97% от всех связей. Молекулы декстранов сильно разветвлены, поскольку наряду с α-1→6 типом связи здесь в точках ветвления имеются α-1→4, α-1→3 и очень редко α-1→2 глюкозидные связи.
Микробиологический синтез осуществляется микроорганизмами, которые используют для этого сахарозу. Бактерии из сахарозы высвобождают фруктозу, а из α-D-глюкопиранозных остатков синтезируют полисахарид:

Декстраны нашли широкое применение в качестве кровезаменителей. С этой целью их подвергают частичной деполимеризации, доводя молекулярную массу до 50 000 – 100 000. При этом на долю α-1→6 связей должно приходиться не менее 95%. Такой декстран называется «клиническим декстраном» и для медицинских целей выпускается под названием «полиглюкин».
Сульфатированные декстраны обладают свойствами антикоагулянтов.
В промышленности на основе декстранов получают молекулярные сита – «Сефадексы», которые имеют сетчатое строение и способны набухать в воде с образованием гелей. Последние характеризуются определенным размером пор в гранулах геля, что позволяет «просеивать» молекулы с определенной молекулярной массой.
Хитин – линейный гомополисахарид, состоящий из остатков N-ацетил-D-глюкозамина, соединенных между собой β-1→4 гликозидными связями.

При дезацетилировании (отщеплении ацетильного остатка) образуется хитозан.
Хитин – главный скелетный полисахарид беспозвоночных и выполняет опорные и механические функции у ракообразных, насекомых (клещи, тараканы).
При гидролизе хитина получают глюкозамин, который в настоящее время широко используется в медицинской практике.
Гетерополисахариды
Альгиновые кислоты. Относятся к полиуроновым кислотам. Они являются главным структурным компонентом клеток бурых водорослей – Laminaria, Macreestis и Fucus. При гидролизе альгиновых кислот образуются β-D-маннуровая и α-L-гулуроновая кислоты в соотношениях от 1:0,5 до 1:3.
Мономерные звенья соединены между собой β-1®4-гликозидными связями. Альгиновые кислоты включают блоки, состоящие преимущественно из одной уроновой кислоты, а также участки с чередованием остатков обеих кислот:
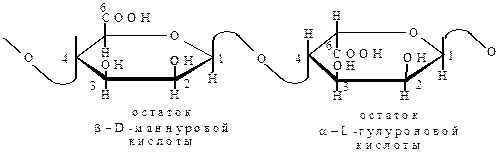
Альгиновые кислоты трудно растворимы в холодной воде, но легче в горячей воде. Склонны к набуханию в воде при комнатной температуре. Образуют гели, и это свойство позволяет широко применять альгиновые кислоты в фармации, в пищевой промышленности, а также в качестве эмульгаторов.
Агар (агар-агар) – полисахариды, содержащиеся в некоторых видах красных водорослей. Преобладающей в агаре фракцией является агароза (примерно 50–70%), представляющая собой линейный полимер, построенный из чередующихся остатков D-галактопиранозы и 3,6-ангидро-L-галактозы, соединённых поочерёдно β-1→4 и α-1→3 связями:

Помимо агарозы в агаре присутствует агаропектин. Агар – аморфный продукт, нерастворимый в холодной воде, но легко растворимый в горячей воде. При охлаждении горячего раствора до 35 – 40оС образуется плотный гель.
Используется в качестве желирующего вещества в пищевой промышленности, а также в фармации, в микробиологии. Будучи сорбентом, агар находит широкое применение как носитель при гельфильтрации и электрофорезе.
Мукополисахариды – кислые полисахариды животного происхождения. Молекулы мукополисахаридов имеют линейное строение и состоят из повторяющихся дисахаридных звеньев, в каждом из которых имеются остатки аминосахара (D-глюкозамина-N-сульфат, N-ацетил-D-глюкозамина или N-ацетил-D-галактозамина), а также уроновой кислоты или очень редко – галактозы. В некоторых случаях отдельные спиртовые гидроксигруппы могут быть сульфированы.
Из представителей этой группы в естественном состоянии только гиалуроновая кислота является чистым полисахаридом. Остальные мукополисахариды, в том числе гепарин, ковалентно связаны с белками, образуя протеогликаны. Эти соединения входят в состав соединительной ткани (в хрящах, сухожилиях, костях, коже, роговице, стекловидном теле глаза), слизистых выделениях, входит в состав клеточных мембран.
Гиалуроновая кислота состоит из чередующихся остатков глюкуроновой кислоты и N-ацетилглюкозамина, связанных между собой β-1→3 связью:

Сами дисахаридные фрагменты соединяются между собой β-(1→4) гликозидными связями.
Расщепление гиалуроновой кислоты в организме происходит под действием фермента гиалуронидазы.
Хондроитинсульфаты – близкие по строению с гиалуроновой кислотой полисахариды, состоящие из остатков глюкуроновой кислоты и сульфатированного N-ацетилглюкозамина, соединённые между собой β-1,3-гликозидной связью.
Известны 4 типа хондроитинсульфатов, которые отличаются друг от друга положением сульфатного остатка в N-ацетилглюкозаминном фрагменте (чаще всего в положениях 4;6 и одновременно 4,6):

Гепарин. Впервые выделен из печени. Содержится во многих тканях, Вырабатывается «тучными» клетками, где накапливается в виде гепарин-белкового комплекса. Регулирует свёртываемость крови (антикоагулянт).
Полисахаридная часть построена из чередующихся остатков β-D-глюкуроновой кислоты, её эпимера по С-5 – α-L-идуроновой кислоты, а также N-ацетата или сульфата глюкозамина. Гидроксигруппы С-6 глюкозамина и С-2 идуроновой кислоты сульфатированы:

Пектины ( пектиновые вещества) – полисахариды, построенные преимущественно из остатков α-D-галактуроновой кислоты, которые связаны между собой α-(1→4) связями. Таким образом, основу пектинов составляет полигалактуроновая, или пектиновая кислота. В различных пектинах карбоксильные группы метилированы в той или иной степени, или же находятся в виде соли:
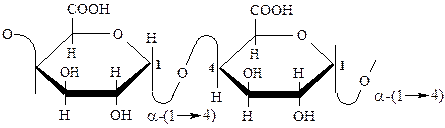
Пектиновые вещества содержатся в ягодах, плодах и корнеплодах. Яблочный и свекловичный пектины широко используются в пищевой промышленности.
Вопросы для самоподготовки
1. Стереоизомерия моноз и их отнесение к D- и L-стереохимическим рядам.
2. Причины цикло-оксо-таутомерии. Размер оксидного цикла (фуранозы, пиранозы). a- и b-Аномеры.
3. Явление мутаротации и её причины.
4. Химические свойства моноз. Качественные реакции на альдозы и кетозы.
5. Особенности строения дисахаридов. Восстанавливающие и невосстанавливающие дисахариды. Цикло-оксотаутомерия восстанавливающих дисахаридов.
6. Строение крахмала (амилоза, амилопектин) и целлюлозы. Отношение полисахаридов и их эфиров к гидролизу.
ГЛАВВА 23. ИЗОПРЕНОИДЫ
Изопреноиды – это обширная группа природных соединений с регулярным строением углеродного скелета, состоящего из изопентановых звеньев (насыщенных и ненасыщенных), связанных в строго определённой последовательности.
Формирование углеродного скелета осуществляется из изопреновых фрагментов, которые соединяются между собой по принципу присоединения «голова к хвосту» (изопреновое правило, Л. Ружичка, 1921г.).
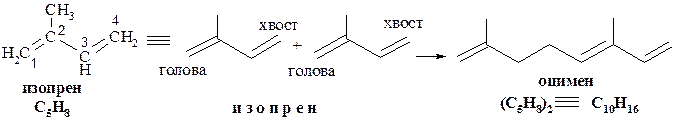
При изображении формул изопреноидов обычно атомы углерода опускают, а метильные группы изображают чёрточками.
Изопреноиды подразделяют на терпены или терпеноиды и стероиды.
Терпены и терпеноиды
Терпены – природные соединения преимущественно растительного происхождения, отвечающие формуле (С5Н8)n, где n≥2.
В соответствии с номенклатурой ИЮПАК термином «Терпены» обозначают углеводороды.
Терпеноиды – это кислородсодержащие производные терпенов (спирты, альдегиды, кетоны, сложные эфиры). Оба понятия как и сами соединения очень тесно взаимосвязаны между собой и поэтому принципиальной разницы в терминологии можно не делать.
Терпены и терпеноиды широко распространены в растительном мире: это, прежде всего, компоненты эфирных масел, живицы хвойных.
Эфирные масла (душистые масла) – многокомпонентные смеси летучих органических соединений, содержащие преимущественно терпены и терпеноиды и способные перегоняться с водяным паром.
Эфирные масла характеризуются приятным запахом и обусловливают аромат всех пахнущих растений (жасмин, роза, лаванда, кориандр, чабрец, полынь, гвоздика и т.д.).
В отличие от жирных масел, эфирные масла, будучи нанесёнными на бумагу, быстро испаряются и не оставляют жирных пятен.
Исторически сложившийся подход к определению понятия терпены связан с тем, что абсолютное большинство известных соединений этой группы отвечали формуле (С5Н8)n и минимальное число атомов углерода при этом составляло 10. Однако, благодаря очень чувствительным инструментальным методам исследования было установлено, что в большинстве эфирномасличных растений в незначительных количествах присутствует изопрен – С5Н8. Современная классификация терпенов представлена в таблице 23.1.
Таблица 23.1. Классификация терпенов – (С5Н8)n.
| Тип
| Значение n
| Число углеродных атомов
|
| Гемитерпены
|
|
|
| Монотерпены
|
|
|
| Сесквитерпены
|
|
|
| Дитерпены
|
|
|
| Сестерпены
|
|
|
| Тритерпены
|
|
|
| Тетратерпены
|
|
|
| Политерпены
|
1,4∙103 – 0,6∙105
каучуки
| от 7∙103 до 3∙105
|
Монотерпены
Среди всех изопреноидов монотерпены наиболее распространены и представляют особую ценность для производства эфирных масел, компонентами которых они являются.
По строению углеродного скелета их подразделяют на следующие группы:
- ациклические монотерпены;
- моноциклические монотерпены;
- бициклические монотерпены.
Ациклические монотерпены обычно представлены ненасыщенными спиртами, реже альдегидами. Очень редко встречаются соединения с карбоксигруппой.
Углеродный скелет ациклических монотерпенов соответствует 2,6-диметилоктану, рассматриваемому в качестве структурного предшественника. Ниже приведены структуры некоторых ациклических монотерпенов. В скобках указаны наиболее богатые источники этих соединений:

Эфирные масла, содержащие перечисленные выше ациклические монотерпены, используют в парфюмерии и пищевой промышленности.
Цитраль применяется в глазной практике при кератитах и конъюнктивитах. Оказывает болеутоляющее и противовоспалительное действие.
Цитраль является исходным веществом для синтеза ретинола (витамина А).
Моноциклические монотерпены. Наиболее распространёнными из этой группы являются соединения ментанового ряда:

Ментан в природе не встречается. Синтетически его можно получить гидрированием цимола (п-метилизопропилбензола):
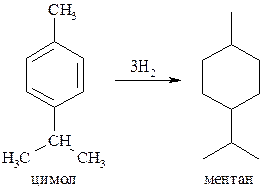
Гидроксипроизводные ментанового ряда широко распространены, поскольку являются составными компонентами многих эфирных масел. Наибольшее практическое значение имеют ментол – ментан-3-ол, а также терпин или ментандиол-1,8.
Ментол. В эфирном масле мяты перечной примерно 40-70% приходится на долю ментола. Получают ментол из эфирного масла мяты перечной или же гидрированием тимола:

Ментол имеет три асимметрических атома углерода (в формуле они отмечены звёздочками), поэтому обладает оптической активностью.
Применяется наружно как отвлекающее, антисептическое и противовоспалительное средство в составе мягких лекарственных форм или в виде аэрозолей для ингаляций. Внутрь назначают в качестве успокоительного средства.
Ментол используется для получения препарата «Валидол», представляющего собой раствор ментола 25% в ментиловом эфире изовалериановой кислоты. Препарат оказывает успокаивающее влияние на ЦНС и обладает умеренным рефлекторным сосудорасширяющим действием.
В промышленности ментол получают из м-крезола, который вначале алкилируется с помощью изопропилхлорида или пропанола-2, а затем образующийся тимол восстанавливается до ментола.
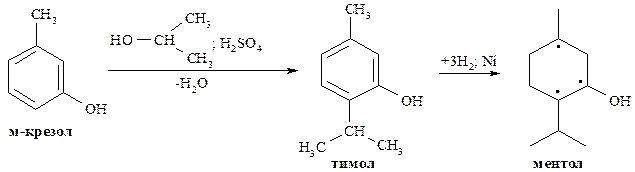
Далее ментол переводят в ментиловый эфир изовалериановой кислоты:

В процессе синтеза образуется смесь восьми стереоизомеров, из которой необходимый левовращающий ментол отделяют с помощью химических и физико-химических методов.
Будучи вторичным спиртом, ментол окисляется до кетона – ментона:

Ментон содержится в мятном, гераниевом и многих других эфирных маслах.
Терпин или ментандиол-1,8. Является двухатомным спиртом. В природных эфирных маслах практически не встречается. Его получают из пинена – важнейшего компонента скипидаров (см. ниже, бициклические монотерпены). В процессе получения терпин кристаллизуется в виде моногидрата, называемого терпингидратом.

Терпингидрат применяется внутрь как отхаркивающее средство при хронических бронхитах.
При действии водоотнимающих средств на терпингидрат можно получить терпинеолы, а также цинеол:

Цинеол или эвкалиптол является внутренним простым эфиром и имеет характерный «камфарный» запах, входит в состав эфирных масел эвкалиптов (до 70%), цитварной полыни (до 80%), благородного лавра (до 50%).
Терпинеолы имеют приятный запах: α-терпинеол – запах сирени; β-терпинеол – запах гиацинта.
При дегидратации α-терпинеола образуется сложная смесь изомерных ментадиенов – лимонен, терпинолен, ментадиен, терпинены, структуры которых были приведены выше.
Оптически активные формы лимонена входят в состав эфирных масел: (+)-лимонен содержится в цитрусовом и тминном маслах, а (-)-лимонен входит в состав живицы хвойных
Рацемат лимонена называется дипентеном. Замещённые дипентены является психоактивными веществами.
Бициклические монотерпены. Ниже представлены структуры углеводородов, лежащих в основе бициклических монотерпенов:

Большинство монотерпенов с бициклическим углеродным скелетом содержится в живицах хвойных.
Живица или терпентин представляет собой жидкую смолу, содержащуюся в смоляных ходах, пронизывающих древесину и вторичную кору сосны. По существу – это бальзам, представляющий собой раствор смолы (канифоли) в эфирном масле (скипидаре).
Очищенный скипидар содержит до 75% пинена.
α-Пинен. Является преобладающим компонентом скипидара. Характеризуется правым вращением. Его структурный изомер – β-пинен также содержится в живице и характеризуется левым вращением. У обоих пиненов по два асимметрических углеродных атома:

Благодаря высокому содержанию в смоле хвойных, пинены служат исходными соединениями для получения многочисленных производных, в основе которых лежат бициклические монотерпены.
Выше было показано, что из α-пинена можно получить терпин и далее терпинеолы и эвкалиптол.
Значительное количество α-пинена используется в промышленности для синтеза лекарственного препарата – камфоры.
В медицинской практике используют:
- натуральную правовращающую камфору, получаемую из камфорного дерева – Cinnamomum camphora (L.) Nees et Eberm.;
- синтетическую левовращающую камфору, получаемую из пихтового масла;
- камфору рацемическую.

Потребность в камфоре не удовлетворяется природными источниками, тем более, что не во всех странах произрастает камфорное дерево. В связи с этим разработаны синтетические и полусинтетические способы получения камфоры.
Левовращающую камфору можно получить из борнилацетата, содержащегося в пихтовом масле (30-40%).
Борнилацетат получают путём фракционной перегонки масла, гидролизуют (омыляют) гидроксидом натрия, после чего окисляют и получают камфору:

Синтетическую камфору (рацемическую) можно получать из пинена, содержащегося в живице по способу В.Е. Тищенко. Пинен в присутствии катализатора – оксида титана (IV) изомеризуется в камфен, который взаимодействует с муравьиной кислотой с образованием борнилформиата. Далее борнилформиат подвергается гидролизу, а полученный спирт борнеол окисляют до камфоры. Ниже приводится общая схема синтеза по Тищенко:

Камфора является кетоном, поэтому по карбонильной группе вступает в реакции, характерные для кетонов, например, образование оксимов, фенилгидразонов и т.д.
Карбонильная группа оказывает значительное влияние на соседнюю метиленовую группу (положение С-3), повышая подвижность атомов водорода. Данное свойство используется при синтезе 3-бромкамфоры:

Камфору применяют в качестве стимулятора ЦНС и кардиотонического средства.
Бромкамфора оказывает успокаивающее действие, а также улучшает сердечную деятельность.
Дитерпены
По репрезентативности представителей отдельных групп дитерпены значительно уступают монотерпенам и сесквитерпенам. Ациклические дитерпены практически представлены единичными представителями, среди которых следует отметить фитол, относящийся к дитерпеновым спиртам. Впервые его получили гидролизом хлорофилла:

Доминирующим компонентом нелетучей части живицы хвойных – канифоли является абиетиновая кислота. Наряду с изомерными ей кислотами входит в группу смоляных кислот.

К группе дитерпенов относятся витамины группы А1, представляющие собой семейство из трёх соединений – ретинола, ретиналя и ретиноевой кислоты:

В основном состоянии все три соединения имеют транс-конфигурацию двойных связей, что наглядно представлено в структурной формуле. Характерно, что благодаря такой своеобразной сопряжённой системе, витамины группы А имеют яркую окраску от жёлтой до оранжевой.
Ретинол, будучи аллильным спиртом, легко окисляется до альдегида –ретиналя и далее до ретиноевой кислоты.
Ретиналь способен взаимодействовать с ε-аминогруппой аминокислотного фрагмента лизина белка опсина, в результате чего образуется хромопротеид – родопсин (зрительный пурпур), выполняющий функцию светочувствительного компонента нашей зрительной системы. Поглощая квант света, остаток транс-ретиналя в родопсине переходит в 11-цис-ретиналь:

Структурно близкими к витаминам группы А1 оказались каротиноиды (или каротиноидные пигменты), которые впервые были выделены из моркови (Daucus carota) в 1831 году Цветом М.С.
Каротиноиды относятся к тетратерпенам – С40Н56 и представляют собой полиеновые сопряжённые системы. Они содержатся в различных органах растений и выполняют важные биологические функции, в том числе, участие в процессах фотосинтеза и светозащитная функция.
Наибольшее значение с точки зрения биологических свойств имеет β-каротин, который содержится в зелёных растениях.
Молекула β-каротина содержит два 1,1,5-триметилциклогексеновых кольца, идентичных кольцу β-ионона:

Обращает на себя внимание и тот факт, что аналогичное триметилциклогексеновое кольцо содержится и в молекуле витамина А, структура которого была рассмотрена выше.
В β-каротине оба триметилциклогексеновых кольца соединены между собой цепью из 18 углеродных атомов, представляющих собой сопряжённую систему с чередующимися простыми и двойными связями.
Для сравнения: витамин А1 (см. выше) содержит одно 1,1,5-триметилциклогексеновое кольцо и сопряжённую боковую цепь из 9 углеродных атомов.
Было установлено, что в организме под влиянием фермента 15,15’-оксигеназы молекула β-каротина расщепляется на две молекулы ретиналя, откуда следует, что он является провитамином А:

Тритерпены
По разнообразию структурных типов углеводородов соединения данной группы значительно уступают остальным изопреноидам. Однако, по распространённости тритерпеноиды превосходят не только изопреноиды, но и очень многие группы природных соединений.
В настоящее время описаны многочисленные производные тритерпенов, которые выделены не только из растений, но и из микроорганизмов, морских организмов, животных, а также найдены в органических геологических сферах (нефть, осадочные породы).
Другой важной особенностью тритерпенов является то обстоятельство, что углеродный скелет этих соединений может претерпевать очень существенные изменения, приводящие к формированию биологически важнейшей группы веществ растительного и животного происхождения – стероидов.
В растениях тритерпены обычно находятся в виде кислородосодержащих производных (спирты, альдегиды, кетоны, кислоты, эфиры), а также их гликозидов, называемых сапонинами. Агликоны сапонинов принято называть сапогенинами. Гликозиды тритерпеновых сапонинов образованы за счёт О-гликозидной связи. Наиболее распространёнными являются гликозиды олеаноловой кислоты, которая относится к тритерпеноидам типа олеанана. В растениях семейства губоцветные и розоцветные чаще встречается урсоловая кислота (тип урсана).
Биогенетическим предшественником тритерпенов (следовательно, стероидов) является сквален – единственный ациклический тритерпен из которого далее формируются многочисленные структурные типы рассматриваемой группы изопреноидов:

Тритерпеноиды и их гликозиды характеризуются широким спектром биологической активности. Они регулируют углеводный и липидный обмен, характеризуются гиполипидемическим и гипохолестеринемическим действием, противоопухолевым, иммуномодулирующим и противовирусным свойством. Обладают гепатопротекторным действием, улучшают мозговое кровообращение.
Чаще всего перечисленные биологические свойства пока описаны для соединений, которые наиболее распространены и доступны с точки зрения их количественного содержания в конкретном растении. Они приведены ниже:

| Олеаноловая кислота
Содержится в плодах облепихи, в аралии маньчжурской, в сахарной свекле, шалфее, чернике, клюкве.
|

| Урсоловая кислота
Содержится в плодах облепихи, яблоках, клюкве, чернике, шалфее и в большинстве растений семейства губоцветных.
|

| Глицерретовая кислота
В виде гликозида – глицирризиновой кислоты содержится в большишх количествах в солодке гладкой и солодке уральской.
|
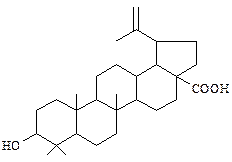
| Бетулиновая кислота
Наибольшее количество этой кислоты и соответствующего ей первичного спирта – бетулинола содержится в коре берёзы (от 10 до 35%).
|
К сожалению, объём учебной программы не позволяет шире освещать материал, касающийся тритерпеноидов.
Стероиды
Стероиды – это обширная группа природных соединений растительного и животного происхождения, биогенетическим предшественником которых является сквален.
В основе всех стероидов лежит углеводород гонан (или иначе стеран), представляющий собой циклопентанпергидрофенантрен. В соответствии с правилами ИЮПАК основные типы углеводородного скелета стероидов обозначают следующими тривиальными названиями: