Константа Михаэлиса равна концентрации субстрата, при которой скорость реакции равна половине максимальной скорости. Она характеризует специфичность фермента по отношению к субстрату (чем меньше, тем специфичнее). Типичные значения KM от 10-6 до 10-1 моль/л.
Константу скорости k3 иногда называют числом оборотов фермента.
Число оборотов фермента - число молекул субстрата, которые превращаются на активном центре фермента в единицу времени (обычно от 10 до 108 мин-1).
Уравнение Михаэлса можно записать в линейных координатах:
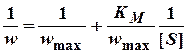 .
.
Для определения параметров уравнения KM и wmax проводят серию измерений начальной скорости реакции от начальной концентрации субстрата и представляют экспериментальные данные в координатах 1/w0 – 1/[S0].
Течение химических реакций может быть заторможено присутствием некоторых веществ. Ингибиторы ферментативного катализа, способны образовывать комплексы с ферментом или фермент-субстратным комплексом.
Вопросы для самоконтроля
1. Что изучает химическая кинетика?
2. Что называется скоростью химической реакции?
3. Напишите выражение для средней скорости реакции. Как она определяется экспериментально?
4. Что собой представляет истинная скорость реакции?
5. По каким признакам классифицируют реакции в кинетике? Приведите эти классификации.
6. Дайте определения понятиям молекулярность, порядок реакции, период полупревращения.
7. Какие факторы влияют на скорость химической реакции?
8. Какова зависимость скорости реакции от концентрации. Сформулируйте основной постулат химической кинетики. Приведите его запись.
9. Что называют константой скорости химической реакции?
10. Запишите кинетические уравнения реакций нулевого, первого, второго порядков.
11. Опишите экспериментальные методы определения скорости и константы скорости реакций.
12. Каким образом увеличение температуры влияет на скорость химической реакции? Сформулируйте правило Вант-Гоффа.
13. Запишите уравнение Аррениуса.
14. Изобразите энергетический профиль реакций с различным тепловым эффектом (энергетическая диаграмма для реакции, протекающей без тепловых эффектов; энергетическая диаграмма для экзотермической реакции, для эндотермической реакции).
15. Что такое энергия активации?
16. Опишите теорию активных соударений (ТАС).
17. Какова роль стерического фактора?
18. Опишите теорию переходного состояния.
19. Дайте определение понятию катализ (гомогенный и гетерогенный катализ). Изобразите энергетический профиль каталитической реакции. Какое влияние оказывает катализатор на выход продуктов реакции?
20. Каковы особенности каталитической активности ферментов? Запишите и проанализируйте уравнение Михаэлиса - Ментен.
Ситуационные задачи
Задачи на правило Вант-Гоффа

Задача №1.
С помощью правила Вант-Гоффа вычислить при какой температуре реакция закончится через 15 минут, если при температуре 293 К реакция идёт в течение 2 часов. Температурный коэффициент Вант-Гоффа реакции равен 3. Константа скорости обратно пропорциональна времени.
Ответ: 312 К.
Задача №2.
Температурный коэффициент реакции равен 3,5. Константа скорости kI при температуре ТI=15°С равна 0,2 с-1. Найти kII при температуре TII=40°С.
Ответ: 0,009 с-1.



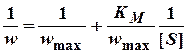 .
.



