

Автоматическое растормаживание колес: Тормозные устройства колес предназначены для уменьшения длины пробега и улучшения маневрирования ВС при...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Автоматическое растормаживание колес: Тормозные устройства колес предназначены для уменьшения длины пробега и улучшения маневрирования ВС при...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...
Топ:
Теоретическая значимость работы: Описание теоретической значимости (ценности) результатов исследования должно присутствовать во введении...
Особенности труда и отдыха в условиях низких температур: К работам при низких температурах на открытом воздухе и в не отапливаемых помещениях допускаются лица не моложе 18 лет, прошедшие...
История развития методов оптимизации: теорема Куна-Таккера, метод Лагранжа, роль выпуклости в оптимизации...
Интересное:
Лечение прогрессирующих форм рака: Одним из наиболее важных достижений экспериментальной химиотерапии опухолей, начатой в 60-х и реализованной в 70-х годах, является...
Инженерная защита территорий, зданий и сооружений от опасных геологических процессов: Изучение оползневых явлений, оценка устойчивости склонов и проектирование противооползневых сооружений — актуальнейшие задачи, стоящие перед отечественными...
Мероприятия для защиты от морозного пучения грунтов: Инженерная защита от морозного (криогенного) пучения грунтов необходима для легких малоэтажных зданий и других сооружений...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Имени В.И. Разумовского» Министерства здравоохранения и социального
Развития Российской Федерации
(ГБОУ ВПО Саратовский ГМУ им. В.И. Разумовского
Минздравсоцразвития России)
Методические указания к лабораторно – практическому занятию
для студентов медицинских специальностей
Кинетика и катализ
Дисциплина: общая химия.
I курс.
Очная форма обучения.
Длительность занятия: 90 минут.
Разработка составлена асс. Куликовой Л.Н.
2011 г
Вопросы для подготовки к занятию
1. Предмет химической кинетики.
2. Скорость реакции, средняя скорость реакции в интервале, истинная скорость.
3. Классификации реакций, применяющиеся в кинетике: реакции, гомогенные, гетерогенные и микрогетерогенные; реакции простые и сложные (параллельные, последовательные, сопряженные, цепные).
4. Молекулярность элементарного акта реакции.
5. Порядок реакции.
6. Период полупревращения.
7. Зависимость скорости реакции от концентрации. Закон действующих масс.
8. Константа скорости химической реакции.
9. Кинетические уравнения реакций нулевого, первого, второго порядков.
10. Экспериментальные методы определения скорости и константы скорости реакций.
11. Зависимость скорости реакции от температуры. Правило Вант-Гоффа. Температурный коэффициент скорости реакции и его особенности для биохимических процессов.
12. Уравнение Аррениуса. Энергетический профиль реакции; энергия активации.
13. Понятие о теории активных соударений.
14. Роль стерического фактора.
15. Понятие о теории переходного состояния.
16. Катализ. Гомогенный и гетерогенный катализ. Энергетический профиль каталитической реакции.
17. Особенности каталитической активности ферментов. Уравнение Михаэлиса - Ментен и его анализ.
|
|
Приложение 2: Краткий теоретический материал
Химическая кинетика изучает закономерности протекания химических процессов во времени.
Основные понятия кинетики:
Скорость реакции – это изменение концентрации реагирующих веществ в единицу времени:
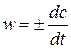 .
.
Поскольку скорость реакции - величина положительная, то “+” ставится, если используется концентрация продуктов реакции, и “-” - для исходных веществ.
Например, для реакции 3H2+N2 = 2NH3.
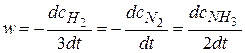 .
.
Общая скорость реакции равна скорости реакции по отдельному веществу, деленная на стехиометрический коэффициент, стоящий перед этим веществом в уравнении химической реакции.
Существует понятие средней и истинной скорости реакции.
Средняя скорость в интервале – изменение концентрации реагирующих веществ за некоторый промежуток времени:
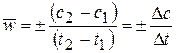 ,
,
Средняя скорость относится к средней концентрации 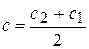
Истинная скорость – изменение концентрации реагирующих веществ в конкретный момент времени и представляет собой предел средней скорости при Dt®0
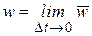 ,
,
Различают простые и сложные реакции.
Простыми называют реакции, протекающие в одну стадию.
Сложными называют реакции, протекающие в несколько стадий.
Выделяют следующие виды сложных реакций:
1) параллельные;
2) последовательные,
3) сопряженные;
4) цепные.
Основной постулат химической кинетики – закон действующих масс
w = 
Скорость реакции пропорциональна произведению концентрации реагирующих веществ, взятых в некоторых степенях. Эти степени называются частными порядками реакции:
p - частный порядок реакции по веществу А,
q - частный порядок реакции по веществу В.
Сумма частных порядков дает полный порядок реакции n: n=p+q.
k - константа скорости реакции, это скорость реакции при концентрации реагирующих веществ, равных единице (удельная скорость ).
Молекулярность реакции - число молекул, реагирующих в одном элементарном акте реакции.
|
|
Для реакций различных порядков зависимость скорости от концентрации реагирующих веществ выражается индивидуальным кинетическим уравнением.
1) Реакции нулевого порядка (n=0).
Вид реакции: A®продукт; в этом случае скорость реакции не зависит от концентрации исходного вещества, т.е. концентрация вещества А поддерживается на одном уровне.
Кинетическое уравнение: 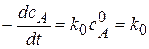 . или
. или
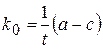 ,
,
где k0 – константа скорости реакции нулевого порядка;
t – время от начала реакции до достижения концентрации с;
а - концентрация вещества А при t =0,
с - концентрация вещества А в момент времени t.
Размерность k 0 определяется выражением k 0 =w, поэтому 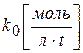 .
.
Время полупревращения t1/2 - время, за которое концентрация исходного вещества уменьшается в 2 раза.
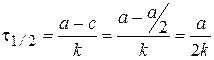 .
.
2) Реакции первого порядка (n=1).
Вид реакции: A ®продукт;
Кинетическое уравнение: 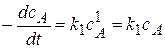 или
или 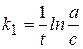 ,
,
Размерность константы скорости: k 1, [t-1].
Время полупревращения t1/2: 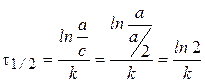 .
.
3) Реакции второго порядка (n=2).
Вид реакции: A + В ®продукт или 2 A ®продукт.
Пусть к началу реакциии концентрации исходных веществ равны 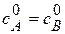 .
.
Кинетическое уравнение: 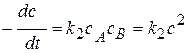 или
или  .
.
Размерность константы скорости: k 2, [конц.-1× t-1].
Время полупревращения t1/2: 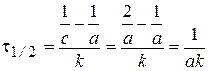 .
.
Размерность константы скорости: k 3, [конц.-2× t -1].
В общем случае 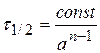 .
.
Экспериментально скорость реакции определяют измерением концентрации реагирующих веществ за определенный промежуток времени с последующим расчетом по формулам средней или истинной скорости реакции.
Константу скорости реакции можно определить представив экспериментальные данные в линейных координатах кинетического уравнения соответствующего порядка.
Катализ
Явление катализа – это изменение скорости реакции под действием некоторых веществ, которые к концу реакции остаются в химически неизменном виде.
Разновидности катализа:
1) положительный – под действием некоторых веществ скорость реакции увеличивается;
2) отрицательный: под действием некоторых веществ скорость реакции уменьшается, такие вещества называются ингибиторами;
3) автокатализ: катализатором являются продукты реакции;
4) гомогенный: катализатор и реагенты находятся в одной фазе (газ или раствор);
5) гетерогенный: катализатор и реагенты находятся в разных фазах;
6) ферментативный: катализатором является биологический фермент.
Принципы катализа:
|
|
1) катализатор принимает участие в химической реакции, образуя промежуточные продукты, но в конце реакции выделяется в химически неизменном виде. Физическое состояние катализатора, входящего в активный комплекс, может существенно изменяться, например, уменьшатся размеры зерен твердого катализатора, изменится структура поверхностных слоев;
2) катализатор не смещает положение равновесия, а лишь увеличивает скорость прямой и обратной реакции в равной степени;
3) действие катализатора является специфичным (селективным);
4) катализатор увеличивает скорость реакции за счет уменьшения Еакт, ведет реакцию по пути с меньшим энергетическим барьером.
Гомогенный катализ
Рассмотрим схему реакции, протекающей без катализатора:
A + B → AB* →C + D.
В присутствии катализатора реакция протекает в несколько стадий:
1. 
2. 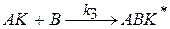
3. 
При условии k3>>k1 скорость образования продуктов можно выразить через концентрации реагентов и катализатора:

Это уравнение лежит в основе кинетики гомогенных каталитических реакций. Из уравнения видно, что скорость процесса прямо пропорциональна концентрации катализатора, исключение составляют лишь случаи, когда катализатор находится в большом избытке, в результате чего скорость процесса лимитируется не кинетическими, а физическими закономерностями, например, диффузией растворенного вещества к катализатору.
Энергетический профиль каталитической реакции представлен на рисунке 4.
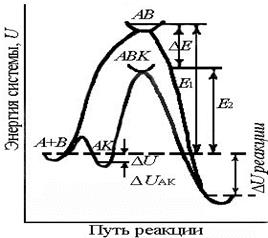
Рис.4. Энергетические профили
реакций с катализатором и без него.
Е1 – энергия активации некаталитической реакции,
Е2 – каталитической реакции
В ранних исследованиях предполагалось, что поверхность катализатора энергетически однородна (Лэнгмюр). В дальнейшем была экспериментально доказана адсорбционная неоднородность поверхности. Возникло представление о том, что каталитически активны только определенные участки поверхности, на которых имеются адсорбционные центры. Здесь вещество способно образовать активное для протекания данного каталитического процесса промежуточное поверхностное соединения, благодаря чему понижается энергия активации реакции.
|
|
Гетерогенный катализ
В случае гетерогенного катализа реакции происходят на границе раздела фаз.
Гетерогенный катализ состоит из следующих стадий:
1. массоперенос реагентов к катализатору;
2. абсорбция – образование абсорбированного комплекса между реагентом и катализатором;
3. каталитическая реакция – образование продукта в основном адсорбированном состоянии;
4. десорбция продукта;
5. внутренний массоперенос (изнутри катализатора);
6. внешний массоперенос (из области реакции).
Общая скорость каталитической реакции определяется скоростью самой медленной из этих стадий. Если не рассматривать диффузию и считать, что равновесие «адсорбция ↔ десорбция» устанавливается быстро, то скорость каталитической реакции определяется скоростью реакции в адсорбционном слое, где роль реагента играют свободные адсорбционные центры. Простейший механизм гетерогенного катализа описывается схемой:
 .
.
Для придания катализаторам большей избирательности, термической стойкости, механической прочности и активности их часто применяют в форме многокомпонентных систем: смешанных, на носителях, промотированных катализаторов.
Промоторы - это вещества, которые не обладают каталитическими свойствами, но добавление их к катализатору значительно увеличивает его активность.
Каталитические яды - это вещества, понижающие активность катализатора.
Активность катализаторов оценивают либо количеством вещества (в молях), реагирующих в единицу времени под воздействием единицы массы катализатора, или количеством вещества (в молях), реагирующих в единицу времени под воздействием единицы поверхности катализатора.
Ферментативный катализ
Ферментативными реакциями называются такие химические процессы в биологических системах, скорость которых регулируется веществами биологического происхождения. Это белковые молекулы, называемые ферментами или энзимами.
Ферментативный катализ играет огромную роль в жизнедеятельности организма. Широкое применение получили ферментные препараты при нарушениях функции желудочно-кишечного тракта, связанных с недостаточной выработкой пищеварительных ферментов (пепсин, панкреатин). При ожогах, гнойных ранах, гнойно-воспалительных заболеваниях легких, когда необходимо разрушить накопившиеся в большом количестве белковые образования, применяются протолитические ферменты, приводящие к быстрому гидролизу белков и способствующие рассасыванию гнойных скоплений. Для лечения инфекционных заболеваний используются препараты лизоцина, которые разрушают оболочку некоторых болезнетворных бактерий. Очень важные ферменты, которые рассасывают тромбы (сгустки крови внутри кровеносных сосудов) – плазмин, трипсин, химотрипсин, на их основе с разными добавками созданы различные лекарственные препараты – стрептокиназа, стрептаза, и т.п., широко применяемые в медицине.
|
|
Выделения ферментов в особый класс катализаторов обусловлен особыми свойствами этих веществ:
1) высокая специфичность;
2) эффективность действия;
3) биологические катализаторы образуются и разрушаются в процессе
жизнедеятельности организма.
По своей каталитической активности биологические катализаторы в тысячи раз превышают неорганические. Специфичность действия связана с особенностями структуры фермента и субстрата. Одни части каталитической системы выполняют функции, главным образом связанные с пространственной организацией системы, другие в этой организационной системе осуществляют собственно катализ. Т.е., как и при неферментативном катализе, в каталитической реакции участвует не вся белковая молекула в целом, а лишь определенные ее участки – активные центры фермента.
Простейшая схема ферментативного катализа включает обратимое образование промежуточного комплекса фермента (Е) с реагирующим веществом (субстратом S) и разрушение этого комплекса с образованием продуктов реакции (Р):
 .
.
При условии, что k3>>k1, с учетом уравнения материального баланса [E]=[E0]-[ES] (индекс «0» означает начальную концентрацию) получаем уравнение Михаэлиса-Ментен. В уравнении скорость образования продукта выражена через начальную концентрацию фермента и текущую концентрацию субстрата:
 ,
,
где w max=k2[E0] – максимальная скорость реакции;
 - это константа Михаэлиса.
- это константа Михаэлиса.
Вопросы для самоконтроля
1. Что изучает химическая кинетика?
2. Что называется скоростью химической реакции?
3. Напишите выражение для средней скорости реакции. Как она определяется экспериментально?
4. Что собой представляет истинная скорость реакции?
5. По каким признакам классифицируют реакции в кинетике? Приведите эти классификации.
6. Дайте определения понятиям молекулярность, порядок реакции, период полупревращения.
7. Какие факторы влияют на скорость химической реакции?
8. Какова зависимость скорости реакции от концентрации. Сформулируйте основной постулат химической кинетики. Приведите его запись.
9. Что называют константой скорости химической реакции?
10. Запишите кинетические уравнения реакций нулевого, первого, второго порядков.
11. Опишите экспериментальные методы определения скорости и константы скорости реакций.
12. Каким образом увеличение температуры влияет на скорость химической реакции? Сформулируйте правило Вант-Гоффа.
13. Запишите уравнение Аррениуса.
14. Изобразите энергетический профиль реакций с различным тепловым эффектом (энергетическая диаграмма для реакции, протекающей без тепловых эффектов; энергетическая диаграмма для экзотермической реакции, для эндотермической реакции).
15. Что такое энергия активации?
16. Опишите теорию активных соударений (ТАС).
17. Какова роль стерического фактора?
18. Опишите теорию переходного состояния.
19. Дайте определение понятию катализ (гомогенный и гетерогенный катализ). Изобразите энергетический профиль каталитической реакции. Какое влияние оказывает катализатор на выход продуктов реакции?
20. Каковы особенности каталитической активности ферментов? Запишите и проанализируйте уравнение Михаэлиса - Ментен.
Ситуационные задачи
Имени В.И. Разумовского» Министерства здравоохранения и социального
развития Российской Федерации
(ГБОУ ВПО Саратовский ГМУ им. В.И. Разумовского
Минздравсоцразвития России)
|
|
|

Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций...

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰)...

Особенности сооружения опор в сложных условиях: Сооружение ВЛ в районах с суровыми климатическими и тяжелыми геологическими условиями...

История создания датчика движения: Первый прибор для обнаружения движения был изобретен немецким физиком Генрихом Герцем...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!