Обычно сопротивление воздушного тракта рассчитывается по методике той же, что и для газового тракта. В рамках курсового проекта допускается применять упрощенную методику. Дутьевой вентилятор должен преодолевать сопротивление воздуховодов и горящего слоя угля на решетке. Для выбора дутьевого вентилятора необходимо знать приведенное сопротивление воздушного тракта и приведенный расход холодного воздуха.
Приведённое сопротивление:
 ;
;
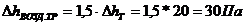 ;
;
Приведённая производительность вентилятора:
 ;
;
где 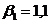 - коэффициент запаса;
- коэффициент запаса;
Расход холодного воздуха:

где 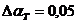 - присос воздуха в топочную камеру;
- присос воздуха в топочную камеру;
 - присос воздуха в воздуховод;
- присос воздуха в воздуховод;
Дутьевой вентилятор выбирают по [2] стр. 406 таблица 14.1.
Выбираем дутьевой вентилятор ВДН-8 (Производительность – 10,2*103 м3/ч; напор – 2,19 кПа; t = 30 0С; η = 83%; масса – 417 кг).
Мощность вентилятора:
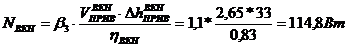 ;
;
| Аэродинамический расчёт котельной установки
| |
где

- коэффициент запаса;
Выбор электродвигателя производится по ближайшей большей мощности и синхронной частоте вращения 1000 об/мин из [2] стр143 таблица 5.28.
Выбираем асинхронный трёхфазный электродвигатель 4А225М2У3 мощностью 15 кВт, массой 26кг.
|
| | | Аэродинамический расчёт котельной установки
| |
ВЫБОР И РАСЧЁТ СИСТЕМЫ ПОДГОТОВКИ ВОДЫ.
ОБЩИЕ СВЕДЕНИЯ О ВОДЕ.
Для водоснабжения энергообъектов используются в большинстве случаев природные воды, как поверхностные (из рек, озер, прудов), так и подземные (из артезианских скважин). Все воды содержат разнообразные примеси, попадающие в воду в процессе ее естественного круговорота в природе. Кроме того, возможно загрязнение водоисточников бытовыми и промышленными стоками.
Все примеси, загрязняющие воду, подразделяются на три вида в зависимости от размера их частиц:
1. Истинно растворенные примеси находятся в воде в виде ионов, отдельных молекул, комплексов или состоят из нескольких молекул. Размер этих частиц менее 10-6 мм. В истинно растворенном состоянии в воде находятся газы (О2, СО2, Н2S, N2), а также катионы и анионы поступивших в воду солей Са2+, Мg2+, Nа+, К+, НСО3-, Сl-, SО42-, NO3-, NО2-.
2. Коллоидно-растворенные примеси имеют размеры частиц порядка 10-6 – 10-4 мм. Каждая из частиц образована большим числом молекул (их может быть несколько тысяч). Эти примеси могут быть как органического, так и минерального происхождения. К первым относятся гуминовые вещества, вымываемые из почвы, ко вторым – кремниевые кислоты, соединения железа.
3. Грубодисперсные примеси имеют размер частиц более 10-4 мм. Это растительные остатки, частицы песка, глины и т.д. Содержание грубодисперсных примесей в природных водах различно в разное время года: для равнинных рек максимальное содержание наблюдается в период паводка (таяния снегов), для горных рек – в паводок и в периоды ливней в горах.
Для оценки качества природных вод и вод энергообъектов на различных стадиях технологического процесса приняты нижеперечисленные показатели:
1. Взвешенные вещества – определяют непосредственно в отобранной пробе, пользуясь весовым методом. ВЗВ – 14 мг/л.
2.
| Выбор и расчёт системы подготовки воды
| |
Сухой остаток СО (мг/л) – определяют путем выпаривания определенного объема предварительно профильтрованной пробы и последующего просушивания остатка при температуре 110-120
оС. Сухой остаток выражает содержание растворенных в воде минеральных и органических примесей, нелетучих при указанной температуре. Содержащиеся в природной воде Са(НСО
3)
2 и Мg(НСО
3)
2
при выпаривании разлагаются с выделением Н2О и СО2, и в сухом остатке появляются СаСО3 и МgСО3.
Это надо иметь в виду, сравнивая сухой остаток с минеральным. С.О – 228 мг/л.
3. Минеральный остаток (общее солесодержание) – подсчитывается путем суммирования концентраций катионов и анионов, определенных при проведении полного химического анализа воды.
4. Прокаленный остаток (мг/л) – характеризует содержание в воде минеральных веществ. Его определяют путем прокаливания при 800 оС сухого остатка. При прокаливании сгорают органические вещества и частично разлагаются карбонаты.
5. Окисляемость – показатель, характеризующий содержание в воде органических веществ. Перманганатная окисляемость – 5,3 мг-экв/л.
6. Общая жесткость Жо (мг-экв/л, мкг-экв/л) – суммарная концентрация в воде катионов кальция и магния. Общую жесткость подразделяют на карбонатную (Жк) и некарбонатную (Жнк): Жо= Жк+ Жнк Карбонатная жесткость обуславливается наличием в воде бикарбонатов и карбонатов кальция и магния, некарбонатная жесткость – присутствием в воде хлоридов и сульфатов кальция и магния. Жо – 4,29 мг-экв/л.
7. Общая щелочность воды Що (мг-экв/л) – суммарная концентрация в воде растворимых гидроксидов и анионов слабых кислот НСО3- и СО32- за вычетом концентрации ионов водорода. Що – 4,1 мг-экв/л.
8. Ионный состав воды. Вода всегда электрически нейтральна, поэтому сумма концентраций содержащихся в ней катионов равна сумме концентраций анионов при условии, что они выражены в мг-экв/л. Этой закономерностью, называемой уравнением электронейтральности раствора, пользуются при проверке правильности выполнения анализа воды. В водах энергетических объектов могут присутствовать ионы, приведенные в таблице:
| Катионы
| Анионы
|
| Водород Н+
Натрий Nа+ - 9,2
Калий К+
Аммоний NН4+
Кальций Са2+
Магний Мg2+
Железо двухвалентное Fe2+
Железо трехвалентное Fe3+
Алюминий Аl3+
Медь Сu2+
| Гидроксильный ОН-
Бикарбонатный НСО3-
Карбонатный СО32-
Нитритный NO2-
Нитратный NO3-
Хлоридный Cl- - 5,3
Фторидный F-
Сульфатный SO42- - 10,0
Силикатный SiO32- - 0,68
Ортофосфатный РО43-
Гидросульфидный НS-
|
| Выбор и расчёт системы подготовки воды
| |
Химически чистая вода является очень слабым электролитом, только одна из десяти миллионов молекул диссоциирует на ионы Н+ и ОН-: Н2ОÛН+ + ОН-.
Отрицательный логарифм концентрации водородных ионов, называемый водородным показателем рН, для химически чистой воды равен 7. В зависимости от значения рН водного раствора оценивают реакцию среды:
| Реакция среды
| Значение рН
|
| Кислая
| 1-3
|
| Слабокислая
| 4-6
|
| Нейтральная
| 7
|
| Слабощелочная
| 8-10
|
| Щелочная
| 11-14
|
Вода для питьевых целей имеет рН=6,5-9,0.
9. Растворимые газы. Для вод, используемых для энергетических целей, важное значение имеют растворенные в воде газы: кислород, углекислота, сероводород, аммиак. Кислород поступает в воду из воздуха, где его содержится около 21%. Концентрация кислорода в поверхностных водах близка к значению растворимости его при данной температуре и давлении. Растворимость О2 при контакте с воздухом при атмосферном давлении 760 мм Нg следующая:
| Температура воды, оС
| 0
| 10
| 20
| 25
| 90
| 100
|
| Содержание О2, мг/л
| 14,6
| 11,3
| 9,1
| 8,3
| 1,6
| 0
|
Основным источником поступления в воду углекислоты (содержание СО2 в воздухе невелико – всего 0,04%) являются биохимические процессы разложения органических веществ в природе. Растворяясь в воде, СО2 реагирует с водой, образуя гидратированную форму Н2СО3.



 ;
;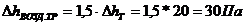 ;
; ;
;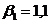 - коэффициент запаса;
- коэффициент запаса;
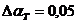 - присос воздуха в топочную камеру;
- присос воздуха в топочную камеру; - присос воздуха в воздуховод;
- присос воздуха в воздуховод;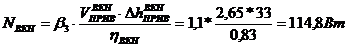 ;
; - коэффициент запаса;
- коэффициент запаса;



