Как правило, скорость химической реакции увеличивается с повышением температуры. Количественно эта зависимость оценивается величиной температурного коэффициента скорости химической реакции γ, который показывает, во сколько раз увеличивается скорость реакции при повышении температуры на 100С (правило Вант-Гоффа): «При повышении температуры на каждые 100С скорость гомогенной реакции увеличивается в γ раз»:
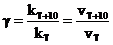 , (3.9)
, (3.9)
где kT– константа скорости при температуре Т; kТ+10 – константа скорости при температуре Т + 10, γ – температурный коэффициент скорости реакции, значение которого обычно лежит в интервале от 2 до 4.
Если изменение температуры составляет величину 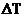 = Т2 - Т1 , то правило Вант-Гоффа запишется в общей форме
= Т2 - Т1 , то правило Вант-Гоффа запишется в общей форме
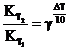 . (3.9а)
. (3.9а)
Более строгую зависимость константы скорости реакции от температуры устанавливает уравнение Аррениуса
k = А∙е– Eoп/RT, (3.10)
lnk = lnА – Eoп/RT , (3.11)
где А − предэкспоненциальный множитель; Eoп– опытная энергия активации; R – универсальная газовая постоянная; T – абсолютная температура.
Необходимым условием взаимодействия молекул является их столкновение, т.е. такое сближение, при котором электроны, атомы, ионы одной молекулы попадают в сферу действия полей электронов, атомов, ионов другой молекулы. Но не каждое соударение приводит к взаимодействию, реагируют только молекулы, обладающие в момент столкновения необходимым избытком энергии. Такие молекулы называются «активными». Энергию, которую надо сообщить молю вещества в стандартном состоянии, чтобы его молекулы стали активными в данной реакции, называют энергией активации. Истинная энергия активации, вообще говоря, не совпадает с опытной энергией активации, определяемой по уравнению (3.10). Чем больше энергия активации, тем меньше в данных условиях активных молекул и тем медленнее протекает реакция.
Величина Еактзависит от природы реагирующих веществ. Значение величины опытной энергии активации легко определить на основании уравнения (3.11) по наклону прямой lnk – Т-1 (рис.. 3.2).
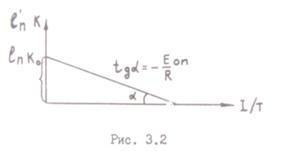
Тангенс угла наклона прямой позволяет определить энергию активации
tgα =  , а отрезок, отсекаемый на оси ординат, – предэкспоненциальный множитель А.. Расчет Еоп можно провести аналитически, интегрируя уравнение Аррениуса в пределах от Т1 до Т2 и от k1 до k2:
, а отрезок, отсекаемый на оси ординат, – предэкспоненциальный множитель А.. Расчет Еоп можно провести аналитически, интегрируя уравнение Аррениуса в пределах от Т1 до Т2 и от k1 до k2:
ln  . (3.12)
. (3.12)
Таким образом, существует две принципиальные возможности ускорения реакции: а) увеличение температуры, б) снижение энергии активации. Последняя осуществляется с помощью катализаторов.
Влияние катализаторов
Для многих реакций можно подобрать такое вещество, которое, присутствуя даже в небольшом количестве в смеси веществ, способствует химической реакции. Такие вещества, которые обязательно участвуют в процессе, но в конце реакции регенерируются и остаются химически неизменными, называются катализаторами. Поскольку принципиальная осуществимость и пределы протекания реакции определяются величиной и знаком изобарно-изотермического потенциала (∆G < 0), катализатор лишь ускоряет время достижения равновесного состояния, но не изменяет его. Действие катализаторов объясняется главным образом тем, что они уменьшают энергию активации реакции. В зависимости от того, находится ли катализатор в той же фазе, что и реагирующее вещество, или образует самостоятельную фазу, говорят о гомогенном или гетерогенном катализе. Механизм каталитического действия для них неодинаков, однако и в том и в другом случае происходит ускорение реакции за счет снижения Еакт. Для гомогенных реакций считают, что катализатор образует в той же фазе промежуточные реакционно-способные продукты. Медленно протекающий процесс, например реакция
А + В = АВ
в присутствии катализатора происходит в две стадии:
А + К = АКи АК + В = АВ + К,
т.е. сначала образуются частицы промежуточного соединения АК, которое, реагируя с веществом В, дает в итоге конечный продукт АВ с регенерацией катализатора К. При гетерогенном катализе ускорение процесса обычно связано с каталитическим действием поверхности твердого катализатора.
Порядок величины ускоряющего действия катализатора может быть оценен по уравнению (3.10). Так как величина Еоп стоит в показателе степени, то даже сравнительно небольшое ее уменьшение под действием катализатора должно привести к значительному увеличению константы скорости.
Цепные реакции
В некоторых случаях при различных энергетических воздействиях молекулы реагентов, поглощая энергию, распадаются на свободные радикалы, т.е. частицы (атомы, группы атомов – осколки молекул), имеющие неспаренный электрон. Свободные радикалы неустойчивы и отличаются высокой химической активностью. Они стремятся использовать свою потенциальную возможность образования ковалентной связи и легко разрушают другие молекулы с образованием новых радикалов. Таким образом, один первичный акт образования активной частицы приводит к химическому превращению огромного ряда частиц. Такие превращения называются цепными реакциями. Если в каждом элементарном акте цепной реакции один атом или радикал дает не более одного нового, цепь называется простой, если же несколько новых – разветвленной. Для цепных реакций характерны три стадии: возникновение цепи, развитие и обрыв цепи.
Примером цепной реакции служит фотохимический синтез хлористого водорода из водорода и хлора, суммарное уравнение этой реакции записывается следующим образом:
Н2 + Cl2 → 2 HCl.
За счет внешнего источника энергии (свет, электроразряд, нагревание, α-. β- или γ-излучение и т.д.) образуются свободные радикалы или атомы, обладающие ненасыщенными валентностями. Так как энергия связи атомов в молекуле хлора ( 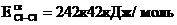 ) ниже, чем в молекуле водорода (
) ниже, чем в молекуле водорода (  ), то легче под внешним воздействием диссоциируют молекулы хлора.
), то легче под внешним воздействием диссоциируют молекулы хлора.
I стадия цепной реакции – инициация (образование радикалов, дающих начало цепи):
Cl2 + hν = 2Cl∙
II стадия (рост цепи), в ходе которой радикалы взаимодействуют с исходными молекулами, причем в каждом звене цепи вновь образуется новая активная частица:
H2 + Cl∙ → HCl + H∙
H· + Cl2 → HCl + Cl∙
Cl· + H2 → HCl + H∙
H· + Cl2 → HCl + Cl∙
III стадия(обрыв цепи)происходит при столкновении двух одинаковых радикалов при условии, что выделяющаяся энергия может быть отдана третьему телу
H∙ + H∙ → H2
Cl∙ + Cl∙ → Cl2
Причиной обрыва может служить также захват радикалов стенкой реакционного сосуда, взаимодействие радикала с примесями и образование малоактивного радикала.
Для простых неразветвленных цепей скорость реакции может быть представлена как произведение длины цепи l на число активных частиц n, зарождающаяся в единице объема за единицу времени:
v = n∙l. (3.13)
Такие реакции описываются обычными уравнениями химической кинетики с константой скорости, увеличенной в l раз.
Примером разветвленной цепной реакции может служить реакция образования воды из простых веществ. Зарождение цепи происходит при нагревании или электроразряде
H2 + О2 + hν → 2ОН∙.
Образовавшиеся радикалы ОН∙ реагируют с молекулой водорода, образуя воду и новые радикалы − атомы водорода:
О H· + Н2 → Н2О + H·.
Радикалы H· в свою очередь реагируют с молекулами кислорода, образуя уже два радикала (разветвление цепи):
О2 + H → ОH· + ОH·.
Для цепных реакций с разветвленной цепью изменение скорости реакции во времени выражается уравнением
v= А (еφτ– 1), (3.14)
где φ – константа нарастания, характеризующая скорость разветвления цепи; τ – время; е − основание натурального логарифма; А – эмпирическая константа для данной реакции.
При значительных величинах τуравнение (3.14) можно записать
v = А еφ τ . (3.15)
Константы φ и А учитывают вероятность разветвления и обрыва цепи
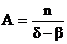 и
и 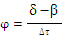 .
.
где n – число активных частиц; δ – вероятность разветвления цепи в данном звене; β − вероятность обрыва цепи в данном звене; Δτ – время между двумя последовательными реакциями в цепи.
Если обрывы цепи преобладают над разветвлениями β>δ, реакция протекает с постоянной скоростью, а при очень значительном их преобладании – с затухающей скоростью. В случае, когда δ>β, реакция идет с возрастанием скорости до воспламенения, а при высоких температурах и давлениях – до взрыва.



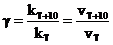 , (3.9)
, (3.9)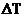 = Т2 - Т1 , то правило Вант-Гоффа запишется в общей форме
= Т2 - Т1 , то правило Вант-Гоффа запишется в общей форме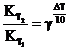 . (3.9а)
. (3.9а)
 , а отрезок, отсекаемый на оси ординат, – предэкспоненциальный множитель А.. Расчет Еоп можно провести аналитически, интегрируя уравнение Аррениуса в пределах от Т1 до Т2 и от k1 до k2:
, а отрезок, отсекаемый на оси ординат, – предэкспоненциальный множитель А.. Расчет Еоп можно провести аналитически, интегрируя уравнение Аррениуса в пределах от Т1 до Т2 и от k1 до k2: . (3.12)
. (3.12)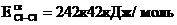 ) ниже, чем в молекуле водорода (
) ниже, чем в молекуле водорода (  ), то легче под внешним воздействием диссоциируют молекулы хлора.
), то легче под внешним воздействием диссоциируют молекулы хлора.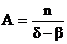 и
и 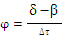 .
. 


