БИОЛОГИЧЕСКАЯ ХИМИЯ –
БИОХИМИЯ ПОЛОСТИ РТА
Индивидуальный практикум
Часть I
Великий Новгород
2014
| ББК 28.707.2
| Печатается по решению
|
| Б 63
| РИС НовГУ
|
Р е ц е н з е н т
профессор Максимюк Н. Н.
Биологическая химия - биохимия полости рта. Индивидуальный практикум/ Часть I/ сост. Л. В. Андреева, Ю.В. Марьяновская, Н.Н. Севостьянова. НовГУ им. Ярослава Мудрого. Великий Новгород, 2014 - 41 с.
Методические указания предназначены для изучения дисциплины «Биологическая химия - биохимия полости рта» для студентов специальности 31.05.03 «Стоматология»
© Л. В. Андреева, Ю.В. Марьяновская, Н.Н. Севостьянова, составители, 2014
© Новгородский государственный университет, 2014
ОГЛАВЛЕНИЕ
|
| С.
|
| ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 1 Правила работы и техника безопасности в биохимической лаборатории. Строение и свойства белков
УЭМ 1 СТРОЕНИЕ И СВОЙСТВА БЕЛКОВ
ЛАБОРАТОРНАЯ РАБОТА 1 Свойства белков
| 4
7
|
| ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 2 Семинар Сложные белки. Коллаген. Эластин. Протеогликаны. Межклеточный матрикс
ЛАБОРАТОРНАЯ РАБОТА 2 Гидролиз нуклеопротеидов дрожжей
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 3 Контрольная работа 1 Простые и сложные белки: строение, свойства, функции
| 11
14
17
|
| УЭМ 2 ФЕРМЕНТЫ
ЛАБОРАТОРНАЯ РАБОТА 3:Витамины и их коферментные функции. Количественное определение витамина С
ЛАБОРАТОРНАЯ РАБОТА 4: Природа и свойства ферментов
|
19
22
|
| ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 4. Семинар Ферменты слюны и ротовой жидкости
| 24
|
| ЛАБОРАТОРНАЯ РАБОТА 5 Определение активности пероксидазы в слюне по Попову
| 26
|
| ЛАБОРАТОРНАЯ РАБОТА 6 Определение активности щелочной фосфатазы в слюне
| 27
|
| ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 5. Контрольная работа 2 Коферментные функции витаминов. Ферменты слюны и ротовой жидкости
УЭМ 3 ЭНЕРГЕТИЧЕСКИЙ ОБМЕН. ОБМЕН УГЛЕВОДОВ
ЛАБОРАТОРНАЯ РАБОТА 7 Тканевое дыхание и окислительное фосфорилирование
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 6. Семинар Энергетический обмен. Фосфорилирование. Тканевое дыхание. Общий путь катаболизма
| 28
30
34
|
| ЛАБОРАТОРНАЯ РАБОТА 8 Определение глюкозы в биологических жидкостях глюкозооксидазным способом
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 7. Семинар Обмен углеводов
| 36
37
|
| ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 8. Контрольная работа 3 Энергетический обмен. Обмен углеводов
ЛАБОРАТОРНАЯ РАБОТА 9 Решение ситуационных задач по темам: Простые и сложные белки. Ферменты. Витамины.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 9 Решение ситуационных задач по темам: Энергетический обмен. Обмен и функции углеводов.
| 38
38
40
|
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 1
Техника безопасности в биохимической лаборатории
УЭМ 1. СТРОЕНИЕ, СВОЙСТВА И ФУНКЦИИ БЕЛКОВ
ЛАБОРАТОРНОЕ ЗАНЯТИЕ 1
Тема: Правила работы и техника безопасности в биохимической лаборатории. Общие принципы и методы биохимических исследований в практическом здравоохранении. Аминокислоты, пептиды, белки. Строение, свойства, функции. Методы выделения, очистки, качественного и количественного определения белков и аминокислот
Основная задача биохимии – объяснить, как функционируют живые системы с точки зрения процессов, протекающих в клетках. В биохимии используются практически все современные методы физико-химического анализа. Это и аналитические, и химические, и специальные (спектроскопия, центрифугирование, хроматография, электрофорез и др.) методы.
Вопросы для подготовки к занятию
- Заполните таблицу:
| № п/п
| Свойства радикала
| Полное и
сокращенное название
аминокислот
| Строение аминокислот
| Название функциональных групп радикалов
|
| 1.
|
Гидрофобные
|
|
|
|
| 2.
|
|
|
|
| 3.
|
|
|
|
| 4.
|
|
|
|
| 5.
|
|
|
|
| 6.
|
|
|
|
| 7.
|
|
|
|
| 8.
|
|
|
|
| 9.
|
|
|
|
| Гидрофильные:
|
| 10.
|
Незаряженные
|
|
|
|
| 11.
|
|
|
|
| 12.
|
|
|
|
| 13.
|
|
|
|
|
| 14.
|
|
|
|
| 15.
|
|
|
|
| 16.
|
Анионные
|
|
|
|
| 17.
|
|
|
|
| 18.
|
Катионные
|
|
|
|
| 19.
|
|
|
|
| 20.
|
|
|
|
| | | | | | |
- Напишите формулу пентапептида:
Асп-Вал-Глу-Фен-Лиз.
- Выделите в пептиде повторяющиеся группы, образующие пептидный остов, и вариабельные группы, представленные радикалами аминокислот.
- Обозначьте в пептиде N- и С-концы.
- Подчеркните пептидные связи.
6. Напишите другой пептид, состоящий из тех же аминокислот.
7. Перечислите связи, формирующие вторичную, супервторичную, третичную и четвертичную структуру белков.
8. Заполните таблицу (укажите аминокислотные остатки, радикалы которых могут участвовать в образовании перечисленных видов связей).
| Гидрофобное взаимодействие
| Водородная связь
| Ионная связь
| Дисульфидная связь
|
|
|
|
|
|
Выполните задания:
ЛАБОРАТОРНАЯ РАБОТА 1
Тема: Свойства белков
Оформление работы
Результаты опытов занести в таблицу:
| Наименование реакций
| Реагент
| Субстрат
| Наблюдаемое окрашивание
| Чем обусловлена реакция
|
| Биуретовая
|
| а) яичный белок
б) желатин
|
|
|
| Нингидриновая
|
| а) яичный белок
б) желатин
|
|
|
| Ксантопротеиновая
|
| а) яичный белок
б) желатин
|
|
|
| Реакция Фоля
|
| а) яичный белок
б) желатин
|
|
|
Оформление работы
Записать осадочные реакции белков. Результаты опытов занести в таблицу.
| № пробирки
| Субстрат
| Осаждающий реагент
| Характер и цвет осадка
| Обратимое или необратимое осаждение
| Чем обусловлена реакция и ее особенности
|
| 1.
|
|
|
|
|
|
| 2.
|
|
|
|
|
|
| 3.
|
|
|
|
|
|
| 4.
|
|
|
|
|
|
| 5.
|
|
|
|
|
|
Вывод:
Дата: Подпись преподавателя:
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 2
ЛАБОРАТОРНОЕ ЗАНЯТИЕ 2
Задания для внеаудиторной работы
9. Соедините химическими связями динуклеотид, состоящий из АМФ и ЦМФ.
10. Покажите водородные связи, образующиеся при соединении А и Т и Г и Ц во вторичной структуре ДНК.
11. Перечислите свойства генетического кода.
ЛАБОРАТОРНАЯ РАБОТА 2
Вопросы к контрольной работе 1 по теме: Белки. Строение, свойства и функции
1. Представление о белках как важнейшем классе органических веществ и структурно – функциональном компоненте организма человека.
2. Химические и физико-химические свойства белков.
3. Аминокислоты, входящие в состав белков, их строение и свойства. Незаменимые аминокислоты.
4. Пептидная связь. Первичная структура белковой молекулы.
5. Уровни структурной организации белков.
6. Конформация пептидных цепей в белках (вторичная, третичная, четвертичная структура).
7. Лабильность пространственной структуры белков и их денатурация.
8. Классы сложных белков.
9. Строение нуклеиновых кислот.
10. Особенности и главные функции ДНК и РНК - важнейших структурных компонентов нуклеопротеидов.
11. Биосинтез ДНК. Субстраты, источники энергии, матрица, ферменты репликативного комплекса.
12. Биосинтез РНК.
13. Трансляция – биосинтез белковой молекулы.
14. Свойства биологического кода.
15. Молекулярные механизмы генетической изменчивости. Мутации.
16. Наследственные и вторичные дефекты иммунной системы. Наследственные болезни; распространенность и происхождение дефектов в генотипе; биохимические механизмы развития болезней. Многообразие наследственных болезней.
17. Строение, свойства и функции коллагена.
18. Строение, свойства и функции эластина.
19. Строение и свойства гликозаминогликанов и протеогликанов.
20. Строение и функции межклеточного матрикса.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 3
ЛАБОРАТОРНОЕ ЗАНЯТИЕ 3
У больных с поврежденными почками, несмотря на нормально сбалансированную диету, часто развивается почечная остеодистрофия – рахитоподобное заболевание, сопровождающееся интенсивной деминерализацией костей. Какой витамин участвует в минерализации костей? Почему повреждение почек приводит к деминерализации?
3. Установите соответствие:
| А. НАД.
| - Производное витамина В6.
|
| Б. Тиаминпирофосфат.
| - Производное витамина В2.
|
| В. КоА.
| - Производное витамина В1.
|
| Г. ФАД.
| - Производное витамина В3.
|
| Д. Пиридоксальфосфат.
| - Производное витамина В5.
|
ЛАБОРАТОРНАЯ РАБОТА 3
ЛАБОРАТОРНОЕ ЗАНЯТИЕ 4
ЛАБОРАТОРНАЯ РАБОТА 4
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 4
ЛАБОРАТОРНАЯ РАБОТА 5
ЛАБОРАТОРНАЯ РАБОТА 6
Проведение анализа
Кинетический метод:
В кювету внести 1 мл рабочего реагента, инкубировать 10 мин при 37°С, затем добавить 0,02 мл слюны и перемешать. Через 90 сек измерить оптическую плотность (Е1). Через 90 сек повторить измерение (Е2). Длина волны 405 (400 – 425) нм, кювета с длиной оптического пути 3мм, раствор сравнения – рабочий реагент.
Активность (А) ЩФ ( Ед/л) рассчитывается по формуле:
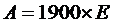
где Е = Е2 – Е1 – изменение оптической плотности в опытной пробе.
Вопросы к контрольной работе по теме: Коферментные функции витаминов. Ферменты слюны и ротовой жидкости
1. Укажите оптимум действия ферментов: амилазы, липазы, пепсина, трипсина.
2. Перечислите виды специфичности. Приведите пример абсолютной и относительной специфичности.
3. Влияние неспецифических факторов на активность фермента (Т, рН и т.д.).
4. Что такое проферменты и изоферменты. Приведите примеры.
5. Какие реакции ускоряют эстеразы, пептидазы, гликозидазы, фосфатазы? К какому классу ферментов они относятся? Какой вид специфичности характерен для этих ферментов?
6. К какому классу относятся и какова функция ферментов: дегидрогеназ, редуктаз, флавиновые ферменты, цитохромы, аминотрансферазы, киназы, декарбоксилазы, карбоксилазы. Какие коферменты входят в состав этих ферментов?
7. К какому классу ферментов относятся ферменты пищеварительного тракта?
8. Что называется энергетическим барьером реакции? Что такое энергия активации? Что понимают под «активированным состоянием»?
9. Какие факторы влияют на скорость ферментативной реакции? Какова структура регуляторных ферментов?
10. Каким образом влияют на активность ферментов структурные аналоги субстратов?
11. Типы обратимого ингибирования ферментов. Охарактеризуйте каждый вид обратимого ингибирования, приведите примеры.
12. Примеры использования ингибиторов ферментов в качестве лекарственных препаратов.
13. Что понимают под энзимопатологией? Приведите примеры энзимопатий, охарактеризуйте их.
14. Что понимают под энзимодиагностикой? В каких объектах определяют активность ферментов с целью диагностики заболеваний?
15. Что понимают под энзимотерапией? Назовите препараты, используемые для энзимотерапии.
16. Суть коферментной функции витаминов. Биологические функции кофермента, образованного из витамина В1, В2, В6, РР (В5).
17. На каких свойствах аскорбиновой кислоты основано ее участие в обменных процессах? Назовите вещества, в синтезе которых участвует аскорбиновая кислота.
18. Какие компоненты слюны выполняют защитную функцию?
19. Какова роль ферментов слюны в минерализации твердых тканей зуба?
20. При каких условиях слюна становится деминерализующей жидкостью?
21. Какую роль выполняют нитраты и нитриты в составе слюны?
22. Какие регуляторные вещества входят в состав слюны?
23. Каковы функции слюнных желез?
24. Антигенспецифические вещества слюны
25. В чем заключается роль кислой и щелочной фосфатаз в процессе минерализации твердых тканей зуба?
26. Какие ферменты участвуют в деструкции пародонта? Как регулируется их активность?
27. Какова роль пищеварительных ферментов, содержащихся в слюне? Каковы их оптимальные рН?
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 5
ЛАБОРАТОРНОЕ ЗАНЯТИЕ 7
Задания для внеаудиторной работы
1. Напишите структурные формулы коферментов НАД, ФАД, УХ в окисленной и восстановленной формах, укажите витамины, входящие в их состав.
2. Напишите активную часть простетической группы цитохромов в окисленной и восстановленной формах.
3. В чем заключаются особенности строения цитохромоксидазы? Изобразите схематично ее строение.
4. Изобразите в виде схемы путь переноса электронов и протонов от субстрата на кислород. Укажите полную, укороченную и короткую дыхательную цепь. Отметьте пункты сопряжения окисления и фосфорилирования. Укажите ингибиторы дыхательной цепи и участки ингибирования.
5. Напишите реакцию фосфорилирования АДФ. Назовите типы фосфорилирования.
6. Изобразите схему окислительного фосфорилирования согласно хемо-осмотической теории Митчелла.
7. Напишите химические формулы веществ - разобщающих агентов окислительного фосфорилирования, укажите механизм разобщения.
Выполните задания:
1. В эксперименте с изолированными митохондриями в качестве доноров водорода использовали два субстрата: изоцитрат и сукцинат. Одинаков ли коэффициент Р/О для этих субстратов? Укажите его значение.
2. К каждой реакции подберите соответствующий фермент:
1. Субстрат-Н2 + НАД+ → Субстрат + НАДН + Н+
2. QН2 + 2 цитохрома С (Fе3+) → Q + 2 цитохрома С (Fе2+)
3. НАДН + Н+ + Флавопротеид → НАД+ + Флавопротеид (восст.)
4. Сукцинат + ФАД → фумарат + ФАДН2
А. НАД-зависимая дегидрогеназа
Б. QН2-дегидрогеназа
В. ФАД-зависимая дегидрогеназа
Г. НАДН-дегидрогеназа
3. Коэффициент Р/О при окислении НАДН в присутствии 2,4-динитрофенола равен:
ЛАБОРАТОРНАЯ РАБОТА 7
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 6
ЛАБОРАТОРНОЕ ЗАНЯТИЕ 8
Задания для внеаудиторной работы
1. Изобразите общую схему источников и путей расходования глюкозы в организме.
2. Укажите, как регулируется транспорт глюкозы (зависит или нет от инсулина):
А) В клетки нервной ткани:
Б) В клетки мышц:
Г) В клетки жировой ткани:
Д) В клетки печени:
3. Напишите реакции анаэробного гликолиза, укажите ферменты, их активаторы и ингибиторы. Рассчитайте количество АТФ, синтезируемое из одной молекулы глюкозы при анаэробном гликолизе.
4. Изобразите в виде схемы аэробный гликолиз. Рассчитайте количество АТФ, синтезируемое из одной молекулы глюкозы при аэробном гликолизе.
5. Укажите норму содержания глюкозы в крови. Перечислите патологии, связанные с количественным содержанием глюкозы в крови, назовите их причины.
Выполните задания:
1.Установите соответствие:
Нарушение обмена углеводов характеризуется:
| 1) сахарный диабет
| а) нарушением обмена гликогена
|
| 2) гипогликемия
| б) резким снижением содержания глюкозы в крови
|
| 3) глюкозурия
| в) повышением концентрации глюкозы в крови
|
| 4) гликогенозы
| г) присутствием глюкозы в моче
|
2. Уровень глюкозы в крови после 40-часового голодания поддерживается за счет:
А) гликолиза;
Б) гликогенолиза;
В) Гликогенолиза и глюконеогенеза;
Г) пентозофосфатного пути;
Д) Глюконеогенеза
3. Установите соответствие:
| A. Глюконеогенез в печени
| 1. Источник глюкозы для других органов
|
| Б. Распад гликогена в печени
| 2. Обеспечивает глюкозой мозг при длительном голодании
|
| В. Оба
| 3. Образует глюкозу, не используя энергию АТФ
|
| Г. Ни один
| 4. Ускоряется в абсорбтивном периоде
|
4. Назовите причины наследственных заболеваний:
А) галактоземия-
Б) фруктоземия-
В) непереносимость лактозы –
Г) непереносимость сахарозы-
ЛАБОРАТОРНАЯ РАБОТА 8
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 7
Семинар Обмен углеводов
Вопросы к контрольной работе по теме: Энергетический обмен. Обмен углеводов
1 Введение в обмен веществ. Питание, метаболизм, выделение продуктов метаболизма.
2 Эндергонические и экзергонические реакции в живой клетке. Реакции с сопряженными потенциалами. Макроэргические соединения.
3 Энергетический обмен. Общие пути катаболизма. Схема катаболизма основных питательных веществ - углеводов, жиров, белков, (аминокислот); понятие о специфических путях катаболизма до образования пирувата из углеводов и большинства аминокислот до образования ацетил-КоА из жирных кислот и некоторых аминокислот и общих путях катаболизма (окисление пирувата и ацетил-КоА).
4 Митохондриальная цепь переноса электронов. Дегидрирование субстратов и окисления водорода (образование воды), как источник энергии для синтеза АТФ. Дегидрогеназы и первичные акцепторы водорода НАД и флавопротеиды; НАД Н - дегидрогеназы.
5 Строение митохондрий, структурная организация цепи переноса электронов и протонов. Цепь переноса электронов как часть системы дыхания, начинающейся вдыханием воздуха и связыванием кислорода.
6 Окислительное фосфорилирование: коэффициент Р/О.
7 Хемио-осмотическая теория Митчелла.
8 Разобщение тканевого дыхания и окислительного фосфорилирования; терморегуляторная функция тканевого дыхания.
9 Окислительное декарбоксилирование пировиноградной кислоты: строение пируватдегидрогеназного комплекса.
10 Цикл лимонной кислоты. Связь между общими путями катаболизма и цепью переноса электронов и протонов.
11 Аллостерические механизмы регуляции цитратного цикла. Образование углекислого газа при тканевом дыхании.
12 Активаторы и ингибиторы ЦТК.
13 Анаболические функции цикла лимонной кислоты.
14 Нарушения энергетического обмена: гипоэнергетические состояния и их причины.
15 Основные углеводы организма человека, их содержание в тканях, биологическая роль. Основание углеводы пищи.
16 Переваривание углеводов. Глюкоза как важнейший метаболит углеводного обмена: общая схема источников и путей расходования глюкозы в организме, катаболизм глюкозы.
17 Анаэробный распад глюкозы (гликолиз). Гликолитическая оксидоредукция; пируват как акцептор водорода; субстратное фосфорилирование. Распределение и физиологические значение анаэробного распада глюкозы.
18 Аэробные распад - основной путь катаболизма глюкозы у человека и других аэробных организмов.
19 Биосинтез глюкозы (глюконеогенез) из молочной кислоты и других веществ.
20 Представление о пентозофосфатном пути превращения глюкозы. Окислительные реакции (до стадии рибулозо-5-фосфат).
21 Обмен фруктозы и галактозы.
22 Обмен сахарозы, лактозы, мальтозы.
23 Наследственные нарушения обмена моносахаридов и дисахаридов: галактоземия, непереносимость дисахаридов.
24 Свойства и распространение гликогена как резервного полисахарида. Биосинтез гликогена. Мобилизация гликогена. Физиологическое значение резервирования и мобилизации гликогена.
25 Роль печени в углеводном обмене.
26 Взаимосвязь гликолиза в мышцах и глюконеогенеза в печени (цикл Кори).
27 Регуляция углеводного обмена.
28 Патологии углеводного обмена.
29 Сахарный диабет, биохимические характеристики патогенеза и стратегия лечения.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 8
ЛАБОРАТОРНОЕ ЗАНЯТИЕ 9
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 9
БИОЛОГИЧЕСКАЯ ХИМИЯ –
БИОХИМИЯ ПОЛОСТИ РТА
Индивидуальный практикум
Часть I
Великий Новгород
2014
| ББК 28.707.2
| Печатается по решению
|
| Б 63
| РИС НовГУ
|
Р е ц е н з е н т
профессор Максимюк Н. Н.
Биологическая химия - биохимия полости рта. Индивидуальный практикум/ Часть I/ сост. Л. В. Андреева, Ю.В. Марьяновская, Н.Н. Севостьянова. НовГУ им. Ярослава Мудрого. Великий Новгород, 2014 - 41 с.
Методические указания предназначены для изучения дисциплины «Биологическая химия - биохимия полости рта» для студентов специальности 31.05.03 «Стоматология»
© Л. В. Андреева, Ю.В. Марьяновская, Н.Н. Севостьянова, составители, 2014
© Новгородский государственный университет, 2014
ОГЛАВЛЕНИЕ
|
| С.
|
| ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 1 Правила работы и техника безопасности в биохимической лаборатории. Строение и свойства белков
УЭМ 1 СТРОЕНИЕ И СВОЙСТВА БЕЛКОВ
ЛАБОРАТОРНАЯ РАБОТА 1 Свойства белков
| 4
7
|
| ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 2 Семинар Сложные белки. Коллаген. Эластин. Протеогликаны. Межклеточный матрикс
ЛАБОРАТОРНАЯ РАБОТА 2 Гидролиз нуклеопротеидов дрожжей
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 3 Контрольная работа 1 Простые и сложные белки: строение, свойства, функции
| 11
14
17
|
| УЭМ 2 ФЕРМЕНТЫ
ЛАБОРАТОРНАЯ РАБОТА 3:Витамины и их коферментные функции. Количественное определение витамина С
ЛАБОРАТОРНАЯ РАБОТА 4: Природа и свойства ферментов
|
19
22
|
| ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 4. Семинар Ферменты слюны и ротовой жидкости
| 24
|
| ЛАБОРАТОРНАЯ РАБОТА 5 Определение активности пероксидазы в слюне по Попову
| 26
|
| ЛАБОРАТОРНАЯ РАБОТА 6 Определение активности щелочной фосфатазы в слюне
| 27
|
| ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 5. Контрольная работа 2 Коферментные функции витаминов. Ферменты слюны и ротовой жидкости
УЭМ 3 ЭНЕРГЕТИЧЕСКИЙ ОБМЕН. ОБМЕН УГЛЕВОДОВ
ЛАБОРАТОРНАЯ РАБОТА 7 Тканевое дыхание и окислительное фосфорилирование
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 6. Семинар Энергетический обмен. Фосфорилирование. Тканевое дыхание. Общий путь катаболизма
| 28
30
34
|
| ЛАБОРАТОРНАЯ РАБОТА 8 Определение глюкозы в биологических жидкостях глюкозооксидазным способом
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 7. Семинар Обмен углеводов
| 36
37
|
| ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 8. Контрольная работа 3 Энергетический обмен. Обмен углеводов
ЛАБОРАТОРНАЯ РАБОТА 9 Решение ситуационных задач по темам: Простые и сложные белки. Ферменты. Витамины.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 9 Решение ситуационных задач по темам: Энергетический обмен. Обмен и функции углеводов.
| 38
38
40
|
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 1