| %
| 1
| 2
| 3
| 4
| 5
| 6
| 7
| 8
| 9
| 10
|
| 1
| 0
| 1,01
| 2,04
| 3,1
| 4,17
| 5,26
| 6,43
| 7,53
| 8,7
| 9,89
|
| 10
| 11,11
| 12,44
| 13,63
| 14,95
| 16,28
| 17,65
| 19,05
| 20,48
| 21,95
| 23,46
|
| 20
| 25,01
| 26,58
| 28,2
| 29,87
| 31,58
| 33,33
| 35,14
| 36,99
| 38,9
| 40,84
|
| 30
| 42,85
| 44,94
| 47,05
| 49,25
| 51,52
| 53,85
| 56,24
| 58,74
| 61,29
| 63,94
|
| 40
| 66,67
| 69,49
| 72,41
| 75,44
| 78,6
| 81,81
| 85,2
| 88,67
| 92,3
| 96,07
|
| 50
| 100
| 104,1
| 108,3
| 112,8
| 117,4
| 122,2
| 127,3
| 132,6
| 138,1
| 143,9
|
| 60
| 150
| 156,4
| 163,2
| 170,3
| 177,8
| 185,7
| 191,2
| 208
| 212,5
| 229,5
|
| 70
| 233,3
| 244,9
| 257,6
| 270,3
| 284,6
| 300
| 316,7
| 334,8
| 354,6
| 376,2
|
| 80
| 400
| 426,3
| 455,5
| 488,3
| 525
| 566,6
| 614,3
| 669,3
| 733,3
| 876,2
|
| 90
| 900
| 1011
| 1150
| 1329
| 1566
| 1900
| 2400
| 3234
| 4900
| 9900
|
При составлении растворов, концентрация которых дана в процентах в таблице, вес раствора принимается за 100%. Поэтому, например, для приготовления 21-процентного раствора едкого кали отмеряют 21 часть этого вещества и 79 частей воды. Такие отвешивания не всегда удобны, поскольку чаще всего приходится исходить из объема или веса необходимого раствора, чтобы не приготовлять его в излишке. Тогда делают арифметические перерасчеты. Однако их можно избежать, если воспользоваться приведенной таблицей, которая позволяет определить, какое количество по весу вещества нужно на 100 частей или 100 см³ воды, если известна концентрация в процентах. Например, на 100 см³ 21- Что необходимо знать о несовместимости химических веществ
Несовместимость химических веществ проявляется в том, что при случайном смешивании, а иногда и при хранении рядом они вступают в реакцию. Если реакция сопровождается выделением большого количества тепла, то может произойти взрыв или самовозгорание. В других случаях воздействие веществ друг на друга приводит к соединению их и потере первоначальных свойств, в результате чего вещества становятся непригодными к употреблению. Вот некоторые несовместимые химические вещества:
Азотная кислота несовместима с глицерином, спиртом, эфирными маслами, смолами, сахаром, фенолом, опилками, ватой.
Алюминиевые квасцы несовместимы с едкими щелочами (едкий натр, едкое кали, нашатырный спирт), клеем и желатиной.
Аммиак (нашатырный спирт) и нашатырь несовместимы с формалином (формальдегидом) и йодом.
Бура несовместима с квасцами, нашатырем, серной кислотой, соляной кислотой.
Йод несовместим с аммиаком (нашатырным спиртом).
Кислоты несовместимы с мылом и щелочами (содой, поташом, известью и др.).
Марганцовокислый калий несовместим с органическими веществами - эфирами, винным спиртом, глицерином, танином, а также с аммиаком, нашатырем, серой, йодом, углем.
Сера несовместима с марганцовокислым калием, хлорной известью.
Серная кислота (купоросное масло) несовместима со скипидаром, спиртом и бензином.
Спирт несовместим с хромовой кислотой, марганцовокислым калием, клеем, желатиной, казеином.
процентного водного раствора едкого кали приходится 26,58 части едкого кали.
Обезжиривание в ваннах с растворителями
Сильно загрязненные детали можно грубо обезжирить промывкой в керосине или скипидаре. После этого детали промывают в техническом бензине, техническом бензоле, ксилоле или толуоле. Тщательное и окончательное обезжиривание достигается погружением или промывкой в чистом бензине, трихлорэтилене или других растворителях.
Недостатком этих веществ является их огне- и взрывоопасность (бензин, бензол, ксилол, толуол) и ядовитость паров (трихлорэтилен, бензин, бензол, ксилол, толуол). Поэтому с ними разрешается работать только в хорошо вентилируемых помещениях.
В настоящее время широко применяются фреоны. В отличие от вышеуказанных веществ фреон не взрывоопасен, не ядовит, не разрушает пластмассы, лакокрасочные покрытия и т.п.
Фреон-113 (трихлортрифторэтан) - самое лучшее обезжиривающее средство из группы фреонов. Это легкоподвижная прозрачная жидкость с низкой температурой кипения (47,6°С). Иногда фреон-113 смешивают с другими растворителями - ацетоном, спиртом и т.д.
Иногда фресковые обезжиривающие ванны снабжают ультразвуковыми излучателями или используют кипящий фреон, что максимально ускоряет растворение жиров. Фреон не имеет широкого применения из-за высокой стоимости.
Химический раствор для обезжиривания цветных металлов
Жидкое стекло 26 г
Тринатрийфосфат 8 г
Углекислый натрии безводный 4 г
Вода до 1 л
Все вещества растворяют в воде и доводят объем до 1 л.
Удаление металлических покрытий с изделий электролитическим способом (реставрация)
Удалить металлические покрытия с металлизированных деталей и изделий можно электролитическим способом, погружая детали и изделия в электролит. Действие электролита можно усилить подключением источника электрического тока к изделию, подвешенному в ванне с электролитом в качестве анода.
Ниже приведено несколько рецептов электролитов для снятия металлических покрытий с деталей и изделий. Указанные вещества растворяют в 500-600 мл воды, а затем объем раствора (электролита) доводят до 1 л.
Электролит для снятия никелевых покрытий со стальных изделий
Хромовый ангидрид 240 г
Борная кислота 30 г
Вода до 1 л
Рабочая температура электролита 85°С, плотность тока 1 А/дм².
Электролит для снятия никелевых покрытий с изделий из меди и латуни
Соляная кислота 14 г
Вода до 1 л
Рабочая температура электролита 18-20°С, плотность тока не более 2 А/дм². Используется постоянный ток при регулярном изменении полярности. Катод угольный.
Электролит для снятия хромовых покрытий с изделий из стали, никеля и сплавов магния
Едкий натр 90 г
Вода до 1 л
Рабочая температура электролита 20°С, плотность тока 2 А/дм².
Электролит для снятия оловянных покрытий с изделий из стали, меди и латуни
Едкий натр 120 г
Вода до 1 л
Рабочая температура электролита 18-20°С. Применяется постоянное напряжение 6 В при регулярном изменении полярности источника тока.
Полирование металлов электролитическим способом
Полируемые предметы подвешивают в электролитической ванне как аноды, т.е. к ним подводят положительный потенциал от источника постоянного тока, выпрямителя или аккумулятора.
Ниже приводятся рецепты для полирования.
Электролит для полирования стали, железа и его сплавов
Серная кислота концентрированная 300 мл
Ортофосфорная кислота концентрированная 600 мл
Вода 100 мл
Электролит готовят в стеклянной или фарфоровой посуде. Температура ванны около 70°С, плотность тока 60-70 А/дм². Полирование длится 1-5 мин. Отполированные детали после извлечения из ванны промывают в проточной воде, погружают в 10%-ный раствор углекислого натрия и снова промывают в проточной воде. Сушат детали в струе теплого воздуха.
Электролит для полирования меди и ее сплавов
Серная кислота концентрированная 10 г
Уксусная кислота 12,5 г
Хромовый ангидрид 12,5 г
Двухромовокислый натрий 37,5 г
Вода 1 л
Рабочая температура электролита 60-75°С, плотность тока 25-50 А/дм².
Электролит для полирования алюминия
Этиловый спирт денатурированный 576 мл
Хлористый аммоний 40 г
Хлористый цинк 180 г
Бутиловый спирт 64 г
Вода 128 мл
Полирование производится при напряжении 20-14 В. Рекомендуется через 1 мин деталь из ванны вынуть (при этом прекращается пассивация) и снова погрузить, повторив это в течение полирования несколько раз.
Декоративная отделка изделий из алюминия и его сплавов
Детали конструкции из алюминия и его сплавов можно окрасить в любой цвет.
С этой целью алюминий и его сплавы подвергают анодному оксидированию с последующей адсорбиционной окраской различными красителями. Делают это следующим образом. Отполированные до зеркального блеска детали подвергают обезжириванию в растворе, состоящем из тринагрийфосфата (50 г), едкого натрия (10 г) и жидкого стекла (силикатного клея) (30 г). Перечисленные химикаты растворяют в 1 л теплой воды в железной посуде (можно в кастрюле), затем детали, которые нужно окрасить, помещают на 1-2 мин в этот раствор, нагретый до 50-60°С.
Если указанные химикаты достать не удастся, обезжирить детали можно обыкновенным хозяйственным мылом с теплой водой. Детали тщательно обрабатывают щетинной щеткой в течение 10 мин.
Обезжиренные детали промывают холодной водой, затем для удаления пленки окислов погружают их на 2-3 мин в 50%-ную азотную кислоту. После чего детали снова тщательно промывают сильной струей воды и немедленно подвешивают в ванну для анодирования.
Электролитом для ванны анодирования служит раствор серной кислоты с удельным весом 1,12-1,13 при температуре 20°С. При смешивании кислоты с водой раствор сильно разогревается, поэтому кислоту следует подливать в воду небольшими порциями, все время перемешивая раствор стеклянной палочкой.
При попадании кислоты на кожу или на одежду необходимо немедленно смыть ее сильной струей воды и промыть крепким раствором соды.
Очень хорошим и более безопасным является электролит, приготовленный из бисульфата натрия (натрий сернокислый кислый), 250-300 г которого растворяют в 1 л воды. Рабочая температура электролита должна быть также не более 20°С. В качестве рабочей ванны можно использовать эмалированные кастрюли, керамические, стеклянные или пластмассовые бачки.
Для катодов при анодировании применяют листовой свинец, а анодом служит обрабатываемая деталь, которую подвешивают между двумя свинцовыми катодами на расстоянии 70-80 мм от них. Электролиз длится 40-50 мин, плотность постоянного тока 1-1,5 А/дм². Источником тока может служить аккумулятор достаточной емкости или выпрямитель, собранный на диодах типа Д303 или Д305. Следует помнить, что анодируются детали только из алюминия или его сплавов. Подвески для деталей изготовляют только из алюминия. Все соединения и контакты должны быть надежными, так как от этого зависит качество анодирования. Загружать детали в ванну и выгружать их следует только под током. После 40-50-минутного пребывания деталей в ванне их выгружают, тщательно промывают холодной водой и опускают в водный раствор анилинового красителя, подогретый до 50-60°С. Раствор красителя следует предварительно профильтровать, так как небольшие крупинки нерастворившегося красителя образуют пятна на поверхности окрашенного металла. Цвет окраски зависит от времени пребывания анодированной детали в красителе, которое не должно превышать 15-20 мин.
Анилиновые красители (порошки для крашения тканей) можно приобрести в хозяйственных магазинах.
После анодирования поверхность чистого алюминия остается блестящей, а некоторые алюминиевые сплавы приобретают матовый, темный оттенок, что зависит от электрического режима анодирования.
Для окрашивания применяют 5-10%-ные водные растворы следующих красителей:
в черный цвет - анилиновый черный М или анилиновый прямой черный-3;
в коричневый - основной коричневый;
в золотисто-желтый - прямой желтый 2Ж или ализариновый желтый;
в красный - красный ализариновый или кислотный рубиновый;
в синий - кислотный синий антрахиноновый или прямой синий М;
в голубой - анилиновый голубой или метиленовый голубой;
в зеленый - прямой зеленый ЖХ или основной ярко-зеленый;
в фиолетовый - основной фиолетовый.
"Краситель оранжевый 2Ж", "Краситель основной фиолетовый" и т.д.- торговые термины.
Имитация под золото заслуживает особого внимания. Окрашенные детали только по весу можно отличить от натурального золота. Окраска получается прочной и светостойкой. Раствор для крашения готовят так. 1 г красителя оранжевого 2Ж растворяют в 0,5 л горячей воды, в раствор добавляют 0,1 г красителя желтого-3 и 0,5 г кальцинированной соды. После охлаждения раствор фильтруют. Отдельно в 0,5 л горячей воды растворяют 0,1 г красителя черного М. Этот раствор также фильтруют. Перед крашением оба раствора смешивают и нагревают до 50-60°С. В зависимости от времени пребывания деталей в этом растворе можно получить окраску под любую пробу золота.
Окрашивать анодированные детали из алюминия и его сплавов можно не только в указанных растворах органических красителей. Для этой цели можно пользоваться и перечисленными ниже цветными неорганическими соединениями, которые образуются непосредственно в порах анодированного металла после последовательного погружения его сначала в водный раствор "а", затем в водный раствор "б".
Например, для окрашивания в белый цвет применяют растворы:
а) свинец уксуснокислый, 10%-ный раствор,
б) сульфат натрия (глауберова соль), 10%-ный раствор;
в синий или голубой цвет:
а) железосинеродистый калий, 50%-ный раствор,
б) хлорное железо, 5-10%-ный раствор;
в золотисто-желтый:
а) гипосульфит, 5%-ный раствор,
б) свинец уксуснокислый, 5%-ный раствор;
в оранжевый:
а) калий хромовокислый, 2-3%-ный раствор,
б) азотнокислое серебро, 5-10%-ный раствор;
в желтый:
а) двухромовокислый калий, 2-5%-ный раствор,
б) свинец уксуснокислый, 10-15%-ный раствор;
в коричневый:
а) железосинеродистый калий, 2-5%-ный раствор,
б) медный купорос, 5-10%-ный раствор.
После адсорбиционного окрашивания детали промывают горячей водой и погружают на 2-3 мин в расплавленный воск или парафин, затем, еще горячие, протирают марлей.
Простейшая установка для гальванического покрытия металлических поверхностей
В ремонтной и любительской практике с успехом можно использовать миниатюрную безванновую гальваническую установку (рис. 1).
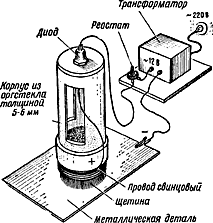
Рис. 1. Миниатюрная гальваническая установка
Она состоит из специальной кисти со щетиной (диаметр кисти 20-25 мм, корпус ее выполнен из органического стекла, внутрь которого заливается электролит), понижающего трансформатора на напряжение 12 В и ток 0,8-1 А или аккумулятора и соединительного шнура. Щетину кисти обматывают свинцовым (в крайнем случае облуженным медным) проводом. Полупроводниковый диод типа Д303-Д305 устанавливают на корпусе кисти. Один из проводов понижающей обмотки трансформатора соединяют с анодом диода, другой с помощью зажима "крокодил" - с покрываемой деталью. Катод диода соединяют с проводом обмотки кисти. Если применяется аккумулятор, диод не нужен.
Покрываемые детали очищают от ржавчины, грязи и жира, протирают сухой чистой тканью и обезжиривают в растворе, содержащем 100-150 г едкого натра, 40-50 г кальцинированной соды и 3-5 г жидкого стекла (силикатный клей) на 1 л. В зависимости от степени загрязнения детали выдерживают в обезжиривающем составе, нагретом до 80-100°С, от 15 мин до 1 ч. Чем ровнее и чище поверхность, тем прочнее будет гальваническое покрытие. Подготовленную деталь соединяют с обмоткой трансформатора, в кисть заливают электролит и включают питание. Равномерно перемещая кисть по поверхности детали, покрывают ее металлом, осаждающимся из электролита. Для получения покрытия достаточной толщины необходимо пройти кистью по одному и тому же месту 20-25 раз. Электролит доливают в кисть по мере его расходования. После нанесения покрытия деталь промывают в проточной воде и полируют в смоченной воде тканью, затем еще раз промывают и сушат. Для каждого вида покрытия приготовляют специальный электролит, составленный по следующим рецептам (в граммах на 1 л раствора):
Электролит для меднения
Медный купорос (сернокислая медь) 200
Серная кислота 50
Этиловый спирт или фенол 1-2
Электролит для никелирования
Сернокислый никель 70
Сернокислый натрий 40
Борная кислота 20
Хлористый натрий 5
Электролит для хромирования
Хромовый ангидрид 250
Серная кислота (уд. в. 1,84) 2,5
Электролит для цинкования
Сернокислый цинк 300
Сернокислый натрий 70
Алюминиевые квасцы 30
Борная кислота 20
Электролит для серебрения
Хлористое серебро свежеосажденное 3-15
Железосинеродистый калий 6-30
Сода кальцинированная 20-25
Электролит для золочения
Хлорное золото 2,65
Железосинеродистый калий 15-50
Сода кальцинированная 20-25
В 200-300 мл дистиллированной воды растворяют первое по порядку вещество, потом второе, третье и т.д., а затем доливают воду до 1 л.
Следует иметь в виду, что, хотя растворы и не содержат сильно ядовитых веществ, обращаться с ними во избежание ожогов и отравления следует с осторожностью. Растворы лучше всего хранить в темной стеклянной посуде с притертой пробкой.
Необходимо также учитывать, что не все покрытия хорошо ложатся на различные металлы. Например, для того чтобы покрыть никелем стальную деталь, ее предварительно покрывают тонким слоем меди, хром же хорошо сцепляется с никелированной поверхностью. Подслой меди перед никелированием или серебрением желательно осадить и на деталях, изготовленных из бронзы. Медные и латунные детали серебрят без подслоя меди.






