

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

История создания датчика движения: Первый прибор для обнаружения движения был изобретен немецким физиком Генрихом Герцем...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

История создания датчика движения: Первый прибор для обнаружения движения был изобретен немецким физиком Генрихом Герцем...
Топ:
Методика измерений сопротивления растеканию тока анодного заземления: Анодный заземлитель (анод) – проводник, погруженный в электролитическую среду (грунт, раствор электролита) и подключенный к положительному...
Установка замедленного коксования: Чем выше температура и ниже давление, тем место разрыва углеродной цепи всё больше смещается к её концу и значительно возрастает...
Интересное:
Искусственное повышение поверхности территории: Варианты искусственного повышения поверхности территории необходимо выбирать на основе анализа следующих характеристик защищаемой территории...
Уполаживание и террасирование склонов: Если глубина оврага более 5 м необходимо устройство берм. Варианты использования оврагов для градостроительных целей...
Аура как энергетическое поле: многослойную ауру человека можно представить себе подобным...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
В результате реакций дезаминирования и окисления биогенных аминов освобождается много аммиака.Аммиак должен подвергаться связыванию в тканях с образованием нетоксичных соединений.
Первый путь-образование глутамина(в мозге,мышцах,сетчатке,печени.) Он транпортирует аммиак в нетоксичной форме.Реакция катализируется глутаминсинтетаой(класс лигаз).
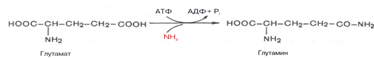
2)образование мочевины
Основным механизмом обезвреживания аммиака в организме является
биосинтез мочевины. На первом этапе синтезируется макроэрги-
ческое соединение карбамоилфосфат – метаболически активная форма
аммиака. 
На втором этапе цикла мочевинообразования происходит конденсация
карбамоилфосфата и орнитина с образованием цитруллина; реакцию ка-
тализирует орнитин-карбамоилтрансфераза.На следующей стадии цитруллин превращается в аргинин в результате
двух последовательно протекающих реакций. Первая из них, энергозави-
симая,– это конденсация цитруллина и аспарагиновой кислоты с обра-
зованием аргининосукцината (эту реакцию катализирует аргининосукцинат-
синтетаза). Аргининосукцинат распадается в следующей реакции на ар-
гинин и фумарат при участии другого фермента – аргининосукцинатлиазы.
На последнем этапе аргинин расщепляется на мочевину и орнитин под
действием аргиназы.
Суммарная реакция синтеза мочевины без учета всех промежуточных
продуктов может быть представлена в следующем виде:
СO2 + NH3 + ЗАТФ + 2Н2O + Аспартат –> Мочевина + 2АДФ + АМФ +
+ Фумарат + 2Рi + РРi.

Роль печени:Токсические вещества из кишечника (продукты распада – фенол, крезол, скатол, индол) в печени подвергаются обезвреживанию. Механизм заключается в образовании парных соединений с серной и глюкуроновой кислотами.
|
|
Декарбоксилирование аминокислот в тканях,дальнейшая судьба образовавшихся аминов.
- процесс отщепления карбоксильной группы в виде СО2.Продуктом реакции являются биогенные амины.Данную реакцию катализирует фермент декарбоксилаза (состоит из белковой части,ктр обеспечивает специфичность действия,и простетической группы-пиридоксальфосфат.)
-механизм реакции заключается в образовании ПФ-субстратного комплекса,представляенного шиффовым основанием ПФ и аминокислоты.
-продуктом декарбоксилирования являются биогенные амины. 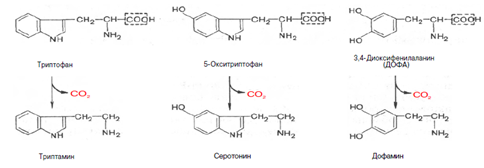
Накопление аминов моэет отрицательно сказаться на физиологическом статусе организма.Однако в организме существуют специальные механизмы их обезвреживания:окислительное дезаминирование этих аминов с образованием соответствующих альдегидов и освобождением аммиака.Эти реакции катализируют ферменты-МАО и ДАО.
 R-CH2-NH2 (МАО,(ФАД)) NH3 + R-COH
R-CH2-NH2 (МАО,(ФАД)) NH3 + R-COH
 (B6(ПИРИДОКСАЛЬФОСФАТ)) R-COOH + NH3 +H2O2
(B6(ПИРИДОКСАЛЬФОСФАТ)) R-COOH + NH3 +H2O2
|
|
|

Адаптации растений и животных к жизни в горах: Большое значение для жизни организмов в горах имеют степень расчленения, крутизна и экспозиционные различия склонов...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Состав сооружений: решетки и песколовки: Решетки – это первое устройство в схеме очистных сооружений. Они представляют...

Автоматическое растормаживание колес: Тормозные устройства колес предназначены для уменьшения длины пробега и улучшения маневрирования ВС при...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!