1. Достраивание активного центра фермента, в результате чего облегчается взаимодействие фермента с субстратом. Таким механизмом обладают в основном ионы металлов.
2. Аллостерический активатор взаимодействует с аллостерическим участком (субъединицей) фермента, через его изменения опосредованно изменяет структуру активного центра и увеличивает активность фермента. Аллостерическим эффектом обладают метаболиты ферментативных реакций, АТФ.
3. Аллостерический механизм может сочетаться с изменением олигомерности фермента. Под действием активатора происходит объединение нескольких субъединиц в олигомерную форму, что резко увеличивает активность фермента. Например, изоцитрат является активатором фермента ацетил-КоА карбоксилазы.
4. Фосфолирирование - дефосфолирирование ферментов относится к обратимой модификации ферментов. Присоединение Н3РО4 чаще всего резко увеличивает активность фермента. Например, два неактивных димера фермента фосфорилазы соединяются с четырьмя молекулами АТФ и образуют активную тетрамерную фосфорилированную форму фермента. Фосфолирирование ферментов может сочетаться с изменением их олигомерности. В некоторых случаях фосфорилирование фермента, наоборот, снижает его активность (например, фосфорилирование фермента гликогенсинтетазы)
5. Частичный протеолиз (необратимая модификация). При этом механизме от неактивной формы фермента (профермента) отщепляется фрагмент молекулы, блокирующий активный центр фермента. Например, неактивный пепсиноген под действием HCL переходит в активный пепсин.
Единицы активности ферментов.
Международная единица (МЕ) активности фермента – это количество фермента, которое катализирует превращение 1 мкмоль субстрата в 1 мин (при оптимальных температурах, pH среды, концентрации субстрата):
МЕ = мкмоль (S) / мин
Катал – количество фермента, способное превращать 1 моль субстрата за 1 сек: катал = моль (S) / сек
• Удельная активность фермента - это число единиц активности фермента (E), приходящихся на 1 мг чистого фермента:
Удельная активность фермента = Е / мг(Ф)
• Молекулярная (молярная) активность фермента – это число молекул субстрата, которое подвергается превращению 1 молекулой фермента за 1 мин. Молекулярная (молярная) активность фермента = Е / мкмоль (Ф)
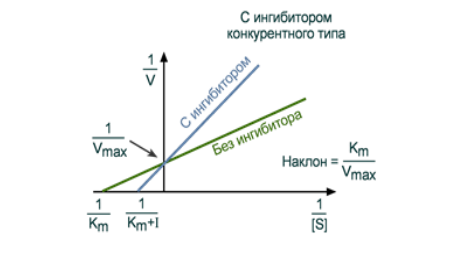
Ингибиторы ферментов. Специфические и неспецифические, обратимые и необратимые, конкурентные и неконкурентные ингибиторы. Уравнение и графики Лайнуивера-Берка.
Ингибиторы – это вещества полностью или частично подавляющие активность ферментов.
Неспецифическое ингибирование –соединения или в-ва, к-е ингибируют все ферменты или большинство групп ферментов. В более высоких конц-х вызывает денатурацию белка (соли тяжелых металлов, алкоголь и тд)
Специфическое ингибирование – действует только на определенный фермент или группу.
Можно выделить два основных направления ингибирования:
· по прочности связывания фермента с ингибитором ингибирование бывает обратимым и необратимым.
· по отношению ингибитора к активному центру фермента ингибирование делят на конкурентное и неконкурентное.
При необратимом ингибировании происходит связывание или разрушение функциональных групп фермента, необходимых для проявления его активности.
Например, вещество диизопропилфторфосфат прочно и необратимо связывается с гидроксигруппой серина в активном центре фермента ацетилхолинэстеразы(АХЭ), гидролизующей АХ в нервных синапсах. Ингибирование этого фермента предотвращает распад АХ в синаптической щели, в результате чего медиатор продолжает оказывать воздействие на свои рецепторы, что бесконтрольно усиливает холинергическую регуляцию.
При обратимом ингибировании происходит непрочное связывание ингибитора с функциональными группами фермента, вследствие чего активность фермента постепенно восстанавливается.
Примером обратимого ингибитора может служить прозерин, связывающийся с ферментом ацетилхолинэстеразой в ее активном центре. Группа ингибиторов холинэстеразы (прозерин, дистигмин, галантамин) используется при миастении, после энцефалита, менингита, травм ЦНС.
Конкурентное ингибирование
При таком виде ингибирования ингибитор по своей структуре похож на субстрат фермента. Поэтому он соперничает с субстратом за активный центр (за контактный участок), что приводит к уменьшению связывания субстрата с ферментом и нарушению катализа. В этом состоит особенность конкурентного ингибирования – возможность усилить или ослабить ингибирование через изменение концентрации субстрата. При данном ингибировании максимальная скорость реакции остается вполне достижимой при создании высоких концентраций субстрата.