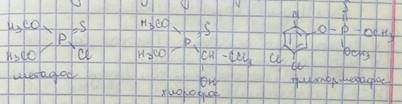ЭНЕРГЕТИКА ХИМИЧЕСКОГО ПРОИЗВОДСТВА
В химическом производстве процессы протекают с выделением энергии, ее затратами, в дальнейших превращениях и переходе одной в другую.
Хим производство является одним из самых энергозатратных. Производя около 6% промышленной продукции, она потребляет 12% от всей используемой продукции. По цене от 5% до 40% в хим реакторах, от 30% до 80% в массообменных процессах, 60-90% в теплообменных процессах.
Одними из самых энергозатратных является производство аммиака 9,5%, производство химических волокон 10,5%, производство полимеров 8,2%, каустической соды 4,6%, мочевина 3,5%, метанол 2.5%.
Энергоемкость химического производства – расход энергии на единицу полученной продукции.
Условная единица топлива – масса твердого топлива (V газообр топлива) с теплотой сгорания 23,3 МДж.
Химические производства: 1 класса (более 2 т.у.т. – хим волокна, ацетилен, капролактан), 2 класса (1-2 т.у.т. – азотная кислота, уксусная кислота. этиленгликоль), 3 класса (менее 1 т.у.т. – карбид кальция, матнол, аммиак).
Виды энергии: Тепловая – обеспечивает тепловой режим процессов, тепловые процессы. Для передачи тепла используются теплоносители (вещества с выс теплосодержанием).
В качестве среды для нагревания исп: топочные газы, водяной пар, горячую воду, масла, расплавы солей.
Для окисления используют системы холодильников, в которых холод образуется при испарении жидкостей – холодный вариант тепловой энергии. Детандер – холод выделяется при резком расширении газов.
Электрическая энергия – исп в осуществлении хим-тех процессов, обеспечивает электротермические процессы, для получения механической энергии в электроприводе.
Топливная энергия используется для производства тепла, в печах особого назначения.
Механическая энергия – исп для работы механических устройств, получения эл и тепловой энергии.
Световая энергия – исп для фотохимических реакций и фотоэлектрических процессов.
Химическая энергия исп для химического источника тока.
Ядерная энергия исп для ядерно-химических реакций, радиационно-химических превращений.
В общем виде из всей энергии 40% - электрическая, 50% - тепловая, 10% - топливная.
Источники получения энергии: топливо для выработки тепловой энергии; теплоэлектроцентрали для получения тепловой и эл энергии, энергия установки излучения.
Энергоресурсы
а) первичные – не зависят от деятельности человека. 1) невозобновляемые – приводит к уменьшению энергии (ядерное топливо, ископаемое, нефть, газ).2) возобновляемое - восполняются планово(биомасса, эн. волн, геотермич энергия, солнечная энергия).
б) вторичные – несут энерг потенциал за счет деятельности человека (отходящие газы).
Характеристика энергетической ценности хим топлива – отношение низшей теплоты сгорания топлива к теплоте сгорания условного топлива. Количество энергии потраченной при сжигании 1 кДж/л.
Количество загрязнителей топлива: угл газа 200 млн т, SO2 – 150 млн т, NO2 – 50 млн т, аэрозоли – 250 млн т.
Преимущества водорода как топлива: распространение водорода и практически неисчерпаемые запасы воды, высокое энергосодержание, простота и дешевизна транспортировки, экологичность.
ТЕХНОЛОГИЧЕСКАЯ ОЧИСТКА ПИТЬЕВОЙ ВОДЫ
Последовательно применяется отстаивание, фильтрование, коагуляция, обеззараживание.
Процесс непрерывный. В отстойниках удаляются грубо дисперсные примеси. Вода через сетки насосами закачивается в смеситель коагуляции, где происходит укрупнение частиц и частичное снижение жесткости.
Для более полного умягчения вводят известковое молоко. Образующиеся хлопья током выносятся в осветлитель. В его боковых частях хлопья находятся во взвешенном состоянии, а после переноса в центральную часть они осаждаются, из нее удаляется уплотненный осадок.
Воды с частью хлопьев выносится на фильтр:
-слой антроцита
-слой чистого песка
-слой гравия на решетках
Фильтр периодически промывают обратным током воды. Отфильтрованную воду обеззараживают хлором. Избыток хлора связывают с аммиаком.
Для хлорирования воды используют: -гипохлорит натрия, CL2O7, хлорамин,иногда на выходе добавляют гексафтороселикатнатрия.
ОЧИСТКА СТОЧНЫХ ВОД
Метод биологической очистки с использованием системы микроорганизмов.
Основной задачей является удаление из воды органических веществ и очистка от соединений азота и фосфора
Тяжелые металлы поглощаются из воды за счет сорбции активным элементом
Из канализационных отстойников (коллекторы городской канализации, отстойники малых предприятий, культурно-бытовых организаций) Вода поступает на сетки и решетки, жироловки, где с поверхности удаляется гидрофобные вещества, затем в песколовки, где осаждается мелкий тяжелый песок, затем в систему первичных отстойников, при длительном отстаивании удаляются тяжелые вещества. На стадии механической отчистки удаляются 60-70% минеральных загрязнений, на 30% снижается потребление кислорода. Вода поступает в аэротенки, где под действии активного ила в аэробных условиях происходит разложение органических веществ до CO2 H2O, переход N – NO2-, нитрификция и удаление соединений фосфора, за счет абсорбции и перехода в нерастворимые фосфаты
Часть воды поступает в аэраторы второго типа, где под действием другого активного металла происходит денитрофикация (образование молекул азота)
Вторая часть воды поступает в систему вторичных отстойников – насосы из нее активный ил и часть воды поступает в систему метантенки, где под действием анаэробных процессов происходит разложение до метана, его сжигают и углекислый газ выбрасывается в атмосферу.
На некоторых предприятиях метан собирают в газбойлеры и используют для отопления. Отчищенную воду вторично отстаивают и очищают от активного ила и собирают в природные водоемы.
РЕАКТОРЫ И ИХ КЛАССИФИКАЦИЯ
Химический реактор – устройство для проведения в нем превращений. Реактор сопряжен с аппаратом подготовки сырья и аппаратами разделение реакционной смеси и очистки целевого продукта.
В реакторе реакционная зона представляет собой несколько слоев катализатора. Исходная смесь попадает через штуцер (патрубок для соединения трубопровода, ёмкостей, вентилей и других деталей газовых и жидкостных передаточных и преобразующих систем.), распределяясь по поверхности теплообменника, в котором потоки могут снова смешиваться. Продукты выводятся через выводное устройство.
Реакционный процесс с участием катализатора, через неподвижный слой которого проходит потом газообразных реактивов.
Реагенты диффундируют на поверхности катализатора, проникают в его поры, на внутренней поверхности происходит химический процесс. Выделяющаяся при этом теплота уносится во внешнюю среду. С поверхности катализатора ресорбируются продукты и переносятся дальше по потоку.
Процессы в слое жидкости, через которую барбатируется газ.
Между пузырями газа и жидкости происходит газообмен. Динамика жидкости складывается из движения около пузырей газа и собственного движения в масштабах слоя. Следовательно, хим. превращение происходит внутри слоя и внутри пузырей газа.
Классификация хим. реакторов. В основе организационно-технической структуры реакторы делятся на периодического и непрерывного действия. Для реакторов периодического действия характерно падение движущей силы процесса во времени, вызванной уменьшением концентрации реагентов в ходе процесса. Режим работы таких реакторов непостоянен и требует изменений для поддержания скорости процесса. В реакторах непрерывного действия движущая сила постоянна вследствие постоянства концентраций. Режим работы постоянен.
Основной показатель работы реактора – интенсивность – время, затраченное на производство.
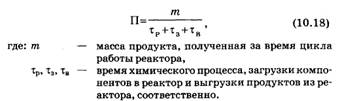
Для непрерывного процесса t3=tв=0.
По тепловому режиму:
1) с адиабатическим режимом: отсутствует теплообмен с окружающей средой, и тепловой эффект затрачивается на изменение температуры в реакторе.
2) с изотермическим режимом: постоянство температуры в реакторе за счет подвода или отвода тепла.
3) политропические реакторы: подвод или отвод тепла, за счет которого происходит изменение температуры.
Для реакторов непрерывного действия по режиму движущихся компонентов:
1) реакторы идеального вытеснения. Поток реагентов движется в одном направлении по длине реактора без перемешивания, движущие силы и скорость по длине изменяются, причем отклонение средней движущей силы от постоянного значения максимальное.
2) Реакторы идеального смешивания: потоки реагентов смешиваются друг с другом, а также и с продуктами реакции, движущая сила процесса и скорость постоянна по длине.
Движущая сила – разность между предельным значением данного параметра процесса и его действующим значением в данный момент времени.
1 и 2 зоны химических реакторов – подвод вещества в зону реакции и вывод продуктов реакции.
В этих зонах процессы подчиняются законам массы – передачи, они ускоряются физическим путем (перемещение, распыление, изменение скорости потоков). 2 зона – зона химических реакций. Где параллельно или последовательно идет ряд химических реакций, характеризуются скоростью (кинетический фактор) и состояние равновесия в системе (термодинамический фактор).
Методы производства.
Камерный метод:
Исп-сятермич или экстракц к-та с конц-ей 50-58% и изб к-ты 110%. Разложение проводят в суперфосфатных камерах непрерывного действия. Ст разложения 75-80%, а обр-ся продукт проходит созревание на складах.
Камерно-поточный метод
Исп-ся кислота 47-49% в стехиомкоэф. Степ разл-я не выше 70% и отсутствует созревание на складах.
Поточный (безкамерный) метод
Неупар 30% к-та. Разложение в 2 ступени. На 1 стразлож-е 50% протекает в реакторах. 2 ст до ст разложения 55% протекает в сушилках.
Производство аммофоса
В основе производства аммофоса лежит гетерогенный экзотермический процесс нейтрализации фосфорной кислоты газообразным аммиаком:
Н3РО4(ж.) + NH3(г.) = NH4H2PO4(тв.) + 147,0 кДж
Процесс ведут при избытке аммиака, поэтому в системе, наряду с реакцией образования моноаммонийфосфата, частично протекает реакция образования диаммонийфосфата:
Н3РО4 + 2NH3(г.) = (NH4)2HPO4(тв.) + 75,4 кДж
в результате чего в составе готового продукта содержится до 10% диаммонийфостфата.
ЯДОХИМИКАТЫ
Ядохимикаты – это хим. продукты, использ. для борьбы с вредителями и болезнями с/х растений.
Формы:
*дусты - порошки для опыления. Смесь ядохим., с использ. наполн., способных разбавлять химикаты (тальк, фосфорит, мука).
*суспензии, эмульсии (водные с добавлением ПАВ для стабилизации).
*растворы в воде или летучих орган.растворителях для опрыскивания или замачивания семян.
*аэрозоли.
*пары летучих веществ.
*отравленные приманки.
Инсектициды (для борьбы с насекомыми)
· Контактные (проникают через покровы тела и вызывают паралич).
-Не раствор.водой (хлорорганика) 
-Фосфор.соединения (могут взаимод. с водой)
Метафос, хлорофос, трихлорметафос 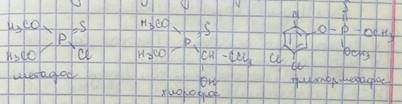
· Внутрирастительные (проникают внутрь растения и уничтожают насекомых, питающихся их соком)
метилмеркаттофос 
· Дыхательные (фумиганты) CH3Br, CCl3NO2 (хлорпикрин)
· Фунгициды (для защиты растений от грибковых заболеваний)
Бордосская смесь: СuSO4•3Ca(OH)2.
Зооциды (для борьбы с грызунами)
Крысид 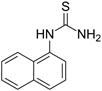
Zn3P2
· Гербициды (для уничтожения сорных растений)
-сплошного действия (хлорат кальция, магния)
-избирательного действия
*контактные (динитрозамещен.Фенол, пентахлор фенол)
*системные
Барабанный способ.
Песок и тонкомолотая негашеная известь поступает в бункера, расположенные над гасильным барабаном. Песок дозируется по объему, известь по массе. В барабане перемешивается по 3-5 минут.
Смесь поступает в непрерывно гасящий барабан, где гасится водой до 40 минут. Она подается в виде острого пара под давлением – 0,15-0,2 Мпа.
Силосный способ.
Песок и известь смешиваются, перемешиваются и увлажняются. Направляются на гашение в силосы – герметичные резервуары, заполненные смесью. В 10 раз дольше чем в барабанном методе. Гашение не используют для кладки фундамента, для выплавки печей и дымовых труб.
ПРОИЗВОДСТВО ОГНЕУПОРОВ
Это неметаллические материалы, характеризующиеся высокой способностью противостоять, не расплавляясь, высоким температурам.
Требования:
1. термическая стойкость – способность сохранять структуру
2. Малый коэффициент термического расширения
3. высокая механическая прочность при температуре эксплуатации
4. устойчивость к действию расплавленных сред
Виды огнеупоров
1. Алюмосиликатные. SiO2, Al2O3
-полукислые. 70-80% SiO2, 15-20% Al2O3. Стойкие к ксилым шлакам и силикатным расплавам. Применяются в металлургических печах
-шамотные.50-70% SiO2, до 40% Al2O3. Стойкие к действию кислых и основных шлаков, термически устойчивы
-высокоглиноземистые.более 45% Al2O3. Повышенная механическая устойчивость. Применяются для кладки сводов металлических печей.
2. Динасовые. от 95% SiO2+СаО. Стойкие к кислым шлакам. Огнеупорны от 1730 Со. Применяются для кладки коксовых и стекловарных печей
3. Магнезитовые. 30%MgO, 45% СаО, 15% SiO2. Устойчивые к действию основных шлаков. Термически нестойкие. Огнеупорность до 2500Со
4. Корундовые Al2O3. Применяется в установках для нагрева и плавления тугоплавких материалов в радиотехники.
5. КарборудновыеSiС. Устойчивы к действию кислых шлаков.Высокая механическая прочность.Применяется для футеровки(облицовки) металлически печей, чехлов термопар.
6. Циркониевые и ториевыеZnO2, ThO2. Высокая огнеупорность. Применяется при изготовлении тиглей
7. Углеродистые. Применяется при выкладке горнов доменных печей.
Производство алюмосиликатных огнеупоров:
Коалин – основной сырьевой компонент
Обжиг коалина – Шамотный порошок (огнеупорная глина) – муллит (минерал)
Al2O3*2SiO2
Диансовые. Производятся из кварцита и СаО при 1500Со
Магнезитовые. Обжигом доломита
Углеродистые - обжиг смеси графита, глины и шамота
Виды фарфора
1. Твердый. Для химической посуды, высоковольтныхизолятов
45-55% глинистого минерала (30-40% коалина, 10-15% огнеупорной глины), 25-30% кварца, 15-20% полевого шпата. Температура: 1350-1450Со
2. Мягкий. Для хозяйственной посуды, художественных изделий.
25-40% глины, 20-45% кварца, 30-35% полевого шпата.
Фаянс
Изготовление сантехнических изделий, глазурированных плиток.
Твердый. 25-30% коалина и глины, 25-30% кварца, до 10% полевого шпата
Мягкий. 30-35% коалина и глины, 35% кварца
Обжиг при температуре 1200-1270Со
Основные требования к сырью: Высокая степень чистоты, низкое содержание железа.
Коалин обогащают отмучиванием суспензии.
Кварц и полевой шпат в сухом виде дробят, затем размалывают мокрым способом.
Изделия получают из пластической керамической массы. Из нее формируют изделия.
Плитки формируются прессом, полусухим способом.
Изделия сложной формы готовят из тонкодисперсной суспензии. Ее заливают в формы из пористого гипса, который впитывает воду из гипса.
В результате получается сырец, который сушат, помещают в закрывающиеся формы из огнеупорных материалов, обжигают в печах непрерывного обжига и глазурируют.
Для покрытия глазури при первом обжиге на поверхность наносится тонкий слой суспензии из тех же составных частей, но с большим содержанием плавней. Затем проводится повторный обжиг, при котором глазурь расплавляется, а при охлаждении образуется стекловидный слой, прочно сцепленный с черепком.
После 1 или 2 обжига возможно нанесение красок.
Печи для обжига обогревают жидким или газообразным топливом. Изделие последовательно проходит зоны подогрева, обжига и охлаждения.
Сырье для варки стекла
Стеклообразователи – основа стекла (SiO2, PbO, Al2O3, Na2CO3)
Красители – ионы меди, железа, кобальта, хрома
Глушители – матовое и молочное стекло (As2O3, SnO2, SnS)
Обесцвечиватели – устраняет желтую и зеленоватую окраску (MnO2)
Осветители – удаляют газовые включения
Стадии
Подготовка шихты – приготовление шихты – варка стекломассы – формование изделия
Подготовка: промывка – сушка - измельчение
Варка – совокупность сложных ф/х процессов, протекающих в гетерогенной системе через стадии
собственная варка – осветление (гомогенизация) – охлаждение массы
Процесс начинается в твердой массе, продолжается в расплавленной.
Скорость зависит от скорости диффузии компонента
до 300Со–удаление влаги, выжигание органических веществ
до 400 – CaCO3 + Na2CO3 = CaNa2(CO3)2; MgCO3 + Na2CO3 = MgNa2(CO3)2
340 – 900 – силикатообразование MgNa2(CO3)2 + 2SiO2 = Na2SiO3 + MgSiO3 + 2CO2
980 -1150 – образование жидкой стекломассы за счет растворенных в расплаве силикатов
MgO + SiO2 = MgSiO3 CaO + SiO2 = CaSiO3
1200 – 1240 – стеклообразование
1400-1500 – гомогенизация, осветление, удаление газов
1200 – охлаждение стекломассы до обретения нужной вязкости
Для формования изделий выбирают условия и время, соответствующие типу стекла и назначению. Для обеспечения нужной вязкости, которая будет возрастать по мере охлаждения расплава.
Для этого используют вытягивание (стекло), выдувание (посуда), прессование (линзы), отливка в формы (художественные изделия), прокат (толстое листовое стекло)
Специальные типы стекла:
1. Закаленное – получают термической обработкой в печах обычного стекла с последующим охлаждением обдувкой воздуха
2. Пеностекло – получают сплавлением стеклообразного порошка с MnO, CaCO3 при 800Со
3. Стеклянное волокно – получают продавливанием стекломассы через фильтры
4. Пирекс – боросиликатное стекло
ПРОИЗВОДСТВО СИТАЛЛОВ
Силикатные кристаллы – материалы из полностью или частично равномерно закристаллизованного стекла.
Состоят из кристаллов менее 1мкм. Аморфная фаза не превышает 50Со
- Литиевые ситаллы (Li2O – Al2O3 – SiO2). Высокие, термостойкие, маленький коэффициент расширения.
- Магниевые. Оптические и радиопрозрачные
Для ситаллов характерны высокая температура плавления, малая пористость и газопроницаемость, химическая и термическая устойчивость, высокая твердость, механическая прочность, высокая износоустойчивость, маленький коэффициент расширения
Применяются для расширения строительных деталей, труб, подшипников, работающих без смазки, детали АВС, режущие элементы
Получают регулируемой принудительной кристаллизацией стекла или стекломассы, путем внесения в расплав центров кристаллизации.
Этапы:
Плавление стекла или шлака
Формование изделия
первая выдержка(500-700Со)
Выдержка до полной кристаллизации
охлаждение изделия
Гашение
Гетерогенный экзотермический процесс
СаО+nН2О = Са(ОН)2*(n-1)Н2О.
Процесс идет в гидраторах периодического и непрерывного действия. СО2 поглощают раствором К2СО3.
СО2+К2СО3+Н2О=2КНСО3
Образующиеся кислые соли снова разлагают СО2. Используют в производстве.
2КНСО3=СО2+К2СО3+Н2О Т=80С
Используется в строительстве для производства хлорной извести, для умягчения воды и для очистки продуктов в сахарном производстве.
СЫРЬЕ. КЛАССИФИКАЦИЯ, СПОСОБЫ ОБОГАЩЕНИЯ
Сырье - вещества и материалы, подвергшиеся определённому воздействию труда и предназначенные для дальнейшей переработки в готовый продукт
Сырьевые ресурсы - источники сырья для переработки в промышленности
Полупродукты - это сырье, подвергшееся обработке на одной или нескольких стадиях производства, но не являющееся конечным целевым продуктом данного производства, а способное при дальнейшей обработке дать этот продукт.
Побочные продукты - вещества образующейся вместе с целевым продуктом, но не является целью данного производства
Попутные продукты - побочные продукты, полученные при добыче сырья и его обогащении.
Отходы производства – остатки сырья, материалов и полупродуктов, образующиеся в производстве и полностью или частично утратившие свои качества
Отходы потребления – бывшие в употреблении вещества, восстановление которых экономически нецелесообразно
Все данные компоненты могут быть рассмотрены в качестве природного сырья
Классификация сырья:
1. по агрегатному состоянию: твердое, жидкое и газообразное
2. по химическому составу: неорганические и органические
3. по видам запасов: возобновляемые и невозобновляемые
Минеральное сырье – добываемые из земных недр полезные ископаемые для дальнейшей переработки в промышленности, они залегают в литосфере на глубине 10 км: минеральные ассоциации в виде осадочных, изверженных и метаморфических горных пород
Рудное минеральное сырье – горные породы и минералы, содержащие извлекаемые металлы
Нерудное минеральное сырье - не содержащие металлы горные породы, или содержащие в количествах, не пригодных для получения этих металлов
Горючие минеральные материалы – содержат углерод: угли, нефть, природный газ, горючие сланцы
В абсолютном большинстве производств исходными веществами являются полупродукты. Поэтому обычно и природные материалы, и полупродукты называют первичным сырьем.
Вторичное сырье — исходные в производстве вещества и материалы, являющиеся отходами других производств и потребления.
Основные пути использования отходов производства и потребления:
1) регенерация непрореагировавшего сырья и материалов с последующим возвратом в производство;
2) извлечение ценных компонентов как продуктов производства;
3) выделение компонентов и придание им с помощью специальных операций товарной ценности;
4) использование в качестве вторичного сырья в других производствах или других отраслях промышленности.
Во всех случаях предполагается одно из двух назначений вторичного сырья как исходного компонента:
a) а) вторичное сырье частично или даже полностью заменяет первичное в каком-либо производстве;
b) б)на основе вторичного сырья создается новый химико-технологический процесс.
Подготовка сырья: цель – придание сырью состава и свойств, обеспечивающих оптимальное протекание процессов переработки.
Операции: 1) классификация – разделение по гранулометрическим фракциям (для придания однородности)
2) Измельчение (для придания однородности).
3) Обезвоживание – для предотвращения биохимической активности, получения постоянной массы, для удаления воды, если она мешает процессу.
4) Обогащение – процесс отщепления полезного компонента от пустой породы для повышения его концентрации.в результате получают концентрат полезного компонента и хвосты.
Процесс обогащения характеризуется величинами: Выход концентрата – отношение массы концентрата к массе сырья. Степень извлечения полезного компонента – отношение массы полезного компонента в
концентрате к массе полезного компонента в сырье. Степень обогащения сырья – отношение массовой доли полезного компонента в концентрате к массовой доле полезного компонента в сырье.
Методы обогащения:
1) механические: а) основаны на разности скоростей оседания частиц в потоке жидкости или газа. б) электромагнитный – основан на различной магнитной проницаемости сырья. в) электроосмотический – основан на различной электрической проницаемости.
2) Химические: растворение и обжиг
3) Физико-химические а) Флотация – метод основан на различной смачиваемости и прилипаемости частиц сырья. Во флотационную ванну подают пульпу (частицы сырья и вода). В нее же подается воздух. Гидрофобные частицы прилипают к пузырькам, которые поднимаются вверх, образуется пена, которую собирают. При необходимости в машину добавляют вещества, изменяющие смачиваемость. Для ускорения смесь либо интенсивно барабатируется воздухом, либо перемешивается.
Для твердого сырья используют разницу в температуры плавления, различную растворимость в разных растворителях – экстракция. Для жидкого – разницу в температуре кипения (перегонка), различную растворимость. Для газов – сорбционные методы, либо химическое связывание.