

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...
Топ:
Характеристика АТП и сварочно-жестяницкого участка: Транспорт в настоящее время является одной из важнейших отраслей народного...
Эволюция кровеносной системы позвоночных животных: Биологическая эволюция – необратимый процесс исторического развития живой природы...
Комплексной системы оценки состояния охраны труда на производственном объекте (КСОТ-П): Цели и задачи Комплексной системы оценки состояния охраны труда и определению факторов рисков по охране труда...
Интересное:
Национальное богатство страны и его составляющие: для оценки элементов национального богатства используются...
Как мы говорим и как мы слушаем: общение можно сравнить с огромным зонтиком, под которым скрыто все...
Мероприятия для защиты от морозного пучения грунтов: Инженерная защита от морозного (криогенного) пучения грунтов необходима для легких малоэтажных зданий и других сооружений...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Основа определяет форму косметического средства. Кремы, гели, растворы, мази, пудры — эти разные косметические формы характеризуются только им присущими физико-химическими и биологическими свойствами. Но в подавляющем большинстве косметических рецептур присутствует вода. И это не случайно.
Вода — универсальный растворитель в живой природе и необходимый компонент в жизни любой клетки. Хотя существуют и безводные рецептуры (например, чистые растительные масла и вазелиновые мази), именно вода, благодаря своим уникальным физико-химическим свойствам позволяет создавать широкое разнообразие рецептур. При растворении в воде различных веществ могут образовываться следующие типы смесей.
Раствор — гомогенная смесь, состоящая из растворенного вещества и растворителя. В гомогенных системах при заданных условиях существует только одна фаза и нет границы раздела. Например, соль в воде образует раствор. Растворы всегда прозрачны.
В гетерогенных (дисперсных) системах в термодинамическом равновесии находятся две или более фаз, между которыми существует поверхность раздела (межфазная поверхность). Устойчивость гетерогенных систем сильно зависит от величины межфазного натяжения на границе раздела фаз. Чем ниже поверхностное натяжение на границе раздела фаз, тем более устойчивой является дисперсная система. Поверхностное натяжение — мера нескомпенсированности межмолекулярных сил на границе раздела фаз, вследствие чего свободная энергия молекул в поверхностном слое выше, чем в объемах соприкасающихся фаз. Стремление любой системы уменьшить свою поверхностную энергию обусловливает существование поверхностного натяжения, действие которого проявляется в стремлении уменьшить площадь контакта между фазами (например, капля жидкости на границе с воздухом принимает сферическую форму).
|
|
(Что такое устойчивость? Почему устойчивость гетерогенных систем сильно зависит от величины межфазного натяжения на границе раздела фаз? Почему чем ниже поверхностное натяжение на границе раздела фаз, тем более устойчивой является дисперсная система? Почему стремление любой системы уменьшить свою поверхностную энергию обусловливает существование поверхностного натяжения, действие которого проявляется в стремлении уменьшить площадь контакта между фазами? Лично мне было интересно углубиться в причины процесса и я хочу поделиться ими с вами. Если вас это не интересует, то можете домотать до окончания и продолжить чтение. Объяснение будет достаточным для тех, кто знаком в некоторой степени с физикой и химией. В процессе чтения вы встретите аббревиатуру ПАВ, что значит поверхностно активные вещества, о них будет сказано ниже.
" План:
1. Характеристика гетерогенных систем.
2. Виды устойчивости гетерогенных систем.
3. Стабилизация гетерогенных систем.
4. Литература
Характеристика гетерогенных систем
Большинство лекарственных форм представляет собой дисперсные системы, дисперсной фазой которых является лекарственное вещество. В зависимости от его свойств системы могут быть гомогенные и гетерогенные.
Гетерогенные системы характеризуются существованием реальных физических поверхностей раздела между фазой и средой. Размеры частиц фазы в этих гетерогенных системах настолько велики по сравнению с молекулами дисперсионной среды, что между ними образуется поверхность раздела.
Суспензии - представляют собой взвеси твердых частиц в жидкой среде. Это грубодисперсная система. Величина частиц дисперсной фазы более 100 мкм. Частицы видимы в микроскоп.
Эмульсии – дисперсная фаза представлена каплями жидкости, не смешивающейся с дисперсионной средой, размером от 1 до 50 мкм.
|
|
Свойства гетерогенных систем:
1. Гетерогенность - наличие фазы и среды.
2. Отсутствие броуновского движения частиц и диффузии из-за большой величины частиц.
3. Суспензии и эмульсии проявляют свойства мутных сред в отраженном и в проходящем свете.
4. В них не наблюдается осмотического давления, так как частицы фазы несоизмеримы с молекулами среды. (У коллоидных растворов - низкое осмотическое давление).
5. Все гетерогенные системы из-за наличия поверхности раздела являются неустойчивыми системами, то есть изменяют свои свойства в течение времени.
Нарушение однородности суспензии или эмульсии приводит к нарушению точности дозирования лекарственных веществ. Поэтому одним из основных требований к суспензиям и эмульсиям является требование стабильности (устойчивости).
Виды устойчивости гетерогенных систем
Под устойчивостью гетерогенных систем понимают способность сохранять свои свойства и состояние в неизменном виде. Устойчивость суспензий и эмульсий условна, она означает лишь некоторую степень постоянства их свойств. Различают следующие виды устойчивости:
< агрегативная; < конденсационная; < кинетическая (седиментационная).
Все виды устойчивости тесно связаны друг с другом, взаимосвязаны.
1) Агрегативная устойчивость - способность частиц фазы противостоять образованию агрегатов. При агрегативной неустойчивости частицы фазы образуют агрегаты, состоящие из первичных исходных частиц. При образовании агрегатов сохраняются сольватные оболочки первичных частиц.
Агрегативно неустойчивая система склонна к разделению фазы и среды. В суспензии образуется осадок, агрегаты легко оседают, в эмульсиях происходит коалесценция.
Агрегация - это неглубокое изменение свойств суспензии, она обратима при взбалтывании.
2. Конденсационная устойчивость - способность частиц фазы противостоять образованию конденсатов. В отличие от агрегации при конденсационной неустойчивости образуются более крупные частицы, некоторые индивидуальные свойства исходных частиц при этом теряются: образуется общая сольватная оболочка.
Конденсация - более глубокое изменение свойств суспензии. При взбалтывании исходное состояние не восстанавливается.
|
|
3. В прямой зависимости от агрегативной и конденсационной устойчивости находится седиментационная устойчивость, или кинетическая.
Кинетическая устойчивость системы - способность противостоять разделению фазы и среды. В суспензии кинетическая неустойчивость выражается седиментацией (оседанием) твердой фазы, а в эмульсиях - коалесценцией (расслаиванием).
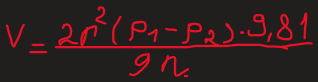
Скорость седиментации является величиной обратной скорости осаждения частиц, которая определяется законом Стокса.
где: V - скорость седиментации, r - радиус частиц фазы.

| - разность плотностей фазы и среды. |
g- ускорение свободного падения.
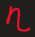 - вязкость среды.
- вязкость среды.
Из формулы можно определить факторы седиментационной устойчивости:
1. Радиус частиц. Чем мельче частицы, тем они медленнее оседают.
2. 
| - вязкость. Чем больше вязкость среды, тем устойчивее система. |
При приготовлении гетерогенных систем учитывают факторы, влияющие на все виды устойчивости.
Стабилизация гетерогенных систем.
Стабилизация гетерогенных систем осуществляется как с помощью технологических приемов, так и с помощью стабилизаторов.
Цель стабилизации (независимо от способов) предотвратить разделение дисперсной системы на фазу и среду, обеспечить однородность.
Технологические приемы стабилизации:
< тщательное измельчение дисперсной фазы. В суспензиях твердая фаза измельчается в присутствии расклинивающей жидкости на стадии приготовления пульпы.
< использование загустителей дисперсионной среды.
Технологические приемы обеспечивают стабильность суспензий лишь гидрофильных веществ, на поверхности которых образуется сольватная (гидратная) оболочка. Однако, при изготовлении суспензий из гидрофобных веществ и эмульсий, на поверхности частиц дисперсной фазы сольватной оболочки не образуется и дисперсионная среда (вода) выталкивает не родственное ей вещество на поверхность, в результате чего происходит флокуляция (в суспензиях) или коалесценция (в эмульсиях). Для стабилизации дисперсной фазы в дисперсионной среде необходимо введение стабилизатора - вспомогательного вещества. Стабилизирующий эффект проявляется в силу действия различных механизмов. Различают несколько механизмов стабилизации гетерогенных систем.
|
|
1. Уменьшение свободной поверхностной энергии при сохранении суммарной поверхности
В связи с наличием поверхности раздела в гетерогенных системах образуется запас свободной поверхностной энергии, которая стремится к минимуму. Это стремление реализуется через укрупнение частиц путем агрегации или конденсации и тем самым уменьшения площади суммарной поверхности. В результате система становится неустойчивой, расслаивается.
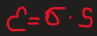 , где
, где
 - свободная поверхностная энергия.
- свободная поверхностная энергия.
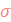 - поверхностное натяжение,
- поверхностное натяжение,
s - суммарная поверхность.
В гетерогенных системах свободная поверхностная энергия может быть уменьшена за счет уменьшения поверхностного натяжения на границе раздела фазы и среды с помощью ПАВ, при этом сохранения суммарной поверхности.
1. Стабилизация может быть обеспечена образованием на поверхности частиц дисперсной фазы двойного электрического слоя.
Такой слой образуют ионогенные стабилизаторы, содержащие в своей молекуле катион и анион. Этот слой аналогичен защитному слою мицеллы в коллоидных растворах. Частицы с двойным электрическим слоем, имея одинаковый внешний заряд, будут отталкиваться друг от друга и, следовательно, сохранять устойчивость гетерогенной системы.
3. Энтропийный механизм стабилизации заключается в том, что молекулы стабилизатора (ВМС) адсорбируются на частице дисперсной фазы частью своей молекулы. В то время как большая часть их молекулы - (цепи)- будет находиться в дисперсионной среде в свободном состоянии и способна совершать некоторое движение. Последнее способствует отталкиванию частиц друг от друга, то есть обеспечивает стабильность.
4. Образование на поверхности частиц фазы твердых оболочек из стабилизатора при использовании твердых "бронирующих" стабилизаторов (бентониты).
Механизм стабилизации гетерогенной системы определяется свойствами стабилизатора. Поскольку все стабилизаторы являются поверхностно-активными веществами, то во всех случаях их использования имеет место первый механизм стабилизации (снижение поверхностной энергии). Дополнительно к нему могут "работать" и другие механизмы в зависимости от индивидуальных свойств стабилизатора.
Литература:
1. Технология лекарственных форм / Под ред. Т. С. Кондратьевой. М.: Медицина, 1991.-T.I.
2. И.А. Муравьев. Технология лекарств.- М.: Медицина, 1980.- Т.2.
3. М.Х. Глузман, Г.С. Башура и др. Поверхностно-активные вещества и их применение.- М., 1972.
|
|
4. Полимеры в фармации / Под ред. А.И. Тенцовой. М. 1985.
5. Справочник фармацевта.
6. Государственная фармакопея XI издания.- Т.2., 1990.")
Суспензия — это гетерогенная система, в котором нерастворимые частицы твердого вещества взвешены вводе и не оседают на дно. Частицы глины или грязи, взвешенные в воде, образуют суспензию. Разновидностью суспензий являются липосомальные и мицеллярные препараты, в которых дискретные частицы липидов, организованных определенным образом, взвешены в водной фазе. Суспензии, как правило, непрозрачны, поскольку частицы обладают светоотражающими свойствами (когда частицы очень мелкие и их концентрация в суспензии невелика, суспензия может казаться прозрачной).
Гель — это гетерогенная система, в которой дисперсионный компонент формирует в воде (дисперсной фазе) непрерывную трехмерную пространственную структуру (сетку). В качестве примера можно привести одно из самых популярных веществ в косметологии — гиалуроновую кислоту, которая при соединении с водой формирует гель. Гель может быть прозрачным и непрозрачным в зависимости от концентрации и типа полимерных веществ.
Эмульсия — дисперсная система, представляющая собой смесь двух жидких несмешивающихся веществ, в которой одно вещество образует дискретную фазу (капли) и равномерно распределено в другом веществе, формирующем непрерывную фазу. К препаратам на эмульсионной основе относятся кремы, косметическое молочко. Эмульсия всегда непрозрачна в связи с оптической неоднородностью фаз.
Вода
Вода и способы ее очистки
Содержание воды в организме в зависимости от водно-солевого баланса составляет от 60 до 70%.
(ВО́ДНО-СОЛЕВО́Й ОБМЕ́Н, совокупность процессов поступления, всасывания, распределения и выделения воды и солей в организмах животных и человека. В.-с. о. обеспечивает постоянство осмоляльности, концентрации каждого из ионов и кислотно-щелочного равновесия жидкостей внутренней среды организма. Осмоляльность определяется как суммарная концентрация всех растворённых осмотически активных веществ и выражается в единицах мосм/кг, т. е. молярным количеством веществ в граммах на килограмм растворителя (в данном случае H2O). В норме процессы поступления воды в организм и её выделения уравновешены. У человека массой 70 кг, напр., суточная потребность в воде (в условиях умеренного климата) составляет ок. 2,5 л, из которых 1,2 л поступает в виде питьевой воды, 1 л – с пищей, 0,3 л образуется в организме при окислении гл. обр. липидов, углеводов и белков. Выделяется вода с мочой, потом и калом, часть её теряется при испарении с поверхности кожи и через лёгкие. Общее содержание воды в теле человека обычно составляет св. 60% от его массы. Потери воды, превышающие 0,5–1,5% от массы тела, вызывают чувство жажды. Наряду с водой организмы нуждаются в поступлении неорганич. веществ: ионов Na+, K+, Ca2+, Mg+2, Cl–, SO2−4, PO3−4, HCO−2, и микроэлементов (Fe, Zn, Co, Cu и др). Всосавшиеся в кишечнике и почечных канальцах ионы поступают в кровь или лимфу и переносятся ко всем клеткам. По солевому составу вне- и внутриклеточные жидкости различаются: в клетках преобладают ионы K+,Mg2+ и фосфаты, вне клеток – ионы Na+,Ca2+и Cl–. Это различие поддерживается деятельностью биологич. мембран и связыванием ионов химич. компонентами клетки (напр., фосфолипидами, белками). В организме имеются также солевые депо: напр., в костной ткани содержится много Ca2+, в печени депонируются микроэлементы.
Регуляция В.-с. о. у позвоночных происходит при участии нервной системы, гормонов и аутакоидов. Изменение осмоляльности крови в организме воспринимается осморецепторами, локализованными в мозге, некоторых органах и тканях. Информация от осморецепторов обрабатывается в центр. нервной системе и передаётся в заднюю долю гипофиза – нейрогипофиз. Повышение осмоляльности крови приводит к увеличению секреции нейрогипофизом антидиуретич. гормона (у млекопитающих – вазопрессин; у птиц, рептилий, амфибий – вазотоцин), который увеличивает реабсорбцию воды и уменьшает её выделение с мочой. Снижение осмоляльности крови (при избытке воды в организме) приводит к понижению секреции этого гормона, что усиливает выделение воды почками. Постоянство объёма жидкостей тела обеспечивается системой волюморегуляции; волюморецепторы реагируют на изменение кровенаполнения крупных сосудов, полостей сердца и др. В результате рефлекторно возрастает секреция гормонов, стимулирующих выделение воды и солей натрия из организма. Важную роль в регуляции баланса воды играют гормоны вазопрессин и глюкокортикоиды, баланс натрия поддерживается альдостероном, атриопептидом и ангиотензином II, кальция – паратиреоидным гормоном, кальцитонином, активными формами холекальциферола (витамина D3). Центр. нервная система координирует деятельность разл. органов и систем, обеспечивая постоянство осн. параметров водно-солевого обмена.
Источник: Лит.: Физиология водно-солевого обмена и почки. СПб., 1993; Фролов Б. А. Физиология и патология обмена натрия и воды в организме. М., 2004.)
Вода является дисперсионной средой цитоплазмы клеток, непосредственно участвует в большинстве биохимических реакций. Вода обеспечивает тургор и осморегуляцию клеточных структур.
(Осморегуляция — физико-химические и физиологические процессы, обеспечивающие постоянство осмотического давления (концентрации осмотически активных веществ; к осмотически активным веществам относят разл. ионы (в т. ч. Na+, K+, Mg2+, Cl−, HCO−3, SO2−4, фосфаты, органич. кислоты), глюкозу, мочевину и др.) внутренней среды организма (внеклеточная жидкость, гемолимфа, лимфа, плазма крови). В результате осморегуляции происходит либо выделение воды и солей из организма, либо выдержка и перераспределение воды в организме. Концентрация осмотически активных веществ выражается в осмолях (сокр. обозначение – осм) – в количестве недиссоциирующего вещества в молях на килограмм воды растворителя (осмоляльность) или на литр раствора (осмолярность). Эволюция животного мира происходила на фоне изменений условий обитания (переход из мор. воды в пресные водоёмы, выход на сушу, вторичное возвращение в мор. воду) и сопровождалась развитием разл. адаптаций. Жизнь в любых средах требует в определённой степени контролируемых физико-химич. условий для клеток каждой особи. К таким условиям относится суммарная концентрация растворённых веществ, концентрация отд. ионов, pH. Существует два типа реакций животных на концентрацию осмотически активных веществ во внешней среде обитания. Пойкилосмотические животные не обладают активной системой стабилизации концентрации осмотически активных веществ в жидкостях внутр. среды, и осмоляльность внеклеточных жидкостей их тела зависит от осмоляльности внешней среды (в осн. мор. беспозвоночные и миксины). Гомойосмотические животные способны поддерживать постоянство концентрации осмотически активных веществ в жидкостях внутр. среды.
У человека и млекопитающих О. обеспечивается т. н. осморегулирующим рефлексом и контролируется осморегулирующей системой, включающей специализир. рецепторы (осморецепторы), информация от которых передаётся через ЦНС к задней доле гипофиза; в О. участвуют надпочечники, разл. сенсорные органы и др. Важное значение имеют изменение скорости секреции гормона аргинин-вазопрессина или лизин-вазопрессина (см. Вазопрессин) и реакция на него почек. Концентрация осмотически активных веществ в сыворотке крови у человека относится к числу наиболее строго контролируемых физико-химич. параметров. Она в течение всей жизни составляет обычно 285–290 мосм/кг H2O, это значение уменьшается при потреблении воды и возрастает во время обезвоживания. Почки быстро обеспечивают восстановление этого показателя, изменяя объём выделяемой воды. Они способны выделять сильно разбавленную (гипотоническую) мочу при избытке воды в организме и более концентрированную мочу – при дефиците воды. При некоторых заболеваниях у человека (сахарный диабет, хронич. почечная недостаточность) требуются дополнит. меры для коррекции осморегуляции.
Источник: Лит.: Общий курс физиологии человека и животных. М., 1991. Кн. 2; Эккерт Р., Рэнделл Д., Огастин Дж. Физиология животных. М., 1992. Т. 2.)
Содержание воды в коже не зависит от воздействия косметических средств, которые могут оказать влияние только на содержание воды в верхнем, роговом слое эпидермиса, где ее в среднем около 15%. Кожа называется сухой, если содержание воды в ней 10 и менее процентов. Ежесуточно кожа теряет в результате испарения около 6 мг/см^2 воды.
Вода находится в составе практически всех косметических средств: входит в состав гелей, шампуней, эмульсионных кремов; биологически активные добавки вводят в косметические композиции в виде водных настоев, отваров; вода является растворителем для многих ПАВ, некоторых полимеров, солей и др. и, следовательно, относится к основным видам сырья для косметической промышленности.
Природная вода содержит различное количество минеральных солей (хлориды, карбонаты, силикаты калия и натрия, кальция и магния, железа и меди). Соли снижают пенообразующую способность моющих средств, изменяют устойчивость кремов (эмульсий). Растворенные соли железа в присутствии некоторых консервантов вызывют нежелательную окраску композиции. Кроме того, природная вода может быть заражена разными микроорганизмами. Поэтому при производстве косметических средств используют воду, соответствующую по своим показателям стандартам (ГОСТу) на питьевую воду.
В технологии косметических средств подготовка воды направлена на снижение содержания неорганических солей, органических примесей и бактериальной флоры. С точки зрения органо-лептических показичелей вода для косметических препаратов должна быть бесцветна, абсолютно прозрачна, не иметь запаха и не иметь вкуса. После длительного отстаивания вода не должна оставлять мути.
С точки зрения химического состава вода не должна содержать неорганические соли в виде примесей. Жесткую воду, которая содержит значительное количество солей магния и кальция, необходимо дополнительно очищать с целью уменьшения её жесткости.
Показателем бактериологической чистоты воды является Coli-титр или Coli-индех. Coli-титр численно равен наименьшему объёму воды в миллилитрах, в котором найдена одна кишечная палочка Bact. coli..
В зависимости от вида водоподготовки различают воду деионизированную, кипячёную, дистиллированную, стерилизованную и апирогенную.
Деионизированную воду получают методом ионного обмена. Катионные ионообменные смолы позволяют удалить из воды практически полностью ионы кальция, железа, магния и, таким образом, умягчить воду. Контроль качества деионизированной воды удобно проводить методом кондуктометрии (Кондуктометрия метод физико-химического анализа веществ, основанный на изменении электрической проводимости растворов).
Чем меньше солей растворено в воде, тем выше электрическое сопротивление такой воды. Основной проблемы при деионизации воды является неудовлетворительная микробиологическая характеристика воды. Поэтому ионообменные смолы периодически обрабатывают формальдегидом или пероксиуксусной кислотой.
Стерилизованную воду получают при ультрафиолетовом облучении, при обработке воды хлором, озоном или с помощью мембранной фильтрации.
Ультрафиолетовое облучение проводят только для оптически прозрачных сред при длине волны 260 нм. Эффективность обеззараживания зависит от времени воздействия. Обычно необходимый уровень облучения составляет около 100 Вт/см^2.
Хлорирование обеспечивает длительный эффект стерилизации за счет неспецифического действия хлора на клеточную мембрану. Активная концентрация хлора должна быть не менее 5 мг/л, что на порядок выше, чем при подготовке питьевой воды. Кислая среда и высокая температура повышают окислительное действие хлора, но наличие органических примесей заметно уменьшает эффективность хлорирования воды. После хлорирования рекомендуется обрабатывать воду активированным углем, содержащим серебро.
Озонирование воды протекает быстро. Время полного распада озона составляет от 2 до 10 минут При этом не изменяются ни цвет, ни запах, ни вкус воды. Однако озонирование гораздо дороже, чем хлорирование.
Мембранная фильтрация позволяет удалять бактерии, коллоидные примеси с размером частиц 0,2—0,3 мкм и более. Обычно мембранную фильтрацию проводят при избыточном давлении с использованием специальных микро- и ультрафильтров. Недостатком этого метода является его длительность.
В современных косметических рецептурах модно использовать воду из минеральных и термальных природных источников. Такая вода обогащена природными минералами, солями металлов, микроэлементами. Добавление такой воды в косметические препараты должно вызывать общее оздоровление организма и улучшение состояния кожи. Однако, необходимо тщательно проверять, как вода из термальных или минеральных источников, которая имеет высокую проводимость и ионную силу из-за наличия в ней растворимых солей, влияет на остальные компоненты косметической рецептуры, не изменяет ли она конформации и состояние полимеров, консервантов, УФ-фильтров и других веществ, которые чувствительны к изменению ионной силы среды.
Эмульсии
Эмульсия — это дисперсия (Дисперсные системы- это гетерогенные системы, состоящие из двух и более фаз (Термодинамическая фаза — гомогенная часть гетерогенной системы, ограниченная поверхностью раздела[1][2].) с сильно развитой поверхностью раздела между ними. Источник определения дисперсной системы Урьев Н. Б. Физико-химическая динамика дисперсных систем // Успехи химии. 2004. Т. 73. № 1; источник определения фазы "Термодинамика. Основные понятия. Терминология. Буквенные обозначения величин / Отв. ред. И. И. Новиков. — АН СССР. Комитет научно-технической терминологии. Сборник определений 1984".)
из двух и более несмешивающихся в норме компонентов. Одна фаза эмульсии, называемая дисперсной (внутренней), растворяется в другой — дисперсионной (внешней) фазе. Эмульсии представляют собой одну из наиболее распространенных форм косметической продукции. Косметическая эмульсия позволяет соединить в одном продукте водо- и жирорастворимые компоненты — в этом ее большое преимущество перед другими косметическими формами. Масляная фаза эмульсионных кремов содержит жиры (насыщенные и/или ненасыщенные), гидрофобные эмоленты (вещества, смягчающие кожу), жирорастворимые активные добавки (например, витамин Е), а в водной фазе находятся консерванты и водорастворимые активные компоненты.
Простые косметические эмульсии делятся на несколько типов:
1. «Масло-в-воде» (м/в) — малый объем масла растворен в большом объеме воды.
2. «Вода-в-масле» (в/м) — малый объем воды растворен в большом объеме масла.
3. «Вода-в-силиконе» (в/с) — технически этот тип эмульсий относится к предыдущей группе. Водная фаза, содержащая этанол или многоатомные спирты, а также водорастворимые активные вещества, составляет примерно 75-90% композиции. «Масляная» фаза состоит из одного летучего и одного нелетучего силиконового масла и силиконового эмульгатора.
4. «Масло-в-воде-в-масле» (м/в/м) — это множественные эмульсии, где в одной из частей превалирует вода с диспергированными в ней масляными каплями, а в другой — масло со взвешенными в нем капельками воды.
5. Безмасляные растворы и гели — о них мы поговорим более подробно далее.
Наиболее распространенным типом эмульсий является «масло-в-воде» (масла мало, воды много) — за счет более низкой стоимости производства, удобства применения и «легкости» текстуры (обычно используется как увлажняющее средство).
Многие косметические средства могут раздражать кожу с нарушением барьерной функции — на этот случай разработаны ламеллярные эмульсии. По своему составу они идентичны липидным бислоям и в целом напоминают роговой слой эпидермиса. Обычные эмульсии, как вы уже знаете, представляют собой «масло-в-воде» или «воду-В-масле», то есть капли одного вещества, окруженные другим веществом и стабилизированные эмульгатором. В ламеллярных же эмульсиях эмульгаторы отсутствуют, а масляные капли окружены не водой, как в эмульсии «масло-в-воде», а липидными бислоям, между которыми располагаются прослойки воды. Сами липидные бислои сформированы преимущественно фосфолипидами (и по сути представляют собой искусственные клеточные мембраны), а вся пластинчатая (ламеллярная) структура имитирует липидный барьер, расположенный между корнеоцитами рогового слоя. Ламеллярные эмульсии обладают хорошими увлажняющими свойствами. Они рекомендуются для чувствительной, сухой кожи (в том числе при атопическом дерматите). Важным преимуществом ламеллярных эмульсий является их приятная текстура — они не оставляют жирного блеска, легко распределяются по коже и хорошо впитываются.
Это как раз тот удачный вариант, когда липиды в косметическом средстве выполняют одновременно функцию технической добавки и активного ингредиента, восстанавливая (а не нарушая, как большинство традиционных эмульгаторов) и укрепляя барьерную функцию кожи. Иными словами, даже «пустые» ламеллярные эмульсии с ценным липидным составом сами по себе — отличные корнеотерапевтические средства (ч. 4, гл. 1), с помощью которых можно поддерживать кожный барьер в хорошем состоянии. А если еще и «нагрузить» ламеллярные эмульсии активными веществами, то получится средство, способное решать по меньшей мере две задачи:
1) специфическое воздействие, связанное со свойствами активного ингредиента;
2) неспецифическое корнеотерапевтическое действие, связанное с присутствием в рецептуре липидов, входящих в состав ламеллярных структур.

Для того чтобы создать достаточно стабильные эмульсии типа «масло в-воде», нужно преодолеть поверхностное натяжение между двумя фазами. Это можно сделать путем простого смешивания, но даже очень мощного
миксера не хватит, чтобы обеспечить длительную стабильность такой эмульсии. Как бы вы ни старались, смешиванием не удастся получить хорошую м/в эмульсию, и вода с маслом быстро разойдутся на фазы.
Для стабилизации «масла-в-воде» необходим еще один компонент, называемый эмульгатором (а лучше — комбинация эмульгаторов).
Эмульгаторы
Эмульгаторы — это вещества, обеспечивающие стабильность эмульсий, путём предотвращения слияния капель дисперсной фазы. Они абсорбируются на границе раздела фаз, образуя связующую пленку между двумя средами (или, как их еще называют, фазами). Из-за особой структуры полярная часть молекулы эмульгатора обладает сродством к воде, а неполярная (насыщенные или ненасыщенные цепи жирных кислот) — к жировой фазе. Эмульгаторы разделяют одну из жидкостей на отдельные капли, удерживая их в другой жидкости во взвешенном состоянии. Поскольку эти капли ограждены защитным слоем молекул эмульгаторов, они не сливаются и друг с другом тоже. В итоге два вещества находятся в стабильной, не расслаивающейся смеси.
|
|
|

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Биохимия спиртового брожения: Основу технологии получения пива составляет спиртовое брожение, - при котором сахар превращается...

Наброски и зарисовки растений, плодов, цветов: Освоить конструктивное построение структуры дерева через зарисовки отдельных деревьев, группы деревьев...

Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ - конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!