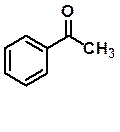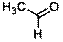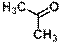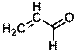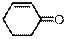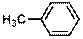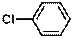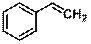Адсорбционная спектроскопия в ультрафиолетовой и видимой области – один из первых методов исследования органических соединений.
Спектры поглощения в ультрафиолетовой и видимой областях (УФ-спектры) обусловлены переходами между электронными состояниями молекулы, поэтому их называют электронными спектрами. Согласно теории молекулярных орбиталей, переход молекулы из основного электронного состояния в возбужденное соответствует переходу валентного электрона без изменения спина с занятой связывающей или несвязывающей орбитали на вакантную антисвязывающую орбиталь. При этом трем типам молекулярных орбиталей – σ, π и n – четыре типа электронных переходов:
σ → σ*, π → π*, n → σ* и n →π*
Ультрафиолетовую область обычно разделяют на две части:
1) ближняя ультрафиолетовая область, диапазон длин волн которой составляет 200-400 нм или 5·104 –2,5·104 см-1, а энергия изменяется в пределах: Е= 10·10-22–5·10-22 кДж / моль;
2) дальняя ультрафиолетовая область с диапазоном длин волн: 100–200 нм или 105–5·104 см-1 и энергией Е = 20·10-22–10·10-22 кДж / моль.
Поглощением света (электромагнитного излучения) называется явление уменьшения энергии световой волны при её распространении в веществе,происходящее вследствие преобразования энергии волны во внутреннююэнергию вещества или в энергию вторичного излучения, имеющего другойспектральный состав и иные направления распространения.
Законы поглощения света определяют соотношение между величиной поглощения и количеством (концентрацией) поглощающего вещества.
Первый закон выражает зависимость между интенсивностью прошедшего излучения и толщиной слоя поглощающего вещества:
I = I 0 k ′ c - l , (3)
где I0 – интенсивность падающего света;
I – интенсивность прошедшего света;
с – молярная концентрация вещества, моль /л;
l – длина пути света, см;
k ′ – коэффициент поглощения (индивидуальная характеристика вещества для каждой длины волны), л/моль∙см.
Второй закон выражает связь между интенсивностью прошедшего излучения и концентрацией поглощающего вещества растворе (уравнение 4)
D = –lgI0/I = ε ∙cl, (4)
| где D – оптическая плотность;
|
| с – молярная концентрация вещества, моль/л;
|
| l – длина пути света, см;
|
| ε – молярный коэффициент экстинкции, л/моль∙см
|
Отклонения от закона Бугера–Ламберта–Бера наблюдаются при использовании немонохроматического света, неравномерном заполнении кюветы или неоднородном распределении поглощающего вещества; пропорциональность оптической плотности и концентрации может нарушаться в относительно концентрированных растворах и при очень большой интенсивности падающего света (например, для лазерного излучения).
Электронные спектры или спектры в ультрафиолетовой и видимойобластях представляют собой зависимость поглощения электромагнитного излучения от длиныволны этого излучения. В качестве меры поглощения используется оптическаяплотность D, коэффициент экстинкции ε или его десятичный логарифм lg ε. Спектрхарактеризуется: положением максимума полосы поглощения – λмакс; интенсивностью поглощения; формой линии поглощения (рис. 4). Если веществоокрашено, то в его спектре наблюдаются полосы поглощения в видимойобласти.
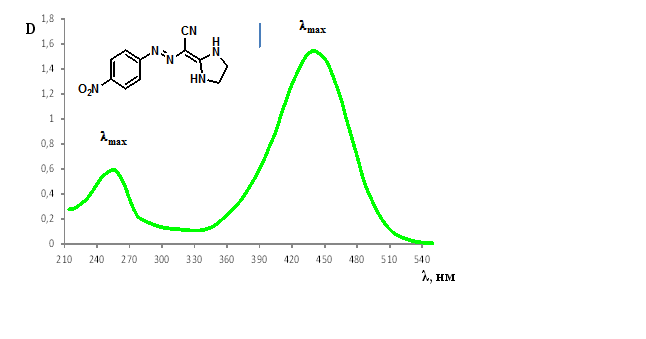 Рис. 4. УФ-спектр гидразоноимидазолидина (С2H5OH)
Рис. 4. УФ-спектр гидразоноимидазолидина (С2H5OH)
При описании электронных спектров используют следующие термины:
полоса поглощения – область спектра, в которой имеется детектируемый сигнал с одним или несколькими максимумами;
тонкая колебательная структура (тонкая структура) – сложный контур полосы поглощения, возникающий за счет перехода на разные колебательные уровни одного и того же электронного состояния;
батохромный (красный) сдвиг – сдвиг полосы поглощения в длинноволновую область спектра (в область больших значений λ)
гипсохромный (синий) сдвиг – сдвиг полосы поглощения в коротковолновую область спектра (в область меньших значений λ);
гиперхромный эффект – увеличение интенсивности поглощения;
гипохромный эффект – уменьшение интенсивности поглощения.
Поглощение вещества в ближнем ультрафиолете и видимой области связано с возбуждением π → π* и n →π* – переходов. Эти переходы могут происходить в молекулах, содержащих ненасыщенные группировки. Атомную группировку, включающую хотя бы одну кратную связь, которая придает веществу способность к поглощению в ближней ультрафиолетовой и видимой области, называют хромофором. Хромофоры могут быть изолированными и сопряженными. Изолированные хромофоры содержат одну кратную связь (С=С, С=О, N=N). Сопряженные хромофоры ‒ это структуры, представляющие собой системы сопряженных кратных связей. Соединения, содержащие сопряженные хромофоры, поглощают в более длинноволновой области.
Атомную группировку, которая не содержит кратных связей и не имеет максимума поглощения в ближнем ультрафиолете, но включение которой в систему хромофора приводит к увеличению длины волны электронного перехода и увеличению интенсивности поглощения, называют ауксохромом (ОН, NH2, SH).
Молекула может давать несколько полос поглощения в
УФ-спектре, если в ее структуре имеется несколько хромофоров. Например: в УФ-спектре ацетофенона (спирт) имеется три полосы поглощения, которые легко соотнести:
| 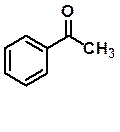
| lmаx, nm
| ε
| log ε
| Тип перехода
|
| 244
| 12600
| 4,1
| π → π*
|
| 280
| 1600
| 3,2
| π → π*
|
| 317
| 60
| 1,8
| n → π*
|
Сопряжение в углеводородной цепи всегда вызывает значительный сдвиг в область длинных волн (батохромный сдвиг) и увеличение интенсивности полосы поглощения (табл. 6).
Таблица 6.
Спектры поглощения соединений, содержащих
С=С связи
| Алкены
| lmаx, nm
| ε
| log ε
|
| СН2=СН2
| 165
| 10000
| 4,0
|
| CH3–CH2–CH=CH–CH2–CH3
| 184
| 10000
| 4,0
|
| СН2=СН–СН=СН2
| 217
| 20000
| 4,3
|
| CH3–СН=СН–СН=СН2
| 224
| 23000
| 4,4
|
| СН2=СН–СН=СН–СН=СН2
| 263
| 53000
| 4,7
|
Все соединения с карбонильной группой имеют слабое поглощение (ε<100) в области 250–350 нм. Для соединений, в которых карбонильная группа находится в сопряжении с кратными связями, наблюдается более сильное поглощение (табл. 7).
Таблица 7.
Спектры поглощения соединений с С=O связями
| Соединение
| Структура
| lmаx, nm
| ε
| log ε
|
| Ацетальдегид
| 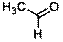
| 293 (гексан)
| 12
| 1,1
|
| Ацетон
| 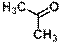
| 279 (гексан)
| 15
| 1,2
|
| Пропеналь
| 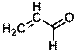
| 207
328
| 12000
20
| 4,1
1,3
|
| Циклогекс-2-ен-1-он
| 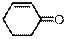
| 225
| 7950
| 3,9
|
| Бензохинон
| 
| 247
292
363
| 12600
1000
250
| 4,1
3,0
2,4
|
Производные бензола имеют несколько полос поглощения в УФ-области (табл. 8). Примеры спектров соединений, приведенные в таблице, имеют в структуре слабые ауксохромы (–СН3, –Сl, –OCH3), группы с кратными связями (–СН=СН2, –С(=О)–R, NO2) и ауксохромы, для которых поглощение зависит от рН (–NH2 и –OH).
Таблица 8.
Полосы поглощения в УФ-спектрах некоторых производных бензола
| Соединение
| Структура
| lmаx, nm
| ε
| log ε
|
| Бензол
| 
| 184
204
256
| 60000
7900
200
| 4,8
3,9
2,3
|
| Толуол
| 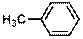
| 208
261
| 8000
300
| 3,9
2,5
|
| Хлорбензол
| 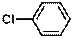
| 216
265
| 8000
240
| 3,9
2,4
|
| Анизол
| 
| 220
272
| 8000
1500
| 3,9
3,2
|
| Стирол
| 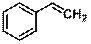
| 244
282
| 12000
450
| 4,1
2,7
|
| Ацетофенон
| 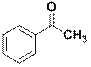
| 244
280
| 12600
1600
| 4,1
3,2
|
| Нитробензол
| 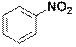
| 251
280
330
| 12600
1600
130
| 4,0
3,0
2,1
|
| Анилин
| 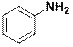
| 230
281
| 8000
1500
| 3,9
3,2
|
| Катион анилиния
| 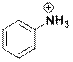
| 203
254
| 8000
160
| 3.9
2.2
|
| Фенол
| 
| 211
270
| 6300
1500
| 3.8
3.2
|
| Феноксид анион
| 
| 235
287
| 9500
2500
| 4.0
3.4
|
Полярность растворителя может влиять на характеристики поглощения, в особенности на положение, поскольку полярность молекулы обычно изменяется, когда электрон перемещается с одной орбитали на другую. Растворитель может смещать длинноволновый максимум карбонильных соединений на 20 нм.



 Рис. 4. УФ-спектр гидразоноимидазолидина (С2H5OH)
Рис. 4. УФ-спектр гидразоноимидазолидина (С2H5OH)