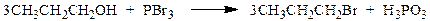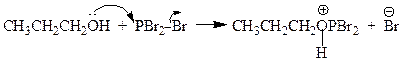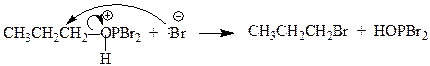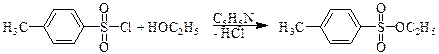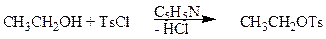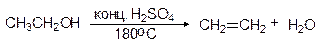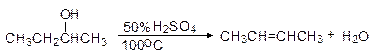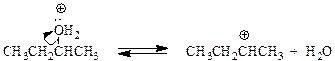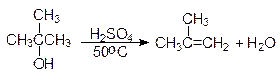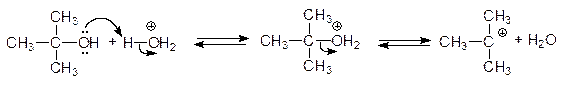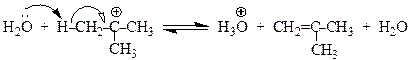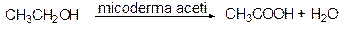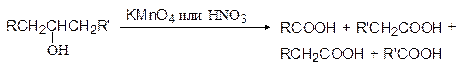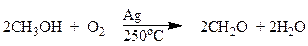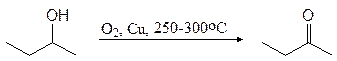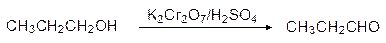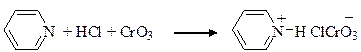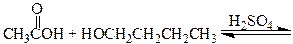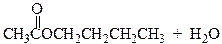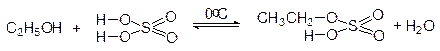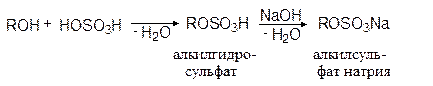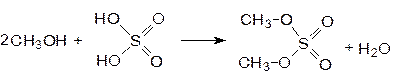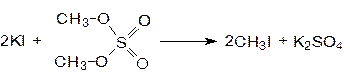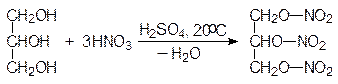Для превращения спиртов в алкилгалогениды применяют различные три- и пентагалогениды фосфора: PBr3, PCl3, POCl3 или PI3. Последний получают из красного фосфора и йода непосредственно во время реакции:
Галогениды и оксигалогениды фосфора относятся к умеренно сильным кислотам Льюиса.
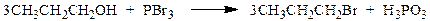
Механизм
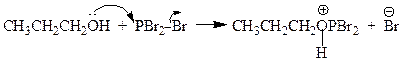
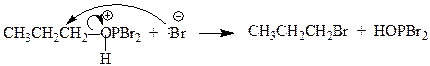
Образующийся HOPBr2 далее реагирует со спиртом по аналогичному механизму, и в конечном итоге все три атома галогена принимают участие в реакции. Замещение гидроксильной группы на галоген в этих реакциях происходит с инверсией конфигурации.
Замещение гидроксильной группы первичных и вторичных спиртов на галоген под действием трибромида фосфора и других галогенидов и оксигалогенидов фосфора происходит с перегруппировками.
Поскольку замещение гидроксильной группы на галоген с помощью галогенидов фосфора часто сопровождается изомеризацией и перегруппировками, эти реагенты следует применять только в простых случаях, где перегруппировка и изомеризация невозможны.
Г. Действием на спирты тионилхлорида
Одним из лабораторных способов превращения спиртов в алкилхлориды является их взаимодействие с тионилхлоридом. Тионилхлорид превращает первичные и вторичные спирты в алкилхлориды с выходом 70-90%. Образующиеся наряду с продуктом замещения хлороводород и диоксид серы газы, что облегчает выделение целевого продукта.

Д. Образование алкилтозилатов
Еще один путь превращения гидроксильной группы спиртов в хорошую уходящую группу - превращение их в тозилаты. Спирты реагируют с п -толуолсульфонилхлоридом (тозилхлоридом Тs¾Cl) превращаясь в алкилтозилаты.
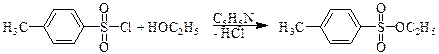
п -толуолсульфонилхлорид этил- п -толуолсульфонат
или
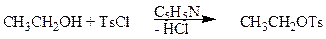
тозилхлорид этилтозилат
Алкилтозилаты вступают во все реакции нуклеофильного замещения. Из них, например, могут быть получены различные галогензамещенные углеводороды. Для этого спирты сначала превращают в алкилтозилаты, которые легко могут быть выделены и очищены. Далее тозилатную группу замещают на другую функциональную группу.
Дегидратация спиртов
Спирты могут быть превращены в алкены путем дегидратации (отщепления или элиминирования воды) от соседних атомов углерода. В лаборатории дегидратацию проводят путем нагревания спиртов с концентрированной серной или 85% фосфорной кислотой.
Условия проведения реакции зависят от строения спирта. Наиболее трудно дегидратируются первичные спирты, наиболее легко - третичные
Первичные спирты дегидратируются по механизму E2 в довольно жестких условиях - 170 - 200оС с использованием концентрированной серной кислоты.
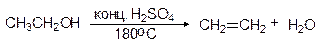
Механизм Е2


Дегидратация вторичных спиртов происходит по механизму Е 1 при температуре 100 - 150оС с менее концентрированными кислотами. Отщепление воды протекает согласно эмпирическому правилу Зайцева: протон отщепляется предпочтительно от наименее гидрогенизированного b-атома углерода. Иными словами, двойная связь образуется у наиболее замещенного атома углерода:
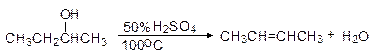

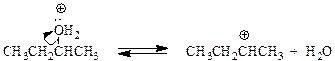

Еще легче отщепляют воду третичные спирты - 50 - 100оС в присутствии более мягких дегидратирующих агентов (разбавленная серная кислота, щавелевая или п -толуолсульфоновая кислота):
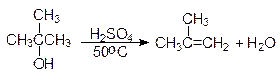
Дегидратация третичных спиртов проходит по механизму Е1.
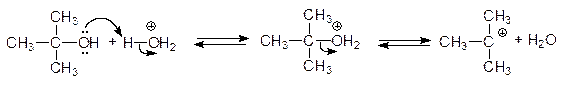
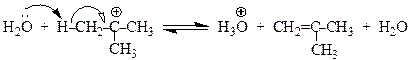
Образующиеся в качестве промежуточных частиц карбокатионы склонны к перегруппировкам, при которых менее стабильные катионы превращаются в более стабильные
Окисление спиртов
Этанол в виде разбавленных растворов, например, в вине окисляется воздухом под действием микроорганизмов в уксусную кислоту (столовый уксус):
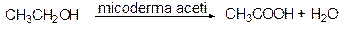
Сильные окислители, такие как щелочной раствор перманганата калия или концентрированная азотная кислота, окисляют спирты до кислот, причем вторичные спирты с разрывом связи С-С с обеих сторон от гидроксильной группы:
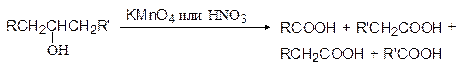
В этой реакции муравьиная кислота (R или R'=H) не образуется, т.к. она легко окисляется далее до СО2. Третичные спирты окисляются сильными окислителями с расщеплением углеродного скелета. Промышленное значение имеет окисление циклогексанола в адипиновую кислоту. Сам же циклогексанол получают гидрированием фенола.

адипиновая кислота
Окисление первичных спиртов до альдегидов представляет определенные трудности, т.к. альдегиды легко окисляются до кислот. Чтобы остановить окисление спиртов на стадии образования альдегидов используют два основных приема – дегидрирование и действие мягких окислителей. Окислением метанола кислородом воздуха получают формальдегид.
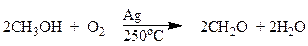

Важный растворитель 2-бутанон (метилэтилкетон) получают в промышленности окислением 2-бутанола.
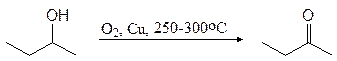
2-бутанол 2-бутанон
Для окисления первичных и вторичных спиртов соответственно до альдегидов и кетонов применяют хромовую кислоту в виде смеси дихроматов натрия (смесь Килиани) или калия (смесь Бекмана) с серной кислотой. Окисление обычно ведут в ацетоне или уксусной кислоте.

Вторичные спирты окисляются с хорошим выходом. С первичными спиртами дело обстоит труднее, т.к. образующиеся альдегиды далее легче, чем спирты окисляются до кислот. Практически альдегид можно получить лишь в том случае, когда его немедленно удается удалить из зоны реакции:
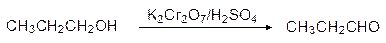
1-пропанол пропаналь
Для окисления первичных спиртов в альдегиды в лабораторной практике широко используется оксид хрома (VI) в виде пиридинийхлорхромата, получаемого растворением СrO3 в соляной кислоте с последующим прибавлением пиридина.
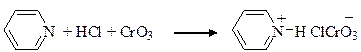
пиридин пиридинийхлорхромат (ПХХ)
или Py.HClCrO3
Окисление пиридинийхлорхроматом (ПХХ) ведут в метиленхлориде.

1-нонанол нонаналь
Используется также смесь оксида хрома (VI) с пиридином (реагент Саррета-Коллинза).
Реакции спиртов с кислотами
Спирты реагируют с карбоновыми кислотами с образованием сложных эфиров (эстеров) по реакции конденсации получившей название этерификация.
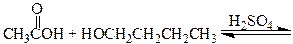
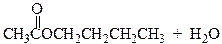
уксусная кислота 1-бутанол бутилацетат
Этерификация катализируется кислотами. Без добавления кислоты равновесие достигается очень медленно, но если же смесь спирта и кислоты нагревать в присутствии небольшого количества концентрированной серной кислоты или хлороводорода равновесие устанавливается достаточно быстро.
С неорганическими кислотами без осложнений реагируют только первичные спирты, в результате чего образуются сложные эфиры (кислые или средние):
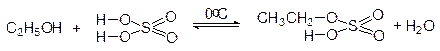
этилгидросульфат
Эта реакция имеет промышленное значение, т.к. с ее помощью из высших спиртов получают синтетические моющие средства:
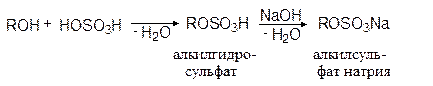
При использовании избытка спирта можно получать диалкилсульфаты. Так при нагревании метанола с олеумом получают диметилсульфат.
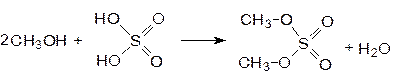
Диметилсульфат используют для получения метилиодида.
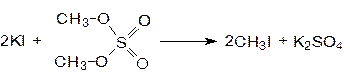
Вторичные и третичные спирты при нагревании с серной кислотой подвергаются дегидратации. При действии на спирты азотной кислоты образуются нитраты.
Нитрованием глицерина получают тринитрат глицерина, неправильно называемый тринитроглицерином. Он является взрывчатым веществом, однако он очень чувствителен к удару, поэтому его применяют в виде динамита, представляющего собой опилки, пропитанные тринитроглицерином. Взрывчатыми веществами являются нитраты и других полиолов.
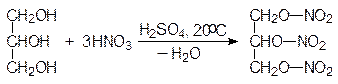
глицерин тринитрат глицерина