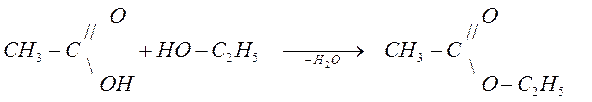Спирты – очень слабые кислоты. Кислород (относительная электроотрицательность 3,5) оттягивает на себя общую электронную плотность с водородом (относительная электроотрицательность 2,1), вызывая поляризацию связи Oδ-←Hδ+. Поэтому возможно замещение атома водорода в спирте на металлы и радикалы:
1) Замещение водорода на металл (Na, K) с образованием алкоголятов - твердых веществ белого цвета.
2СН3—СН2—ОН + 2Na→2СН3— СН2—ОNa + H2
этиловый спирт этилат натрия
Строение углеводородного радикала существенно влияет на подвижность атома водорода в гидроксильной группе. Легче всего замещается водород в метаноле, трудней всего в третичных спиртах.
Сила спиртов определяется подвижностью атома водорода, его способностью замещаться на металл, его окислительными свойствами, она в ряду уменьшается.
СН3


 CH3OH > СН3 —СН2—OH > СН3 —СН—СН3 > CН3 —С—ОН
CH3OH > СН3 —СН2—OH > СН3 —СН—СН3 > CН3 —С—ОН
OH СН3
Расположим углеводородные радикалы по мере убывания их элктронодонорного* воздействия в ряд:
 CH3
CH3
CН3 —С— СН3 —СН— СН3 —СН2— —СН3
CH3 CH3
Максимальным электронодонорным* воздействием обладает радикал третичный бутил, а минимальным – метил.
CH3
↓
CH3→ C →O—H
↑
CH3
третбутиловый спирт
Смещая электронную плотность в сторону атома кислорода (явление смещения электронной плотности по системе σ-связей в сторону более электроотрицательного элемента называется индуктивным эффектом) третичный бутил уменьшает, таким образом, поляризацию связи Oδ-←Hδ+. Уменьшается подвижность атома водорода, его способность к замещению и уменьшается сила спирта.
Если Кдисс воды составляет 10-14(при 25 °С), для метилового спирта эта обладают меньшей кислотностью, и она убывает от метилового спирта к этиловому.
Если ввести в радикал третичный бутил электроноакцепторные* группы или атомы, то кислотные свойства спирта (сила спирта) значительно усиливаются:
CF3
↑
Например, спирт F3C←C←O←H,
↓
CF3
за счет элетроноакцепторного действия фтора обладает более сильными кислотными свойствами и способен вытеснить угольную кислоту из её солей. В этом случае наблюдается отрицательный индуктивный эффект со стороны фтора, приводящий к подвижности водорода Hδ+.
2) Взаимодействие спиртов с магнийорганическими соединениями (реакция Чугаева, Цереветинова). При этом образуются углеводород и производные спиртов - алкоголяты:
С2Н5ОН + СН3—MgI→СН4 ↑ + С2Н5—О—Mg—I
этиловый метилмагниййодид метан этоксимагниййодид
спирт
Реакция используется для количественного определения спирта по объему выделившегося метана.
__________________________________________________________________
* электродонорные (отдающие электроны)
*электроакцепторные (принимающие электроны)
3) Образование простых эфиров
Взаимодействие алкоголятов с галогеналкилами.
С2Н5—О—Na + I—С2Н5  С2Н5—О— С2Н5
С2Н5—О— С2Н5
этилат натрия йодистый этил диэтиловый эфир
Эта реакция не является химическим свойством спирта, но на ее примере можно видеть способность к замещению водорода в спирте на углеводородный радикал, с образованием простого эфира.
4) Образование сложных эфиров (реакция этерификации)
Сложные эфиры можно рассматривать как продукты замещения водородного атома в гидроксильной группе на остаток карбоновой кислоты  , который называется ацил , для муравьиной кислоты
, который называется ацил , для муравьиной кислоты 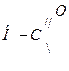 - форнил, для уксусной
- форнил, для уксусной 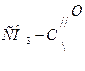 - ацетил, для пропионовой
- ацетил, для пропионовой 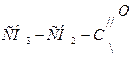 - пропионил.
- пропионил.
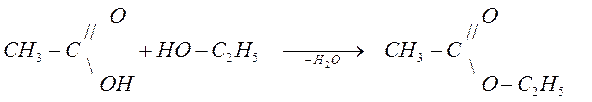
уксусная кислота этиловый спирт уксусноэтиловый эфир
(этилацетат)
Важно запомнить, что выделяющаяся при этерификации молекула воды образуется из гидроксила кислоты и водорода спирта, а не наоборот. Это было установлено методом "меченых атомов": в молекулу спирта был введен изотоп кислорода 18О, который затем был обнаружен в молекуле сложного эфира.





 С2Н5—О— С2Н5
С2Н5—О— С2Н5 , который называется ацил , для муравьиной кислоты
, который называется ацил , для муравьиной кислоты 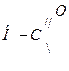 - форнил, для уксусной
- форнил, для уксусной 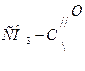 - ацетил, для пропионовой
- ацетил, для пропионовой 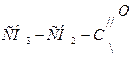 - пропионил.
- пропионил.