

Своеобразие русской архитектуры: Основной материал – дерево – быстрота постройки, но недолговечность и необходимость деления...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Своеобразие русской архитектуры: Основной материал – дерево – быстрота постройки, но недолговечность и необходимость деления...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...
Топ:
Марксистская теория происхождения государства: По мнению Маркса и Энгельса, в основе развития общества, происходящих в нем изменений лежит...
Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов...
Интересное:
Лечение прогрессирующих форм рака: Одним из наиболее важных достижений экспериментальной химиотерапии опухолей, начатой в 60-х и реализованной в 70-х годах, является...
Как мы говорим и как мы слушаем: общение можно сравнить с огромным зонтиком, под которым скрыто все...
Национальное богатство страны и его составляющие: для оценки элементов национального богатства используются...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Введение
Падение промышленного производства в Украине в январе 2012 года по сравнению с декабрем 2011 года составило 12,7%, по сравнению с январем прошлого года отмечен рост на 2%. Об этом информирует Государственная служба статистики Украины.
Так, в январе по сравнению с декабрем прошлого года в добывающей промышленности падение составило 8,4%, к январю 2011-го - рост 3,4%. В обрабатывающей промышленности объемы производства в январе снизились по сравнению с декабрем 2011 года на 17%, к аналогичному периоду прошлого года - рост на 1,2%. Легкая промышленность в январе 2012 года по сравнению с прошлым месяцев показала падение на 23,5%, по отношению к январю прошлого года - падение на 12,1%.
В химической и нефтехимической промышленности в январе отмечено падение производства на 13,9%, по сравнению с январем 2011 года - рост на 1,9%. В металлургии и производстве готовых изделий из металла в январе 2012 года по сравнению с декабрем 2011 года падение составило 1,7%, по сравнению с январем прошлого года - падение на 1,6%. В машиностроении в январе по сравнению с декабрем 2011 года зафиксировано падение на 24,3%, по отношению к январю 2011-го - рост на 11,7.
В Украине многие химические производства загрязняют своими отходами воду. Для того чтобы загрязнение вод было минимальное, производства предусматривают различные очистки сточных вод.[1]
Прогрессивным направлением в технологии очистки природных и сточных вод является применение электрохимических методов, в частности, метода очистки воды в электролизерах с растворимыми электродами, известного в литературе под названием «электрокоагуляция».[2]
Этот метод обеспечивает высокий эффект удаления из воды загрязнений в виде взвесей (минерального, органического и биологического происхождения), коллоидов (соединений железа, веществ, обусловливающих цветность воды и т.д.), а также отдельных веществ, находящихся в молекулярном и ионном состоянии. Существенным преимуществом электрокоагуляции перед реагентными методами очистки воды является возможность отказа от строительства громоздких очистных сооружений, занимающих значительные производственные площади. Электрокоагуляция позволяет осуществлять процесс очистки воды в компактных, автоматически действующих и легко обслуживаемых установках и особенно удобна для небольших автономных объектов (на судах речного флота, в сельском хозяйстве, для малых поселков и т.д.).
|
|
Высокая сорбционная способность электрохимически получаемой гидроокиси алюминия по отношению к загрязнениям воды и ряд других преимуществ метода электрокоагуляции позволяют использовать этот метод для очистки технических, питьевых и сточных вод.
Таким образом, использование сорбционных свойств гидроокисей металлов, получаемых при электролизе, является высокоэффективным, а иногда единственным способом извлечения из воды загрязнений. Вместе с этим возможность осуществления процесса очистки воды в компактных и автоматически действующих установках делают применение метода электрокоагуляции особенно перспективным.
Методы очистки воды
Рассмотрим методы очистки промышленных сточных вод от загрязнений.
Для очистки сточных вод от загрязнений применяют:
механические;
физико-химические;
химические;
биологические методы.
Из механических практическое значение имеют отстаивание, центрифугирование и фильтрование; из физико-механических - флотация, коагуляция, электрокоагуляция и сорбция; из химических - хлорирование и озонирование.
Механическая очистка
Механическую очистку сточных вод от загрязнений применяют преимущественно как предварительную. Механическая очистка обеспечивает удаление взвешенных веществ из бытовых сточных вод на 60-65%, а из некоторых производственных сточных вод на 90-95%. Задачи механической очистки заключаются в подготовке воды к физико-химической и биологической очисткам. Механическая очистка сточных вод является в известной степени самым дешевым методом их очистки, а поэтому всегда целесообразна наиболее глубокая очистка сточных вод механическими методами.[6]
|
|
Механическую очистку проводят для выделения из сточной воды находящихся в ней нерастворенных грубодисперсных примесей путем процеживания, отстаивания и фильтрования.
Для задержания крупных загрязнений и частично взвешенных веществ применяют процеживание воды через различные решетки и сита. Для выделения из сточной воды взвешенных веществ, имеющих большую или меньшую плотность по отношению к плотности воды, используют отстаивание. При этом тяжелые частицы оседают, а легкие всплывают.
Сооружения, в которых при отстаивании сточных вод выпадают тяжелые частицы, называются песколовками.
Сооружения, в которых при отстаивании загрязненных промышленных вод всплывают более легкие частицы, называются в зависимости от всплывающих веществ жироловками, маслоуловителями, нефтеловушками и другие.
Фильтрование применяют для задержания более мелких частиц. В фильтрах для этих целей используют фильтровальные материалы в виде тканей (сеток), слоя зернистого материала или химических материалов, имеющих определенную пористость. При прохождении сточных вод через фильтрующий материал на его поверхности или в поровом пространстве задерживается выделенная из сточной воды взвесь.
Механическую очистку как самостоятельный метод применяют тогда, когда осветленная вода после этого способа очистки может быть использована в технологических процессах производства или спущена в водоемы без нарушения их экологического состояния. Во всех других случаях механическая очистка служит первой ступенью очистки сточных вод.
Песколовки
Песколовки предназначены для выделения механических примесей с размером частиц 200-250 мкм. Необходимость предварительного выделения механических примесей (песка, окалины и др.) обуславливается тем, что при отсутствии песколовок эти примеси выделяются в других очистных сооружениях и тем самым усложняют эксплуатацию последних.
|
|
Принцип действия песколовки основан на изменении скорости движения твердых тяжелых частиц в потоке жидкости.
Песколовки делятся на горизонтальные, в которых жидкость движется в горизонтальном направлении, с прямолинейным или круговым движением воды, вертикальные, в которых жидкость движется вертикально вверх, и песколовки с винтовым (поступательно-вращательным) движением воды. Последние в зависимости от способа создания винтового движения разделяются на тангенциальные и аэрируемые.
Самые простейшие горизонтальные песколовки представляют собой резервуары с треугольным или трапециидальным поперечным сечением. Глубина песколовок 0,25-1 м. Скорость движения воды в них не превышает 0,3 м/с. Песколовки с круговым движением воды изготавливаются в виде круглого резервуара конической формы с периферийным лотком для протекания сточной воды. Осадок собирается в коническом днище, откуда его направляют на переработку или отвал. Применяются при расходах до 7000 м3/сут. Вертикальные песколовки имеют прямоугольную или круглую форму, в них сточные воды движутся с вертикальным восходящим потоком со скоростью 0,05 м/с.
Конструкцию песколовки выбирают в зависимости от количества сточных вод, концентрации взвешенных веществ. Наиболее часто используют горизонтальные песколовки. Из опыта работы нефтебаз следует, что горизонтальные песколовки необходимо очищать не реже одного раза в 2-3 суток. При очистке песколовок обычно применяют переносный или стационарный гидроэлеватор.
Отстойники
Отстаивание - наиболее простой и часто применяемый способ выделения из сточных вод грубо дисперсных примесей, которые под действием гравитационной силы оседают на дне отстойника или всплывают на его поверхности.
Гидроциклоны
Осаждение взвешенных частиц под действием центробежной силы проводят в гидроциклонах и центрифугах.
Для очистки сточных вод используют напорные и открытые (безнапорные) гидроциклоны.
При вращении жидкости в гидроциклонах на частицы действуют центробежные силы, отбрасывающие тяжелые частицы к периферии потока, силы сопротивления движущегося потока, гравитационные силы и силы инерции. Силы инерции, незначительны и ими можно пренебречь. При высоких скоростях вращения центробежные силы значительно больше сил тяжести.
|
|
Напорные гидроциклоны
В напорные гидроциклоны вода подается через тангенциально направленный патрубок в цилиндрическую часть. В гидроциклоне вода, двигаясь по винтовой спирали наружной стенки аппарата, направляется в коническую его часть. Здесь основной поток изменяет направление движения и перемещается к центральной части аппарата. Поток осветленной воды в центральной части аппарата по трубе выводится из гидроциклона, а тяжелые примеси вдоль конической части перемещаются вниз и выводятся через патрубок шлама.
Промышленность выпускает напорные гидроциклоны нескольких типоразмеров. Для грубой очистки применяют гидроциклоны больших диаметров. Эффективность гидроциклонов находится на уровне 70%.
Безнапорные гидроциклоны
Одним из технических приспособлений для сбора нефтяной пленки с поверхности воды является безнапорный гидроциклон.
Если в предыдущих конструкциях для вращения жидкости в гидроциклоне применяли подачу воды в гидроциклон по патрубку, расположенному по касательной в цилиндрической части, то в данном случае проводят отсос воды из гидроциклона по патрубку, расположенному по касательной внизу конической части гидроциклона. Такое расположение патрубка дает возможность образовывать внутри гидроциклона вращение жидкости, причем поступление воды из водоема происходит в верхней части гидроциклона.
Собранная с поверхности воды пленка нефтепродуктов, попадая в гидроциклон как более легкая, собирается в центре гидроциклона. По мере увеличения количества нефтепродуктов в гидроциклоне внутри него образуется конус из нефтепродуктов, который, увеличиваясь в размере, достигает нефтяного отборного патрубка, расположенного в центре гидроциклона. Нефтепродукты по этому патрубку сбрасываются в специальные емкости на берегу водоема.
Центрифуги
Для удаления осадков из сточных вод могут быть использованы фильтрующие или отстойные центрифуги.
Центробежное фильтрование достигается вращением суспензии в перфорированном барабане, обтянутом сеткой или фильтровальной тканью. Осадок остается на стенках барабана. Его удаляют вручную или ножевым съемом. Такое фильтрование наиболее эффективно, когда надо получать продукт наименьшей влажностью и требуется промывка осадка.
Центрифуги могут быть периодического или непрерывного действия; горизонтальными, вертикальными или наклонными; различаются по расположению вала в пространстве; по способу выгрузки осадка из ротора (с ручной, с ножевой, поршневой или центробежной выгрузкой). Они могут быть в герметизированном и негерметизированном исполнении.
|
|
Фильтры
Метод фильтрования приобретает все большее значение в связи с повышением требований к качеству очищенной воды. Фильтрование применяют после очистки сточных вод в отстойниках или после биологической очистки. Процесс основан на прилипании грубодисперсных частиц нефти и нефтепродуктов к поверхности фильтрующего материала. Фильтры по виду фильтрующей среды делятся на тканевые или сетчатые, каркасные или намывные, зернистые или мембранные.
Фильтрование через различные сетки и ткани обычно применяют для удаления грубо дисперсных частиц. Более глубокую очистку нефтесодержащей воды можно осуществлять на каркасных фильтрах. Пленочные фильтры очищают воду на молекулярном уровне.
Микрофильтры
Микрофильтры представляют собой фильтровальные аппараты, в качестве фильтрующего элемента использующие металлические сетки, ткани и полимерные материалы. Микрофильтры обычно выпускают в виде вращающихся барабанов, на которых неподвижно закреплены или прижаты к барабану фильтрующие материалы. Барабаны выпускают диаметром 1,5-3 м и устанавливают горизонтально. Очищаемая вода поступает внутрь барабана и фильтруется через фильтр наружу. Микрофильтры широко используют для осветления природных вод.
В промышленности применяют микрофильтры различных конструкций. Процесс фильтрации происходит только за счет разности уровней воды внутри и снаружи барабана. Полотно сетки не закреплено, а лишь охватывает барабан в виде бесконечной ленты, натягиваемой с помощью натяжных роликов.
Микросетки изготовляют из различных материалов: капрона, латуни, никеля, нержавеющей стали, фосфористой бронзы, нейлона и др.
Физико-химическая очистка
К физико-химическим методам очистки сточных вод от нефтепродуктов относят коагуляцию, электрокоагуляцию, флотацию и сорбцию.
Коагуляция
Это процесс укрупнения дисперсных частиц в результате их взаимодействия и объединения в агрегаты. В очистке вод ее применяют для ускорения процесса осаждения тонкодисперсных примесей и эмульгированных веществ. Коагуляция наиболее эффективна для удаления из воды коллоидно-дисперсных частиц, то есть частиц размером 1-100 мкм. Коагуляция может происходить самопроизвольно или под влиянием химических и физических процессов. В процессах очистки сточных вод коагуляция происходит под влиянием добавляемых к ним специальных веществ - коагулянтов. Коагулянты в воде образуют хлопья гидроксидов металлов, которые быстро оседают под действием силы тяжести. Хлопья обладают способностью улавливать коллоидные и взвешенные частицы и агрегировать их. Так как коллоидные частицы имеют слабый отрицательный заряд, а хлопья коагулянтов слабый положительный заряд, то между ними возникает взаимное притяжение.[7]
Электрокоагуляция
Метод электрокоагуляции основан на физико-химическом процессе оседания (коагуляции) коллоидных систем при воздействии на них постоянным электрическим током. С помощью стальных или алюминиевых анодов сточные воды подвергаются электролизу, в результате чего происходит электрохимическое растворение металлов, загрязняющих воду. Окислительно-восстановительные реакции, протекающие в водной среде, при очистке воды для дома электрохимическими методами многоступенчаты и довольно сложны. Целый ряд факторов оказывает влияние на скорость и механизмы протекания определенных химических реакций в общей цепи, от чего во многом зависит и качество очистки воды методом электрокоагуляции.[8]
Так при очистке воды электрокоагуляцией решающее значение имеет не только материал анодов, но и расстояние между ними. Для получения очищенной жидкости, с определенными показателями качества, исходя из химического состава сточных вод, подвергающихся электрокоагуляции, учитывают такие факторы, как скорость движения воды между анодами, температура водной среды, а также плотность и напряжение постоянного тока.
Как уже отмечалось выше, очищение жидкости методом электрокоагуляции преимущественно используется в промышленном производстве. Сам прибор для проведения данного способа, как правило, представляет собой ванну, в которой установлены электроды. Чаще всего используют пластинчатые электрокоагуляторы с параллельным или вертикальным током воды. Существуют однопоточные системы водоочистки и водоподготовки, в которых вода движется последовательно от электрода к электроду, многопоточные с параллельным соединением каналов (в них вода проходит одновременно через все электроды) и смешанные. Преимуществом однопоточных агрегатов является большая скорость тока воды, однако, использование многопоточных установок позволяет снизить пассивацию электродов, т.е. замедление электродной реакции из-за воздействия собственных ее продуктов. Подобный метод отлично зарекомендовал себя при обработке водной среды, насыщенной эмульсиями нефтепродуктов, жиров и масел, степень удаления которых из сточных вод методом коагуляции составляет 92-99 % и 54-68 % соответственно.
Метод очистки воды электрокоагуляцией обладает как преимуществами, так и рядом недостатков. К достоинствам можно отнести компактность установки и простота управления. При этом отсутствует такая статья расходов, как реагенты. Еще одним положительным качеством установки для проведения электрокоагуляции сточных вод является ее независимость к резким изменениям таких показателей, как температура, уровень кислотно-щелочного баланса среды, появление токсичных элементов.[9]
К тому же подобный процесс обладает высокой бактерицидной эффективностью. Постоянный электрический ток большой плотности разрушает химические соединения и выделением ионов кислорода, который является одним из мощных средств обеззараживания.
Среди недостатков метода водоочистки способом электрокоагуляции сточит отметить энерго- и металлоемкость процесса, относительно невысокую производительность, образование большого объема шлама (хотя вторичные отходы зачастую имею хорошие структурно-механические свойства), нередки случаи, когда в процессе коагуляции образуются токсичные реагенты.
Специалисты не рекомендуются осуществлять очистку воды электрокоагуляцией для бытовых нужд по ряду причин, основной из которых заключается в том, что результат воздействия постоянного электрического тока на воду непредсказуем. В процессе в водной среде могут образоваться вещества, опасные для здоровья живых организмов. Безопасность полученной после очистки воды с точки зрения химического состава может показать только анализ, который проводить в бытовых условиях, увы, невозможно.
Электрокоагуляция применяется во многих технологиях очистки воды: обесцвечивание и осветление воды, удаление из воды водорослей, обескислороживание воды, десеребрение воды и самое главное очистка сточных вод. Рассмотрим эти технологии.
Определение хлоридов
Общие сведения. Хлориды в воде источников водоснабжения могут быть косвенными показателями загрязнения воды органическими веществами животного происхождения. В данном случае имеет значение не только концентрация хлоридов, сколько ее изменения на протяжении водоисточника и во времени.[20]
Большие концентрации хлоридов могут наблюдаться в колодезной воде в местах солончаковой почвы. У такой воды солоноватый привкус. Содержание хлоридов в ней не должно превышать 350 мг/л.
Качественная реакция. 5 мл исследуемой воды наливают в пробирку и подкисляют 2-4 каплями азотной кислоты, которая исключает из реакции карбонаты и фосфаты. Затем прибавляют 3 капли 10% раствора нитрата серебра (азотнокислое серебро) и определяют степень помутнения воды. Если образуется слабая белая муть, то в исследуемой воде около 1-10 мг/л хлор-ионов, при сильной мути- 10-15 мг/л; если медленно осаждается хлопья, то в воде 50-100 мг/л хлор-ионов; при образовании белого творожистого осадка хлор-ионов более 100 мг/л.
Количественное определение. Принцип метода (по Мору) основан на осаждении хлора натратом серебра в присутствии хромовокислого калия в качестве индикатора.
При титровании хлора нитратом осадок выпадает вначале в хлористое серебро. После связывания всего хлора нитратом серебра вступает в реакцию с хромовокислым калием, в результате чего образуется хромовокислое серебро шоколадно-красного цвета, а окраска титруемой жидкости переходит из зеленоватой в оранжево-желтую.
Реакция проходит следующим образом:
+ AgNO3 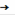
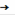 AgCl + NaNO3 (осадок белого цвета), (12)
AgCl + NaNO3 (осадок белого цвета), (12)
AgNO3 + K2CrO4 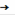
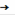 AgCrO4 + 2KNO3 (красно-бурый осадок) (13)
AgCrO4 + 2KNO3 (красно-бурый осадок) (13)
Посуда и реактивы. 1. Титрованный раствор хлорида натрия (1 мл которого содержит 1 мг хлора) готовят, растворяя 1,649 г х.ч., высушенного при 105оС хлорида натрия в 1 л дистиллированной воды. 2. Титрованный раствор нитрата серебра (1 мл которого может осадить 1 мг хлора) готовят, растворяя 4,80 г нитрата серебра в 1 л дистиллированной воды, и хранят в склянке из темного стекла. 3. Нитрат серебра, 10% раствора. 4. Азотная кислота. 5. Раствор хромовокислого калия растворяют 50 г нейтрального калия хромата в небольшом количестве дистиллированной воды, прибавляют нитрат серебра до образования легкого красного осадка. Через 1-2 дня фильтруют и разбавляют фильтрат до 1 л дистиллированной водой. 6. Колба вместимостью 1 л. 7. Колба коническая вместимостью 250 мл.
Установка титра нитрата серебра. В коническую колбу вносят бюреткой или пипеткой 10 мл хлорида натрия и 90 мл дистиллированной воды, прибавляют 1 мл раствора хромовокислого калия и титруют по каплям раствором азотнокислого серебра до перехода зеленоватой окраски мутного раствора в оранжево-желтую, не исчезающую при перемешивании в течение 15-20 с.
Для получения более точного результата к оттитрованному раствору прибавляют 1-2 капли раствора хлорида натрия до исчезновения красноватого оттенка и эту пробу используют как цветной стандарт при повторном определении. Новую порцию хлорида-натрия аналогично титруют нитратом серебра до получения незначительной разницы оттенков (оранжевого в титруемом растворе и зеленоватого в стандарте).
По результатам трех титрований рассчитывают поправочный коэффициент к титру нитрата серебра:
k = 30/ (n1 + n2 + n3) (3)
где n1, n2, n3- количество нитрата серебра, пошедшего на каждое из трех титрований.
Подготовка пробы. На результаты титрования могут оказывать влияние цветные воды, активная реакция (рН), присутствие большого количества органических веществ, сероводорода и др.
Если цветность воды превышает 30о, то ее следует прокипятить с перекисью водорода (на 100 мл воды 2 мл перекиси) в течение 10 мин или коагулировать добавлением сернокислого алюминия и затем профильтровать. Активная реакция исследуемой воды должна быть в пределах 6-10. Если вода резко кислая или резко щелочная, то ее следует нейтрализовать по фенолфталеину 0,1 N раствором серной кислоты при щелочной реакции или 0,1 N раствором едкого натра при кислой.
Нейтрализацию кислых вод ведут до появления слабо-розовой окраски, которую перед определением хлора устраняют продувкой воздуха или взбалтыванием воды.
Сероводород удаляют кипячением воды с перекисью водорода.
При окисляемости выше 15 мг на 1 л О2 органические вещества разрушаются кипячением 100 мл воды с кристалликом перманганата калия. При избытке перманганата калия раствор при кипячении не обесцвечивается и сохраняется розовая окраска. Избыток перманганата калия разрушается в результате прибавления нескольких капель этилового спирта. Затем воду отфильтровывают от образовавшихся хлопьев перекиси марганца, охлаждают и доводят дистиллированной водой до 100 мл.
Методика определения. В две конические колбы вместимостью 250 мл пипеткой вносят по 100 мл исследуемой воды (при большом содержании хлоридов берут по 10-50 мл и доводят до 100 мл дистиллированной водой). Прибавляют по 1 мл раствора хромата калия и одну пробу титруют из бюретки со стеклянным краном раствором нитрата серебра до появления не исчезающей в течении 15-20 с слабо-розовой окраски. Вторую пробу используют как цветной стандарт.
Содержание хлоридов Х (миллиграммы хлор-иона на 1 л воды) рассчитывают по формуле:
Х = а ∙ k ∙ 1000/V (4)
где а - количество раствора нитрата серебра, пошедшее на титрование, мл; k-поправочный коэффициент к титру нитрата серебра; V- объем воды, взятый для определения, мл.
Определение окисляемости
Общие сведения. Определение органических веществ в воде представляет большую трудность, поэтому разработан косвенный метод, при котором о содержании органических веществ судят по окисляемости. Она выражается показателем количества кислорода, в миллиграммах расходуемого на окисление органических веществ в 1л воды. Определение окисляемости перманганатным методом основано на способности перманганата калия при кипячении в присутствии серной кислоты, окислять органические вещества и переходить при этом в сульфат марганца:
2KMnO4 + H2SO4 
 K2SO4 + 3H2O + 5O + 2MnSO4 (14)
K2SO4 + 3H2O + 5O + 2MnSO4 (14)
Избыток внесенного в воду перманганата калия восстанавливается щавелевой кислотой:
2KMnO4 + 5H2C2O4 + 3H2SO4 
 K2SO4 + 2MnSO4 + 10CO2 + 8H2O (15)
K2SO4 + 2MnSO4 + 10CO2 + 8H2O (15)
Избыток прибавляемой щавелевой кислоты оттитровывают раствором перманганата калия. Результаты выражают в миллиграммах на 1 л кислорода (мг/л О2).[21]
Реактивы. 1. 0,01 N раствор перманганата калия. Растворяют 0,316 г KMnO4 в 1 л дистиллированной воды. 1 мл такого раствора соответствует 0,08 мг кислорода.
Раствор надо хранить в темной склянке с притертой пробкой и проверять титр по щавелевой кислоте при каждой серии исследований.
. 0,01 N раствор щавелевой кислоты. Раствор 0,63 г H2C2O4 в 1 л дистиллированной воды. 1 мл раствора требует для своего окисления 0,02 мг О2.
. 25% H2SO4получают разбавлением 1 части (относительная плотность 1,84) в 3 частях дистиллированной воды (1:3).
Ход анализа. К 100 мл исследуемой воды прибавляют 5 мл разбавленной (1:3) серной кислоты. Для равномерного кипения желательно также прибавить несколько кусочков пемзы или стеклянных капилляров. Потом прибавляют 10 мл 0,01 N раствора перманганата калия и нагревают сначала на сильном огне до кипения и кипятят ровно 10 мин на слабом огне. Затем к раствору прибавляют 10 мл 0,01 N раствора щавелевой кислоты и титруют 0,01 N раствором перманганата калия до бледно-розового окрашивания. После этого прибавляют 10 мл 0,01 N раствора щавелевой кислоты и титруют 0,01 N раствором перманганата калия для определения поправки (к) последнего.
Окисляемость Х (мг/л О2) вычисляют по формуле:
Х = [(V1 + V2) ∙ k - 10] ∙ 0,08 ∙ 1000/V (5)
где V1- количество KMnO4, прибавленное до начала кипения (10 мл); V2 - количество KMnO4, израсходованное на обратное титрование; k- поправочный коэффициент в титру 0,01 N KMnO4; 10- количество мл прибавленной щавелевой кислоты; 0,08- количество миллиграммов О2 выделяемое в реакции 1 мл 0,01 N раствором KMnO4; 1000- пересчет на 1л; V- количество воды, взятое на исследование (100мл).
Если k = 1, то формула будет иметь следующий вид:
Х = V2 ∙ 0,08 ∙10 (6)
Определение мутности в воде
Общие сведения. Мутность воды вызвана присутствием тонкодисперсных взвесей органического и неорганического происхождения. Мутность воды может быть вызвана самыми разнообразными причинами - присутствием карбонатов, гидроксидов алюминия, высокомолекулярных органических примесей гумусового происхождения, появлением фито- и изопланктона, а также окислением соединений железа и марганца кислородом воздуха. Высокая мутность является признаком наличия в воде неких примесей, возможно токсичных, кроме того, в мутной воде лучше развиваются различные микроорганизмы.[22]
Мутность определяют фотометрически (турбидиметрически - по ослаблению проходящего света или нефелометрически - по светорассеянию в отраженном свете), а также визуально - по степени мутности столба высотой 10-12 см в мутномерной пробирке. В последнем случае пробу описывают качественно следующим образом: прозрачная; слабо опалесцирующая; опалесцирующая; слабо мутная; мутная; очень мутная (ГОСТ 1030). Указанный метод мы и приводим далее в качестве наиболее простого в полевых условиях.
Метод качественного определения мутности
Оборудование: пробирка стеклянная высотой 10-12 см, лист темной бумаги (в качестве фона).
Выполнение анализа:
Таблица 1
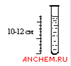
| 1. Заполните пробирку водой до высоты 10-12 см. |
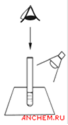
| 2. Определите мутность воды, рассматривая пробирку сверху на темном фоне при достаточном боковом освещении (дневном, искусственном). Выберите подходящее из приведенных в табл.1. Таблица 1 Мутность воды Мутность не заметна (отсутствует) Слабо опалесцирующая Опалесцирующая Слабо мутная Мутная Очень мутная |
Фотометрический метод определения мутности
Определение мутности производят не позднее, чем через 24 ч после отбора пробы. Мутность воды определяют фотометрическим путем сравнения проб исследуемой воды со стандартными суспензиями.
Для проведения испытаний применяют фотоэлектроколориметр марок ФЭК-57, ФЭК-60 с зеленым светофильтром (X - 530 нм), кюветы с толщиной поглощающего свет слоя 5 - 10 см.
Стандартные суспензии изготавливают из каолина (глина). Для этого каолин просеивают через шелковое сито с диаметром отверстий 0,1 мм, хорошо взбалтывают с 3 - 4 л дистиллированной воды и оставляют стоять 24 ч. Через 24 ч сифоном, не взмучивая, осадка, отбирают среднюю неосветлившуюся часть жидкости. К оставшейся части вновь приливают воду, сильно взбалтывают, снова оставляют в покое на 24 ч и вновь отбирают среднюю неосветлившуюся часть. Так повторяют до тех пор, пока не накопится достаточное количество суспензии с неосаждающейся мутью в течение 3 суток. Затем удаляют жидкость над осадком, как содержащую слишком мелкие частицы.
Из полученного осадка готовят стандартную суспензию так, чтобы в 1 л ее содержалось 100 мг взвеси каолина.
Для проверки концентрации отбирают 250 мл суспензии, фильтруют через промытый беззольный фильтр, осадок промывают, высушивают и прокаливают до постоянной массы. Затем готовят эталонную шкалу, для чего приготовленную рабочую стандартную суспензию мутности взбалтывают и точно отмеренное ее количество разбавляют дистиллированной водой с нулевой мутностью.
Готовят следующие рабочие стандартные суспензии: 0; 0,2; 0,3; 0,4; 0,5; 1,0; 1,5; 2,0; 5,0 мг/дм3. Для приготовления стандартных суспензий можно использовать порошок трепела (SiO2), не содержащий железа.
Определение прозрачности
Общие сведения. Прозрачность воды является важным признаком ее доброкачественности. Прозрачность зависит от содержания в воде механических взвешенных веществ (мути), химических примесей, солей железа. Цветение водоемов ведет также к понижению прозрачности воды. Питьевая вода должна быть прозрачной. Мутная, непрозрачная вода неэстетична и всегда подозрительна в эпидемическом отношении, так как в мутной воде создаются оптимальные условия для размножения микроорганизмов.[22]
Ход определения. Определение прозрачности производят на месте отбора проб воды. Исследуемую воду после взбалтывания наливают в цилиндр Снеллена, отградуированный по высоте в сантиметрах, с прозрачным плоским дном и имеющий у своего основания тубус для выпуска воды, на который надета резиновая трубка с зажимом. Цилиндр ставят на расстоянии 4 см от дна до печатного шрифта Снеллена № 1, смотрят сверху вниз через столб воды, выпускают через нижнюю трубку воду, пока не будет отчетливо виден шрифт. Высота этого столба воды в сантиметрах определяет степень прозрачности воды. Минимально допустимая прозрачность питьевой воды - не менее 30 см по шрифту Снеллена. Вода с прозрачностью от 20 до 30 см - слабо мутная, от 10 до 20 см - мутная, до 10 см - очень мутная.
Измерение рН воды
Общие сведения. Измерения рН относятся к наиболее распространенным измерениям в химии. Правильные названия для рН - водородный показатель, показатель кислотности, «пэ-аш».
В настоящее время основным методом измерения рН является использование специального прибора - рН-метра. Принцип действия такого прибора потенциометрический, то есть измеряемой величиной является напряжение между двумя электродами, опущенными в раствор. Обычно напряжение между такими электродами изменяется на десятки и сотни милливольт. Таким образом, рН - метр представляет собою милливольтметр. Особенностью такого милливольтметра является очень маленький входной ток, так что он может измерять напряжение с самых разных электродов, в том числе стеклянных, через который большой ток не проходит. Кроме того, у рН-метра имеется система пересчета напряжения в рН (а в более совершенных моделях и в некоторые другие величины, например в градусы Тернера для кислотности молока).[24]
Прибор для измерения рН состоит из двух основных элементов - измерительного прибора, шкала которого градуирована в единицах рН, с устройством для автоматической компенсации температуры и устройством для настройки и калибровки прибора по буферным растворам; а также штатива с укрепленными электродами.
Принцип работы. Прибор включают в сеть и прогревают не менее 30 мин. Перед проведением испытаний осуществляют проверку прибора по стандартным буферным растворам с рН 3,57; 4,00; 5,00; 6,88; 9,22 при температуре 20°С по прилагаемым к приборам инструкциям. После проверки электроды тщательно промывают дистиллированной водой <http://www.znaytovar.ru/new832.html>.
Затем концы электродов погружают в предварительно подготовленный испытуемый раствор, и после того, как показания прибора примут установившееся значение, отсчитывают величину рН по шкале прибора. После каждого измерения электроды тщательно промывают дистиллированной водой. Прибор измерения рН указан на рисунке 4.

Рис. 4 - рН- метр-миливолтметр рН - 121: 1 - чувствительный элемент; 2 - измерительный электрод; 3 - внутренний контактный электрод; 4 - вспомогательный электрод; 5 - хлорсеребряный электрод; 6 - электролитический ключ; 7 - рН-метр-миливолтметр
Экспериментальная часть
Очистка сточных вод методом электрокоагуляции, обеспечивает высокий эффект удаления из воды разных видов загрязнений.
При проведении очистки сточных вод, основным оборудованием был выбран электролизер рис. 5.

Рис. 5 - Безнапорный пластинчатый электролизер горизонтального типа
Представляющий собой пластинчатый безнапорный электролизер горизонтального типа. Пластины метала, расположены вертикально на расстоянии 3-20 мм одна от другой и удерживаются изолирующими вставками, электрический ток подводится к каждой пластине. Для очистки сточных вод был выбран железный анод вместо алюминиевого, который в большинстве случаев применяются для подготовки питьевой воды.
Эксперимент проводили на установке, изображенной на рис. 6, которая состоит из насоса для перекачки воды, электролизера, снабженным двумя активными электродами и одним пассивным, который расположен в межкатодном пространстве. За счет возникновения потенциала, который возникает между активными электродами, пассивный электрод также растворяется с выделением гидроокиси, что в свою очередь приводит к более полной очистке загрязненной воды. С электролизера вода с осажденными примесями электрокоагулянта поступает на фильтр, который представляет собой резервуар, заполненный фильтрующим элементом, минеральной ватой. Очищенная таким образом вода использовалась для дальнейших исследований на качество воды. Скорость движения воды в электрокоагуляторе регулировалась скоростью вращения насоса с помощью латера.
Исследования показали, что очищенная таким способом вода, имеет достаточно глубокую очистку, при этом удельный расход электроэнергии составляет 0,08-0,5 кВт∙час/м3.
Расход электроэнергии на обработку единицы объема воды при постоянной плотности тока и повышении температуры воды от 2 до 80оС значительно уменьшается. Например, при плотности тока 2 ма/см2 и температуре воды 2оС расход электроэнергии составляет 4 вт-ч/ м3, а при 80оС уменьшается в 3 раза.
Зависимость расхода электроэнергии от температуры воды приведена в таблице 2.
Таблица 2 - Зависимость расхода электроэнергии от температуры воды
| Наименование показателей | Единица измерения | Температура воды, оС | ||||||||
| 2 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | ||
| Напряжение | в | 4,5 | ||||||||
|
|
|
|||||||||

Архитектура электронного правительства: Единая архитектура – это методологический подход при создании системы управления государства, который строится...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Индивидуальные очистные сооружения: К классу индивидуальных очистных сооружений относят сооружения, пропускная способность которых...

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!