

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Типы оградительных сооружений в морском порту: По расположению оградительных сооружений в плане различают волноломы, обе оконечности...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Типы оградительных сооружений в морском порту: По расположению оградительных сооружений в плане различают волноломы, обе оконечности...
Топ:
Марксистская теория происхождения государства: По мнению Маркса и Энгельса, в основе развития общества, происходящих в нем изменений лежит...
Отражение на счетах бухгалтерского учета процесса приобретения: Процесс заготовления представляет систему экономических событий, включающих приобретение организацией у поставщиков сырья...
Характеристика АТП и сварочно-жестяницкого участка: Транспорт в настоящее время является одной из важнейших отраслей народного хозяйства...
Интересное:
Уполаживание и террасирование склонов: Если глубина оврага более 5 м необходимо устройство берм. Варианты использования оврагов для градостроительных целей...
Финансовый рынок и его значение в управлении денежными потоками на современном этапе: любому предприятию для расширения производства и увеличения прибыли нужны...
Средства для ингаляционного наркоза: Наркоз наступает в результате вдыхания (ингаляции) средств, которое осуществляют или с помощью маски...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Что собой представляет электромагнитная волна, легко представить на следующем примере. Если на водную гладь бросить предмет, то на поверхности образуются расходящиеся кругами волны. Они движутся от источника их возникновения (возмущения) с определенной скоростью распространения. Для электромагнитных волн возмущениями являются передвигающиеся в пространстве электрические и магнитные поля. Меняющееся во времени электромагнитное поле обязательно вызывает появление переменного магнитного поля, и наоборот. Эти поля взаимно связаны.
АТОМ БОРА
Весь последующий период развития квантовой науки неразрывно связан с именем еще одного из «младших отцов‑основателей нового взгляда на материю» – Нильса Бора (1885–1962). Этот знаменитый датский ученый начал свою научную карьеру в святом для каждого физика месте – Кавендишской лаборатории Кембриджского университета. Именно здесь молодой ученый приступил под руководством самого сэра Резерфорда к построению новых моделей атомных структур. В этот период на небосводе науки засверкал первый более‑менее достоверный планетарный атом Резерфорда. Эта модель своей наглядностью, простотой и глубоким смыслом (Вселенная в атоме!) еще долго привлекала внимание публики, до сих пор (!) встречаясь в некоторых неудачных учебниках и научных популяризациях. Почему неудачных?
Дело в том, что, вращаясь с центростремительным ускорением вокруг атомного ядра, электрон по законам электродинамики должен мгновенно излучить энергию и упасть. Разрешить эту проблему и направить физиков по верному пути понимания атомной структуры удалось молодому датскому теоретику Нильсу Бору, прибывшему на стажировку в Англию после защиты докторской диссертации у себя на родине. За отправную точку Бор принял новые постулаты квантовой механики, согласно которым на субатомном уровне энергия испускается исключительно квантовыми порциями.
|
|
Согласно хрестоматийным постулатам Бора, электрон не излучает энергию, находясь на неких «стационарных» орбитах. При этом сам акт излучения кванта электромагнитной энергии сопоставляется с переходом: «высокая» орбита – «низкая» орбита.
Объяснить странные правила поведения электронов внутри атома Бор в то время не мог, но он уже тогда высказал догадку, что эти отдельные, дискретные орбиты как‑то связаны с еще науке неизвестными квантовыми закономерностями движения. Предположения Бора основывались на том, что именно своеобразие квантового движения выделяет отдельные орбиты из всей возможной их совокупности.
Все это уже серьезно расходилось с планетарной аналогией, ведь по законам классической механики орбиты электронов должны были бы быть совсем иными. Получалось, что именно особенности квантового движения внутри атома проявлялись в наличии лишь некоторых избранных состояний трансдислокации электронов.
Впоследствии, после завершения основных этапов развития квантовой науки, выяснилось, что атомные постулаты Бора об устойчивых орбитах на самом деле органически вытекают из нее, как некое приближенное правило. При этом существует орбита с наименьшей из возможных энергий, на которой электрон может находиться неограниченное время. Говоря научным языком, Бор показал, что электрон не может находиться на произвольном удалении от атомного ядра, а может быть лишь на ряде фиксированных орбит, получивших название «разрешенные орбиты». Электроны, находящиеся на таких орбитах, не могут излучать электромагнитные волны произвольной интенсивности и частоты, иначе им, скорее всего, пришлось бы перейти на более низкую, неразрешенную орбиту. Поэтому они и удерживаются на своей более высокой орбите, подобно самолету в аэропорту отправления, когда аэропорт назначения закрыт по причине нелетной погоды.
|
|
Однако электроны могут переходить на другую разрешенную орбиту. Как и большинство явлений в мире квантовой механики, этот процесс не так просто представить наглядно. Электрон просто исчезает с одной орбиты и материализуется на другой, не пересекая пространства между ними. Этот эффект назвали «квантовым прыжком» или «квантовым скачком». Боровские правила квантования атомных орбит объяснили не только удивительную стабильность окружающих нас атомов, но и тот удивительный факт, что атомы испускают свет строго определенных частот. Данные частоты Бор выразил через величины зарядов ядра и электрона, их массы и постоянную Планка. Таким образом, загадочные по своему смыслу правила квантования Бора стали описывать все главнейшие свойства атомов.
Следующим этапом торжества квантовой физики стал анализ природы света, а более широко – электромагнитного излучения, которое, как оказалось состоит из квантов – фотонов. Для создания современной картины мира важным событием оказалось то, что (это было показано экспериментально) рассеяние света свободными электронами происходит по законам упругого столкновения двух частиц. Так были выявлены корпускулярные свойства света и экспериментально доказано, что наряду с волновыми свойствами свет как бы состоит из частиц. В этом проявляется двойственность (дуализм) света, его корпускулярно‑волновая природа. Возникло логическое противоречие: для объяснения одних явлений надо было считать, что свет имеет волновую природу, для объяснения других – корпускулярную. Разрешение этого противоречия и привело к созданию физических основ квантовой механики.
Когда Джон Дальтон впервые в истории современной науки предложил атомную теорию строения вещества, атомы представлялись ему неделимыми, наподобие микроскопических бильярдных шаров. Однако на протяжении всего девятнадцатого столетия становилось всё очевиднее, что такая модель неприемлема. Поворотной точкой здесь стали открытия выдающихся английских физиков‑экспериментаторов Джозефа Джона Томсона и Ричарда Резерфорда. После опытов этих ученых стало совершенно ясно, что атом не просто делим, но что он еще и обладает сложной структурой: состоит из массивного положительно заряженного центрального ядра и движущихся вокруг него легких отрицательно заряженных электронов. Тут же возникла новая проблема – составной атом не был устойчив и должен был мгновенно распадаться.
|
|
Противоречие снял Бор, применив квантовую теорию к состоянию электронов на атомных орбитах.
Если электрон перескакивает на более низкую орбиту, он теряет энергию и, соответственно, испускает квант света – фотон определенной энергии с фиксированной длиной волны. На глаз мы различаем фотоны разных энергий по цвету, так, раскаленный металл имеет желтовато‑белый цвет, вольфрамовая проволочка в электрической лампочке – желтый, угли костра – насыщенно‑красный, всеми цветами радуги светятся различные инертные газы в лампах неоновой рекламы. А для перехода на более высокую орбиту электрон должен, соответственно, поглотить фотон.
В картине атома по Бору, таким образом, электроны переходят вниз и вверх по орбитам дискретными скачками – с одной разрешенной орбиты на другую, подобно тому, как мы поднимаемся и спускаемся по ступеням лестницы. Каждый скачок обязательно сопровождается испусканием или поглощением кванта энергии электромагнитного излучения – фотона.
Сейчас специалисты в области атомных спектров довольно легко рассчитывают характеристики этих волн и интерпретируют их для объяснения свойств самых сложных по структуре атомов. Однако первые шаги в данном направлении сделал именно Бор в далеком 1913 году, обрисовав в озарении практически все основные черты современной квантовой механики атомной физики.
Следующий судьбоносный шаг в новой науке сделал в 1924 году выдающийся французский физик, впоследствии нобелевский лауреат Луи де Бройль. Де Бройль долго раздумывал над объяснением атомных постулатов Бора и о принципах квантования атомных орбит. В итоге своих размышлений он выдвинул гипотезу о всеобщности корпускулярно‑волнового дуализма. Согласно этой гипотезе, каждой частице, независимо от ее природы, надо поставить в соответствие волну, длина которой связана с импульсом частицы. То есть не только фотоны, но и все «обыкновенные частицы» (электроны, протоны и др.) обладают волновыми свойствами, которые, в частности, должны проявляться в дифракции частиц.
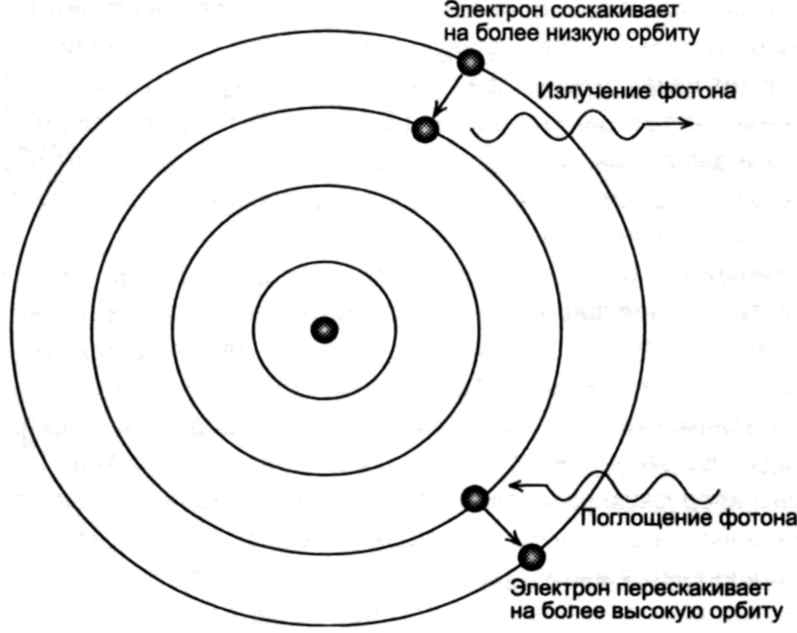
Модель атома Бора
С планетарной моделью атома возникли принципиальные проблемы. Прежде всего, согласно физическим законам, такой атом не мог бы просуществовать дольше доли мгновения. В соответствии с законами механики, электрон, находящийся на орбите, движется с ускорением. Следовательно, он должен излучать электромагнитную энергию и вскоре упасть на ядро. Противоречия классической модели решил Бор, в его формальной модели атома электрон движется по стационарным орбитам не излучая; излучением кванта электромагнитного поля сопровождается его переход на более низкую орбиту, а поглощением того же фотона – скачок на более высокий уровень.

|
|
|

Своеобразие русской архитектуры: Основной материал – дерево – быстрота постройки, но недолговечность и необходимость деления...

Историки об Елизавете Петровне: Елизавета попала между двумя встречными культурными течениями, воспитывалась среди новых европейских веяний и преданий...

История развития хранилищ для нефти: Первые склады нефти появились в XVII веке. Они представляли собой землянные ямы-амбара глубиной 4…5 м...

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰)...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!