

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Особенности сооружения опор в сложных условиях: Сооружение ВЛ в районах с суровыми климатическими и тяжелыми геологическими условиями...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Особенности сооружения опор в сложных условиях: Сооружение ВЛ в районах с суровыми климатическими и тяжелыми геологическими условиями...
Топ:
Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов...
Характеристика АТП и сварочно-жестяницкого участка: Транспорт в настоящее время является одной из важнейших отраслей народного...
Эволюция кровеносной системы позвоночных животных: Биологическая эволюция – необратимый процесс исторического развития живой природы...
Интересное:
Искусственное повышение поверхности территории: Варианты искусственного повышения поверхности территории необходимо выбирать на основе анализа следующих характеристик защищаемой территории...
Финансовый рынок и его значение в управлении денежными потоками на современном этапе: любому предприятию для расширения производства и увеличения прибыли нужны...
Лечение прогрессирующих форм рака: Одним из наиболее важных достижений экспериментальной химиотерапии опухолей, начатой в 60-х и реализованной в 70-х годах, является...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Ракетного двигателя.
Энтальпия топлива, поступающего в камеру ЖРД (рис.19, сечение"H"), складывается из энтальпии компонентов топлива в баках (рис.19, сечение "O") и энергии, полученной на насосах, т. е.  ,
,  ,
,  .
.
Из курса "Топливо" известно, что  и определяется при стандартных условиях (
и определяется при стандартных условиях ( ).
).
 , и, следовательно,
, и, следовательно, 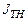 больше
больше  , но, так как жидкость несжимаема, а для идеальных газов
, но, так как жидкость несжимаема, а для идеальных газов  ), то значение
), то значение 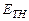 не превышает 0.5 %
не превышает 0.5 %  . Следовательно, с достаточной для практики точностью, можно принять, что
. Следовательно, с достаточной для практики точностью, можно принять, что 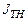 равно
равно  .
.
Аналогичные рассуждения можно провести и для ЖРД, выполненного по схеме с дожиганием генераторного газа (рис.20). Действительно  , где
, где  – энергия, затраченная в турбине турбонасосного агрегата, которая связана с энергией топлива, полученной на насосах, соотношением
– энергия, затраченная в турбине турбонасосного агрегата, которая связана с энергией топлива, полученной на насосах, соотношением
 ,
,
где  – коэффициент полезного действия ТНА, учитывающий безвозвратные потери энергии. Тогда, учитывая, что
– коэффициент полезного действия ТНА, учитывающий безвозвратные потери энергии. Тогда, учитывая, что  , получим:
, получим:
 , т. е.
, т. е. 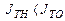 .
.
Однако, с достаточной для практики точностью, так же как и в первом случае, можно принять 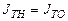 .
.
2.3. Аналитический метод определения теоретических параметров.
Для определения идеальной температуры горения необходимо составить уравнение теплового баланса. Если начальная температура компонентов топлива равна 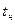 , а конечная температура продуктов сгорания
, а конечная температура продуктов сгорания  , то уравнение теплового баланса для случая полного адиабатического сгорания будет иметь следующий вид:
, то уравнение теплового баланса для случая полного адиабатического сгорания будет иметь следующий вид:

где  - мольная теплоемкость компонентов топлива
- мольная теплоемкость компонентов топлива 
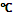 ;
;
 - мольная теплоемкость продуктов сгорания;
- мольная теплоемкость продуктов сгорания;
 - стандартный тепловой эффект рассматриваемой реакции -
- стандартный тепловой эффект рассматриваемой реакции -  .
.
Если допустить, что первоначальная температура компонентов топлива равна 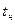 = 250
= 250  , т. е. соответствует температуре, при которой определяется стандартный тепловой эффект
, т. е. соответствует температуре, при которой определяется стандартный тепловой эффект  , то предыдущее уравнение запишется в следующем более простом виде:
, то предыдущее уравнение запишется в следующем более простом виде:
|
|
 =
= 
Следовательно, для определения идеальной температуры горения необходимо знать тепловой эффект реакции сгорания топлива и зависимость теплоемкости продуктов сгорания от температуры.
Величины теплового эффекта реакции сгорания различных топлив, т. е. теплотворность, можно найти в справочной литературе.
В тех случаях, когда эти данные отсутствуют, тепловой эффект реакции можно определить по закону Гесса согласно которому тепловой эффект химической реакции зависит только от начального и конечного состояний системы, но не зависит от пути, по которому протекает процесс.
В частности, из этого закона следует, что тепловой эффект реакции равен сумме теплот образования продуктов сгорания (конечных продуктов) за вычетом суммы теплот образования компонентов топлива (исходных веществ).
Следовательно, для определения теплового эффекта химической реакции достаточно знать теплоту образования из элементов исходных и конечных продуктов. При сгорании топлива, состоящего из горючего, описываемого формулой  , и окислителя описываемого формулой
, и окислителя описываемого формулой  , для стехиометрического соотношения
, для стехиометрического соотношения  уравнение реакции будет иметь следующий вид:
уравнение реакции будет иметь следующий вид:
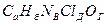 =
= 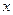


Здесь коэффициенты,  и
и  указывают количество атомов соответственно углерода, водорода, азота, хлора и кислорода в молекулах горючего и окислителя;
указывают количество атомов соответственно углерода, водорода, азота, хлора и кислорода в молекулах горючего и окислителя; 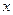 - необходимое число молекул окислителя для полного окисления одной молекулы горючего.
- необходимое число молекул окислителя для полного окисления одной молекулы горючего.
Если обозначить теплоту образования одной молекулы горючего из элементов через  , а теплоту образования одной молекулы окислителя через
, а теплоту образования одной молекулы окислителя через  и теплоты образования конечных продуктов через
и теплоты образования конечных продуктов через 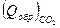 ,
,  ,
, 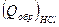 тогда тепловой эффект реакции, определяемой ур-нием (1), будет равен
тогда тепловой эффект реакции, определяемой ур-нием (1), будет равен

Воспользовавшись данными по теплотам образования  ,
,  и
и  , получим
, получим

Для вычисления теплового эффекта по ф-ле (3) необходимо теплоту образования компонентов топлива, которая может быть взята из справочных таблиц или вычислена из энергии образования связей. Кроме того, надо знать величину коэффициента 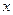 , которая может быть найдена из уравнения материального баланса кислорода. Из ур-ния (1) следует, что
, которая может быть найдена из уравнения материального баланса кислорода. Из ур-ния (1) следует, что
|
|

откуда

Тепловой эффект, вычисленный по ф-ле (III-29), отнесен к суммарному количеству реагирующих веществ. Для упрощения расчет обычно ведется либо на один моль, либо на 1 кг рабочего тела (продуктов сгорания).
Тепловой эффект, отнесенный к одному молю продуктов сгорания, будет равен

Тепловой эффект, отнесенный в 1 кг продуктов сгорания, будет равен

Для определения зависимости теплоемкости от температуры можно пользоваться следующими известными уравнениями

или

Значения коэффициентов этих уравнений приведены для справок в таблице 1.
Теплоемкость газов может быть приближенно выражена также уравнением, полученным на основании статистических законов термодинамики. В этом случае изобарная теплоемкость складывается из постоянной части, зависящей от числа поступательных и вращательных степеней свободы и переменной части, соответствующей вибрационной энергии

где  - число поступательных и вращательных степеней свободы молекулы;
- число поступательных и вращательных степеней свободы молекулы;
 - характеристическая температура, соответствующая данной частот колебаний;
- характеристическая температура, соответствующая данной частот колебаний;
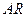 - универсальная (мольная) газовая постоянная.
- универсальная (мольная) газовая постоянная.
Суммирование производится по всем возможным частотам. Количество возможных частот зависит от структуры молекулы. Так, например, двухатомные молекулы имеют только по одной частоте  - четыре, а
- четыре, а  - три. В табл. 2 приведены частоты колебаний и характеристические температуры для некоторых часто встречающихся молекул газа. В более точных расчетах необходимо учитывать агармоничность колебаний (изменение вращательной энергии молекулы вследствие изменения момента ее инерции) и изменение электронного состояния молекул. В связи с применением спектроскопических методов исследования газов в настоящее время получены довольно точные величины теплоемкости различных газов в широком диапазоне температур в виде табличных данных.
- три. В табл. 2 приведены частоты колебаний и характеристические температуры для некоторых часто встречающихся молекул газа. В более точных расчетах необходимо учитывать агармоничность колебаний (изменение вращательной энергии молекулы вследствие изменения момента ее инерции) и изменение электронного состояния молекул. В связи с применением спектроскопических методов исследования газов в настоящее время получены довольно точные величины теплоемкости различных газов в широком диапазоне температур в виде табличных данных.
|
|
Таблица 1
| Вещество | А | В*10 
| 
| С*10 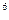
| Рекомендуемый температурный интервал °абс | Вероятная ошибка в % | 
|
 (г) (г)
| 4,97 | - | - | - | - | - | 4,97 |
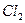 (г) (г)
| 7,576 | 2,424 | - | -0,9660 | 300-1500 | 1,13 | 8,212 |
 (г) (г)
| 
| 1,836 2,091 | - - | -0,280 -0,459 | 300-1500 300-2000 | - 1,38 | - 6,965 |

| 
| 8,533 2,74 | - -1,955 | 2,475 - | 300-2000 - | 1,38 - | 8,874 - |

| 6,947 | -0,2 | - | 0,48 | 300-1500 | 0,49 | 6,891 |

| 7,219 | 2,374 | -0,267 | - | 298-1500 | 0,96 | 8,025 |

| 
| 0,202 0,524 | -1,030 -2,972 | - - | 298-1500 600-3000 | 0,13 0,5 | 7,017 - |

| 6,732 | 0,433 | - | 0,37 | 300-1500 | 0,98 | 6,893 |
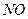
| 6,529 | 10,515 | -3,571 | - | 298-1500 | 1,26 | - |

| 3,422 | 17,845 | - | -4,165 | 291-1500 | 0,71 | 8,536 |
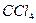
| 22,675 | 3,274 | -3,264 | - | 273-773 | 0,57 | 19,96 |

| 6,449 | 1,413 | -0,081 | - | 300-1500 | 1,35 | 6,96 |
Таблица 2
| Молекулы | Частота колебаний  [1/см] [1/см]
| Характеристическая температура 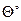 абс абс
| Примечание |

| 4282 | 6130 | |

| 2345 | 3350 | |
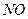
| 1892 | 2705 | |

| 1556 | 2224 | |

| 2155 | 3085 | |

| 3649 | 5222 | |

| 1595 | 2280 | Деформационные колебания |

| 3600 | 5150 | Валентные колебания |

| 3756 | 5360 | Валентные колебания |

| 667 | 954 | Деформационные колебания |

| 667 | 954 | Деформационные колебания |

| 1340 | 1920 | Валентные колебания |

| 2350 | 3360 | Валентные колебания |
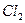
| - | 801 | |

| - | 4130 |
|
|
|

Автоматическое растормаживание колес: Тормозные устройства колес предназначены для уменьшения длины пробега и улучшения маневрирования ВС при...

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Архитектура электронного правительства: Единая архитектура – это методологический подход при создании системы управления государства, который строится...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!