Спирты по количеству гидроксильных групп бывают одно-, двух-, многоатомными. Для одно- и многоатомных реакции различны.
Качественные реакции на одноатомные спирты:
1) Простейшая качественная реакция на спирты — окисление спирта оксидом меди. Для этого пары спирта пропускают над раскаленным оксидом меди. Затем полученный альдегид улавливают фуксинсернистой кислотой, раствор становится фиолетовым:
CH3-CH2-OH + CuO —t—> CH3-CHO + Cu + H2O
2) Еще одним известным методом является иодоформная проба:
CH3-CH2-OH + 4I2 + 6NaOH ——> CHI3 + 5NaI + HCOONa + 5H2O
3) Спирты идентифицируются пробой Лукаса — конц. раствор соляной кислоты и хлорида цинка. При пропускании вторичного или третичного спирта в такой раствор образуется маслянистый осадок соответствующего алкилхлорида:
CH3-CHOH-CH3 + HCl —ZnCl2—> CH3-CHCl-CH3 + H2O
Первичные спирты в реакцию не вступают.
Качественные реакции на многоатомные спирты.
Наиболее известная качественная реакция на многоатомные спирты — взаимодействие их с гидроксидом меди (II). Гидроксид растворяется, образуется хелатный комплекс темно-синего цвета. Обратите внимание на то, что в отличии от альдегидов многоатомные спирты реагируют с гидроксидом меди (II) без нагревания. К примеру, при приливании глицерина образуется глицерат меди (II):
Лабораторная работа №7
Тема: Цветные реакции фенолов с феррум (III) хлоридом
Цель: изучить цветные реакции фенолов с хлоридом железа (III), которые используются для качественного определения фенолов, установить общие и отличительные признаки данных реакций.
Реактивы и оборудование: фенольная вода, 1 %-ные водные растворы пирокахетина, резорцина, гидрохинона, пирогаллола и 1 %-ные спиртовые растворы α - и β –нафтолов, 1 %-ный раствор железа (III) хлорида, этанол, дист. вода, пипетки, пробирки.
Ход работы
В пробирку помещают 3 капли прозрачной фенольной воды и добавляют 1 каплю 1%-ного раствора железа (III) хлорида.
Наблюдают появление фиолетового окрашивания, обусловленного образованием смеси комплексных соединений C6H5OFeCl2, (C6H5O)2FeCl, (C6H5O)3Fe. Интенсивность окраски раствора усиливается при разбавлении водой, ослабевает или полностью исчезает при добавлении этанола. Реакцию выполняют с 1 %-ными водными растворами пирокатехина, резорцина, гидрохинона, пирогаллола и 1 %-ными спиртовыми растворами α - и β –нафтолов. Отмечают различную окраску растворов:
· пирокатехин (1,2-дигидроксибензол) — зелёная;
· резорцин (1,3- дигидроксибензол) — синяя;
· пирогаллол (1,2,3-тригидроксибензол) — красная;
· α -нафтол — фиолетовая;
· β -нафтол — зелёная;
· гидрохинон (1,4- дигидроксибензол) —зелёная, быстро переходящая в жёлтую. Зафиксировать зелёную окраску в реакции с гидрохиноном удаётся лишь на фоне белой бумаги в момент попадпния в пробирку капли железа (III) хлорида.
Появление быстро изменяющейся зелёной окраски указывает на то, что при окислении гидрохинона в n- хинон образуется промежуточное соединение - хингидрон:

Вопросы для самостоятельной работы
- Найдите дополнительную информацию о применении используемых в лабораторной работе веществ (пирокахетин, резорцин, гидрохинон, пирогаллол и α - и β –нафтолы) в медицине и фармакологии. Напишите их структурные формулы.
- Какие ещё спирты и фенолы и для чего используются в медицине?
Лабораторная работа №8
Тема: Окисление формальдегида
Цель: изучить реакции окисления формальдегида реактивом Толленса («реакция серебряного зеркала») и раствором меди (II) гидроксида (проба Троммера), написать соответствующие уравнения реакций, сделать выводы.
Реактивы и оборудование: 10%-ный раствор натрия гидроксида, 2%-ный раствор меди (II) гидроксида, 1%-ный раствор серебра нитрата,2%-ный водный раствор аммиака, 40%-ный раствор формальдегида, пробирки, пипетки, водяная баня.
Ход работы
Опыт №1 Окисление альдегидов меди (II) гидроксидом в щелочном растворе (проба Троммера)
Помещаем в пробирку 5 капель 10%-ного раствора натрия гидроксида, воды и 1 каплю 2%-ного раствора меди (II) гидроксида.
При взаимодействии щёлочи и гидроксида меди (II) образуется синий осадок:

Затем в пробирку добавляем 3 капли 40%-ного раствора формальдегида. Содержимое встряхиваем и нагреваем до начала кипения.
При нагревании альдегиды легко окисляются до карбоновых кислот, восстанавливая соединения двухвалентной меди до одновалентной (или до металлической меди).
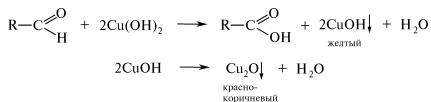
Формальдегид в этих условиях не только окисляется, но и в присутствии катализатора меди (I) оксида взаимодействует со щёлочью:

Образующийся при этом водород восстанавливает соединения меди до свободного металла. При этом наблюдается образование красно-коричневого осадка или медного налёта на стенках пробирки («медное зеркало»).










