Чистое вещество среди смесей
A) Очищенная вода.
B) Дождевая вода.
C) Речная вода.
D) Воздух.
E) Морская вода.
В реакцию соединения может вступать
A) Только два простых вещества.
B) Только одно простое вещество.
C) Только одно сложное вещество.
D) Только несколько сложных веществ.
E) Несколько простых или сложных веществ.
Сумма всех коэффициентов в реакции обмена
Al(OH)3 + H2SO4 = Al2(SO4)3 + H2O равна
A) 12.
B) 8.
C) 6.
D) 9.
E) 10.
В данном ряду химических соединений CaO, MgO, ВаО валентность металлов равна
A) Двум.
B) Единице.
C) Трем.
D) Четырем.
E) Восьми.
Масса 0,1 моль оксида кальция равна
A) 5,6г.
B) 56г.
C) 11,2г.
D) 112г.
E) 0,56г.
6.Массовая доля кислорода в карбонате кальция CaCO3
A) 48%
B) 12%
C) 40%
D) 56%
E) 60%
7.Кислород – это простое вещество в утверждении:
A) Газ кислород входит в состав воздуха.
B) Кислород в соединениях имеет чаще всего степень окисления -2
C) Кислород в соединениях двухвалентен
D) Химическое соединение кислорода с каким-либо элементом называется оксидом.
E) Кислород входит в состав серной кислоты.
К основному оксиду относится
A) Оксид магния.
B) Оксид алюминия.
C) Угарный газ.
D) Сернистый газ.
E) Оксид цинка.
Основной источник получения водорода в промышленности - это
A) Взаимодействие воды с щелочными металлами.
B) Взаимодействие воды с щелочноземельными металлами.
C) Взаимодействие некоторых металлов с кислотами
D) Разложение кислот E) Из природного газа
Бескислородная кислота
A) Соляная.
B) Азотная
C)Угольная.
D) Серная
E)Кремниевая.
Cредняя соль.
A) MgSO4
B) Mg(OH)Cl
C) K2NaPO4
D) Na[Al(OH)4]
E) KHSO4
12.Вода не реагирует с:
A) Оксидом меди.
B) Оксидом лития.
C) Оксидом натрия.
D) Оксидом кальция.
E) Оксидом бария.
13.В ядре атома натрия (23Na) число протонов равно
A) 12.
B) 11.
C) 23.
D) 13.
E) 15
В атоме кадмия число энергетических уровней равно
A) 7.
B) 6.
C) 5.
D) 2.
E) 3.
Наибольшее значение электроотрицательности имеет
A) Фосфор.
B) Магний.
C) Алюминий.
D) Кремний.
E) Натрий.
16.Сера имеет степень окисления +6 в соединении
A) SO3
B) SO2
C) H2SO3
D) S
Е) H2S
Электролитом среди не электролитов является
А) H2SO4
B) CH4
C) O2
D) C2H5OH
E) CO2
Сумма всех коэффициентов в ионном полном уравнении реакции
Ca(NO3)2 + K2CO3 =
А) 11
B) 3
С) 9
D) 12
E) 15
В растворе соляной кислоты лакмус фиолетовый окрашивается в
А) Синий
B) Желтый
С) Красный
D) Бесцветный
E) Оранжевый
Количество вещества осадка, полученного при взаимодействии 9,8 г серной кислоты и 104 г хлорида бария
А) 0,1 моль
B) 0,5 моль
C) 1 моль
D) 1,5 моль
E) 2 моль
21.Вещество А в цепи превращения: H2S→SO2→A→H2SO4→SO2
A) Оксид серы (VI)
B) Сероводород
C) Сера
D) Сульфид натрия
E) Сульфат натрия
22.Формула гидроксида, характерного для азота:
A) HRO3
B) H2RO3
C) HRO2
D) H2RO4
E) H2RO3
23.Поглощение газообразных или растворенных веществ поверхностью твердого вещества – это:
A) Адсорбция
B) Дифракция
C) Десорбция
D) Денатурация
E) Коагуляция
Относительная плотность аммиака по водороду
А) 8,5
B) 11,5
С) 9,5
D) 12,5
E) 15,5
25.К галогенам не относится
A) Радон
B) Фтор
C) Йод
D) Бром
E) Хлор
Из предложенных элементов к металлам относится
A) Калий
B) Кремний
C) Аргон.
D) Мышьяк
E) Бор
Электронная формула атома кальция
А) 1s22s22p63s23p64s2
B) 1s22s22p63s2
C) 1s22s2
D) 1s22s22p63s23p64s24p2
E) 1s22s22p63s23p64s24p3
Амфотерность алюминия проявляется во взаимодействии с
А) NaOH, HCl
B) NaOH, KOH
C) HCl, H2SO4
D) NaOH, H2O
E) S, HCl
29.Количество моль азота (н.у.), необходимого для получения 11,2 л аммиака (NH3), равно
A) 1 моль.
B) 2 моль.
C) 0,5 моль
D) 0,25 моль
E) 5 моль.
30.Вещество Х в ряду превращений Ba→ Х→ Ba(OH)2→BaCl2
A) BaO
B) BaO2
C) BaS
D) BaSO4
E) Ba3(PO4)2
31.Смесь среди чистых веществ:
A) Нефть.
B) Железо.
C) Сульфат натрия.
D) Медь.
E) Серная кислота.
В реакцию обмена может вступать
A) Два сложных вещества.
B) Одно простое и одно сложное.
C) Два простых вещества.
D) Несколько простых и сложных веществ.
E) Два простых вещества.
Сумма коэффициентов в правой части реакции обмена
P2O5 + KOH = K3PO4 + H2O
A) 5.
B) 4.
C) 7.
D) 3.
E) 11.
34.В данном ряду химических соединений BaS, К2S, Аl2S3 валентность серы равна
A) Двум.
B) Единице.
C) Трем.
D) Четырем.
E) Шести.
Масса 0,2 моль карбоната кальция равна
A) 20г.
B) 200г.
C) 0,2г.
D) 2г.
E) 500г.
36.Массовая доля углерода в карбонате кальция CaCO3
A) 12%
B) 40%
C) 48%
D) 56%
E) 60%
Верное утверждение физического свойства кислорода
A) Газ кислород легче воздуха.
B) Кислород имеет высокую электропроводность.
C) Кислород хорошо растворяется в воде.
D) Кислород имеет резкий запах.
E) Кислород тяжелее воздуха.
К амфотерному оксиду относится
A) Оксид германия.
B) Оксид бора.
C) Оксид меди
D) Оксид кремния.
E) Оксид калия.
Утверждение, относящееся к химическому элементу водороду
A) Водород горит в атмосфере хлора.
B) Смесь водорода с кислородом взрывоопасна
C) Водород – это самый легкий газ.
D) Водород восстанавливает металлы из их оксидов.
E) Водород входит в состав воды.
Одноосновная кислота
A) Соляная
B) Фосфорная
C) Кремниевая
D) Угольная
E) Серная
Кислая соль
A) KHSO4
B) Mg(OH)Cl
C) K2NaPO4
D) Na[Al(OH)4]
E) MgSO4
12.Вода при комнатной температуре взаимодействует с
A) Калием.
B) Углеродом.
C) Медью.
D) Свинцом.
E) Серой.
43.У алюминия (27Al) 13 протонов, а нейтронов
A) 14.
B) 27.
C) 13.
D) 12.
E) 15.
Водород взаимодействует
A) С активными металлами
B) С кислотными оксидами
C) С основаниями
D) С водой.
E) С кислотами
Основная соль
A) Mg(OH)Cl
B) KHSO4
C) K2NaPO4
D) Na[Al(OH)4]
E) MgSO4
62.Выделяется водород и образуется гидроксид металла при взаимодействии воды с:
A) Натрием.
B) Железом.
C) Свинцом.
D) Цинком.
E) Медью.
63.В ядре атома элемента № 21 (45X)содержится нейтронов
A) 23.
B) 24.
C) 22.
D) 19.
E) 17.
64.У элементов третьего периода наиболее ярко выражены металлические свойства
A) Алюминия.
B) Кремния.
C) Магния.
D) Натрия.
E) Аргона.
Амфотерное основание
A) Гидроксид цинка.
B) Гидроксид натрия.
C) Гидроксид меди (II)
D) Гидроксид бария
E) Гидроксид кальция.
Аммиак не взаимодействует с
A) Азотной кислотой
B) Кислородом
C) Водой
D) Соляной кислотой
E) Гидроксидом бария
CaO взаимодействует с
А) HCl
B) Na2O
C) CaCl2
D) NaOH
E) K2O
107.Сумма всех коэффициентов в схеме реакции Al2O3 + HCl ® AlCl3 + H2O
А)12
B) 14
C)15
D)16
E) 17
Воздух - это
A) Смесь только кислорода и азота.
B) Смесь простых и сложных веществ.
C) Смесь только сложных веществ.
D) Кислород
E) Смесь только простых веществ.
Не реагирует с водой оксид
A) Кремния.
B) Фосфора
C) Серы
D) Натрия.
E) Бария.
Водород не применяют
A) Для экологически чистого топлива.
B) Для синтеза аммиака.
C) Для восстановления металлов из их оксидов.
D) Для получения соляной кислоты.
E) Для окисления чистых веществ
110.Неправильно названа соль:
A) Fe(NO3)2 – нитрит железа (II)
B) K3PO4 – ортофосфат калия
C) CuSO4 – сульфат меди (II)
D) NaCl – хлорид натрия
E) ZnS – сульфид цинка
Реакция соединения - это
A) 2H2 +O2 =2H2O
B) 2H2O = 2H2 + O2
C) 2KClO3 = 2KCl + 3O2
D) Ca +2HCl = CaCl2 + H2
E) CаCO3 = CaO + CO2
133.Сумма коэффициентов в уравнении реакции разложения NaNO3 = NaNO2 + O2
A) 5
B) 6
C) 7
D) 8
E) 9
134.В данном перечне оксидов атомы всех
элементов имеют валентность, равную двум
A) CaO, NO, MgO
B) Fe2O3, Al2O3, P2O3.
C) K2O, CaO, Fe2O3.
D) Al2O3, N2O3, K2O.
E) N2O3, P2O5, H2O.
135.Число молекул в 0,1 моль углекислого газа CO2
A) 6 . 1023.
B) 6 . 1022.
C) 1, 2 . 1023.
D) 1, 2 . 1022.
E) 0, 6 . 1022.
136.Массовая доля кислорода в оксиде серы (IV) SO2
A) 50%
B) 12%
C) 48%
D) 40%
E) 60%
Элемент стронций относится
A) s-элементам
B) р-элементам.
C) d-элементам
D) f-элементам
E) h-элементам
143.Среди элементов шестой группы наиболее ярко выражен неметаллический характер у
A) Кислорода.
B) Серы.
C) Селена.
D) Теллура.
E) Полония.
CaО не взаимодействует с
А) S
B) HCl
C) KC l
D) H2O
E) H2SO4
157.Не является физическим свойством алюминия
А) Плохо проводит тепло
B) Легкий (плотность= 2,7г/см3)
C) Серебристо-белый
D) Ковкий, пластичный
E) Электропроводный
158.Масса цинка, необходимая для вытеснения 11,2л водорода из соляной кислоты
A) 32, 5 г
B) 33, 7 г.
C) 21 г.
D) 25 г.
E) 22, 5 г.
Реакция разложения - это
A) 2KClO3 = 2KCl + 3O2
B) 2H2 +O2 =2 H2O C) S + O2 = SO2
D) Fe + CuSO4 = FeSO4 + Cu
E) Ca +2 HCl = CаCl2 + H2
163.Сумма коэффициентов в уравнении реакции соединения P2O5 + K2O = K3PO4
A) 6
B) 5
C) 7
D) 8
E) 9
164.В данном перечне оксидов атомы всех элементов имеют валентность, равную одному
A) K2O, H2O, N2O.
B) Fe2O3, Al2O3, P2O3.
C) N2O3, P2O5 CaO,.
D) Al2O3, N2O3, K2O.
E) CaO, N2O3, P2O3.
165.Порция 1,5 . 1023 молекул диоксида углерода соответствует количеству вещества
A) 0, 5 моль.
B) 1 моль.
C) 0, 25 моль.
D) 0, 75 моль.
E) 1, 5 моль.
Слабый электролит
А) H2CO3
Б) HNO3
C) H2SO4
D) HCl
E) BaCl2
177.Сумма всех коэффициентов в ионном полном уравнении реакции AlCl3+ NaOH =
А) 17
B) 11
C) 3
D) 12
E) 14
178.Появляется запах сероводорода при взаимодействии K2S с
А) H2
B) KOH
C) HCl
D) NaCl
E) SiO2
Са не взаимодействует с
А) Hg
B) H2O
C) KC l
D)CuO
E) NaCl
Реакция замещения - это
A) Fe + CuSO4 = FeSO4 + Cu
B) CаCO3 = СаО + CO2
C) S + O2 = SO2
D) 2CO + O2 = 2CO2
E) 2H2 +O2 =2 H2O
Сильный электролит
А) H2O
Б) Ba(OH)2
C) H2S
D) H3PO4
E) H2CO3
207.Сумма всех коэффициентов в ионном полном уравнении реакции Fe(NO3)2 + KOH=
А) 12
B) 11
C) 9
D) 3
E) 14
208.Появляется запах сернистого газа при взаимодействии K2SO3 с
А) HCl
B) KOH
C) SiO2
D) NaCl
E) H2
Одноосновная кислота - это
A) HNO3
B) H2SO4
C) H2CO3
D) H2SiO3
E) H3PO4
220.В реакции между оксидом калия и сернистым газом образуется:
A) Сульфит калия.
B) Сульфид калия.
C) Сульфат калия.
D) Гидросульфид калия.
E) Гидросульфат калия.
При нагревании разлагается
A) NaOH
B) Ba(OH)2
C) KOH
D) LiOH
E) Fe(OH)3
222.Число электронов в анионе S2- равно
A) 16.
B) 18.
C) 32.
D) 34.
E) 28.
В данной цепи превращений
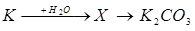 вещество Х – это:
вещество Х – это:
A) KOH
B) K2O
C) KO2
D) H2
E) KHCO3
Реакция замещения - это
A) Fe + CuSO4 = FeSO4 + Cu
B) CаCO3 = СаО + CO2
C) S + O2 = SO2
D) 2CO + O2 = 2CO2
E) 2H2 +O2 =2 H2O
Бескислородная кислота
A) Соляная.
B) Азотная
C)Угольная.
D) Серная
E)Кремниевая.
Cредняя соль.
A) MgSO4
B) Mg(OH)Cl
C) K2NaPO4
D) Na[Al(OH)4]
E) KHSO4
292.Вода не реагирует с:
A) Оксидом меди.
B) Оксидом лития.
C) Оксидом натрия.
D) Оксидом кальция.
E) Оксидом бария.
293.В ядре атома натрия (23Na) число протонов равно
A) 12.
B) 11.
C) 23.
D) 13.
E) 15
Чистое вещество среди смесей
A) Очищенная вода.
B) Дождевая вода.
C) Речная вода.
D) Воздух.
E) Морская вода.



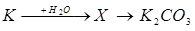 вещество Х – это:
вещество Х – это:

