

Архитектура электронного правительства: Единая архитектура – это методологический подход при создании системы управления государства, который строится...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Архитектура электронного правительства: Единая архитектура – это методологический подход при создании системы управления государства, который строится...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...
Топ:
Характеристика АТП и сварочно-жестяницкого участка: Транспорт в настоящее время является одной из важнейших отраслей народного...
Эволюция кровеносной системы позвоночных животных: Биологическая эволюция – необратимый процесс исторического развития живой природы...
Интересное:
Средства для ингаляционного наркоза: Наркоз наступает в результате вдыхания (ингаляции) средств, которое осуществляют или с помощью маски...
Уполаживание и террасирование склонов: Если глубина оврага более 5 м необходимо устройство берм. Варианты использования оврагов для градостроительных целей...
Национальное богатство страны и его составляющие: для оценки элементов национального богатства используются...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Область применения: Катализаторы конверсии метана ГИАП-8, ГИАП-25, ГИАП-36Н применяются для воздушной конверсии газообразных углеводородов в эндотермических генераторах контролируемых атмосфер при температурах 1030-1050 °С. Могут применяться также для воздушной конверсии сжиженных газов (пропан и пропанобутановой фракции) в тех же целях. Используются также в различных отраслях машиностроительной промышленности, где контролируемые атмосферы используются для термообработки металлических изделий и деталей машин.
Основные данные: Катализаторы отвечают требованиям ТУ 11303382-86. Нанесенная часть катализаторов содержит оксиды никеля, алюминия и кальция.
Внешний вид: кирпичики серого цвета (ГИАП-25), цилиндрические гранулы серого цвета (ГИАП-8 и ГИАП-36Н).

Рис.9. Катализаторы конверсии метана ГИАП-8, ГИАП-25, ГИАП-36Н.
Размеры: 32 х32 (ГИАП-25), диаметр 15-18 мм, высота 15-18 мм (ГИАП-8,ГИАП-36Н). Массовая доля никеля в пересчете на оксид никеля: 7.5 + 1.5 % (для ГИАП-8, ГИАП-36Н) и до 12 % (для ГИАП-25).
ДКР-1
ДРК – 1 новый вид катализатора, предназначен для паровой и пароуглекислотной конверсии газообразных углеводородов в трубчатых печах крупнотоннажных агрегатов по производству аммиака, метанола, установок получения технического водорода. Катализатор представляет собой промотированный оксид никеля, нанесенный на высокоглиноземистый носитель в виде циллиндрических колец, имеет более высокую активность и стабильность.
Физико-химические характеристики ТУ 2171-94-002038015-97
|
|
|
Условия эксплуатации | |
| Температура, на выходе трубчатой печи, ºС | 790-810 |
| Давление, МПа | 3,3-3,6 |
| Объемная скорость, ч-1: соотношение ПАР:ГАЗ | 1500-18003,7-4,0 |
| Остаточная объемная доля метана на выходе из печи, % | 9-11 |
| Гарантируемый срок службы, лет | 4 |
Расчет процесса конверсии
Рассчитать процесс конверсии метана водяным паром по следующим данным:
| Производительность по метану | 1000 м3/час |
| Состав газа | метан – 98% |
| азот – 2% | |
| Степень конверсии | 70% |
| Температура | на входе 105°С |
| на выходе 900°С |
СН  + Н
+ Н  О
О  СО + 3Н
СО + 3Н 

1. Расчет термодинамических параметров.
СН 
| Н  О О
| СО | Н2 | |
 Н Н  
| -74,85 | -241,81 | -110,53 | 0 |
D S  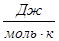
| 186,27 | 188,72 | 197,55 | 130,52 |
D G  
| -50,85 | -228,61 | -137,15 | 0 |
1.1. По закону Гесса находим тепловой эффект химической реакции при нормальных условиях:
D Н  =(S ni D Н
=(S ni D Н  )
)  - (S ni D Н
- (S ni D Н  )
) 
DН  = 0×3 - 110,53 + 241,81 + 74,85 = 206,13 кДж / моль
= 0×3 - 110,53 + 241,81 + 74,85 = 206,13 кДж / моль
1.2. Найдем энтропию реакции:
D S  = (S ni D S
= (S ni D S  )
)  - (S ni D S
- (S ni D S  )
) 
DS  =3×130,52 +197,55 -188,72 -186,27= 214,12 Дж / моль × К
=3×130,52 +197,55 -188,72 -186,27= 214,12 Дж / моль × К
1.3. Найдем изменение энергии Гиббса в ходе реакции при нормальных условиях:
D G  = (S ni D G
= (S ni D G  )
)  -(S ni D G
-(S ni D G  )
) 
DG  = 3×0-137,15+288,61+50,85=142,31 кДж / моль
= 3×0-137,15+288,61+50,85=142,31 кДж / моль
2. Найдем функцию зависимости теплоемкости от температуры С  = f(Т)
= f(Т)
|
|
СН 
| Н  О О
| СО | Н 
| |
| a | 14,32 | 30 | 28,41 | 27,28 |
| b | 74,66×10 
| 10,71×10 
| 4,1×10 
| 3,26×10 
|
| с’ | 0,33×10 
| -0,46×10 
| 0,5×10 
| |
| с | -17,43×10 
|
Ср(СН4) = 14,32 + 74,66×10  Т - 17,43×10
Т - 17,43×10  Т
Т 
Ср(Н2О) = 30 + 10,71×10-3Т + 0,33×105Т-2
Ср(СО) = 28,41+ 4,1×10-3×Т - 0,46×105Т-2
Ср(Н2) = 27,28 + 3,26×10-3Т + 0,5×105Т-2
D Ср = D а + D bT + D с’Т2+ D c Т-2
DСр = (3×27,28+28,41-30-14,32) + (3×3,26+4,1-10,71-74,66)×10-3Т +
+ (3×0,5-0,46-0,33)×105Т-2 - 17,43×10-6Т2
DСр = 65,93 - 71,49×10-3Т + 0,71×105Т-2 - 17,43×10-6Т2 Дж / моль × К
2.1. Для азота зависимость теплоемкости от температуры выглядит следующим образом:
Ср(N2) = 27,88 + 4,27×10-3Т
3.1. Найдем изменение энтропии в ходе реакции при нагревании от t 1 =25  C до t 2 =900
C до t 2 =900  C:
C:
DS= 
 dТ =
dТ =


D S =16.54 Дж/моль × К
3.2. Найдем изменение энтальпии в ходе реакции при нагревании от t 1 =25 ° C до t 2 =900 ° C:

DH= 65,93 (1173-298) -  ×71,49×10-3(11732-2982) -
×71,49×10-3(11732-2982) -  -
- 
D Н= - 2375 Дж/моль
3.3. Рассчитаем энергию Гиббса на выходе t 2 =900 ° С:


4. Найдем константу равновесия:
D G ° =- RTlnKp
Kp = exp (- D G ° / RT)
Kp = exp (-(-62058,71/8,31 × 1173))=582,04
4.1. Рассчитаем равновесную степень превращения метана. При температуре от 827°С и составе исходной смеси СН4 : Н2О = 1: 2 необходимо проводить процесс при абсолютном давлении 10 атм.
СН4 + Н2О ® СО + 3Н2
т.к. водяной пар в избытке, то РН2О = 2РСН4
Робщ = РСН4 + 2РСН4= 3РСН4
РСН4 = Робщ/3 = 10/3 атм.
При равновесии:






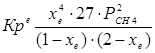



xe = 0,8115 и xe = - 2,29
Равновесная степень превращения равна 0,8115.
Вывод: равновесная степень превращения метана xe=0,8115,степень конверсии a = 0,7, данный процесс, возможно, провести в указанных условиях.
5. Составим материальный баланс.
| Приход | Расход | ||||
| Исходное вещество | m, кг | V,м3 | Продукт | m, кг | V,м3 |
| СН4 | 714,29 | 1000 | СН4 | 214,29 | 300 |
| N2 | 25,51 | 20,41 | N2 | 25,51 | 20,41 |
| Н2О | 1607,14 | 2000 | Н2О | 1044,64 | 1300 |
| СО | 875 | 700 | |||
| Н2 | 187,5 | 2100 | |||
| Итого: | 2346,94 | 3020,41 | Итого: | 2346,94 | 4420,41 |
5.1.Найдем количество поступающего метана (в час):
по закону эквивалентов

 (кг)
(кг)
Найдем количество конвертируемого метана:
V=0, 7×1000=700 (м3)

После реакции осталось:
m(СН4) = 714,29 – 500 = 214,29 (кг)
V(СН4)= 1000 – 700 = 300 (м3)
5.2. Найдем необходимое количество воды для осуществления реакции:

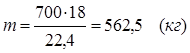
В промышленном производстве для осуществления процесса воду и метан берут в отношении 2:1. Исходя из этого условия рассчитаем количество поступающего водяного пара:
V = 2 × 1000 = 2000 (м3)
|
|

Не прореагировало водяного пара:
m(Н2О) = 1607,14 – 500 = 214,29 (кг)
V(Н2О) = 2000 – 700 = 300 (м3)
5.3. В реактор поступает  :
:
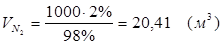
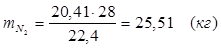
Т.к. азот не участвует в химической реакции, то на выходе:
m = 25,51 (кг)
V = 20,41 (м3)
5.4. Найдем количество образовавшегося в ходе реакции СО:


5.5. Найдем количество образовавшегося водорода:


Вывод:  . Материальный баланс сошелся.
. Материальный баланс сошелся.
6. Составим энергетический баланс:
| Приход | кДж | % | Расход | кДж | % |
| Q(СН4) | 675,87 | 4 | Q(СН4) | 1224,04 | 7,2 |
| Q(N2) | 10,16 | 0,06 | Q(N2) | 35,15 | 0,2 |
| Q(Н2О) | 1156,9 | 6,87 | Q(Н2О) | 4460,2 | 26,4 |
| Qподв | 15029,6 | 89,07 | Q(СО) | 1216,5 | 7,23 |
| Q(Н2) | 3420,87 | 20,24 | |||
| Qх.р. | 6515,8 | 38,62 | |||
| Итого: | 16872,53 | 100% | Итого: | 16872,56 | 100% |
6.1. Найдем тепло, которое поступает с исходными веществами – физическое тепло:

где T 1 – температура на входе, (t 1 =105  C); Ср – теплоемкость, будем считать, что теплоемкость зависит от температуры (п.2).
C); Ср – теплоемкость, будем считать, что теплоемкость зависит от температуры (п.2).
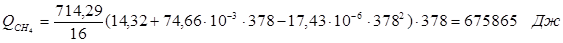


Реакция конверсии водяным паром сильно эндотермична, поэтому необходимо подогревать исходную реакционную смесь. В промышленности для подогрева системы используют природный газ, за счет сжигания которого выделяется необходимое количество тепла Q.
6.2. Найдем тепло веществ на выходе из реактора:

где T 2 – температура на выходе из реактора.
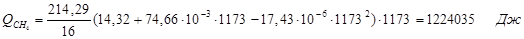




6.3. Найдем теплоту, поглощенную в ходе химической реакции:


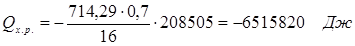
6.4. Найдем количество теплоты, которое необходимо затратить на подогрев исходной смеси:

6.5. Найдем количество природного газа, которое необходимо затратить для подогрева исходной смеси, считая, что природный газ на 95% состоит из метана (состав природного газа зависит от месторождения, колеблется от 55-99%):
По справочнику:
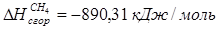

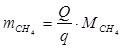


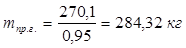
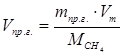

СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
1. А. Г. Аншиц, Е. Н. Воскресенская. Окислительная конденсация метана – новый процесс переработки природного газа.
2. Сосна М.Х., Энтин Б.М., Лейтес И.Л. Нонограммы для определения состава газа конверсии метана//Химическая промышленность. – 1989. - №7. - с.59
3. Крейндель Э.М. Конверсия метана природного газа. Л.:-1964.
4. Г.С. Яблонский. Кинетические модели гетерогенно-каталитических реакций. Элементы теории кинетики сложных химических реакций. Глава 1. В сб.: Химическая и биологическая кинетика / Под ред. Н.М. Эмануэля, И.В. Березина, С.Д. Варфоломеева. М.: Изд-во Моск. ун-та, 1983.
|
|
5. Водород. Свойства, получение, хранение, транспортирование, применение: Справ. изд./Д.Ю. Гамбург, В.П. Семенов,, Л.Н. Смирнова; Под ред. Д.Ю. Гамбурга, Н.Ф. Дубовкина. – М.: Химия, 1989.
|
|
|

Историки об Елизавете Петровне: Елизавета попала между двумя встречными культурными течениями, воспитывалась среди новых европейских веяний и преданий...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Таксономические единицы (категории) растений: Каждая система классификации состоит из определённых соподчиненных друг другу...

Типы сооружений для обработки осадков: Септиками называются сооружения, в которых одновременно происходят осветление сточной жидкости...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!