Для практических расчётов принимают, что воздух состоит из 21% кислорода и 79% азота. Таким образом, объёмное соотношение азота и кислорода в воздухе составит:
 (1.1)
(1.1)
где  2,
2,  2 - это объёмное (% об.) содержание азота и кислорода в окислительной среде.
2 - это объёмное (% об.) содержание азота и кислорода в окислительной среде.
Следовательно, на 1м3 (кмоль) кислорода в воздухе приходится 3,76м3(кмоль) азота.
Весовое соотношение азота и кислорода в воздухе можно определить, исходя из соотношения:
 =
= 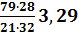
где М N 2,  2 -молекулярные массы соответственно кислорода и азота.
2 -молекулярные массы соответственно кислорода и азота.
Для удобства расчётов горючие вещества разделяют на три типа (таб.1.1).Индивидуальные химические соединения (метан, уксусная кислота и т.п., вещества сложного состава (древесина, торф, сланцы, нефть и т. п.),смесь газов (генераторный газ и т.д.)
Таблица 1.1
Здесь: V 0 B - теоретическое количество воздуха;
nr , 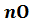 2
2  2 количество горючего, кислорода. и азота получаемые из уравнения химической реакции горения кмоль;
2 количество горючего, кислорода. и азота получаемые из уравнения химической реакции горения кмоль;
М- молекулярная масса горючего;
V 0- объем 1 моля газа при нормальных условиях (22,4 м3)
C, H, S, O -весовое содержание соответствующих элементов в составе горючего, %;
 ri -коцентрация i-того горючего компонента, %;
ri -коцентрация i-того горючего компонента, %;
 О 2 концентрация кислорода в составе горючего газа, %об.;
О 2 концентрация кислорода в составе горючего газа, %об.;
 2 i -количество кислорода необходимое для окисления одного i-того кмоля горючего компонента, ккмоль.
2 i -количество кислорода необходимое для окисления одного i-того кмоля горючего компонента, ккмоль.
Для определенного объема воздуха при горении в условиях, отличных от нормальных, пользуются следствием из уравнения состояния идеальных газов:
 =
=  (1.6)
(1.6)
где,  нормальное давление, Па.
нормальное давление, Па.
 температура, К.
температура, К.
 объем воздуха при нормальных условиях;
объем воздуха при нормальных условиях;
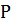 1
1 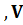 1
1  Т1
Т1 
 заданные условия горения.
заданные условия горения.
Практическое количество воздуха V0 –объем воздуха, фактически поступивший в зону горения.
Отношение практического объема воздуха к теоретическому называется коэффициентом избытка воздуха  :
:
 =
=  (1.7)
(1.7)
Разность между практическим и теоретическим объемами воздуха называется избытком воздуха ∆  :
:
∆  (1.8)
(1.8)
Из (1.7)и (1.8) следует, что
∆  -1) (1.9)
-1) (1.9)
Если известно содержание кислорода в продуктах горения, то коэффициент избытка воздуха определяется по формуле:
 =1+
=1+  (1.10) где
(1.10) где  концентрация кислорода в составе горючего газа, % об.;
концентрация кислорода в составе горючего газа, % об.;
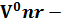 теоретический объем продуктов горения.
теоретический объем продуктов горения.
Для вещества, у которых объем продуктов горения равен объему израсходованного воздуха(например, горение серы и углерода),формула (1.10) упрощается:
 =
=  (1.11)
(1.11)
Если содержание кислорода в окислительной среде отличается от содержания его в воздухе, то формулу(1.10) можно записать в виде:
 =1+
=1+  (1.12)
(1.12)
и соответственно формулу (1.11)
 =
=  (1.13),
(1.13),
где  2 -содержание кислорода в окислительной среде, % об.
2 -содержание кислорода в окислительной среде, % об.
Примеры решения задач.
Пример №1.
Определить теоретическое количество воздуха, необходимого для горения 1м3 метана при нормальных условиях.
Решение: Горючее вещество является индивидуальным химическим соединением, поэтому для расчета его объема надо пользоваться формулой (1.3.а). Запишем уравнение химической реакции горения СН4 в воздухе:
СН4+ 2О2+2∙3,76N2=CО2+2Н2О+2∙3,76N2
Из уравнения находим: no2=2; nN2=2∙3,76=7,52; nCH2=1;тогда
V0B=  м3/ м3 или кмоль/кмоль
м3/ м3 или кмоль/кмоль
Пример №2
Определить объем теоретического количества воздуха, необходимого для горения 1кг бензола.
Решение: горючее – индивидуальное химическое соединение, поэтому для расчета по формуле (1.3.б) запишем уравнение химической реакции горения:
С2Н2+7,75O2+7,75∙3,76N2=6CO2+3H2O+7,75∙3,75N2 и найдем:
nО2=7,75; nN2=7,5∙3,76=28,2; nr=1,
Молекулярная масса бензола М=6∙12+6∙1=78 объем 1 кмоля газа при нормальных условиях составляет 22.4м3:
V0B=y m:val="p"/></m:rPr><w:rPr><w:rFonts w:ascii="Cambria Math" w:h-ansi="Times New Roman"/><wx:font wx:val="Cambria Math"/><w:color w:val="000000"/><w:sz w:val="28"/><w:sz-cs w:val="28"/></w:rPr><m:t>=10,3</m:t></m:r></m:oMath></m:oMathPara></w:p><w:sectPr wsp:rsidR="00000000"><w:pgSz w:w="12240" w:h="15840"/><w:pgMar w:top="1134" w:right="850" w:bottom="1134" w:left="1701" w:header="720" w:footer="720" w:gutter="0"/><w:cols w:space="720"/></w:sectPr></w:body></w:wordDocument>"> 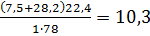 м3/кг
м3/кг
Пример №3
Определить объем воздуха, необходимого для горения 1кг органической массы состава: С-60%, О-25%, N-5%, W-%(влажность), если коэффициент избытка воздуха  а температура воздуха 305К, давление 995ГПа.
а температура воздуха 305К, давление 995ГПа.
Решение: Так как горючее вещество сложного состава, то теоретическое количество воздуха при нормальных условиях определим по формуле (1.4):
V0B=0,269( )=5,9 м3/кг
)=5,9 м3/кг
Из формулы (1.7) рассчитаем практическое количество воздуха при нормальных условиях:
V0B=  V0B=2,5∙5,9=14,75 м3/кг
V0B=2,5∙5,9=14,75 м3/кг
Находим количество воздуха, пошедшего на горение вещества при заданных условиях горения; используя формулу (1.6), получим:
VB(р,т)=  =16,8 м3/кг
=16,8 м3/кг
Пример №4.
Определить объем воздуха, необходимого для горения 5м3смеси газов, состоящих из 20% СН4, 10% СО, 5%N, 35%О2, если коэффициент избытка воздуха равен 1,8.
Решение: Горючее-смесь газов. Поэтому для расчета объема воздуха, пошедшего на сгорание, воспользуемся формулой (1.5). Для определения стехиометрических коэффициентов при кислороде nо2 запишем уравнение реакции горения горючих компонентов в кислороде:
СН4+2О2=СО2+2Н2О;
С 2Н2+2,5О2=2СО2+Н2О; СО+0,5О2=СО2 тогда
V0B=  =5,7 м3/кг
=5,7 м3/кг
Для горения 5м3 газовой смеси необходимый теоретический объем воздуха составит: V0B=5∙5,7 =32,5 м3 Практическое количество воздуха: V0B=1,8∙32,5=58,5 м3.
Пример №5
Определите коэффициент избытка воздуха при горении уксусной кислоты, если на горение 1кг поступило 3 м3 воздуха.
Решение: Для определения коэффициента избытка воздуха по формуле (1.7) необходимо рассчитать его теоретическое количество. Молекулярная масса уксусной кислоты-60.
СН3СООН+2О2+2∙3,76N2=2СО2+2∙3,76 N2;
V0B=  м3/кг
м3/кг
тогда коэффициент избытка воздуха равен:


Горение протекало при недостатке воздуха.
Пример №6
Определить объем воздуха, пошедшего на окисление 1м3 аммиака:
NН3+0,75О2 +0,75 3,76 N2=1,5Н2О+0,5N2+0,75∙3,76N2,
тогда
V0B=  м3/кг
м3/кг
Для определения коэффициента избытка воздуха по формуле (1.10) необходимо рассчитать теоретическое количество продуктов горения 1м3аммиака (см. след параграф 1.2 формула (1.14)):
V0пр=  м3/кг
м3/кг
Пример №7
Определить объем окислительной среды, состоящей из 60%О2 и 40%N2,необходимый для горения 1 кг изопропилового спирта, если ее температура равна 295К, давление 620гПа.
Решение: так как окислительная среда отличается по составу от воздуха, определим по формуле (1.1) объемное соотношение кислорода и азота: 40:60+0,67
Уравнение реакции горения изопропилового спирта:
С3Н7ОН+4,5О2+4,5 0,67N2=3СО2+4Н2О+4,5⋅0,67 N2
Теоретический объем окислительной среды при нормальных условиях рассчитаем по формуле (1.3). Молекулярная масса горючего-60.
V0ос=  =2,8 м3/кг
=2,8 м3/кг
Объем окислительной среды при заданных условиях горения определим из формулы (1.6):
V0ос(рr)=  м3/кг
м3/кг
Пример № 8
Определить сколько кг динитротолуола сгорело в герметичном объеме 100м3, если содержание кислорода в продуктах сгорания составило 12%.
Решение: Так как в продуктах горения содержится кислород, то горение протекало в избытке воздуха, коэффициент избытка которого определим по формуле (1.10). Для этого запишем уравнение горения:
С7Н6(NO2)2+6,5O2+6,5∙3,76N2=7CO2+3H2O+N2+6,5∙3,76N2
Молекулярная масса горючего-182.Теоретический объем воздуха равен:
V0B=  =3,8 м3/кг
=3,8 м3/кг
Теоретический объем продуктов горения (формула1.14):
V0пr= 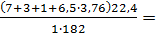 4,4 м3/кг
4,4 м3/кг

Практический объем воздуха, пошедший на горение:
VB= 2,55 ∙3.8=9,7 м3/кг
Тогда массу сгоревшего динитротолуола Р определим из соотношения:
Рr =  , Рr =
, Рr =  =10,3 кг
=10,3 кг
Контрольные задачи
1. Определить количество (теоретическое) воздуха, необходимое для горения 1кг: метилового, этилового, пропилового и амилового спиртов. Построить график зависимости объема воздуха от молекулярной массы спирта.
2. Определить теоретический объем воздуха, необходимого для горения 1м3: метана, этана, пропана, бутана и пентана. Построить график зависимости объема воздуха от положения вещества в гомологическом ряду (содержания углерода в молекуле вещества).
3. Определить теоретический объем воздуха, пошедший на горение 1кг: метана, метилового спирта. Объяснить причину влияния состава вещества на объем воздуха, требуемый для их горения.
4. Определить объем воздуха, пошедший на горение 1 кг древесины состава: С-47%, Н-8%, О-40%, W -5% если коэффициент избытка воздуха равен 2,8; давление 900ГПа, температура 285К.
5. Сколько воздуха поступило на горение 1кг углерода, если в продуктах горения содержание кислорода составило 17%?
6. Сколько воздуха требуется подать на сжигание 200м3 генераторного газа состава: СО-29%, Н2-14%, СН4-3%, СО2-6,5%, N 2 -45%, O 2 -2,5% если коэффициент избытка воздуха равен 2,5?
7. Определить количество сгоревшего толуола, кг. в помещении объемом 400 м3,если после пожаре при отсутствии газообмене установлено, что содержание кислорода снизилось до 17%.
8. Сколько м3хлора поступило на горение 300м3 водорода, если в продуктах горения избыток окислителя составил 80м3?
9. Определить избыток воздуха в продуктах горения газовой смеси состава: СО-15%, С4Н10-45%,О2-30%, N 2 -10% если коэффициент избытка равен 1,2;температура 265К; давление 850ГПа
10. Сколько м3 окислительной среды, состоящей из 50% кислорода, 50% азота, необходимо для горения 8кг этилацетата, если коэффициент избытка равен 1,2; температура 265К; давление 850 ГПа.
11. Определить коэффициент избытка окислительной среды, состоящей из 70% кислорода и 30% азота, если при горении серы содержание кислорода снизилось до 55%. Определить количество сгоревшей серы, кг, если объем помещения равен 180 м3.
12. Сколько антрацита (принять, что содержание углерода равно 100%) сгорело в помещении объемом 150м3, если прекращение горения наступило при снижении кислорода до 13%, газообмен не учитывать
Домашнее задание к теме: «Расчёт количества воздуха,



 (1.1)
(1.1) 2,
2,  2 - это объёмное (% об.) содержание азота и кислорода в окислительной среде.
2 - это объёмное (% об.) содержание азота и кислорода в окислительной среде. =
= 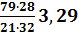
 2 -молекулярные массы соответственно кислорода и азота.
2 -молекулярные массы соответственно кислорода и азота.



 )
)


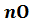 2
2  2 количество горючего, кислорода. и азота получаемые из уравнения химической реакции горения кмоль;
2 количество горючего, кислорода. и азота получаемые из уравнения химической реакции горения кмоль; ri -коцентрация i-того горючего компонента, %;
ri -коцентрация i-того горючего компонента, %; О 2 концентрация кислорода в составе горючего газа, %об.;
О 2 концентрация кислорода в составе горючего газа, %об.; 2 i -количество кислорода необходимое для окисления одного i-того кмоля горючего компонента, ккмоль.
2 i -количество кислорода необходимое для окисления одного i-того кмоля горючего компонента, ккмоль. =
=  (1.6)
(1.6) нормальное давление, Па.
нормальное давление, Па. температура, К.
температура, К. объем воздуха при нормальных условиях;
объем воздуха при нормальных условиях;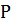 1
1 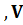 1
1  Т1
Т1 
 заданные условия горения.
заданные условия горения. :
: =
=  (1.7)
(1.7) :
: (1.8)
(1.8) -1) (1.9)
-1) (1.9) (1.10) где
(1.10) где  концентрация кислорода в составе горючего газа, % об.;
концентрация кислорода в составе горючего газа, % об.;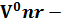 теоретический объем продуктов горения.
теоретический объем продуктов горения. (1.11)
(1.11) (1.12)
(1.12) (1.13),
(1.13), 2 -содержание кислорода в окислительной среде, % об.
2 -содержание кислорода в окислительной среде, % об. м3/ м3 или кмоль/кмоль
м3/ м3 или кмоль/кмоль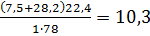 м3/кг
м3/кг а температура воздуха 305К, давление 995ГПа.
а температура воздуха 305К, давление 995ГПа. )=5,9 м3/кг
)=5,9 м3/кг V0B=2,5∙5,9=14,75 м3/кг
V0B=2,5∙5,9=14,75 м3/кг =16,8 м3/кг
=16,8 м3/кг =5,7 м3/кг
=5,7 м3/кг м3/кг
м3/кг

 м3/кг
м3/кг м3/кг
м3/кг =2,8 м3/кг
=2,8 м3/кг м3/кг
м3/кг =3,8 м3/кг
=3,8 м3/кг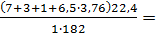 4,4 м3/кг
4,4 м3/кг
 , Рr =
, Рr =  =10,3 кг
=10,3 кг

