Пусть в сосуде в виде куба со стороной l находится N молекул. Рассмотрим движение одной из молекул. Пусть молекула движется из центра куба в одном из 6 возможных направлений (рис.1), например параллельно оси Х со скоростью v. Ударяясь о стенку А куба молекула оказывает на него давление (см. рис. 2). Найдем его. Согласно второму закону Ньютона сила давления  , где
, где 
 . Предполагая, что происходит абс. упругий удар, имеем v1=v2=v. Изменение импульса
. Предполагая, что происходит абс. упругий удар, имеем v1=v2=v. Изменение импульса 
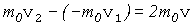 . Молек. вернется в исходное состояние (в центр куба) спустя время dt=(0.5l+0.5l)/ v= l/ v. В итоге получаем выражение для силы давления, оказываемого на стенку сосуда 1 молекулой
. Молек. вернется в исходное состояние (в центр куба) спустя время dt=(0.5l+0.5l)/ v= l/ v. В итоге получаем выражение для силы давления, оказываемого на стенку сосуда 1 молекулой 

Е 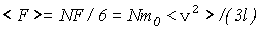 сли число молекул в сосуде N, то к cтенке А движетсяв среднем N/6 молекул и они создают среднюю силу давления на стенку, где <v 2> - cредний квадрат скорости молекул.
сли число молекул в сосуде N, то к cтенке А движетсяв среднем N/6 молекул и они создают среднюю силу давления на стенку, где <v 2> - cредний квадрат скорости молекул.
Давление, оказываемое на стенку сосуда, площадь которой S=l2, 
Учитывая, что N/l3=N/V=n, т.е. равно концентрации молекул, а также, что  -средняя кинетическая энергия поступательного движения молекулы газа, получаем из (12) основное уравнение молекулярно-кинетической теории идеального газа
-средняя кинетическая энергия поступательного движения молекулы газа, получаем из (12) основное уравнение молекулярно-кинетической теории идеального газа  . (14) Такое же давление производят молекулы на другие стенки сосуда, поскольку молекулы газа движутся хаотически и не имеют какого-либо преимущественного направления движения.
. (14) Такое же давление производят молекулы на другие стенки сосуда, поскольку молекулы газа движутся хаотически и не имеют какого-либо преимущественного направления движения.
Молекулярно-кинетическое толкование абсолютной температуры. С точки зрения молекулярно-кинетической теории абсолютная температура есть величина, пропорциональная средней энергии поступательного движения молекулы. <eпост>=3/2kT
Билет №6
Вопрос №1
Энергия как функция состояния системы. Кинетическая энергия. Теорема об изменении кинетической энергии. Потенциальная энергия (Б4). Связь силы с изменением потенциальной энергии (Б4).
Разность между теплотой и работой при заданных начальных и конечных параметрах системы является величиной постоянной и не зависит от пути процесса, т.е. представляет собой функцию состояния системы.
Кин. энергия мат. точки - скалярная мера механического движения, равная половине произведения массы точки на квадрат ее ск-ти.
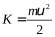 или
или 
Теорема: Пусть мат. точка массой m под действием приложенной к ней силы F получила перемещение на dl. Спроецировав векторы ур-ия ma=F на касательную к траектории в месте положения точки, получим  .
.
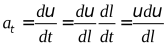

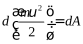


Изменение кин. э. равно работе приложенных к точке сил.
Сл. энергия имеет такую же размерность как и работа.
Билет №6
Вопрос №2
Предмет молекулярной физики. Статистический и термодинамический методы. Основные положения МКТ. Размеры и сечение столкновения молекул. Число столкновений и длина свободного пробега молекул. Число Ван-дер-Ваальса. Число Кнудсена. Идеальный газ.
Молек.ф. представляет собой раздел ф., изучающий строение и свойства вещ-ва, исходя из молекул.-кинет. представлений. Согласно этому любое тело-состоит из большого кол-ва очень маленьких обособленных частиц. Они находятся в хаотическом движении. Его интенсивность зависит от температуры вещ-ва. Док-вом этого служит броуновское движение. МКТ ставит себе целью истолковать свойства тел наблюдаемые на опыте (давление, температуру) как суммарный результат действия молекул.
Статистический метод-использую лишь средними величинами, кот. хар. движение огромной совокупности частиц. Изучением различных св-в тел и изменений сост. в-ва занимается термодинамика.
Положения МКТ: 1) все тела состоят из большого числа мельчайших частиц.2) эти частицы непрерывно и хаотически движутся. 3)частицы взаимодействуют друг с другом. молекулы газа находясь в тепловом движении непрерывно сталкиваются друг с другом.
Будем представлять молекулы в виде твердых шариков со вполне определенным диаметром.
Мин. расстояние d между центрами сблизившихся при соударении молекул наз. эффективным диаметром молекулы.
Величина σ=πd^2(м^2) наз=ся эффективным сечением столкновения.
Число соударений в единицу времени ν=(√2)πd^2<V>n=(√2)σ <V>n
Средняя длина свободного пробега молекулы: λ=<V>/ν=1/(√2)σn
Число Ван-дер-Ваальса Na = (6,022045±0,000031)*10 23
Число Кнудсена (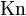 ) — один из критериев подобия движения разрежённых газов:
) — один из критериев подобия движения разрежённых газов:

Идеальным называется газ, молекулы которого имеют пренебрежимо малый собственный объем и не взаимодействуют друг с другом на расстоянии.
Билет №7
Вопрос №1



 , где
, где 
 . Предполагая, что происходит абс. упругий удар, имеем v1=v2=v. Изменение импульса
. Предполагая, что происходит абс. упругий удар, имеем v1=v2=v. Изменение импульса 
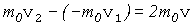 . Молек. вернется в исходное состояние (в центр куба) спустя время dt=(0.5l+0.5l)/ v= l/ v. В итоге получаем выражение для силы давления, оказываемого на стенку сосуда 1 молекулой
. Молек. вернется в исходное состояние (в центр куба) спустя время dt=(0.5l+0.5l)/ v= l/ v. В итоге получаем выражение для силы давления, оказываемого на стенку сосуда 1 молекулой 

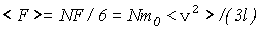 сли число молекул в сосуде N, то к cтенке А движетсяв среднем N/6 молекул и они создают среднюю силу давления на стенку, где <v 2> - cредний квадрат скорости молекул.
сли число молекул в сосуде N, то к cтенке А движетсяв среднем N/6 молекул и они создают среднюю силу давления на стенку, где <v 2> - cредний квадрат скорости молекул.
 -средняя кинетическая энергия поступательного движения молекулы газа, получаем из (12) основное уравнение молекулярно-кинетической теории идеального газа
-средняя кинетическая энергия поступательного движения молекулы газа, получаем из (12) основное уравнение молекулярно-кинетической теории идеального газа  . (14) Такое же давление производят молекулы на другие стенки сосуда, поскольку молекулы газа движутся хаотически и не имеют какого-либо преимущественного направления движения.
. (14) Такое же давление производят молекулы на другие стенки сосуда, поскольку молекулы газа движутся хаотически и не имеют какого-либо преимущественного направления движения.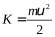 или
или 
 .
.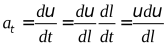

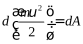


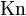 ) — один из критериев подобия движения разрежённых газов:
) — один из критериев подобия движения разрежённых газов:



